01/11/2015
W świecie chemii organicznej istnieje grupa związków, które wyróżniają się niezwykłą stabilnością, unikalną budową i wszechstronnym zastosowaniem. Mowa o węglowodorach aromatycznych, zwanych również arenami. Odgrywają one kluczową rolę nie tylko w przemyśle i technologii, ale także w biologii, będąc fundamentalnymi składnikami wielu naturalnie występujących substancji. Zrozumienie ich struktury, właściwości i wpływu na otoczenie jest niezwykle ważne dla każdego, kto zgłębia tajniki chemii, a także dla świadomości ekologicznej i zdrowotnej. W tym artykule zanurzymy się w świat aren, aby odkryć, co czyni je tak wyjątkowymi i dlaczego są przedmiotem nieustannych badań.
Czym są Węglowodory Aromatyczne?
Węglowodory aromatyczne to specyficzna klasa związków organicznych charakteryzujących się obecnością jednego lub wielu pierścieni aromatycznych w swojej strukturze. Najczęściej spotykanym i zarazem najprostszym przykładem jest benzen (C6H6), który stanowi prototyp tej grupy. Pierścień aromatyczny to zazwyczaj sześcioczłonowy pierścień węglowy, w którym atomy węgla połączone są ze sobą w specyficzny sposób, tworząc układ sprzężonych wiązań podwójnych i pojedynczych. W przeciwieństwie do zwykłych alkenów, gdzie wiązania podwójne są zlokalizowane, w arenach elektrony tworzące te wiązania są zdelokalizowane na całym pierścieniu.
Ta delokalizacja elektronów π (pi) jest kluczowa dla właściwości aromatycznych. Oznacza to, że elektrony nie są przypisane do konkretnych wiązań podwójnych między dwoma atomami węgla, ale rozprzestrzeniają się po całym pierścieniu, tworząc swego rodzaju "chmurę" elektronową powyżej i poniżej płaszczyzny pierścienia. Zjawisko to, formalnie opisywane jako rezonans chemiczny, prowadzi do znacznej stabilizacji cząsteczki. Energia całej cząsteczki aromatycznej jest znacznie niższa niż energia hipotetycznej cząsteczki o zlokalizowanych wiązaniach (np. cykloheksa-1,3,5-trienu w przypadku benzenu). Tę różnicę nazywa się "energią stabilizacji aromatycznej" lub "energią rezonansu".
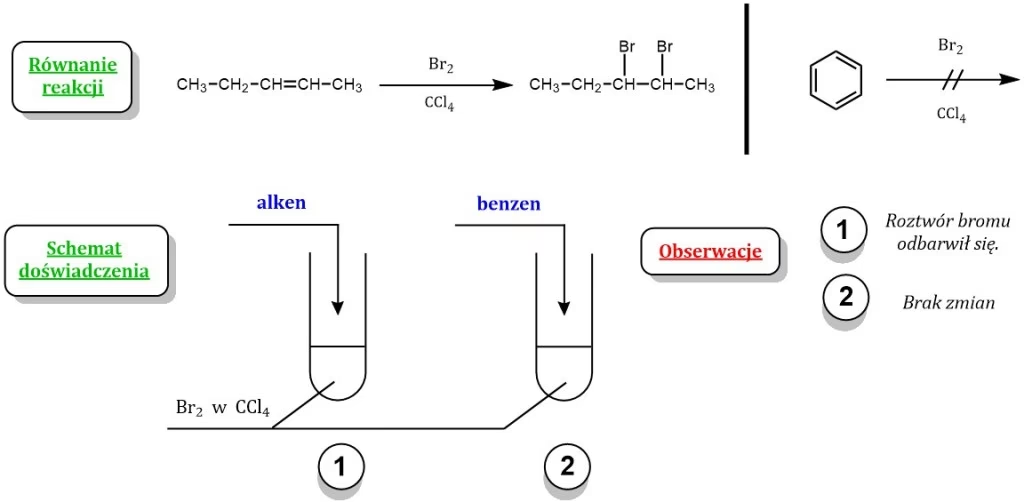
Wszystkie atomy węgla w pierścieniu aromatycznym posiadają hybrydyzację sp2, co sprawia, że cząsteczki te są płaskie. Ta płaska geometria, wraz z delokalizacją elektronów, jest fundamentalnym warunkiem aromatyczności. Dzięki tej unikalnej budowie, węglowodory aromatyczne wykazują niezwykłą trwałość i odmienną reaktywność w porównaniu do innych węglowodorów nienasyconych. Zamiast typowych dla alkenów reakcji addycji, dla arenów charakterystyczne są reakcje substytucji elektrofilowej, katalizowane często kwasami Lewisa, takie jak na przykład reakcja Friedla-Craftsa.
Jak rozpoznać Związek Aromatyczny? Reguła Hückla i Kryteria Aromatyczności
Nie każdy cykliczny związek zawierający wiązania wielokrotne jest aromatyczny. Aby związek został zakwalifikowany jako aromatyczny, musi spełnić kilka kluczowych kryteriów:
- Musi być związkiem cyklicznym.
- Musi być płaski.
- Musi posiadać pełne sprzężenie wiązań w pierścieniu, co oznacza, że wszystkie atomy w pierścieniu muszą mieć orbital p dostępny do tworzenia układu π (np. hybrydyzacja sp2 lub sp).
- Musi spełniać regułę Hückla, która mówi, że liczba elektronów π w pierścieniu musi być równa 4n+2, gdzie "n" jest dowolną liczbą naturalną (0, 1, 2, 3...).
Reguła Hückla jest szczególnie skuteczna dla układów monocyklicznych. Na przykład, benzen ma 6 elektronów π (n=1, 4*1+2=6), cyklopentadienylowy anion ma 6 elektronów π, a cyklooktatetraen (4n=8) nie jest aromatyczny. Warto jednak zauważyć, że istnieją policykliczne związki aromatyczne, takie jak piren, które niekoniecznie spełniają regułę 4n+2 w odniesieniu do wszystkich pierścieni naraz, ale nadal wykazują właściwości aromatyczne ze względu na złożony układ delokalizacji elektronów w całym systemie skondensowanych pierścieni.
Związki, które są cykliczne, płaskie i w pełni sprzężone, ale posiadają 4n elektronów π, nazywane są związkami antyaromatycznymi. Są one znacznie mniej stabilne niż ich liniowe odpowiedniki i często wykazują dużą reaktywność. Przykładem może być cyklobutadien. Z kolei związki, które nie spełniają jednego z pozostałych kryteriów (np. nie są płaskie lub nie mają pełnego sprzężenia), są po prostu związkami niearomatycznymi.
Unikalna struktura wiązań w arenach sprawia, że ich reaktywność znacząco różni się od innych węglowodorów nienasyconych. Zamiast ulegać reakcjom addycji (typowym dla alkenów), areny preferują reakcje substytucji elektrofilowej, w których atom wodoru w pierścieniu jest zastępowany przez inny podstawnik. Te reakcje są często katalizowane przez kwasy Lewisa, co podkreśla ich stabilność i specyficzny charakter chemiczny.
Przykłady i Zastosowanie Węglowodorów Aromatycznych
Węglowodory aromatyczne są wszechobecne i odgrywają kluczową rolę w wielu aspektach naszego życia. Ich źródłem w przemyśle jest głównie rafinacja ropy naftowej oraz destylacja smoły węglowej.
Kluczowe Przykłady Arenów:
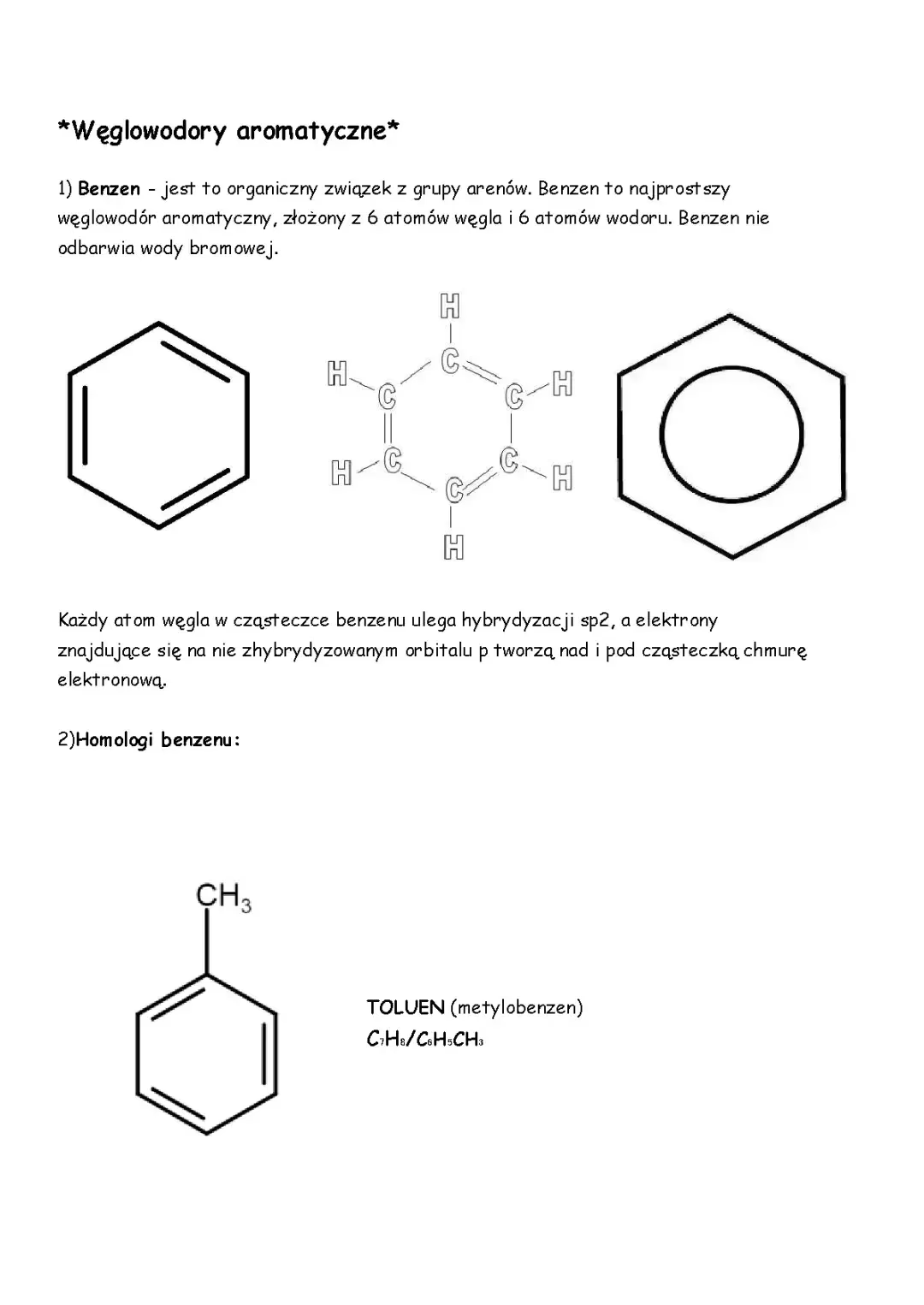
- Benzen (C6H6): Najprostszy i najważniejszy węglowodór aromatyczny, będący podstawą wielu innych związków.
- Toluen (metylobenzen, C7H8): Benzen z grupą metylową, szeroko stosowany jako rozpuszczalnik i substrat w syntezie organicznej.
- Naftalen (C10H8): Związek z dwoma skondensowanymi pierścieniami benzenowymi, znany z zapachu kulek na mole.
- Antracen (C14H10) i Fenantren (C14H10): Trzy skondensowane pierścienie benzenowe, izomery o różnej konfiguracji, stosowane w barwnikach i farmacji.
- Pentacen, Heksacen, Heptacen: Związki o większej liczbie skondensowanych pierścieni, często o interesujących właściwościach optycznych i elektronicznych.
Zastosowania Przemysłowe:
Węglowodory aromatyczne są niezwykle cennymi surowcami w przemyśle chemicznym:
- Paliwa: Stanowią ważny składnik benzyn, zwiększając ich liczbę oktanową.
- Rozpuszczalniki: Ze względu na swoje właściwości rozpuszczające, są używane w farbach, lakierach, klejach i wielu procesach chemicznych.
- Substraty do produkcji polimerów: Są kluczowymi prekursorami w syntezie tworzyw sztucznych, takich jak nylon, styren (monomer do produkcji polistyrenu), fenol, anilina i wiele innych.
- Farmaceutyka i agrotechnika: Służą do syntezy leków, pestycydów i herbicydów.
- Barwniki: Wiele barwników organicznych ma w swojej strukturze pierścienie aromatyczne.
Występowanie w Przyrodzie i Biologiczne Znaczenie:
Pierścienie benzenowe i inne układy aromatyczne są powszechne w świecie żywym:
- Rośliny: Są zdolne do syntezy pierścieni benzenowych z prostych związków nieorganicznych, takich jak dwutlenek węgla i woda, w procesach fotosyntezy i metabolizmu wtórnego. Tworzą w ten sposób szeroką gamę związków, w tym flawonoidy, ligniny czy niektóre alkaloidy.
- Zwierzęta: Organizmy zwierzęce nie posiadają zdolności syntezy związków aromatycznych de novo, dlatego muszą je pozyskiwać z pożywienia. Przykładami kluczowych związków aromatycznych niezbędnych w diecie są aminokwasy egzogenne: fenyloalanina, tyrozyna i tryptofan. Są one budulcem białek i prekursorami neuroprzekaźników.
- Witaminy: Wiele ważnych witamin, takich jak witamina K, witamina B2 (ryboflawina) i witamina B9 (kwas foliowy), zawiera w swojej strukturze pierścienie aromatyczne.
- Leki: Znaczna część leków stosowanych w medycynie posiada w swojej strukturze pierścienie benzenowe lub inne układy aromatyczne, co często wpływa na ich aktywność biologiczną i interakcje z celami molekularnymi. Heterocykliczne związki aromatyczne, zawierające w pierścieniu atomy inne niż węgiel (np. azot, tlen, siarka), również wykazują unikalne i istotne właściwości medyczne.
Nazewnictwo i Wzory Węglowodorów Aromatycznych
Poprawne nazewnictwo i przedstawianie wzorów węglowodorów aromatycznych jest kluczowe w chemii organicznej. Najprostszy aren, benzen, może być przedstawiany na kilka sposobów, co odzwierciedla jego unikalną budowę:
- Wzory Kekulégo: Przedstawiają benzen jako cykloheksa-1,3,5-trien, z trzema zlokalizowanymi wiązaniami podwójnymi i trzema pojedynczymi. Chociaż jest to wygodne w zapisie, błędnie sugeruje, że wiązania są stałe i zmieniają położenie.
- Struktury rezonansowe: Bardziej poprawne przedstawienie to ukazanie dwóch możliwych wzorów Kekulégo jako skrajnych struktur rezonansowych, między którymi cząsteczka ciągle "przełącza się".
- Wzór z okręgiem: Najbardziej trafne przedstawienie, gdzie okrąg wewnątrz sześciokąta symbolizuje delokalizację sześciu elektronów π na całym pierścieniu, podkreślając brak zlokalizowanych wiązań podwójnych.
Dla bardziej złożonych arenów, takich jak naftalen, również stosuje się analogiczne przedstawienia, ukazujące skondensowane pierścienie i delokalizację elektronów.
Nomenklatura Arenów:
- Związki niepodstawione skondensowane: Często używa się nazw zwyczajowych, np. benzen, naftalen, antracen, fenantren. Dla arenów o większej liczbie skondensowanych pierścieni (powyżej czterech) dodaje się sufiks "-acen" do greckiego rdzenia liczby pierścieni (np. pentacen, heksacen).
- Areny jednopodstawione: Do nazwy arenu dodaje się jako przedrostek przekształconą nazwę podstawnika. Na przykład, benzen z grupą metylową to metylobenzen, powszechnie znany jako toluen. Etylobenzen to benzen z grupą etylową.
- Areny wielopodstawione: W nazwie wymienia się lokanty (numery pozycji) wszystkich grup i atomów, tak aby ich suma była najmniejsza, a numer lokantu pierwszego podstawnika (według alfabetu) był jak najniższy.
Dla pochodnych benzenu z dwoma podstawnikami, oprócz numeracji, powszechnie stosuje się oznaczenia przedrostkowe, które określają wzajemne położenie podstawników:
- orto- (o-): Podstawniki znajdują się obok siebie, w pozycjach 1,2.
- meta- (m-): Podstawniki znajdują się w pozycjach 1,3, czyli są oddzielone jednym niepodstawionym atomem węgla.
- para- (p-): Podstawniki znajdują się naprzeciwko siebie, w pozycjach 1,4.
Związki różniące się tylko położeniem podstawników są izomerami konstytucyjnymi typu orto, meta, para. Klasycznym przykładem są izomery ksylenu (dimetylobenzenu):
| Nazwa zwyczajowa | Nazwa systematyczna | Położenie podstawników |
|---|---|---|
| o-ksylen | 1,2-dimetylobenzen | orto (1,2) |
| m-ksylen | 1,3-dimetylobenzen | meta (1,3) |
| p-ksylen | 1,4-dimetylobenzen | para (1,4) |
Wpływ Węglowodorów Aromatycznych na Środowisko i Zdrowie Człowieka
Mimo swoich licznych zastosowań i obecności w naturze, węglowodory aromatyczne stanowią również poważne wyzwanie dla środowiska i zdrowia publicznego. Są one klasyfikowane jako lotne związki organiczne (LZO) i są znaczącym składnikiem zanieczyszczeń atmosferycznych.
Wpływ na Środowisko:
- Emisje: Główne źródła emisji to spaliny samochodowe (szczególnie z pojazdów napędzanych benzyną), użycie rozpuszczalników, a także spalanie biomasy. Szacuje się, że areny stanowią około 10% całkowitej globalnej antropogenicznej emisji niemetanowych związków organicznych (NMOC).
- Tworzenie smogu fotochemicznego: Węglowodory aromatyczne są wysoce reaktywne w atmosferze i w obecności tlenków azotu (NOx) oraz światła słonecznego przyczyniają się do powstawania ozonu troposferycznego (ozonu przypowierzchniowego) i innych fotoutleniaczy. Ozon ten na poziomie gruntu jest szkodliwy dla zdrowia ludzi i roślin. Szacuje się, że areny mogą odpowiadać za 30-40% produkcji ozonu w miejskiej atmosferze.
- Powstawanie wtórnych aerozoli organicznych (SOA): Procesy utleniania węglowodorów aromatycznych w atmosferze prowadzą do tworzenia się cząstek stałych, znanych jako wtórne aerozole organiczne. SOA są szkodliwe dla zdrowia ludzkiego, zmniejszają widoczność i przyczyniają się do zmian klimatycznych. Badania wykazały, że potencjał tworzenia aerozoli organicznych przez opary benzyny wynika głównie z jej frakcji aromatycznej.
Wpływ na Zdrowie Człowieka:
Narażenie na węglowodory aromatyczne może nastąpić poprzez wdychanie oparów, spożycie lub kontakt skórny. Ich toksyczność jest złożona i zależy od konkretnego związku, dawki i czasu ekspozycji.
- Rakotwórczość: Wiele węglowodorów aromatycznych, zwłaszcza wielopierścieniowych, jest potencjalnie rakotwórcze. Benzen jest uznawany za silny czynnik rakotwórczy dla ludzi (klasyfikowany jako czynnik rakotwórczy grupy A przez Amerykańską Agencję Ochrony Środowiska, US EPA). Jego płaska struktura umożliwia mu wślizgiwanie się między nukleotydy DNA, co prowadzi do uszkodzeń genetycznych, mutacji i zwiększonego ryzyka rozwoju białaczki oraz innych nowotworów szpiku kostnego. Badania laboratoryjne wykazały również, że fotoutlenianie innych węglowodorów aromatycznych prowadzi do powstawania produktów mutagennych.
- Wpływ na ośrodkowy układ nerwowy (OUN): Arene mają wysoki potencjał hamujący OUN, prowadząc do obniżenia aktywności, senności, zmęczenia, zaburzeń koordynacji ruchowej, a w ciężkich przypadkach do drgawek i utraty świadomości. Dzieje się tak poprzez nieswoiste, lipofilowe oddziaływania z błonami komórkowymi, co zmienia działanie neuroprzekaźników.
- Wpływ na serce: Posiadają niewielki potencjał kardiotoksyczny.
- Inne objawy ostrego zatrucia:
- Po spożyciu: ból jamy ustnej i gardła, nudności, wymioty.
- Po ekspozycji oczu: podrażnienie, zapalenie spojówek, obrzęk i otarcia rogówki.
- Po wdychaniu par: przebiega dwufazowo – początkowe pobudzenie OUN, a następnie faza depresji OUN. W skrajnych przypadkach zgon może nastąpić w wyniku niedotlenienia lub zaburzeń pracy serca.
- Trwałe zanieczyszczenia organiczne (TZO): Niektóre areny należą do tej grupy, co oznacza, że długo utrzymują się w środowisku, bioakumulują się w łańcuchach pokarmowych i mogą być transportowane na duże odległości, stanowiąc globalne zagrożenie.
Leczenie zatrucia węglowodorami aromatycznymi jest wyłącznie objawowe (np. podanie tlenu, wspomaganie oddechu). Nie istnieje specyficzna odtrutka.
W grupie najważniejszych aromatycznych węglowodorów emitowanych do atmosfery często wyróżnia się BTEX, czyli Benzen, Toluen, Etylobenzen i Xyleny. Są to związki, które ze względu na swoją powszechność i potencjalną toksyczność są monitorowane w powietrzu miejskim.
Najczęściej Zadawane Pytania (FAQ)
Poniżej przedstawiamy odpowiedzi na najczęściej pojawiające się pytania dotyczące węglowodorów aromatycznych, aby jeszcze lepiej zrozumieć ich naturę i znaczenie.
Czy wszystkie związki cykliczne z wiązaniami podwójnymi są aromatyczne?
Nie, nie wszystkie. Aby związek był aromatyczny, musi spełniać kluczowe kryteria: musi być cykliczny, płaski, posiadać pełne sprzężenie wiązań w pierścieniu (czyli wszystkie atomy w pierścieniu muszą mieć orbital p dostępny do tworzenia układu π) oraz spełniać regułę Hückla, czyli posiadać 4n+2 elektronów π w pierścieniu (gdzie n to liczba całkowita 0, 1, 2...). Brak spełnienia któregokolwiek z tych warunków oznacza, że związek jest niearomatyczny lub antyaromatyczny.
Jaki jest ogólny wzór węglowodorów aromatycznych?
Nie istnieje jeden prosty wzór ogólny, który obejmowałby wszystkie węglowodory aromatyczne ze względu na ich ogromną różnorodność strukturalną (pojedyncze pierścienie, skondensowane pierścienie, obecność różnych podstawników). Najprostszy aren, benzen, ma wzór C6H6. Dla monocyklicznych arenów z jednym pierścieniem benzenowym i podstawnikami alkilowymi, wzór można przybliżyć jako CnH2n-6, ale to uproszczenie nie obejmuje złożonych, wielopierścieniowych czy heterocyklicznych struktur.
Dlaczego niektóre węglowodory aromatyczne są rakotwórcze?
Wiele węglowodorów aromatycznych, zwłaszcza tych wielopierścieniowych (WWA), charakteryzuje się płaską strukturą. Ta cecha umożliwia im wślizgiwanie się między zasady azotowe w podwójnej helisie DNA, w procesie zwanym interkalacją. Interkalacja może prowadzić do uszkodzeń DNA, takich jak mutacje, pęknięcia nici czy nieprawidłowe replikacje, co w konsekwencji może zapoczątkować proces nowotworowy. Benzen jest szczególnie znany ze swoich właściwości rakotwórczych, prowadzących do białaczki.
Czym jest grupa związków BTEX?
BTEX to akronim używany w kontekście zanieczyszczeń powietrza, odnoszący się do czterech najważniejszych lotnych węglowodorów aromatycznych: Benzenu, Toluenu, Etylobenzenu i Xylenów. Są to powszechne składniki paliw (np. benzyny) i rozpuszczalników, a ich emisje do atmosfery mają znaczący wpływ na jakość powietrza i zdrowie publiczne ze względu na ich toksyczność i udział w tworzeniu smogu fotochemicznego.
Węglowodory aromatyczne to klasa związków chemicznych o dwojakiej naturze. Z jednej strony są niezastąpionymi surowcami przemysłowymi i ważnymi składnikami procesów biologicznych, napędzającymi współczesną cywilizację. Z drugiej strony, ich wszechobecność w środowisku i potencjalna toksyczność, zwłaszcza w kontekście zanieczyszczeń powietrza i ryzyka nowotworowego, wymagają ciągłej uwagi i rygorystycznych regulacji. Zrozumienie ich chemii, zastosowań i zagrożeń jest kluczowe dla zrównoważonego rozwoju i ochrony zdrowia człowieka oraz środowiska naturalnego.
Zainteresował Cię artykuł Węglowodory Aromatyczne: Klucz do Zrozumienia Chemii? Zajrzyj też do kategorii Chemia, znajdziesz tam więcej podobnych treści!