16/02/2025
Przygotowanie do matury z chemii to często wyzwanie, które wymaga gruntownej wiedzy z wielu dziedzin. Jedną z kluczowych partii materiału są kwasy, a w szczególności kwasy tlenowe, które regularnie pojawiają się w arkuszach egzaminacyjnych. Ten artykuł to kompleksowy przewodnik, który pomoże Ci opanować niezbędne informacje o tych związkach, zrozumieć ich właściwości i zasady nazewnictwa, a także przygotować się na typowe zadania maturalne.
Kwasy Tlenowe: Podstawy, Nazewnictwo i Wzory
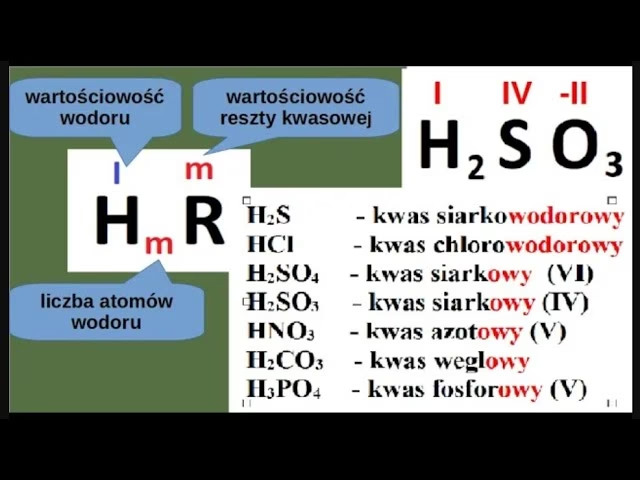
Kwasy tlenowe to związki chemiczne, które w swojej strukturze zawierają atomy tlenu, połączone z atomem centralnym (najczęściej niemetalem) oraz atomami wodoru. W przeciwieństwie do kwasów beztlenowych (np. HCl), w kwasach tlenowych wodór jest związany z resztą kwasową zawierającą tlen.
Kluczową umiejętnością na maturze jest rozpoznawanie i prawidłowe nazywanie kwasów tlenowych. Tablice maturalne zawierają wzory i nazwy wielu z nich, jednak zrozumienie zasad nazewnictwa znacząco ułatwia naukę i pozwala na logiczne odtwarzanie informacji. Nazewnictwo kwasów tlenowych opiera się na wartościowości atomu centralnego, która jest często wskazywana rzymską cyfrą w nawiasie po nazwie niemetalu (np. kwas azotowy(V)).
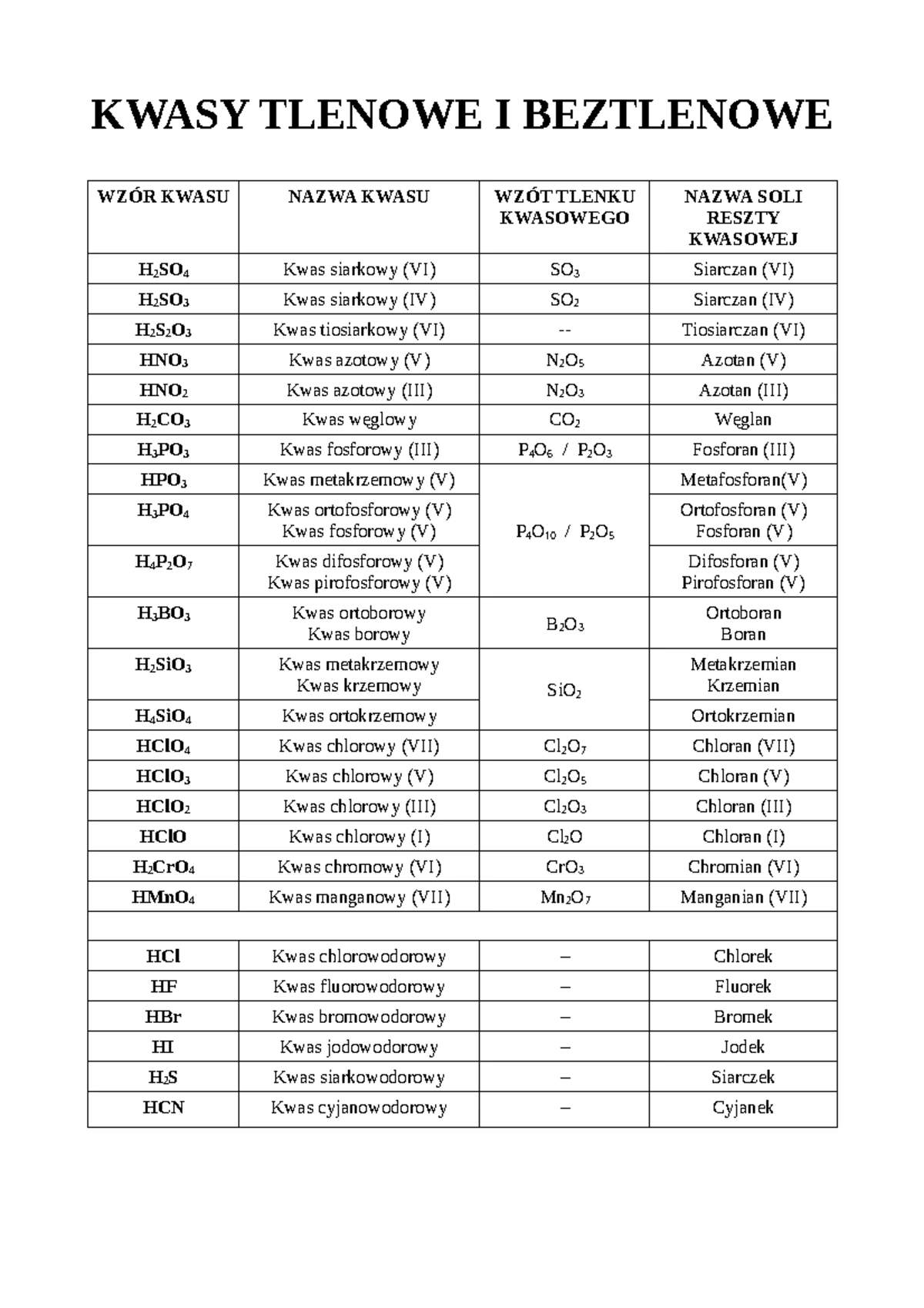
Poniższa tabela przedstawia najważniejsze kwasy tlenowe, które musisz opanować przed egzaminem:
| Wzór kwasu | Nazwa | Wartościowość atomu centralnego | Wartościowość reszty kwasowej | Stopień utlenienia atomu centralnego |
|---|---|---|---|---|
| HNO2 | kwas azotowy(III) | III | I | +III |
| HNO3 | kwas azotowy(V) | V | I | +V |
| H2SO3 | kwas siarkowy(IV) | IV | II | +IV |
| H2SO4 | kwas siarkowy(VI) | VI | II | +VI |
| H2CO3 | kwas węglowy(IV) | IV | II | +IV |
| H3PO4 | kwas fosforowy(V) | V | III | +V |
| HClO | kwas chlorowy(I) | I | I | +I |
| HClO2 | kwas chlorowy(III) | III | I | +III |
| HClO3 | kwas chlorowy(V) | V | I | +V |
| H3AsO3 | kwas arsenowy(III) | III | III | +III |
| H3AsO4 | kwas arsenowy(V) | V | III | +V |
| H3BO3 | kwas borowy(III) | III | III | +III |
Warto zwrócić uwagę, że wartościowość reszty kwasowej odpowiada liczbie atomów wodoru w cząsteczce kwasu. Jest to fundamentalna zasada, która pomaga w pisaniu wzorów soli i równań reakcji chemicznych.
Właściwości Kwasów Tlenowych: Moc i Czynniki Wpływające
Podobnie jak wszystkie kwasy, kwasy tlenowe w roztworach wodnych ulegają dysocjacji, uwalniając jony wodorowe (H+), co nadaje im charakterystyczny odczyn kwasowy. Moc kwasu, czyli jego zdolność do dysocjacji, zależy od kilku kluczowych czynników.
Zgodnie z informacjami zawartymi w tablicach maturalnych, moc kwasów tlenowych rośnie wraz ze wzrostem liczby atomów tlenu w reszcie kwasowej, które nie są bezpośrednio związane z atomami wodoru. Im więcej takich atomów tlenu, tym silniej przyciągają one elektrony od wiązania O-H, osłabiając je i ułatwiając odszczepienie protonu (H+). Doskonałym przykładem jest szereg kwasów chlorowych: kwas chlorowy(VII) (HClO4) jest mocniejszy od kwasu chlorowego(V) (HClO3), który z kolei jest mocniejszy od kwasu chlorowego(III) (HClO2) i kwasu chlorowego(I) (HClO).

Drugim istotnym czynnikiem wpływającym na moc kwasów tlenowych jest elektroujemność atomu centralnego. Im większa elektroujemność atomu centralnego, tym mocniejszy jest kwas. Można to zaobserwować, porównując kwasy w obrębie tej samej grupy układu okresowego. Na przykład, kwas siarkowy(VI) (H2SO4) jest mocniejszy od kwasu selenowego(VI) (H2SeO4), ponieważ siarka jest bardziej elektroujemna niż selen.
Wybrane Kwasy Tlenowe na Maturze: Właściwości i Reakcje
Kwasy Azotowe: HNO3 i HNO2
Kwas azotowy(V) (HNO3), powszechnie znany jako kwas azotowy, to jedna z najważniejszych substancji w chemii. Jest to bezbarwna ciecz, charakteryzująca się bardzo silnymi właściwościami kwasowymi i utleniającymi. Stężony kwas azotowy(V) dymi na powietrzu, a pod wpływem światła stopniowo żółknie. Zjawisko to wynika z jego rozkładu, podczas którego wydziela się tlenek azotu(IV) (NO2).
Otrzymywanie kwasu azotowego(V) w laboratorium często odbywa się poprzez reakcję tlenku azotu(V) z wodą:
N2O5 + H2O → 2 HNO3
Reakcja rozkładu, odpowiedzialna za zmianę barwy kwasu, przebiega następująco:
4HNO3 → 4NO2 + 2H2O + O2
Kwas azotowy(III) (HNO2) jest znacznie mniej trwały niż jego odpowiednik(V). Występuje głównie w roztworach wodnych oraz w postaci soli, nazywanych azotynami(III). Jest kwasem o średniej mocy. Cechą charakterystyczną kwasu azotowego(III) jest jego zdolność do ulegania reakcji dysproporcjonowania, zwłaszcza podczas ogrzewania lub zatężania, co oznacza, że jednocześnie pełni funkcję utleniacza i reduktora:
3HNO2 → HNO3 + 2NO + H2O
Azotyny(III), sole kwasu azotowego(III), znajdują szerokie zastosowanie w chemii analitycznej jako utleniacze i reduktory. Przykładem jest reakcja azotynu(III) z jodkami w środowisku kwaśnym, która prowadzi do wydzielenia wolnego jodu (I2). Reakcja ta jest wykorzystywana do identyfikacji jodków:
2KI + 2NaNO2 + 4HCl → I2 + 2NO + 2H2O + 2NaCl + 2KCl
Kwasy Siarkowe: H2SO4 i H2SO3
Kwas siarkowy(VI) (H2SO4), czyli kwas siarkowy, to kolejny związek o fundamentalnym znaczeniu w chemii i przemyśle. Jest to oleista, bezbarwna ciecz, wyróżniająca się silnymi właściwościami higroskopijnymi (pochłania wodę) oraz kwasowymi. Stężony kwas siarkowy(VI) wykazuje również silne właściwości utleniające, szczególnie w podwyższonej temperaturze.
Dysocjacja kwasu siarkowego(VI) przebiega dwuetapowo. Pierwszy etap jest całkowity, natomiast drugi jest częściowy:
H2SO4 → HSO4- + H+ (dysocjacja całkowita)
HSO4- ⇌ SO42- + H+ (dysocjacja częściowa)
Charakterystyczne dla stężonego kwasu siarkowego(VI) są reakcje z niemetalami, takimi jak węgiel czy siarka, które są typowymi reakcjami utleniania-redukcji i często pojawiają się w zadaniach maturalnych:
C + 2H2SO4 → CO2 + 2SO2 + 2H2O
S + 2H2SO4 → 3SO2 + 2H2O
Kwas siarkowy(IV) (H2SO3), znany również jako kwas siarkawy, jest znacznie mniej stabilny niż kwas siarkowy(VI) i nie udało się go wyizolować w stanie wolnym. W roztworach wodnych dwutlenek siarki (SO2) reaguje z wodą, tworząc kwas siarkowy(IV), jednak równowaga tej reakcji jest silnie przesunięta w stronę substratów:
SO2 + H2O ⇌ H2SO3
Mimo niestabilności kwasu, jego sole – siarczyny(IV) – są dobrze znane i znajdują zastosowanie. W zadaniach maturalnych i reakcjach chemicznych, w których teoretycznie powinien powstać kwas siarkowy(IV), zazwyczaj zapisuje się produkty jako SO2 i H2O, podkreślając jego nietrwałość.
Kwas Fosforowy(V) (H3PO4)
Kwas fosforowy(V) (H3PO4), czyli kwas ortofosforowy(V), jest trójprotonowym kwasem o średniej mocy. Jego cząsteczka zawiera trzy atomy wodoru, które mogą ulec dysocjacji. Otrzymuje się go m.in. w reakcji tlenku fosforu(V) z wodą:
P4O10 + 6H2O → 4H3PO4
Dysocjacja kwasu fosforowego(V) przebiega trójstopniowo, co oznacza, że może tworzyć trzy rodzaje soli:
H3PO4 ⇌ H+ + H2PO4-
H2PO4- ⇌ H+ + HPO42-
HPO42- ⇌ H+ + PO43-
Kwas Borowy(III) (H3BO3)
Kwas borowy(III) (H3BO3) wyróżnia się na tle innych kwasów tlenowych ze względu na swoje nietypowe właściwości. Jest to bardzo słaby kwas jednoprotonowy, ale co istotne, działa jako kwas Lewisa, a nie kwas Brønsteda w roztworze wodnym. Oznacza to, że w odróżnieniu od większości kwasów nie oddaje protonów, lecz przyjmuje jony wodorotlenkowe (OH-):
H3BO3 + 2H2O ⇌ B(OH)4- + H3O+
Ta specyficzna właściwość wynika z obecności wolnego orbitalu p na atomie boru, co umożliwia mu przyjęcie pary elektronowej od jonu hydroksylowego.

Ogólne Właściwości Kwasów
Poza szczegółowymi informacjami o kwasach tlenowych, na maturze warto znać ogólne cechy charakterystyczne dla kwasów. Należą do nich:
- Kwaśny smak (choć nigdy nie należy próbować kwasów!).
- Budowa kowalencyjna.
- Zdolność do rozpuszczania niektórych metali, z wydzieleniem wodoru, w reakcji pojedynczego podstawienia (np. Zn(s) + H2SO4 (aq) → ZnSO4 (aq) + H2 (g)).
- Zdolność do zobojętniania zasad, w reakcjach z którymi tworzą sole.
- W roztworze wodnym ulegają dysocjacji, tworząc kationy wodoru (H+) i aniony reszty kwasowej.
- Wodne roztwory kwasów przewodzą prąd elektryczny.
Kwasy w Życiu Codziennym
Kwasy towarzyszą nam na co dzień, często nie zdając sobie z tego sprawy. Oto kilka przykładów:
- Kwas cytrynowy (C6H8O7): Odpowiada za kwaśny smak cytrusów, np. cytryn i pomarańczy.
- Kwas jabłkowy (C4H6O5): Obecny w jabłkach.
- Kwas mlekowy (C3H6O3): Powstaje w mleku podczas trawienia oraz w mięśniach podczas intensywnego wysiłku.
- Kwas octowy (CH3COOH): Główny składnik octu, powszechnie używanego w kuchni.
- Kwas siarkowy (H2SO4): Używany w starszych akumulatorach samochodowych do magazynowania energii.
- Kwas garbnikowy (C76H52O46) i kwas szczawiowy (C2H2O4): Występują w herbacie i kawie.
Najczęściej Zadawane Pytania (FAQ)
Czym jest kwas?
Kwas to substancja, która w roztworze wodnym uwalnia jony wodorowe (H+) (definicja Arrheniusa). Zgodnie z definicją Brønsteda-Lowry'ego, kwas to związek zdolny do oddawania protonu (H+). Natomiast w ujęciu Lewisa, kwas to akceptor pary elektronowej.
Jakie są różnice między kwasami a zasadami?
Kwasy to związki o kwaśnym smaku (nie należy ich próbować!), zawierające jony wodorowe (H+), które barwią niebieski papierek lakmusowy na czerwono. Zasady natomiast mają gorzki smak, zawierają jony wodorotlenkowe (OH-) i barwią czerwony papierek lakmusowy na niebiesko. Kwasy reagują z metalami aktywnymi, wydzielając wodór, podczas gdy zasady zazwyczaj nie reagują z metalami w ten sposób. Zarówno kwasy, jak i zasady w roztworach wodnych przewodzą prąd elektryczny.
Podaj przykłady kwasów i zasad.
Przykłady kwasów: kwas solny (HCl), kwas siarkowy(VI) (H2SO4), kwas azotowy(V) (HNO3), kwas mlekowy (C3H6O3), kwas bromowodorowy (HBr). W życiu codziennym: cytryny (kwas cytrynowy), ocet (kwas octowy), sok żołądkowy (kwas solny).
Przykłady zasad: wodorotlenek potasu (KOH), wodorotlenek sodu (NaOH), wodorotlenek wapnia (Ca(OH)2), wodorotlenek litu (LiOH), wodorotlenek cezu (CsOH). W życiu codziennym: mydło, pasta do zębów (lekko zasadowa), soda oczyszczona (wodorowęglan sodu), amoniak (środek czyszczący).
Jakie są typy kwasów?
Możemy wyróżnić trzy główne typy kwasów:
- Kwasy beztlenowe (binarne): Atomy wodoru są bezpośrednio połączone z atomami niemetali (np. HCl, H2S).
- Kwasy tlenowe (oksykwasy): Zawierają jeden lub więcej wiązań O-H, gdzie wodór jest połączony z tlenem, a tlen z atomem centralnym (np. H2SO4, HNO3).
- Kwasy karboksylowe: Są to organiczne kwasy zawierające grupę karboksylową (-COOH). Tylko atom wodoru w tej grupie może być zjonizowany i przyczyniać się do kwasowości (np. CH3COOH - kwas octowy).
Podsumowanie
Gruntowna znajomość kwasów tlenowych, ich nazewnictwa, wzorów, właściwości fizycznych i chemicznych, a także charakterystycznych reakcji, jest absolutnie niezbędna do osiągnięcia sukcesu na maturze z chemii. Pamiętaj, aby nie tylko zapamiętywać wzory, ale przede wszystkim starać się zrozumieć logikę i mechanizmy rządzące właściwościami tych związków. Korzystaj z tablic maturalnych jako wsparcia, ale dąż do głębokiego zrozumienia tematu. Powodzenia na egzaminie!
Zainteresował Cię artykuł Kwasy Tlenowe na Maturze: Pełny Przewodnik? Zajrzyj też do kategorii Chemia, znajdziesz tam więcej podobnych treści!