23/04/2018
Czy kiedykolwiek zastanawiałeś się, z czego składa się otaczający nas świat? Jak naukowcy potrafią określić skład chemiczny odległych gwiazd, zbadać strukturę nowych materiałów, a nawet rozpoznać zanieczyszczenia w wodzie? Kluczem do tych i wielu innych zagadek jest spektroskopia – potężna dziedzina nauki, która pozwala nam zajrzeć w głąb materii, analizując jej interakcje z różnymi formami energii. To nie tylko skomplikowane laboratorium, ale fascynująca podróż do świata atomów i cząsteczek, gdzie światło staje się językiem, którym materia opowiada o sobie.
Co to jest Spektroskopia?
W swej istocie, spektroskopia to nauka zajmująca się powstawaniem i interpretacją widm. Widma te są niczym unikalne "odciski palców" substancji, powstające w wyniku oddziaływań wszelkich rodzajów promieniowania (elektromagnetycznego, akustycznego, cząstek elementarnych) z materią. Możemy ją rozumieć jako szerokie pole technik analitycznych, które generują i interpretują te widma, dostarczając bezcennych informacji o składzie, strukturze i właściwościach badanej próbki. Jej znaczenie wykracza daleko poza same techniki laboratoryjne. Co ciekawe, to właśnie dyskusje nad złożonością widma absorpcyjnego atomu wodoru stały się jednym z motorów napędowych rozwoju całej teorii kwantowej, pokazując fundamentalny związek spektroskopii z podstawami fizyki.
Obiektem badań spektroskopowych mogą być rozmaite formy energii – od fal elektromagnetycznych (takich jak światło widzialne, podczerwień, ultrafiolet, promieniowanie rentgenowskie czy radiowe), przez cząstki (np. elektrony, neutrony), aż po fale akustyczne. Ze względu na różnorodność metod i zakresów parametrów fizycznych badanego zjawiska, spektroskopię dzieli się na wiele specjalistycznych gałęzi. Każda z nich oferuje unikalną perspektywę na badany materiał.
Jak Działa Spektroskopia? Rodzaje Oddziaływań
Sposób, w jaki promieniowania oddziałuje z materią, jest kluczowy dla zrozumienia różnych technik spektroskopowych. W zależności od tego, czy promieniowanie jest pochłaniane, emitowane, odbijane czy rozpraszane, uzyskujemy odmienne typy widm, które dostarczają specyficznych informacji:
Spektroskopia Absorpcja: Ta technika polega na analizie widma powstającego po przejściu promieniowania przez warstwę badanej substancji. Materia pochłania selektywnie określone długości fal (energie), a analiza tego, co "brakuje" w widmie po przejściu przez próbkę, pozwala na identyfikację obecnych związków chemicznych. Na przykład, spektroskopia UV-Vis (ultrafioletowo-widzialna) często wykorzystuje absorpcję, aby określić stężenie substancji w roztworze. Istnieje również specyficzna odmiana, taka jak Absorpcja ze Stanów Wzbudzonych (ESA), która bada pochłanianie promieniowania przez cząsteczki już znajdujące się w stanie wzbudzonym, co dostarcza dodatkowych informacji o ich dynamice i strukturze energetycznej.
Spektroskopia Emisyjna: W tej metodzie bada się widma emitowane przez badaną substancję. Emisja może być wywołana przez różnego rodzaju bodźce fizyczne, takie jak podgrzanie próbki do wysokiej temperatury (jak w spektroskopii emisyjnej atomów), naświetlenie promieniowaniem (fluorescencja, fosforescencja) czy też wzbudzenie elektryczne (jak w lampach wyładowczych). Widma emisyjne są charakterystyczne dla atomów i jonów, ponieważ każdy pierwiastek emituje światło o ściśle określonych długościach fal, tworząc unikalny "kod kreskowy", który pozwala na jego identyfikację. Może to być również emisja spontaniczna, wynikająca z naturalnych procesów rozpadu czy relaksacji energetycznej.

Spektroskopia to dziedzina nauki, która obejmuje metody badania materii przy u\u017cyciu promieniowania elektromagnetycznego, które mo\u017ce by\u0107 w danym uk\u0142adzie wytworzone (emisja) lub mo\u017ce z tym uk\u0142adem oddzia\u0142ywa\u0107 (adsorbcja). Spektroskopia Odbiciowa: Jak sama nazwa wskazuje, w ramach tej techniki badane są widma, które powstały w wyniku odbicia promieniowania od powierzchni analizowanej substancji. Jest to szczególnie przydatne do badania materiałów nieprzezroczystych lub powierzchni, gdzie promieniowanie nie może przejść przez próbkę. Analiza odbitego światła może dostarczyć informacji o składzie chemicznym powierzchni, jej chropowatości czy też o obecności specyficznych grup funkcyjnych na niej.
Spektroskopia Rozproszeniowa: Jest to szczególna odmiana spektroskopii odbiciowej, która skupia się na badaniu widma powstałego w wyniku rozpraszania promieniowania. Zamiast czystego odbicia, promieniowanie jest rozpraszane w różnych kierunkach po interakcji z cząsteczkami w gazowych lub cieczowych zawiesinach analizowanej substancji. Przykładem jest spektroskopia Ramana, która bada niewielkie zmiany energii rozproszonego światła, dostarczając unikalnych informacji o drganiach molekularnych i strukturze chemicznej.
Spektroskopia Inwazyjna: Ten rodzaj spektroskopii polega na badaniu widm powstających na skutek niszczenia lub modyfikacji struktury analizowanej substancji przez przechodzące przez nią promieniowanie. Może to obejmować badanie widm promieniowania, które spowodowało zniszczenie po jego przejściu przez substancję, jak i widm produktów rozpadu. Choć jest to technika "niszcząca", bywa niezbędna w specyficznych przypadkach, gdy inne metody są niewystarczające do uzyskania pożądanych informacji o najbardziej fundamentalnych właściwościach materiału lub jego reakcji na ekstremalne warunki.
Co Spektroskopia Mówi Nam o Materii?
Łącząc różne rodzaje promieniowania z różnymi sposobami jego oddziaływania z badaną próbką, otrzymujemy rozmaite techniki spektroskopowe. Te zróżnicowane metody dają możliwość uzyskania niezwykle różnorodnych informacji o badanej substancji. Spektroskopia jest w stanie odpowiedzieć na cztery kluczowe pytania:
- Jaki jest skład atomowy? Dzięki analizie widm emisyjnych lub absorpcyjnych, możemy zidentyfikować, jakie pierwiastki chemiczne są obecne w próbce, a nawet określić ich stężenie.
- Jaka jest budowa chemiczna? Spektroskopia, zwłaszcza w podczerwieni (IR) czy rezonansu magnetycznego (NMR), pozwala na identyfikację grup funkcyjnych i wiązań chemicznych, ujawniając jak atomy są ze sobą połączone w cząsteczkach.
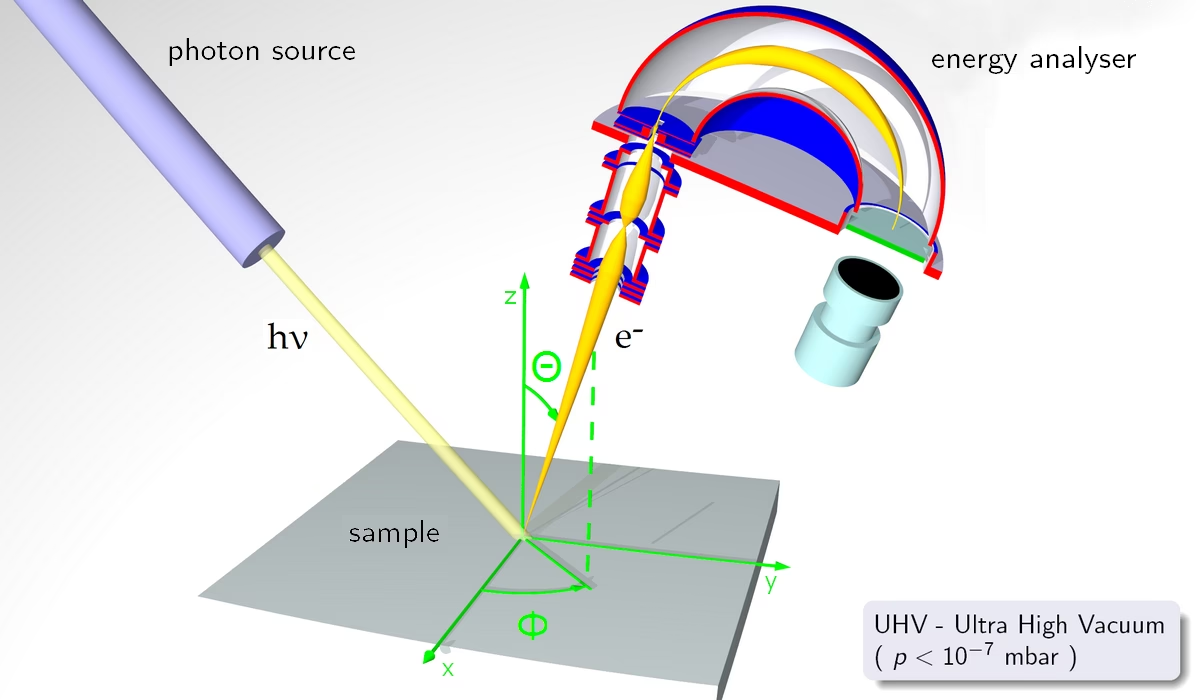
- Jaka jest struktura powierzchni? Techniki takie jak spektroskopia odbiciowa czy fotoelektronowa (XPS) dostarczają informacji o składzie i stanie chemicznym zewnętrznych warstw materiału.
- Jakie są właściwości źródła światła? Analizując widmo emitowane przez źródło, możemy dowiedzieć się o jego temperaturze, składzie, a nawet procesach fizycznych zachodzących wewnątrz.
Tabela Porównawcza: Widmo Słońca vs. Widmo Świetlówki Fluorescencyjnej
Aby lepiej zrozumieć, jak różne źródła światła opowiadają o sobie poprzez swoje widma, przyjrzyjmy się dwóm przykładom:
| Cecha | Widmo Słońca (Emisja Ciągła) | Widmo Świetlówki Fluorescencyjnej (Emisja Liniowa) |
|---|---|---|
| Charakter | Ciągłe, płynne przejście barw. | Dyskretne pasma kolorów, oddzielone ciemnymi przerwami. |
| Wygląd | Pełna tęcza, od fioletu do czerwieni, bez przerw. Intensywność zmienia się płynnie, osiągając szczyt w okolicach 450 nanometrów (niebiesko-zielony). | Seria wyraźnych, wąskich pasm światła o różnych kolorach (np. fioletowe, niebieskie, żółto-zielone, pomarańczowe, czerwone), odpowiadających konkretnym długościom fal. Brak światła pomiędzy pasmami. |
| Pochodzenie | Promieniowanie ciała doskonale czarnego z fotosfery Słońca, rozgrzanej do milionów stopni Celsjusza. | Emisja światła przez wzbudzone atomy gazów (np. rtęci) wewnątrz świetlówki, po przejściu prądu elektrycznego. Każde pasmo odpowiada konkretnemu przejściu elektronowemu w atomie. |
| Informacja | Temperatura źródła, ogólny skład atmosfery (poprzez linie absorpcyjne Fraunhofera, choć niewidoczne na tym uproszczonym widmie). | Skład chemiczny gazu w lampie (identyfikacja pierwiastków), charakterystyka przejść energetycznych w atomach. |
Ta prosta ilustracja pokazuje fundamentalną różnicę między źródłami termicznymi (jak Słońce) a źródłami opartymi na przejściach elektronowych w atomach (jak świetlówka). Spektroskopia pozwala nam "przeczytać" te różnice i wyciągnąć wnioski o naturze badanych obiektów.

Spektroskopia w Podczerwieni (IR) – Klucz do Grup Funkcyjnych
Jedną z najczęściej stosowanych technik w analizy chemicznej jest spektroskopia w podczerwieni (IR). Jest ona niezwykle przydatna do identyfikacji grup funkcyjnych w cząsteczkach organicznych i nieorganicznych. Jej podstawy fizyczne są fascynujące:
Promieniowanie elektromagnetyczne z zakresu podczerwieni (IR) ma częstotliwość zbliżoną do częstotliwości drgań cząsteczek. Kiedy promieniowanie IR przechodzi przez próbkę badanej substancji, jest selektywnie pochłaniane. To pochłanianie zwiększa amplitudę drgań w cząsteczkach tej substancji lub w kryształach. W analizie tych pasm dla układów wieloatomowych stosuje się pojęcie drgań normalnych, traktując każde pasmo jako wynik wzbudzenia jednego (tzw. tony podstawowe) lub kilku (tzw. tony kombinacyjne) drgania normalnego. Od symetrii cząsteczki zależy, które drgania normalne znajdą swoje odzwierciedlenie w widmie absorpcyjnym w zakresie podczerwieni, co jest kluczowe dla interpretacji.
Absorpcji promieniowania podczerwonego towarzyszą zmiany energii oscylacyjnej cząsteczek. Ponieważ energia ta jest skwantowana – czyli może przyjmować tylko określone, dyskretne wartości – absorbowane jest tylko promieniowanie o pewnych ściśle określonych energiach. Te energie są charakterystyczne dla konkretnych grup funkcyjnych wykonujących drgania. Dzięki temu wartości częstości drgań charakterystycznych mogą być ujęte w formie odpowiednich tabel, a absorpcyjne widmo IR umożliwia precyzyjne ustalenie, jakie grupy funkcyjne występują w analizowanej próbce. Warunkiem absorpcji promieniowania (czyli możliwości wzbudzenia drgania przez promieniowanie) jest zmienność momentu dipolowego cząsteczki w trakcie tego drgania. W absorpcyjnym widmie IR dominują pasma związane z tonami podstawowymi drgań cząsteczek, choć możliwa jest także rejestracja znacznie słabszych nadtonów oraz tonów kombinacyjnych i różnicowych (jednoczesnych przejść w dwóch lub więcej oscylatorach), które dostarczają jeszcze bardziej szczegółowych informacji.
Spektroskopia IR jest nieocenionym narzędziem w chemii organicznej do identyfikacji nieznanych związków, monitorowania reakcji chemicznych, a także w kontroli jakości produktów. Istnieją również zaawansowane techniki pochodne, takie jak spektroskopia ATR (Attenuated Total Reflection) w podczerwieni, która pozwala na badanie powierzchni próbek bez konieczności ich przygotowania, co jest niezwykle praktyczne w wielu zastosowaniach.
Gdzie Stosuje się Spektroskopię?
Uniwersalność i precyzja spektroskopii sprawiają, że jest ona powszechnie stosowana w wielu dziedzinach nauki i przemysłu:
- Chemia: Niezbędna do identyfikacji związków chemicznych, określania ich struktury, monitorowania przebiegu reakcji, analizy składu mieszanin i kontroli jakości w przemyśle farmaceutycznym, spożywczym czy petrochemicznym.
- Fizyka: Wykorzystywana do badania właściwości materiałów, struktury krystalicznej, dynamiki cząsteczek, a także do zrozumienia podstawowych zjawisk kwantowych.
- Astronomia: Spektroskopy na teleskopach pozwalają astronomom określać skład chemiczny gwiazd, planet, galaktyk, ich temperaturę, prędkość ruchu, a nawet obecność wody czy innych związków organicznych w odległych mgławicach.
- Medycyna i Biologia: Stosowana w diagnostyce chorób (np. analiza krwi, moczu), obrazowaniu medycznym (np. spektroskopia MR), badaniu interakcji leków z organizmem czy analizie struktury białek i DNA.
- Przemysł: Kluczowa w kontroli jakości surowców i produktów, w procesach produkcyjnych (np. monitorowanie procesów spalania), w przemyśle półprzewodnikowym do kontroli czystości, a także w kryminalistyce do analizy śladów.
- Ochrona Środowiska: Używana do monitorowania zanieczyszczeń powietrza i wody, identyfikacji źródeł skażenia oraz analizy składu gleby.
Najczęściej Zadawane Pytania (FAQ)
- Do czego służy spektroskopia?
- Spektroskopia służy do badania składu chemicznego, budowy molekularnej i struktury materiałów, a także do analizy właściwości źródeł promieniowania. Pozwala identyfikować substancje, mierzyć ich stężenie i monitorować procesy chemiczne.
- Czy spektroskopia jest zawsze techniką nieniszczącą?
- Większość technik spektroskopowych jest nieniszcząca, co oznacza, że próbka może być ponownie użyta po badaniu. Jednakże, jak wspomniano, istnieje również spektroskopia inwazyjna, która może powodować zmiany lub zniszczenia w badanej substancji.
- Jakie rodzaje promieniowania są używane w spektroskopii?
- W spektroskopii wykorzystuje się szerokie spektrum promieniowania elektromagnetycznego (od radiowego, przez podczerwień, światło widzialne, ultrafiolet, promieniowanie rentgenowskie, po promieniowanie gamma), a także promieniowanie cząstkowe (np. elektrony, neutrony) i akustyczne.
- Czy można badać wszystkie substancje spektroskopią?
- Prawie wszystkie substancje można badać za pomocą jakiejś formy spektroskopii. Jednak konkretne techniki mają swoje ograniczenia; na przykład, w spektroskopii IR cząsteczka musi wykazywać zmianę momentu dipolowego podczas drgania, aby była aktywna w podczerwieni.
- Jaki jest związek spektroskopii z teorią kwantową?
- Związek jest fundamentalny. Widma, które obserwujemy w spektroskopii, są bezpośrednim dowodem na kwantyzację energii w atomach i cząsteczkach. Analiza tych widm wymaga zrozumienia mechaniki kwantowej, która opisuje, jak elektrony i jądra atomowe absorbują i emitują energię w dyskretnych "porcjach" (kwantach).
Spektroskopia to dziedzina, która nieustannie się rozwija, oferując coraz to nowe możliwości badania otaczającego nas świata na niewyobrażalnie precyzyjnym poziomie. Od podstawowych badań naukowych po zastosowania przemysłowe i medyczne – jej rola jest nie do przecenienia w postępie naukowym i technologicznym.
Zainteresował Cię artykuł Spektroskopia: Odkryj Tajemnice Materii? Zajrzyj też do kategorii Nauka, znajdziesz tam więcej podobnych treści!
