09/12/2025
Czy kiedykolwiek zastanawiałeś się, z czego zbudowany jest otaczający Cię świat? Krzesło, na którym siedzisz, powietrze, którym oddychasz, a nawet Ty sam – wszystko to składa się z niewiarygodnie małych, ale fundamentalnych jednostek zwanych atomami. Zrozumienie budowy atomu to klucz do pojęcia podstaw chemii, fizyki i całej materii. Chociaż atom jest niewidoczny gołym okiem, jego struktura jest zaskakująco złożona i pełna fascynujących tajemnic, które naukowcy odkrywają od wieków. Wyruszmy w podróż do wnętrza atomu, aby poznać jego składowe i zrozumieć, jak funkcjonuje.
Z czego składa się atom? Podstawowe elementy
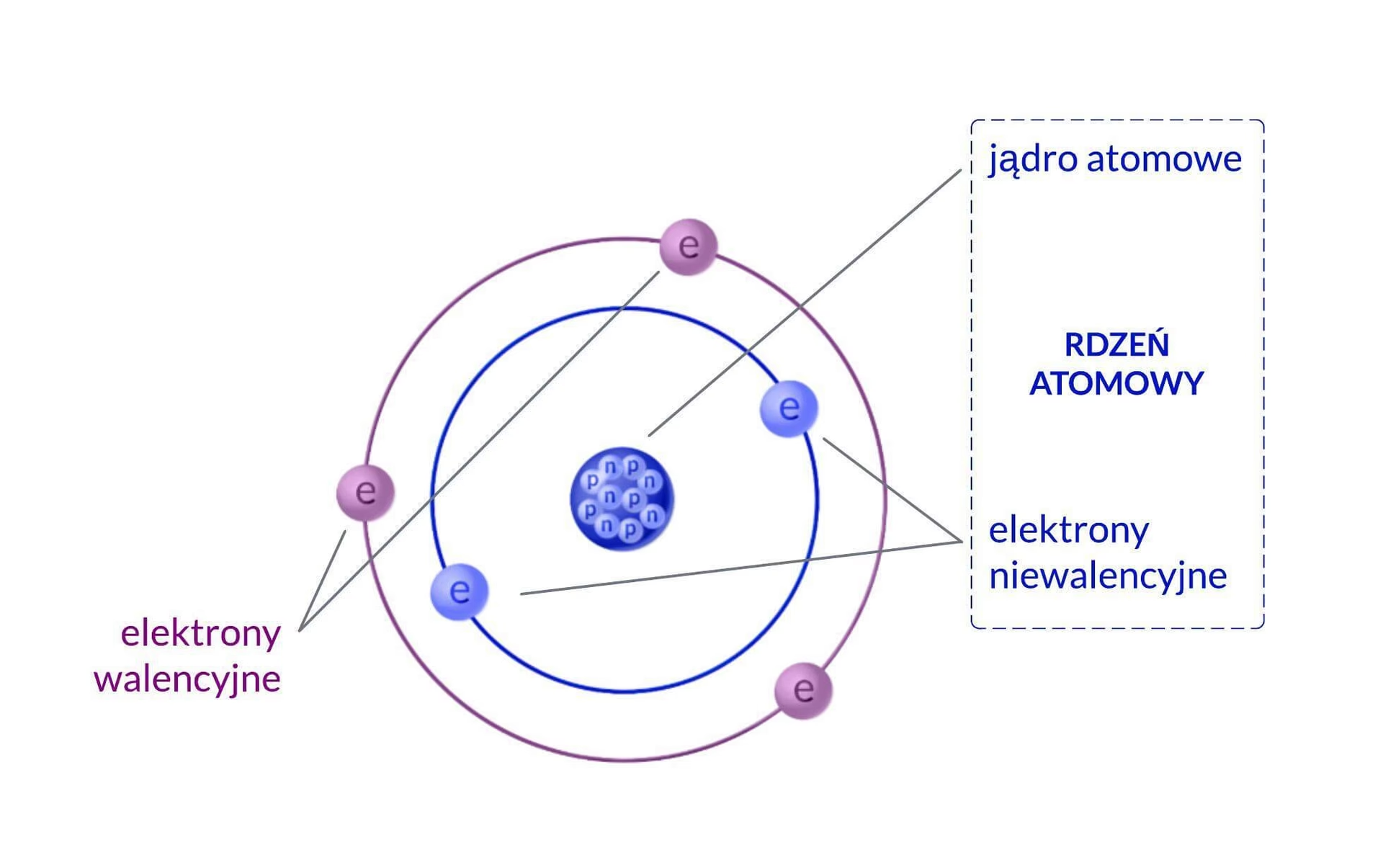
W najprostszym ujęciu, atom składa się z dwóch głównych części: gęstego, centralnego jądra oraz krążących wokół niego elektronów. Można by pomyśleć, że to koniec tej opowieści, ale prawdziwa złożoność tkwi w szczegółach każdego z tych elementów.
Jądro atomowe: serce atomu
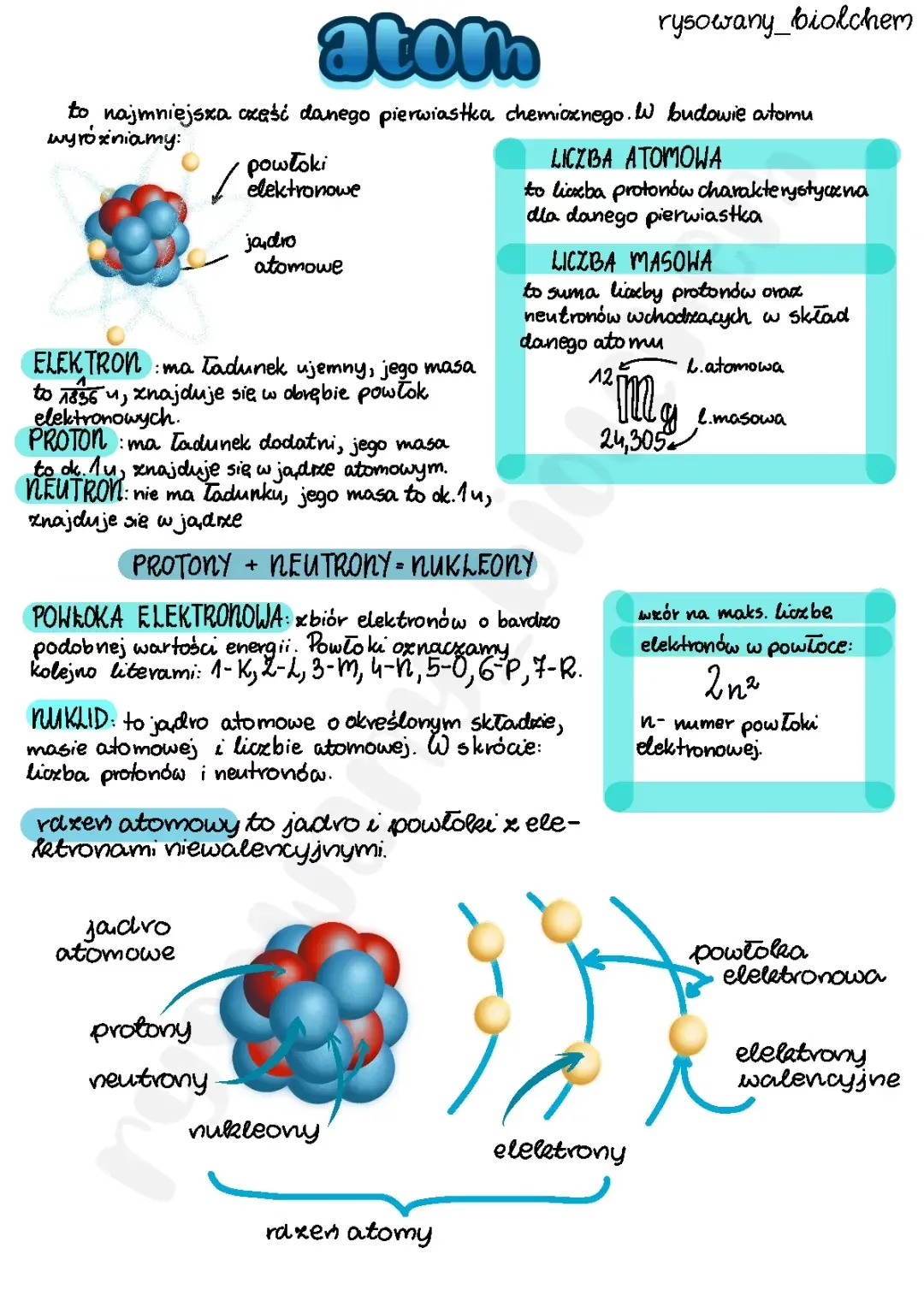
Jądro atomowe jest niezwykle małe, ale koncentruje w sobie niemal całą masę atomu. Składa się ono z dwóch rodzajów cząstek:
- Protonów: Są to cząstki posiadające dodatni ładunek elektryczny. To liczba protonów w jądrze decyduje o tym, jaki pierwiastek chemiczny reprezentuje dany atom. Na przykład, każdy atom wodoru ma jeden proton, a każdy atom helu ma dwa.
- Neutronów: Jak sama nazwa wskazuje, neutrony są elektrycznie neutralne, czyli nie posiadają ładunku. Odgrywają kluczową rolę w stabilizowaniu jądra atomowego, zwłaszcza w przypadku cięższych pierwiastków. Różna liczba neutronów dla tego samego pierwiastka prowadzi do powstawania izotopów.
Kwarki: budulec protonów i neutronów
Co ciekawe, historia nie kończy się na protonach i neutronach. Te cząstki, choć uważane kiedyś za elementarne, same są zbudowane z jeszcze mniejszych obiektów, zwanych kwarkami. Każdy proton i każdy neutron składa się z trzech kwarków. Kwarki są obecnie uważane za jedne z najbardziej fundamentalnych cząstek materii, a ich istnienie zostało potwierdzone w eksperymentach fizyki wysokich energii. Ich oddziaływania są niezwykle silne i to one wiążą je ze sobą, tworząc stabilne protony i neutrony.
Elektrony: krążące wokół jądra
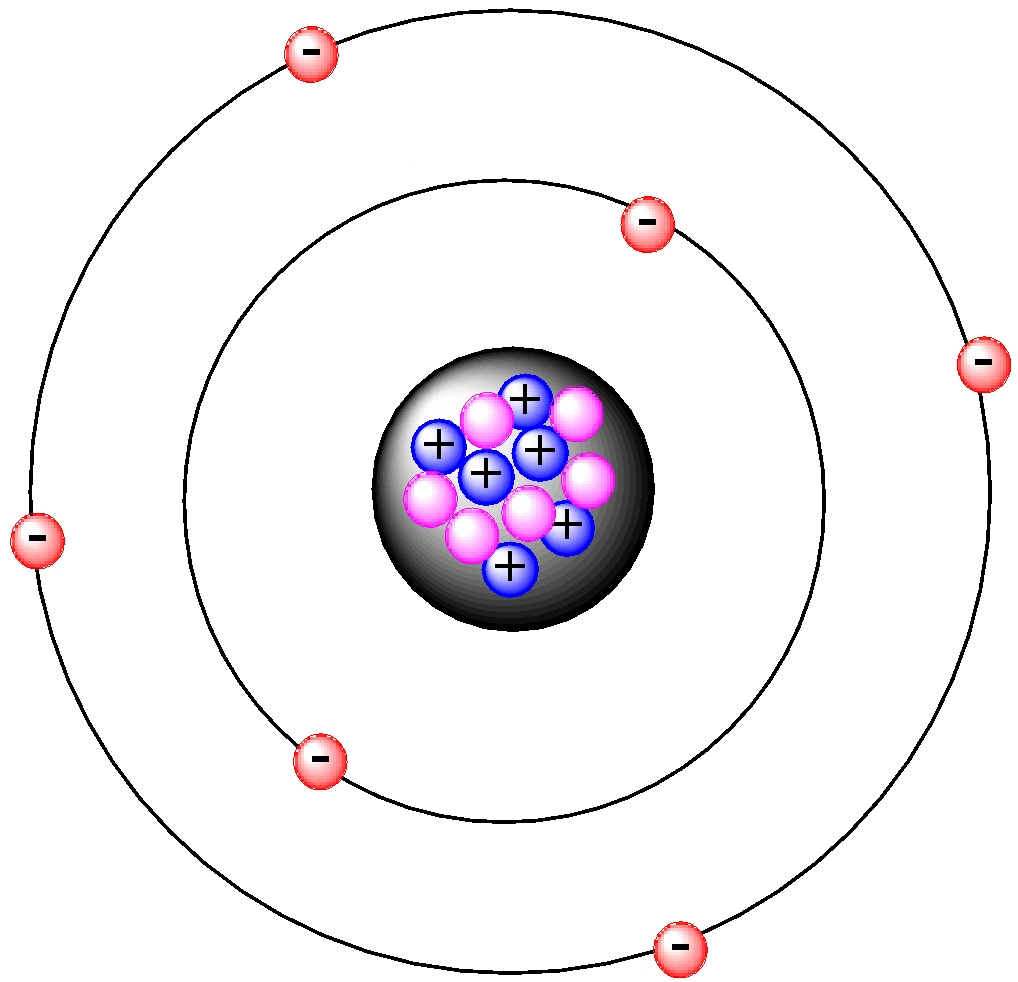
Wokół gęstego jądra atomowego poruszają się elektrony. Są to cząstki o ujemnym ładunku elektrycznym, a ich masa jest znacznie mniejsza niż masa protonów czy neutronów. Liczba elektronów w neutralnym atomie jest równa liczbie protonów, co sprawia, że atom jako całość jest elektrycznie obojętny. Jeśli atom zyska lub straci elektrony, staje się jonem, posiadającym ładunek dodatni lub ujemny.
Sposób poruszania się elektronów jest jednym z najbardziej intrygujących aspektów budowy atomu. Początkowo sądzono, że elektrony krążą wokół jądra w sposób przypominający krążenie planet wokół słońca. Ten pogląd został ujęty w tak zwanym „modelu układu słonecznego” atomu, za który odpowiedzialny jest słynny duński fizyk Niels Bohr.
| Cząstka | Ładunek elektryczny | Położenie w atomie | Dalszy skład (jeśli znany) |
|---|---|---|---|
| Proton | Dodatni (+1) | Jądro atomowe | Trzy kwarki |
| Neutron | Neutralny (0) | Jądro atomowe | Trzy kwarki |
| Elektron | Ujemny (-1) | Poza jądrem (powłoki elektronowe) | Elementarny (niepodzielny) |
Ewolucja modeli atomowych: od Bohra do orbitali
Model atomu Nielsa Bohra, choć intuicyjny i łatwy do zrozumienia, okazał się zbyt uproszczony i niepoprawny w wielu aspektach. Mimo to, jest on nadal uczony na lekcjach chemii w szkole, ponieważ wystarcza do pewnych podstawowych obliczeń i pomaga w zrozumieniu koncepcji kwantyzacji energii. Bohr wprowadził ideę, że elektrony mogą krążyć tylko po ściśle określonych orbitach, posiadając konkretne poziomy energii. Był to rewolucyjny pomysł, który stanowił pomost między klasyczną fizyką a rodzącą się mechaniką kwantową.
Jednakże, rzeczywistość okazała się bardziej skomplikowana. Ostatecznie model Bohra został zastąpiony bardziej złożonym modelem orbitali atomowych. Wynika to z faktu, że elektrony, podobnie jak fotony (cząstki światła), mają właściwości zarówno cząsteczek, jak i fal. To zjawisko nazywane jest dualizmem korpuskularno-falowym i jest jednym z filarów mechaniki kwantowej. W modelu orbitali atomowych nie mówimy już o precyzyjnych orbitach, ale o obszarach przestrzeni wokół jądra, gdzie istnieje największe prawdopodobieństwo znalezienia elektronu. Te obszary nazywane są właśnie orbitalami i mają różne, złożone kształty, odzwierciedlające prawdopodobny rozkład elektronów.
Rozumienie tych subtelności jest kluczowe dla wyjaśnienia zachowania atomów w reakcjach chemicznych i właściwości materii. Chociaż model Bohra jest przydatnym narzędziem dydaktycznym, to model orbitali atomowych znacznie lepiej oddaje kwantową naturę elektronów i ich nieprzewidywalny, probabilistyczny ruch.
Znaczenie zrozumienia budowy atomu
Zrozumienie, z czego składa się atom i jak jego elementy oddziałują ze sobą, jest fundamentalne dla wielu dziedzin nauki i technologii. To właśnie dzięki tej wiedzy jesteśmy w stanie wyjaśnić, dlaczego różne pierwiastki mają odmienne właściwości, jak tworzą się wiązania chemiczne, jak działają materiały półprzewodnikowe, a nawet jak funkcjonują gwiazdy. Od medycyny nuklearnej po rozwój nowych materiałów, od energetyki po nanotechnologię – atom jest wszędzie, a jego poznanie otwiera drzwi do niezliczonych odkryć i innowacji. To wciąż aktywny obszar badań, a naukowcy nieustannie pogłębiają naszą wiedzę o tych najmniejszych, ale jakże potężnych jednostkach materii.
Często zadawane pytania (FAQ)
Czym jest atom?
Atom to podstawowa jednostka materii, najmniejsza cząstka pierwiastka chemicznego, która zachowuje jego właściwości chemiczne. Składa się z jądra atomowego i krążących wokół niego elektronów.
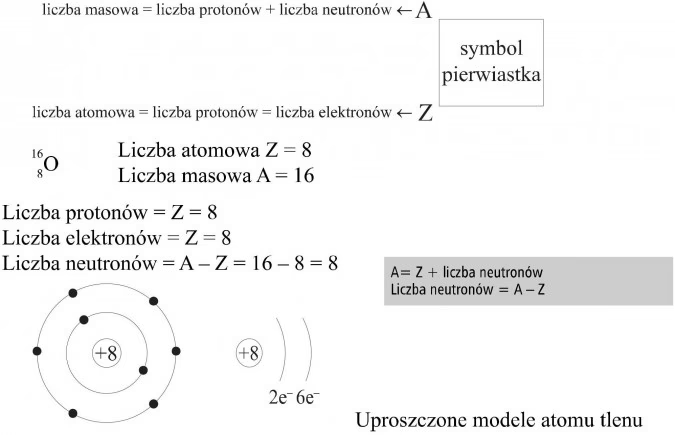
Z czego składa się jądro atomowe?
Jądro atomowe składa się z protonów (cząstek z ładunkiem dodatnim) i neutronów (cząstek neutralnych). Zarówno protony, jak i neutrony, są zbudowane z jeszcze mniejszych cząstek zwanych kwarkami.
Jak poruszają się elektrony wokół jądra?
Elektrony poruszają się wokół jądra w sposób dość nieprzewidywalny, tworząc tzw. chmurę elektronową lub rozkład prawdopodobieństwa. Nie krążą po precyzyjnych orbitach jak planety, co wyjaśnia bardziej zaawansowany model orbitali atomowych. Posiadają zarówno właściwości cząstek, jak i fal.
Czy model atomu Nielsa Bohra jest nadal aktualny?
Model Bohra jest zbyt uproszczony i nie do końca poprawny w świetle współczesnej wiedzy o mechanice kwantowej. Jednakże, jest on nadal używany w celach dydaktycznych i do pewnych obliczeń, ponieważ ułatwia zrozumienie podstawowych koncepcji kwantyzacji energii w atomie. Został zastąpiony bardziej złożonym modelem orbitali atomowych.
Co to są kwarki?
Kwarki to jeszcze mniejsze, fundamentalne cząstki, z których zbudowane są protony i neutrony. Każdy proton i neutron składa się z trzech kwarków. Są one jednymi z najbardziej podstawowych znanych składników materii.
Zainteresował Cię artykuł Atom: Podstawowe Elementy i Zagadki? Zajrzyj też do kategorii Nauka, znajdziesz tam więcej podobnych treści!