03/11/2016
Chemia, często nazywana „centralną nauką przyrodniczą”, jest dziedziną, która bada naturę i właściwości substancji, a przede wszystkim fascynujące przemiany, jakie między nimi zachodzą. Odpowiada na fundamentalne pytania dotyczące budowy materii, jej zachowania i możliwości przekształcania. W świecie, w którym żyjemy, każdy element – od powietrza, którym oddychamy, przez żywność, którą spożywamy, po leki, które nas leczą – jest wynikiem złożonych procesów chemicznych. Zrozumienie, co jest najważniejsze w tej obszernej dyscyplinie, pozwala nie tylko docenić jej znaczenie, ale także otworzyć drzwi do dalszych, głębszych odkryć. Chemia nie jest jedynie zbiorem wzorów i reakcji; to dynamiczna nauka, która nieustannie poszerza nasze horyzonty, wpływając na medycynę, technologię, energetykę i ochronę środowiska.

Chemia i jej miejsce wśród nauk przyrodniczych
Często trudno jest precyzyjnie rozróżnić, gdzie kończy się chemia, a zaczyna fizyka, ponieważ obie te nauki badają naturę i właściwości substancji. Jednak chemia skupia się przede wszystkim na przemianach materii, czyli na tym, jak substancje zmieniają się w inne. Fizyka natomiast, choć również zajmuje się materią, koncentruje się bardziej na energii i siłach, które działają na cząstki. Niemniej jednak, chemia i fizyka wzajemnie się przenikają, tworząc solidne fundamenty dla wszystkich pozostałych nauk przyrodniczych. Biologia, geografia, metalurgia, a nawet astronomia czerpią z wiedzy chemicznej, aby wyjaśnić zjawiska zachodzące w ich dziedzinach. Bez zrozumienia zasad chemii, niemożliwe byłoby zrozumienie procesów życiowych, składu Ziemi czy ewolucji gwiazd. To właśnie sprawia, że chemia jest tak fundamentalna – stanowi pomost między światem mikrocząstek a makroskopowymi zjawiskami, które obserwujemy każdego dnia. Współczesna chemia, w przeciwieństwie do alchemii, jest nauką całkowicie eksperymentalną, opartą na faktach i rzetelnych danych, a nie na magiczno-mistycznej otoczce. Jej rozwój jest dynamiczny; do 2007 roku zarejestrowano ponad 31 milionów związków chemicznych, a każdego dnia przybywa średnio 4000 nowych. To pokazuje ogrom i złożoność tej dziedziny.
Podstawowe cegiełki: Atom, cząsteczka i wiązania chemiczne
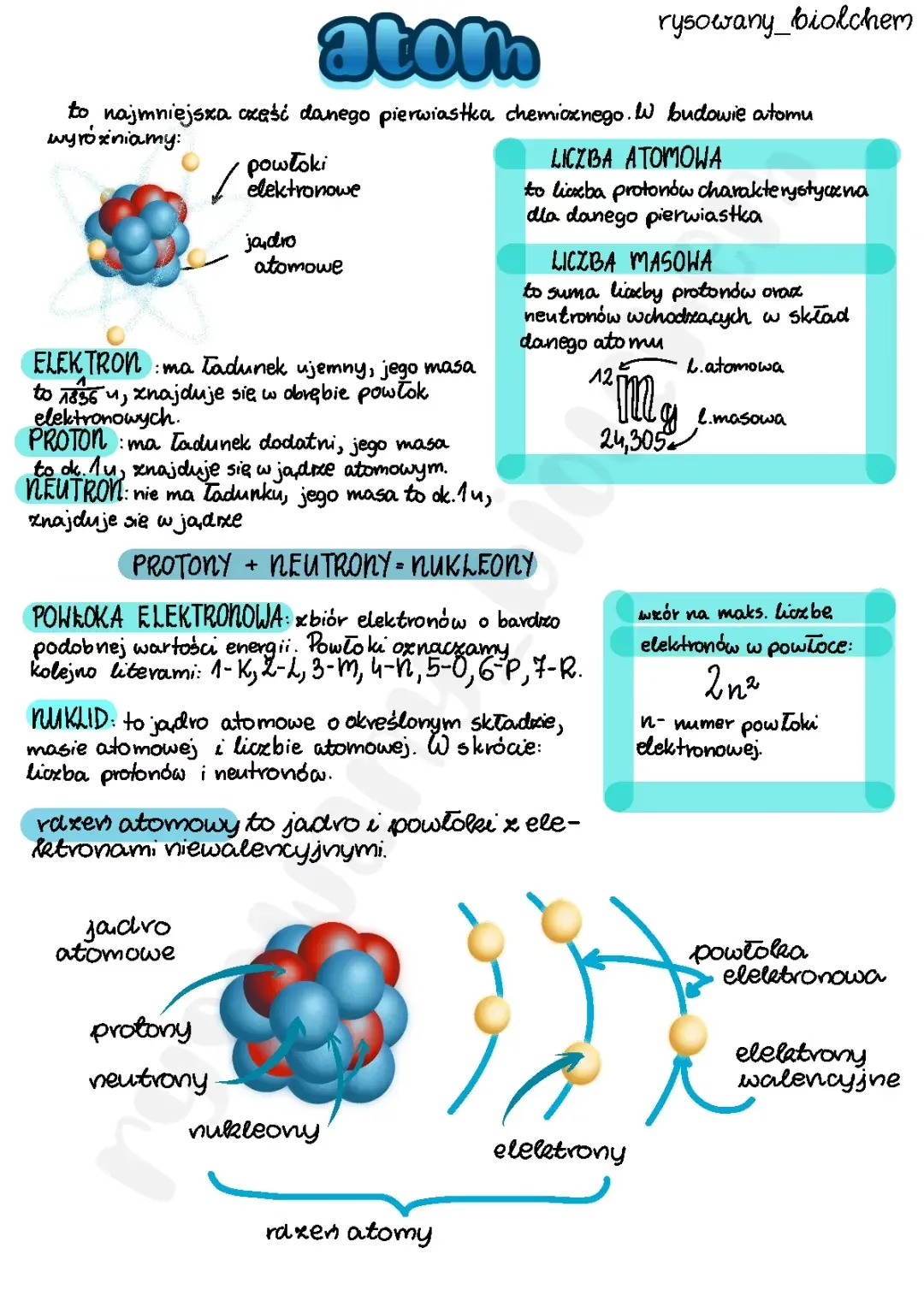
W sercu chemii leży koncepcja atomu. To podstawowa jednostka materii, która zachowuje właściwości pierwiastka chemicznego. Atom składa się z jądra atomowego oraz chmury elektronów. O ile badanie jądra atomowego jest domeną fizyki jądrowej, o tyle chemia skupia się na zachowaniu i naturze chmury elektronowej. To właśnie elektrony, a zwłaszcza te znajdujące się na najbardziej zewnętrznej powłoce (tzw. powłoce walencyjnej), decydują o zdolności atomów do łączenia się w większe obiekty – cząsteczki. Cząsteczka to nic innego jak grupa atomów, które są trwale połączone ze sobą poprzez wymianę, uwspólnianie lub przeniesienie elektronów. W wyniku tego procesu powstają wiązania chemiczne, które są siłami utrzymującymi atomy razem. Mogą to być wiązania jonowe (transfer elektronów), kowalencyjne (uwspólnianie elektronów) lub metaliczne. Zrozumienie natury atomu i cząsteczki oraz mechanizmów powstawania wiązań chemicznych jest absolutnie kluczowe dla pojęcia wszelkich procesów chemicznych. To one determinują, dlaczego stal jest twardsza od żeliwa (atomy żelaza tworzą bardziej zwartą strukturę krystaliczną), dlaczego drewno się pali (celuloza ulega utlenianiu), a cukier rozpuszcza się w wodzie i jest słodki (sacharoza przenika do kubków smakowych poprzez biochemiczne reakcje). Bez tych fundamentalnych pojęć, współczesna chemia nie mogłaby istnieć, a jej wyjaśnienia byłyby powierzchowne i niepełne.
Katalog materii: Pierwiastki, związki chemiczne i mieszaniny
Aby uporządkować ogromną różnorodność substancji w otaczającym nas świecie, chemia wprowadziła kilka kluczowych pojęć klasyfikacyjnych, które są niezbędne do precyzyjnego opisu materii i jej przemian:
- Pierwiastek chemiczny: Według klasycznej definicji, jest to substancja, której nie da się rozłożyć na prostsze substancje metodami chemicznymi. Współcześnie wiemy, że pierwiastki tworzone są przez atomy posiadające jednakową liczbę protonów w jądrze. Koncepcja pierwiastka wywodzi się z alchemii, ale została zrewolucjonizowana przez Roberta Boyle’a, który zerwał z mistycznymi listami pierwiastków na rzecz podejścia eksperymentalnego. Obecnie istnieje ponad 100 znanych pierwiastków, z których każdy ma unikalne właściwości chemiczne i fizyczne. Przykłady to tlen (O), wodór (H), żelazo (Fe), złoto (Au).
- Indywiduum chemiczne: Jest to substancja, w której występuje jeden rodzaj molekuł. Indywiduum chemiczne może być pierwiastkiem (np. czysty tlen O2) lub związkiem chemicznym.
- Związek chemiczny: Jest to szczególny rodzaj indywiduum chemicznego, w którym molekuły składają się z co najmniej dwóch różnych pierwiastków połączonych chemicznie w stałych proporcjach. W przeciwieństwie do mieszanin, składniki związku chemicznego tracą swoje pierwotne właściwości i tworzą nową substancję o unikalnych cechach. Przykłady to woda (H2O), dwutlenek węgla (CO2), sacharoza (C12H22O11).
- Jony: Są to atomy lub cząsteczki, które posiadają niezerowy wypadkowy ładunek elektryczny (dodatni – kationy, lub ujemny – aniony). Powstają w wyniku utraty lub zyskania elektronów i odgrywają kluczową rolę w procesach biologicznych (np. przewodnictwo nerwowe) oraz w roztworach elektrolitów (np. Na+, Cl-, SO42-).
- Rodniki: To atomy lub cząsteczki posiadające przynajmniej jeden niesparowany elektron. Są bardzo reaktywne i dążą do stabilizacji poprzez tworzenie nowych wiązań. Odgrywają ważną rolę w wielu procesach chemicznych (np. polimeryzacja) i biologicznych (np. procesy starzenia, obrona antyoksydacyjna).
Oprócz czystych pierwiastków i związków chemicznych, w naturze powszechnie występują mieszaniny. Mieszaniny to układy składające się z dwóch lub więcej substancji, które nie są ze sobą połączone chemicznie. Mogą być rozdzielone na swoje składniki za pomocą metod fizycznych, co odróżnia je od związków chemicznych. Rozróżnia się:
- Mieszaniny jednorodne (homogeniczne): Składniki są ze sobą tak dokładnie wymieszane, że nie można ich rozróżnić gołym okiem ani za pomocą prostych metod mechanicznych. Mają jednolity skład i właściwości w całej objętości. Przykłady to roztwór soli w wodzie, powietrze, stopy metali takie jak mosiądz.
- Mieszaniny niejednorodne (heterogeniczne): Składniki można łatwo rozróżnić i często rozdzielić metodami mechanicznymi. Mają niejednolity skład i właściwości w różnych miejscach. Przykłady to piasek z wodą, granit, sałatka warzywna.
Zdolność do rozróżniania tych kategorii materii jest fundamentem dla każdego chemika, pozwalając na precyzyjne opisywanie, klasyfikowanie i manipulowanie substancjami w laboratorium i przemyśle.
Dynamika zmian: Reakcje chemiczne
Sednem chemii są reakcje chemiczne – procesy, w których następuje tworzenie lub zrywanie wiązań chemicznych, prowadzące do powstania nowych substancji. To dzięki nim z tlenu i wodoru powstaje woda, a z prostych cukrów złożone polimery. Zwykle reakcje chemiczne mają złożony przebieg, często będąc sumą wielu następujących po sobie lub odbywających się jednocześnie aktów zrywania i powstawania wiązań. Chemicy rozróżniają:
- Równania reakcji: To symboliczny zapis sumarycznego przebiegu reakcji, pokazujący substraty (substancje wyjściowe) po lewej stronie i produkty (substancje powstałe) po prawej, połączone strzałkami. Równania muszą być zbilansowane, co oznacza, że liczba atomów każdego pierwiastka po obu stronach równania musi być taka sama, co odzwierciedla zasadę zachowania masy. Strzałki mogą symbolizować różne aspekty, np. jednokierunkowość, odwracalność, wydzielanie gazu czy osadu.
- Mechanizmy reakcji: To pełny opis wszystkich elementarnych aktów zrywania i powstawania wiązań chemicznych, które składają się na daną reakcję. Mechanizmy pozwalają zrozumieć, dlaczego reakcje zachodzą w określony sposób, jakie są etapy pośrednie, które wiązania ulegają rozrywaniu, a które powstają, oraz jakie czynniki (np. temperatura, ciśnienie, obecność katalizatora) wpływają na ich szybkość. Badanie mechanizmów jest kluczowe dla optymalizacji procesów chemicznych i projektowania nowych, efektywniejszych syntez.
Badanie reakcji chemicznych jest kluczowe dla syntezy nowych materiałów (np. tworzyw sztucznych, włókien), opracowywania leków (np. antybiotyków, leków przeciwnowotworowych), rozumienia procesów metabolicznych w organizmach żywych (np. fotosynteza, oddychanie komórkowe) czy kontrolowania procesów przemysłowych (np. produkcja amoniaku, kwasu siarkowego). To właśnie reakcje chemiczne są motorem napędowym wszelkich zmian w materii i podstawą dynamiki chemicznego świata.
Język chemii: Wzory, mole i stechiometria
Chemia, jak każda nauka, posiada swój uniwersalny język, który umożliwia precyzyjne opisywanie substancji i ich przemian. Tym językiem są wzory chemiczne i równania reakcji. Wzory strukturalne (pokazujące rozmieszczenie atomów i wiązań w przestrzeni, jak np. dla LSD), empiryczne (pokazujące najprostszy stosunek atomów) czy sumaryczne (pokazujące liczbę atomów każdego pierwiastka w cząsteczce, np. H2O) pozwalają na symboliczną reprezentację budowy cząsteczek, używając symboli pierwiastków (jedno-, dwu- lub trzyliterowych skrótów ich nazw) i kresek symbolizujących wiązania chemiczne (pojedyncza kreska oznacza uwspólnioną parę elektronową). Zestawianie tych wzorów w równania pozwala w poglądowy sposób przedstawić przebieg reakcji chemicznych, umieszczając substraty po lewej, a produkty po prawej stronie, połączone różnego rodzaju strzałkami.
Jednak chemia to nie tylko jakościowy opis przemian, ale także precyzyjne pomiary i obliczenia ilościowe. Tutaj na pierwszy plan wysuwa się pojęcie molu. Mol to podstawowa jednostka liczności materii w układzie SI, reprezentująca określoną liczbę cząstek (atomów, cząsteczek, jonów) – dokładnie 6,02214076 × 1023, czyli liczba Avogadra. Znaczenie molu jest nie do przecenienia, ponieważ pozwala on na powiązanie mas substancji (mierzonych w gramach) z liczbą reagujących cząstek, co jest absolutnie fundamentalne dla wszelkich obliczeń chemicznych. Dzięki molowi możemy mówić o proporcjach, w jakich substancje reagują ze sobą, niezależnie od ich indywidualnych mas atomowych czy cząsteczkowych.
Na podstawie pojęcia molu i zbilansowanych równań reakcji chemicznych opiera się stechiometria – dział chemii zajmujący się ilościowymi zależnościami między substratami a produktami reakcji. Dzięki zasadom stechiometrii chemicy mogą precyzyjnie ustalić, jaka masa lub objętość jednego związku może przereagować z drugim, aby uzyskać pożądane produkty w optymalnych ilościach. Teoretyczną podstawą tych obliczeń jest prawo zachowania masy oraz koncepcja współczynnika stechiometrycznego, który określa stosunek molowy reagujących substancji. Koncepcja stężenia, rozumianego jako molowy lub procentowy udział związków chemicznych w mieszaninie (np. roztworze), umożliwia z kolei dokonywanie analogicznych obliczeń ilości reagujących substancji, nawet gdy nie są one jednorodne. Bez opanowania molu i stechiometrii, niemożliwe byłoby projektowanie procesów przemysłowych, synteza nowych związków w laboratorium czy nawet precyzyjne dawkowanie leków, co czyni te pojęcia absolutnym fundamentem praktycznej chemii.
Energia w świecie chemii: Trwałość i przebieg reakcji
Nieodłącznym elementem chemii jest zagadnienie energii. Energia odgrywa kluczową rolę zarówno w trwałości związków chemicznych (np. stabilność cząsteczek zależy od energii wiązań), jak i w przebiegu reakcji. Działem chemii zajmującym się tymi zagadnieniami jest chemia fizyczna, która czerpie garściami z termodynamiki i kinetyki. To właśnie dzięki niej rozumiemy, dlaczego niektóre reakcje zachodzą spontanicznie, uwalniając energię (reakcje egzotermiczne), podczas gdy inne wymagają dostarczenia energii (reakcje endotermiczne).
W ramach chemii fizycznej wprowadzono szereg pojęć i wielkości, które służą do opisu zagadnień energetycznych odnoszących się do związków i reakcji chemicznych:
- Entalpia (ΔH): Mierzy ciepło wydzielone lub pochłonięte w reakcji chemicznej przy stałym ciśnieniu. Ujemna entalpia wskazuje na reakcję egzotermiczną (wydzielającą ciepło), dodatnia na endotermiczną (pochłaniającą ciepło).
- Entropia (ΔS): Mierzy stopień nieuporządkowania lub losowości układu. Reakcje często dążą do zwiększenia entropii, co jest jednym z czynników wpływających na ich spontaniczność.
- Energia swobodna Gibbsa (ΔG): Jest kluczową wielkością termodynamiczną, która pozwala przewidzieć spontaniczność reakcji chemicznej w danych warunkach temperatury i ciśnienia. Reakcja jest spontaniczna, jeśli ΔG jest ujemne. Łączy w sobie aspekt entalpii i entropii.
- Energia aktywacji: Minimalna energia, którą muszą posiadać cząsteczki substratów, aby doszło do efektywnego zderzenia i zapoczątkowania reakcji chemicznej. Jest to bariera energetyczna, którą należy pokonać. Katalizatory działają poprzez obniżanie energii aktywacji.
Zrozumienie energetycznych aspektów reakcji jest niezbędne do kontrolowania procesów chemicznych, np. w produkcji paliw, materiałów wybuchowych, w projektowaniu baterii i ogniw paliwowych, a także w zrozumieniu efektywności energetycznej procesów metabolicznych w organizmach żywych. Chemia, bez uwzględnienia energii, byłaby jedynie statycznym opisem substancji, a nie dynamiczną nauką o ich przemianach i ich praktycznym wykorzystaniu.

Chemia eksperymentalna i jej korzenie
Współczesna chemia jest przede wszystkim nauką eksperymentalną, całkowicie pozbawioną magiczno-mistycznej otoczki typowej dla alchemii. Jej podstawę faktograficzną stanowią reakcje chemiczne przeprowadzane w kontrolowanych warunkach w laboratoriach, z użyciem specjalistycznej aparatury oraz wyniki dokładnych badań produktów tych reakcji. To właśnie dzięki precyzyjnym eksperymentom, naukowcy są w stanie odkrywać nowe związki, badać ich właściwości i mechanizmy reakcji. Ten empiryczny charakter odróżnia ją od jej historycznego poprzednika – alchemii.
Początki chemii sięgają starożytności, kiedy to z ogólnych rozważań filozoficznych wyłoniła się alchemia, której przedstawiciele działali jeszcze na początku XIX wieku. Przez wieki alchemicy poszukiwali kamienia filozoficznego (substancji zdolnej do transmutacji metali nieszlachetnych w złoto) i eliksiru życia, często opierając się na mistycznych wierzeniach, astrologii i symbolice. Jednak ich praktyczne eksperymenty, choć prowadzone w celu osiągnięcia nierealnych celów, położyły podwaliny pod rozwój technik laboratoryjnych (np. destylacji, sublimacji), metod oczyszczania substancji i obserwacji chemicznych. Przełom nastąpił wraz z odejściem od magiczno-mistycznej otoczki i przyjęciem metody naukowej, co zapoczątkowało erę współczesnej chemii, której podstawą jest eksperyment, obiektywna analiza danych i logiczne wnioskowanie, a nie spekulacje czy dogmaty. Kluczowe było również wprowadzenie precyzyjnego języka i symboliki chemicznej, która zastąpiła ezoteryczne opisy alchemików.
Dlaczego chemia jest kluczowa dla przyszłości?
Podsumowując, co jest najważniejsze w chemii? To kompleksowe zrozumienie wzajemnych zależności między budową materii (na poziomie atomów i cząsteczek), jej właściwościami, a przede wszystkim jej zdolnością do przemian. Kluczowe są pojęcia takie jak atom, cząsteczka, wiązania chemiczne, pierwiastek, związek chemiczny, reakcja chemiczna oraz ilościowe narzędzia, jak mol i stechiometria, a także zrozumienie roli energii. To one stanowią szkielet, na którym opiera się cała wiedza chemiczna i umożliwiają jej praktyczne zastosowanie.
Znaczenie chemii wykracza daleko poza mury laboratoriów. Jest ona siłą napędową innowacji w niezliczonych dziedzinach, wpływając bezpośrednio na jakość naszego życia i zdolność do rozwiązywania globalnych wyzwań:
- Medycyna i farmacja: Chemia jest podstawą projektowania i syntezy nowych leków, od antybiotyków po terapie przeciwnowotworowe. Umożliwia diagnostykę chorób na poziomie molekularnym i zrozumienie złożonych procesów metabolicznych w organizmach żywych.
- Materiały: Tworzenie nowych stopów, polimerów, ceramiki, kompozytów i nanomateriałów o specyficznych właściwościach (np. wytrzymałość, lekkość, przewodnictwo), niezbędnych w budownictwie, elektronice, przemyśle motoryzacyjnym, lotniczym czy opakowaniowym.
- Energetyka: Rozwój odnawialnych źródeł energii (np. ogniwa fotowoltaiczne, ogniwa paliwowe), efektywniejszych baterii do pojazdów elektrycznych i magazynowania energii, a także optymalizacja procesów spalania paliw kopalnych.
- Ochrona środowiska: Monitorowanie zanieczyszczeń w wodzie, powietrzu i glebie, opracowywanie technologii oczyszczania ścieków i emisji przemysłowych, rozwój metod recyklingu i utylizacji odpadów, tworzenie biodegradowalnych materiałów.
- Rolnictwo i żywność: Opracowywanie nawozów, pestycydów i herbicydów zwiększających plony, rozwój metod konserwacji żywności, badanie wartości odżywczej produktów i bezpieczeństwa żywności.
- Technologia informacyjna: Rozwój materiałów półprzewodnikowych, ciekłych kryształów do wyświetlaczy, nowych nośników danych.
Bez chemii niemożliwe byłoby zrozumienie struktury świata, w którym żyjemy, ani projektowanie rozwiązań dla współczesnych i przyszłych wyzwań, takich jak zmiany klimatyczne, niedobór wody czy nowe pandemie. To nauka, która nieustannie się rozwija, oferując nieskończone możliwości odkrywania i tworzenia, a jej podstawowe pojęcia są kluczem do odblokowania tych możliwości.
Najczęściej zadawane pytania (FAQ)
- Czym różni się chemia od fizyki?
- Choć obie badają materię i wzajemnie się przenikają, chemia skupia się przede wszystkim na składzie, strukturze i przemianach substancji, czyli na tym, jak atomy łączą się i rozdzielają, tworząc nowe związki. Bada zachowanie elektronów, które odpowiadają za wiązania chemiczne. Fizyka natomiast bada podstawowe prawa wszechświata, energię, siły i ruch, często na poziomie subatomowym, kosmicznym lub makroskopowym, nie wnikając w skład chemiczny substancji, chyba że jest to fizyka jądrowa lub fizyka materii skondensowanej, gdzie granice te się zacierają.
- Dlaczego chemia jest nauką eksperymentalną?
- Współczesna chemia opiera się na obserwacji i weryfikacji hipotez poprzez kontrolowane eksperymenty laboratoryjne. To właśnie dzięki precyzyjnym pomiarom i doświadczeniom naukowcy są w stanie odkrywać nowe substancje (jak te 4000 dziennie), badać ich właściwości, określać ich skład i potwierdzać mechanizmy reakcji. Eksperymenty pozwalają na zbieranie faktów, które następnie są uogólniane w teorie i prawa, co odróżnia chemię od jej alchemicznych korzeni, gdzie dominowały spekulacje i mistyczne wierzenia.
- Co to jest mol i dlaczego jest ważny?
- Mol to podstawowa jednostka liczności materii w układzie SI. Definiuje on określoną liczbę cząstek (atomów, cząsteczek, jonów) – dokładnie 6,02214076 × 1023, czyli liczbę Avogadra. Jest kluczowy, ponieważ pozwala przeliczać masy substancji (łatwo mierzalne w laboratorium) na liczbę reagujących cząstek. To jest niezbędne do precyzyjnych obliczeń stechiometrycznych w reakcjach chemicznych, co umożliwia kontrolowanie ilości produktów i substratów w syntezie związków oraz w procesach przemysłowych.
- Jakie są podstawowe pojęcia chemii?
- Do podstawowych pojęć chemii należą: atom (podstawowa jednostka materii, z jądrem i chmurą elektronową), cząsteczka (zbiór atomów połączonych wiązaniami), wiązanie chemiczne (siła łącząca atomy), pierwiastek chemiczny (substancja złożona z atomów o tej samej liczbie protonów), związek chemiczny (substancja złożona z dwóch lub więcej pierwiastków połączonych chemicznie), reakcja chemiczna (proces przemiany substancji), mol (jednostka liczności materii) oraz energia (wpływająca na trwałość związków i przebieg reakcji).
- Czy chemia ma zastosowanie w życiu codziennym?
- Absolutnie! Chemia jest wszechobecna i fundamentalna dla wielu aspektów naszego codziennego życia. Od składu żywności, którą jemy (makroskładniki, witaminy, konserwanty), przez detergenty, którymi sprzątamy (działanie powierzchniowo czynne), leki, które przyjmujemy (mechanizmy działania na poziomie molekularnym), po materiały, z których zbudowane są nasze domy i telefony (polimery, metale, półprzewodniki). Zrozumienie chemii pozwala lepiej świadomie korzystać z produktów i procesów w codziennym życiu oraz podejmować bardziej świadome decyzje konsumenckie i środowiskowe.
| Typ materii | Definicja | Przykłady | Metody rozdzielania |
|---|---|---|---|
| Pierwiastek chemiczny | Substancja, której nie da się rozłożyć chemicznie na prostsze składniki; składa się z atomów o tej samej liczbie protonów w jądrze. | Tlen (O2), Żelazo (Fe), Złoto (Au), Wodór (H2) | Nierozdzielny chemicznie (możliwa transmutacja jądrowa, ale to domena fizyki) |
| Związek chemiczny | Substancja złożona z dwóch lub więcej pierwiastków połączonych chemicznie w stałych proporcjach, tworząca nowe właściwości. | Woda (H2O), Dwutlenek węgla (CO2), Sól kuchenna (NaCl), Sacharoza (C12H22O11) | Rozdzielny chemicznie na pierwiastki składowe (np. elektroliza wody) |
| Mieszanina jednorodna | Dwie lub więcej substancji wymieszanych na poziomie molekularnym, nierozróżnialne gołym okiem, o jednolitym składzie. | Roztwór cukru w wodzie, Powietrze, Mosiądz (stop miedzi i cynku), Ocet | Rozdzielna metodami fizycznymi (np. destylacja, krystalizacja, chromatografia) |
| Mieszanina niejednorodna | Dwie lub więcej substancji, których składniki są wyraźnie widoczne i łatwo rozróżnialne, o niejednolitym składzie. | Piasek z wodą, Granit, Sałatka warzywna, Zawiesina kredy w wodzie | Rozdzielna metodami mechanicznymi (np. filtracja, dekantacja, segregacja ręczna) |
Zainteresował Cię artykuł Co najważniejsze w chemii?? Zajrzyj też do kategorii Nauka, znajdziesz tam więcej podobnych treści!

