23/02/2019
Stechiometria to jeden z filarów chemii, często postrzegany jako skomplikowany i zniechęcający. Jednakże, zrozumienie jej zasad jest absolutnie kluczowe do opanowania chemii na głębszym poziomie, zarówno w szkole średniej, jak i na studiach. To właśnie stechiometria pozwala nam przewidzieć, ile substancji potrzebujemy do przeprowadzenia danej reakcji chemicznej i ile produktów z niej powstanie. Bez niej chemia byłaby jedynie zbiorem abstrakcyjnych faktów, a nie nauką o precyzyjnych przemianach materii. W tym artykule rozłożymy stechiometrię na czynniki pierwsze, wyjaśniając jej podstawowe pojęcia i pokazując, jak poradzić sobie z najczęstszymi wyzwaniami.

Czym są obliczenia stechiometryczne i dlaczego są tak ważne?
W swej istocie, obliczenia stechiometryczne polegają na ilościowym opisie reakcji chemicznych. Dzięki nim możemy dokładnie określić, ile reagentów (substratów) jest potrzebnych do przeprowadzenia reakcji chemicznej, a także ile produktów powstanie w wyniku tej reakcji. Jest to możliwe dzięki zasadzie zachowania masy oraz znajomości równań chemicznych, które opisują proporcje, w jakich cząsteczki reagują ze sobą. Wyobraź sobie, że pieczesz ciasto – musisz wiedzieć, ile mąki, jajek i cukru użyć, aby uzyskać pożądaną liczbę porcji. W chemii stechiometria pełni podobną rolę, zapewniając, że nie marnujemy surowców i uzyskujemy oczekiwane ilości produktów. Bez precyzyjnych obliczeń stechiometrycznych niemożliwe byłoby prowadzenie badań naukowych, produkcja leków, tworzyw sztucznych czy nawozów.
Dlaczego stechiometria bywa postrzegana jako trudna?
Stechiometria często sprawia trudności uczniom, ponieważ jest to dziedzina, która wymaga połączenia wielu indywidualnych umiejętności. Aby odnieść sukces, należy opanować szereg podstawowych zagadnień i nauczyć się planować strategię rozwiązywania problemów. Trudność nie wynika z samej matematyki – ta jest zazwyczaj prosta, jeśli potrafisz ją zwizualizować i zaplanować. Kluczem jest zrozumienie podstawowych koncepcji i ich wzajemnych powiązań. Wiele osób czuje się przytłoczonych mnogością wzorów i definicji, a także koniecznością myślenia analitycznego i logicznego. Brak solidnych fundamentów w takich obszarach jak pojęcie mola, równania chemiczne czy przeliczanie jednostek, może prowadzić do frustracji i poczucia, że stechiometria jest nie do opanowania. Jednak z odpowiednim podejściem i systematyczną pracą, każdy jest w stanie ją zrozumieć.
Stechiometria w programie nauczania: Kiedy się z nią spotykamy?
W wielu systemach edukacji, w tym w kanadyjskim programie nauczania szkół średnich, uczniowie po raz pierwszy spotykają się z tematem stechiometrii w klasie 11. Na tym etapie wprowadza się koncepcję mola i jej związek z ilościowymi aspektami reakcji chemicznych. Oczekuje się, że uczniowie będą stosować wiedzę o równaniach chemicznych i teorii molowej, wraz z różnymi koncepcjami matematycznymi, do określania reagentów ograniczających, wydajności teoretycznych i wydajności eksperymentalnych. To właśnie wtedy edukatorzy często uświadamiają uczniom, że „jeden plus jeden niekoniecznie daje dwa” w kontekście chemii, co dla wielu jest nowością i wyzwaniem. Jest to złożony temat, dlatego nic dziwnego, że wielu uczniów początkowo uważa go za trudny. Nierzadko zdarza się, że w klasie 12, a nawet na pierwszym roku studiów, studenci zapominają wiele aspektów stechiometrii. Problemy pojawiają się np. przy obliczaniu moli substratów w stanie ciekłym lub w reakcjach, które nie wykazują stosunków stechiometrycznych 1:1. Sugeruje to, że powtórne przećwiczenie koncepcji stechiometrii w klasie 12 byłoby bardzo korzystne, aby utrwalić tę kluczową wiedzę.
Podstawowe pojęcia stechiometrii – nie taka straszna, jak ją wyliczają
Aby oswoić się ze stechiometrią, warto najpierw zrozumieć jej fundamentalne elementy. Oto najważniejsze z nich:
Mol: To podstawowa jednostka ilości substancji w chemii. Mol jest niczym „chemiczny tuzin” – reprezentuje określoną liczbę cząstek (atomów, cząsteczek, jonów). Ta liczba to stała Avogadra, wynosząca około 6,022 x 10^23. Jak łatwo to zapamiętać? Pomyśl o liczbie 12. Tak jak tuzin to 12 sztuk, tak mol to ogromna liczba cząstek. Zrozumienie mola jest absolutnie kluczowe dla wszystkich obliczeń stechiometrycznych. Bez niego ani rusz!
Masa molowa (M): Jest to masa jednego mola danej substancji, wyrażona w gramach na mol (g/mol). Numerycznie jest równa masie atomowej (dla pierwiastków) lub masie cząsteczkowej (dla związków), ale wyrażona w innych jednostkach. Na przykład, masa molowa wody (H₂O) wynosi około 18 g/mol, co oznacza, że jeden mol wody waży 18 gramów.
Stężenie molowe (Cm): Określa liczbę moli substancji rozpuszczonej w jednym decymetrze sześciennym (litrze) roztworu. Wyraża się je w molach na decymetr sześcienny (mol/dm³). Jest to niezbędne w obliczeniach dotyczących roztworów chemicznych.
Objętość molowa gazów (Vm): W warunkach normalnych (0°C i 1 atmosfera ciśnienia) jeden mol dowolnego gazu zajmuje objętość około 22,4 dm³. Ta wartość jest niezwykle przydatna w obliczeniach dotyczących reakcji z udziałem gazów.
Stechiometria związków chemicznych (wzór empiryczny i wzór rzeczywisty): Stechiometria pozwala również na określanie składu związków chemicznych. Wzór empiryczny (minimalny) przedstawia najprostszy stosunek liczby atomów pierwiastków w związku, natomiast wzór rzeczywisty (sumaryczny) podaje faktyczną liczbę atomów w cząsteczce. Obliczenia stechiometryczne są niezbędne do ich ustalenia na podstawie danych eksperymentalnych.
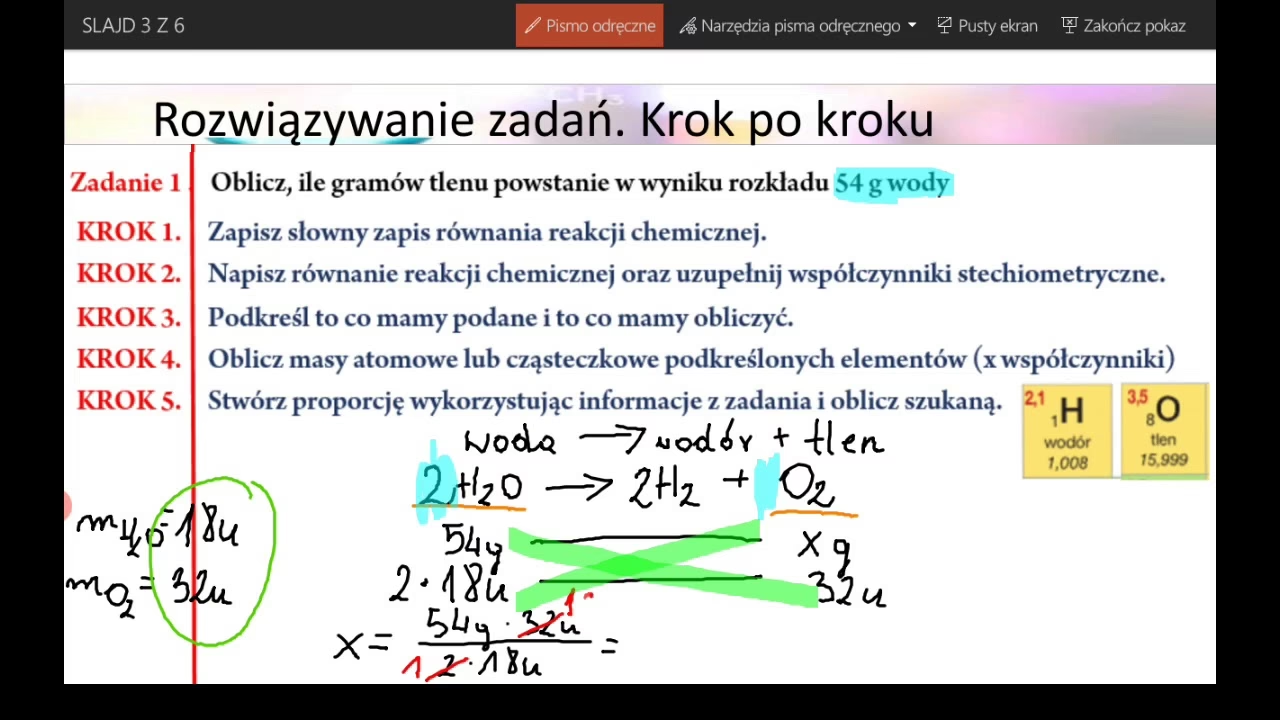
Stechiometria równań reakcji: To serce stechiometrii. Zbilansowane równanie chemiczne dostarcza informacji o proporcjach molowych, masowych i objętościowych (dla gazów) reagentów i produktów. Na przykład, w reakcji 2H₂ + O₂ → 2H₂O, widzimy, że 2 mole wodoru reagują z 1 molem tlenu, tworząc 2 mole wody.
Reagenty (substraty i produkty): Substraty to substancje, które reagują ze sobą, a produkty to substancje, które powstają w wyniku reakcji. W kontekście stechiometrii często mówimy o reagencie ograniczającym, czyli tym, który zużywa się jako pierwszy i ogranicza ilość powstającego produktu, oraz o reagencie w nadmiarze.

Prawo zachowania masy: Jedna z fundamentalnych zasad chemii, mówiąca, że w układzie zamkniętym masa wszystkich substratów zużytych w reakcji jest równa masie wszystkich produktów. Oznacza to, że w reakcjach chemicznych atomy nie znikają ani nie pojawiają się znikąd – jedynie zmieniają swoje połączenia.
Znaczenie zmieszania substratów w stosunku stechiometrycznym: Kiedy substraty są zmieszane w stosunku stechiometrycznym, oznacza to, że wszystkie reagenty zostaną zużyte w całości, a żaden z nich nie pozostanie w nadmiarze. To idealna sytuacja w laboratorium i przemyśle, pozwalająca na maksymalne wykorzystanie surowców.
Wydajność reakcji: To stosunek masy produktu faktycznie otrzymanego w eksperymencie (wydajność rzeczywista) do masy produktu, którą teoretycznie można by uzyskać (wydajność teoretyczna), wyrażony w procentach. Wydajność reakcji nigdy nie wynosi 100% ze względu na różne czynniki, takie jak niekompletność reakcji, reakcje uboczne czy straty podczas izolacji produktu. Pojęcie to ma związek z teorią zdarzeń aktywnych, która mówi o tym, że nie wszystkie zderzenia cząsteczek prowadzą do efektywnej reakcji.
Ułamek masowy, ułamek objętościowy i ułamek molowy: Te pojęcia służą do wyrażania składu mieszanin i roztworów. Ułamek masowy to stosunek masy składnika do masy całej mieszaniny, ułamek objętościowy – objętości składnika do objętości całej mieszaniny (dla gazów lub cieczy), a ułamek molowy – liczby moli składnika do całkowitej liczby moli w mieszaninie.

Jak skutecznie uczyć się stechiometrii?
Kluczem do opanowania stechiometrii jest systematyczna praktyka i zrozumienie krok po kroku. Oto kilka wskazówek:
- Opanuj podstawy: Upewnij się, że doskonale rozumiesz pojęcia takie jak mol, masa molowa, stężenie molowe i objętość molowa gazów. To fundamenty, na których buduje się cała reszta.
- Równania chemiczne: Naucz się bilansować równania chemiczne. Bez poprawnie zbilansowanego równania, wszystkie dalsze obliczenia będą błędne.
- Strategia rozwiązywania zadań: Rozkładaj złożone problemy na mniejsze, łatwiejsze do zarządzania etapy. Zawsze zaczynaj od zapisania danych i szukanych, a następnie planuj kolejne kroki.
- Wizualizacja: Spróbuj wizualizować, co dzieje się na poziomie atomowym i molekularnym podczas reakcji. To pomaga w intuicyjnym zrozumieniu proporcji.
- Ćwicz, ćwicz, ćwicz: Nie ma drogi na skróty. Rozwiązuj jak najwięcej zadań, od najprostszych do najbardziej złożonych. Powyżej 100 zadań z różnych podrozdziałów stechiometrii to doskonały sposób na nabranie pewności.
- Analizuj błędy: Nie zniechęcaj się błędami. Każdy błąd to okazja do nauki. Zastanów się, gdzie popełniłeś pomyłkę i dlaczego.
Przykładowe kroki w rozwiązywaniu zadania stechiometrycznego:
Poniżej przedstawiono ogólny schemat, który możesz zastosować do większości zadań stechiometrycznych:
| Krok | Opis | Przykład (reakcja: N₂ + 3H₂ → 2NH₃) |
|---|---|---|
| 1. Zapisz i zbilansuj równanie reakcji | Upewnij się, że równanie jest poprawne i zbilansowane pod względem atomów. | N₂ + 3H₂ → 2NH₃ (już zbilansowane) |
| 2. Określ dane i szukane | Wypisz wszystkie podane wartości (masy, objętości, stężenia) i to, co musisz obliczyć. | Dane: 28 g N₂, Szukane: masa NH₃ |
| 3. Przelicz dane na mole | Jeśli dane są w gramach, objętościach lub innych jednostkach, przelicz je na mole, używając mas molowych, objętości molowych lub stężeń molowych. | M(N₂) = 28 g/mol; 28 g N₂ = 1 mol N₂ |
| 4. Użyj stosunków molowych z równania | Na podstawie zbilansowanego równania określ stosunek molowy między danymi a szukanymi substancjami. | Z równania: 1 mol N₂: 2 mole NH₃ |
| 5. Oblicz mole szukanej substancji | Wykorzystaj proporcję molową do obliczenia liczby moli szukanej substancji. | 1 mol N₂ daje 2 mole NH₃. Więc 1 mol N₂ daje 2 mole NH₃. |
| 6. Przelicz mole na wymagane jednostki | Jeśli wynik ma być w gramach, objętościach itp., przelicz mole z powrotem na te jednostki. | M(NH₃) = 17 g/mol; 2 mole NH₃ = 2 * 17 g = 34 g NH₃ |
Często zadawane pytania (FAQ)
Na czym polegają obliczenia stechiometryczne?
Obliczenia stechiometryczne pozwalają na dokładne określenie ilości reagentów potrzebnych do przeprowadzenia reakcji chemicznej oraz ilości produktów powstających w wyniku tej reakcji, bazując na zbilansowanych równaniach chemicznych i prawie zachowania masy.
Dlaczego stechiometria jest tak trudna?
Stechiometria jest trudna, ponieważ wymaga połączenia wielu indywidualnych umiejętności, takich jak zrozumienie pojęcia mola, bilansowanie równań, przeliczanie jednostek i umiejętność logicznego planowania strategii rozwiązywania problemów. Trudność leży w synchronizacji tych umiejętności, a nie w skomplikowanej matematyce.
Czy stechiometria jest w klasie 11?
Tak, w wielu programach nauczania, np. w kanadyjskim programie szkół średnich, stechiometria jest wprowadzana w klasie 11. Uczniowie poznają wtedy koncepcję mola oraz jej zastosowanie w ilościowych aspektach reakcji chemicznych, w tym obliczanie reagentów ograniczających i wydajności.
Czy stechiometria jest trudna do opanowania?
Stechiometria może wydawać się trudna na początku, ale nie jest niemożliwa do opanowania. Z odpowiednim podejściem, systematyczną nauką i regularnym rozwiązywaniem zadań, staje się znacznie prostsza. Kluczem jest zrozumienie podstaw, takich jak mol, masa molowa i prawo zachowania masy, oraz cierpliwe ćwiczenie. Wielu uczniów, którzy początkowo mieli z nią problemy, z czasem osiąga mistrzostwo, co otwiera im drogę do studiów medycznych, farmaceutycznych czy stomatologicznych.
Podsumowanie
Stechiometria to bez wątpienia jeden z najważniejszych i najbardziej praktycznych działów chemii. Choć początkowo może wydawać się skomplikowana, jej opanowanie otwiera drzwi do głębszego zrozumienia procesów chemicznych i pozwala na precyzyjne przewidywanie wyników reakcji. Pamiętaj, że kluczem do sukcesu jest solidne opanowanie podstawowych pojęć, takich jak mol i prawo zachowania masy, oraz nieustanne ćwiczenie. Rozbijaj zadania na mniejsze etapy, analizuj swoje błędy i nie bój się prosić o pomoc. Z czasem zobaczysz, że obliczenia stechiometryczne staną się dla Ciebie intuicyjne, a chemia przestanie być źródłem stresu, a stanie się fascynującą dziedziną wiedzy. Powodzenia w nauce!
Zainteresował Cię artykuł Stechiometria: Opanuj Klucz do Chemii!? Zajrzyj też do kategorii Chemia, znajdziesz tam więcej podobnych treści!

