14/03/2023
W sercu materii, na poziomie atomowym, dzieją się procesy, które choć niewidzialne dla ludzkiego oka, mają fundamentalne znaczenie dla naszego świata. Jednym z najbardziej intrygujących i kluczowych zjawisk jest rozpad promieniotwórczy. To właśnie on leży u podstaw wielu technologii, od medycyny po energetykę, a także pozwala nam zaglądać w przeszłość Ziemi i Wszechświata. Centralnym pojęciem w zrozumieniu tego procesu jest czas połowicznego rozpadu – parametr, który charakteryzuje, jak szybko niestabilne atomy transformują się w inne. Ale czym dokładnie jest ten czas? Dlaczego jest tak ważny i jak różni się dla poszczególnych pierwiastków? Zapraszamy do zgłębienia tajemnic tego niezwykłego zjawiska.
Czym jest Czas Połowicznego Rozpadu? Definicja i Podstawy
Czas połowicznego rozpadu, znany również jako okres półrozpadu, okres połowicznego zaniku, czy po angielsku half-life (często oznaczany jako t1/2 lub T1/2), to fundamentalna wielkość fizyczna opisująca szybkość rozpadu promieniotwórczego. Mówiąc najprościej, jest to czas, po którym połowa początkowej liczby jąder atomów danego izotopu promieniotwórczego ulegnie rozpadowi. Oznacza to, że jeśli masz próbkę zawierającą milion atomów promieniotwórczych, po upływie jednego okresu półrozpadu pozostanie ich pięćset tysięcy. Po kolejnym okresie – dwieście pięćdziesiąt tysięcy i tak dalej.
Warto podkreślić, że rozpad promieniotwórczy ma charakter statystyczny. Nie możemy przewidzieć, kiedy konkretny atom ulegnie rozpadowi, ale możemy precyzyjnie określić, ile atomów rozpadnie się w danej próbce w określonym czasie. Szybkość tego procesu jest unikalna dla każdego izotopu i zależy od tzw. stałej rozpadu. Co niezwykle istotne, czas połowicznego rozpadu danego jądra atomowego jest niezależny od warunków zewnętrznych. Oznacza to, że ani temperatura, ani ciśnienie, ani stan skupienia, ani nawet obecność atomu w cząsteczce związku chemicznego nie mają wpływu na szybkość jego rozpadu. Jest to cecha wewnętrzna samego jądra atomowego, co czyni go niezawodnym "zegarem" w wielu zastosowaniach naukowych i technicznych.
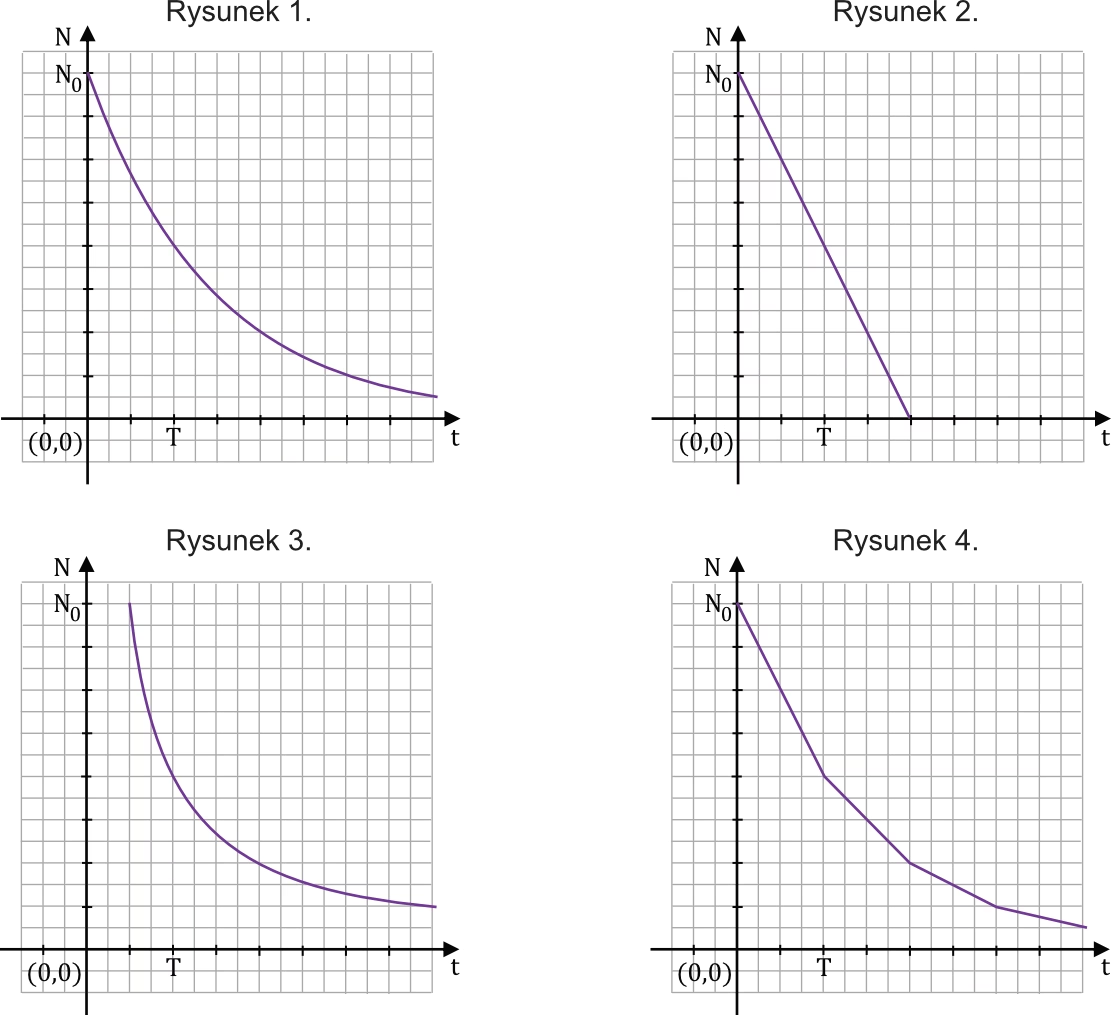
Matematycznie, liczba obiektów N (jąder atomowych, cząstek elementarnych, atomów, cząsteczek w stanach wzbudzonych) zmienia się z upływem czasu t zgodnie z zależnością:
N(t) = N0 ⋅ (1/2)t/T1/2
Gdzie:
N(t)to liczba obiektów w czasie t.N0to początkowa liczba obiektów w chwili t = 0.T1/2to czas połowicznego rozpadu.
Z tego wzoru wynika, że po czasie równym jednemu T1/2, czyli gdy t = T1/2, otrzymujemy:
N(T1/2) = N0 ⋅ (1/2)T1/2/T1/2 = N0 ⋅ (1/2)1 = N0 ⋅ 1/2
Co potwierdza definicję – po upływie czasu połowicznego rozpadu pozostaje połowa początkowej liczby jąder. Warto również pamiętać, że po upływie każdego kolejnego okresu półrozpadu, aktywność promieniotwórcza próbki również zmniejsza się o połowę.
Różnorodność Czasów Połowicznego Rozpadu: Od Milisekund do Miliardów Lat
Spektrum czasów połowicznego rozpadu jest niezwykle szerokie, obejmując zakres od ułamków milisekund do miliardów lat. Ta ogromna rozpiętość sprawia, że izotopy promieniotwórcze znajdują zastosowanie w bardzo różnych dziedzinach, a ich właściwości są kluczowe dla zrozumienia stabilności materii. Najcięższe, syntetyczne pierwiastki transuranowe często charakteryzują się ekstremalnie krótkimi czasami półrozpadu, co sprawia, że są trudne do badania i istnieją tylko przez chwilę. Z drugiej strony, niektóre pierwiastki mają tak długi czas półrozpadu, że w praktyce uznaje się je za trwałe, choć teoretycznie ulegają bardzo powolnemu rozpadowi.
Poniżej przedstawiamy przykłady najczęściej spotykanych izotopów i ich czasów połowicznego rozpadu, wraz z krótkim opisem ich występowania lub zastosowań. Ta tabela pokazuje, jak różnorodne są te pierwiastki i jak wszechstronne są ich role w naturze i technologii:
| Izotop | Czas Połowicznego Rozpadu (T1/2) | Uwagi i Zastosowania |
|---|---|---|
| Bizmut Bi-214 | 20 minut | Powstaje w atmosferze jako produkt rozpadu radonu-222. Krótki czas życia. |
| Itr Y-90 | 64.4 godziny | Produkt rozpadu strontu-90. Stosowany w medycynie, np. w radioterapii. |
| Radon Rn-222 | 3.82 dnia | Występuje w piwnicach, kopalniach, wydzielany przy rozpadzie radu-226. Gaz szlachetny, zagrożenie dla zdrowia. |
| Jod I-131 | 8 dni | Stosowany w diagnostyce izotopowej i radioterapii (tarczyca). Skażenie po wybuchach nuklearnych. |
| Iryd Ir-192 | 74 dni | Wykorzystywany w defektoskopii przemysłowej do badania materiałów. |
| Polon Po-210 | 138 dni | Obecny w dymie papierosowym, antystatycznych szczoteczkach do winyli, szkolnych spintaryskopach. Toksyczny. |
| Kobalt Co-60 | 5.7 lat | Źródła kontrolne, czujniki przemysłowe, naświetlania medyczne (radioterapia nowotworów). |
| Tryt H-3 | 12.33 lat | Współczesne świecące zegarki, kompasy i celowniki do broni wojskowej (bezpieczne źródło światła). |
| Stront Sr-90 | 28 lat | Lotnicze czujniki oblodzenia, źródła kalibracyjne. Groźne skażenie po wybuchach nuklearnych, gromadzi się w kościach. |
| Cez Cs-137 | 30 lat | Odgromniki iskrowe, źródła kalibracyjne. Skażenie po wybuchach nuklearnych, gromadzi się w mięśniach. |
| Ameryk Am-241 | 432.2 lat | Główny składnik jonizacyjnych czujek dymu. |
| Rad Ra-226 | 1599 lat | Stare świecące zegarki, kompasy i wskaźniki lotnicze, igły do brachyterapii. |
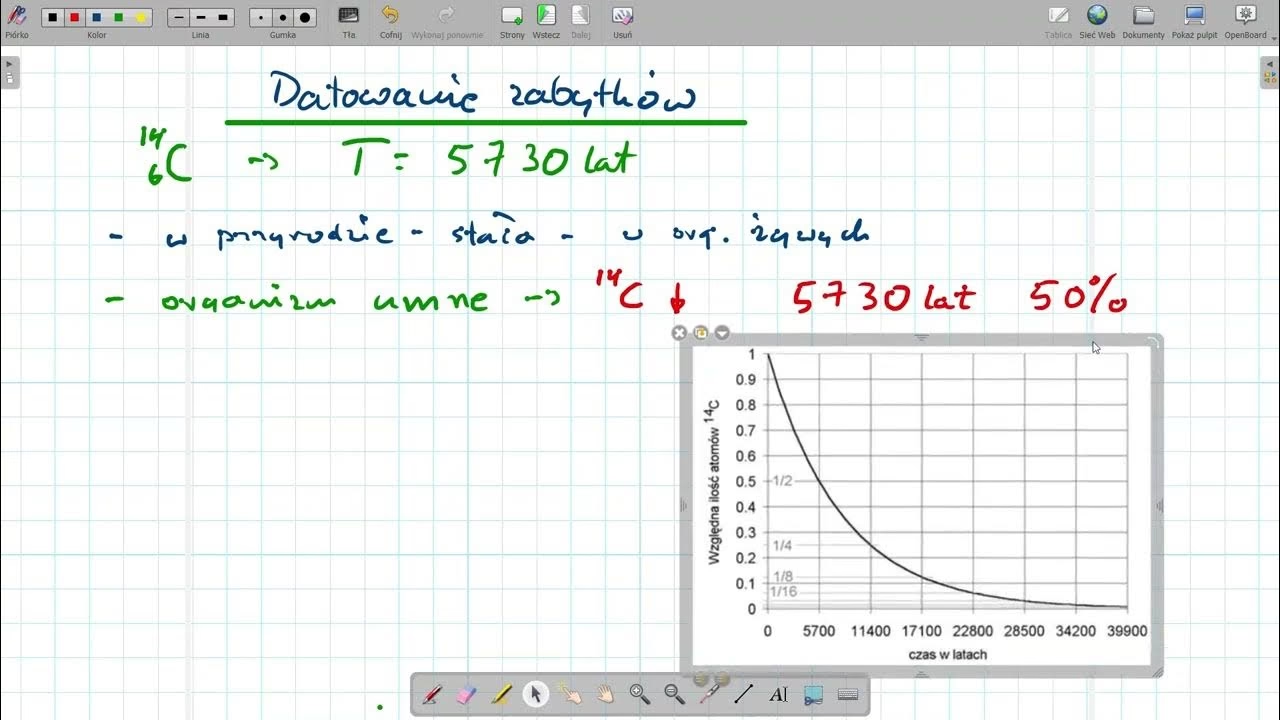
| Węgiel C-14 | 5730 lat | Powstaje w atmosferze pod wpływem promieniowania kosmicznego. Kluczowy w datowaniu radiowęglowym. |
| Pluton Pu-239 | 24 tys. lat | Materiał rozszczepialny w bombach jądrowych i reaktorach. Stare czujki dymu, generatory termoelektryczne. |
| Uran U-235 | 700 mln lat | Paliwo jądrowe w reaktorach atomowych. |
| Potas K-40 | 1.2 mld lat | Obecny we wszystkich związkach potasu (nawozy, żywność). Naturalnie występujący izotop promieniotwórczy. |
| Uran U-238 | 4.5 mld lat | Dominujący izotop uranu naturalnego. Stosowany w szkle i ceramice uranowej. |
| Tor Th-232 | 14 mld lat | Siatki żarowe do lamp gazowych, elektrody spawalnicze, obiektywy fotograficzne, "zdrowotne" medaliony Quantum Pendant. |
Fizyczny vs. Biologiczny Czas Półtrwania
Oprócz fizycznego czasu połowicznego rozpadu, który jest niezmienny i niezależny od warunków zewnętrznych, istnieje także pojęcie biologicznego czasu półtrwania. Ten drugi termin odnosi się do szybkości, z jaką dana substancja (w tym izotop promieniotwórczy) jest wydalana z organizmu żywego. Biologiczny czas półtrwania jest kluczowy w medycynie i toksykologii, ponieważ określa, jak długo substancja pozostaje aktywna w ciele i potencjalnie szkodliwa.
Przykładem różnicy między tymi dwoma pojęciami jest cez-137 i stront-90. Obie są produktami rozszczepienia jądrowego i mogą stanowić poważne zagrożenie po katastrofach nuklearnych. Fizyczny czas połowicznego rozpadu cezu-137 wynosi około 30 lat, a strontu-90 około 28 lat – są więc zbliżone. Jednak ich biologiczne czasy półtrwania znacząco się różnią. Cez-137 ma powinowactwo do potasu i gromadzi się głównie w mięśniach. Z mięśni jest stosunkowo szybko wypłukiwany z organizmu, co oznacza krótszy biologiczny czas półtrwania. Z kolei stront-90, mający powinowactwo do wapnia, jest wbudowywany w kości. Z kości jest wydalany znacznie wolniej, co skutkuje dłuższym biologicznym czasem półtrwania i większym zagrożeniem dla organizmu, ponieważ dłużej naświetla szpik kostny i tkanki kostne.
Reguła "10 Okresów Półrozpadu"
W praktyce, zwłaszcza w kontekście bezpieczeństwa radiologicznego i utylizacji odpadów promieniotwórczych, przyjęło się, że po upływie około 10 okresów połowicznego rozpadu można uznać, że cały izotop uległ rozpadowi do poziomu, który jest praktycznie nieistotny. Po 10 okresach półrozpadu zawartość pierwotnego izotopu spadnie do zaledwie 0,097% początkowej wartości. Jest to bardzo niewielka ilość, często poniżej progu wykrywalności lub bezpieczna dla środowiska. Sprawdźmy to na przykładzie izotopów z naszej tabeli. Dla bizmutu Bi-214, którego T1/2 wynosi 20 minut, po 10 okresach (czyli po 200 minutach, czyli 3 godzinach i 20 minutach) jego ilość spadnie do poniżej 0,1%. Dla cezu Cs-137 (T1/2 = 30 lat), "bezpieczny" czas to 300 lat. A dla uranu U-238 (T1/2 = 4.5 mld lat), jest to niewyobrażalne 45 miliardów lat – znacznie dłużej niż wiek Wszechświata!
Praktyczne Zastosowania i Znaczenie
Zrozumienie i wykorzystanie czasu połowicznego rozpadu ma ogromne znaczenie w wielu dziedzinach. Oto kilka kluczowych obszarów:
- Datowanie Radiowęglowe (C-14): Jedno z najbardziej znanych zastosowań. Węgiel-14, powstający w atmosferze pod wpływem promieniowania kosmicznego, jest wbudowywany w organizmy żywe. Po śmierci organizmu, C-14 przestaje być uzupełniany, a jego ilość stopniowo maleje zgodnie z czasem połowicznego rozpadu (5730 lat). Mierząc pozostałą ilość C-14, naukowcy mogą określić wiek próbek organicznych, takich jak starożytne artefakty, kości czy drewno, datując je na dziesiątki tysięcy lat.
- Medycyna Nuklearna: Izotopy o stosunkowo krótkim czasie połowicznego rozpadu, takie jak jod-131 (8 dni) czy itr-90 (64.4 godziny), są nieocenione w diagnostyce i terapii. Jod-131 jest używany do diagnozowania i leczenia chorób tarczycy, a itr-90 w radioterapii celowanej na nowotwory. Krótki czas rozpadu oznacza, że izotop szybko zanika w organizmie, minimalizując długotrwałe narażenie na promieniowanie.
- Energetyka Jądrowa: Uran-235 (700 mln lat) i pluton-239 (24 tys. lat) są kluczowymi paliwami w reaktorach jądrowych. Ich długie czasy rozpadu, w połączeniu z możliwością wywołania reakcji łańcuchowej, czynią je efektywnymi źródłami energii.
- Przemysł i Bezpieczeństwo: Kobalt-60 (5.7 lat) jest wykorzystywany w sterylizacji medycznej i przemysłowej, a także w defektoskopii do prześwietlania materiałów. Ameryk-241 (432.2 lat) to powszechny składnik jonizacyjnych czujek dymu, gdzie jego alfa-promieniowanie jest wykorzystywane do wykrywania cząstek dymu. Tryt (12.33 lat) jest używany w samozapalających się zegarkach i celownikach, zapewniając bezpieczne i długotrwałe źródło światła.
- Geochronologia: Izotopy o bardzo długim czasie połowicznego rozpadu, takie jak uran-238 (4.5 mld lat), tor-232 (14 mld lat) czy potas-40 (1.2 mld lat), są wykorzystywane do datowania skał i określania wieku Ziemi. Ich rozpad dostarcza informacji o geologicznej historii naszej planety.
Często Zadawane Pytania (FAQ)
Co to jest czas połowicznego rozpadu?
Czas połowicznego rozpadu to czas, po którym połowa początkowej liczby jąder atomów danego izotopu promieniotwórczego ulegnie rozpadowi. Jest to fundamentalna miara szybkości rozpadu promieniotwórczego.

Czy czas połowicznego rozpadu zależy od temperatury lub ciśnienia?
Nie, fizyczny czas połowicznego rozpadu jądra danego izotopu promieniotwórczego jest niezależny od czynników zewnętrznych, takich jak temperatura, ciśnienie, stan skupienia czy obecność atomu w związku chemicznym. Jest to cecha wewnętrzna jądra atomowego.
Jakie są przykłady izotopów o krótkim i długim czasie połowicznego rozpadu?
Przykłady izotopów o krótkim czasie połowicznego rozpadu to Bizmut Bi-214 (20 minut) czy Jod I-131 (8 dni). Izotopy o bardzo długim czasie to np. Uran U-238 (4.5 miliarda lat) czy Tor Th-232 (14 miliardów lat).
Czym różni się fizyczny od biologicznego czasu półtrwania?
Fizyczny czas półtrwania odnosi się do naturalnej szybkości rozpadu jądra atomowego. Biologiczny czas półtrwania to czas, w którym połowa danej substancji jest wydalana z organizmu żywego. Biologiczny czas półtrwania może być krótszy lub dłuższy niż fizyczny, w zależności od metabolizmu organizmu i sposobu, w jaki substancja jest przetwarzana lub magazynowana w ciele.
Ile czasu potrzeba, aby izotop całkowicie się rozpadł?
Teoretycznie, izotop nigdy nie rozpadnie się "całkowicie", ponieważ proces jest asymptotyczny (ilość substancji zbliża się do zera, ale nigdy go nie osiąga). Jednak w praktyce, po około 10 okresach połowicznego rozpadu, ilość pierwotnego izotopu spada do mniej niż 0,1% początkowej wartości, co jest często uznawane za bezpieczny poziom.
Gdzie wykorzystuje się izotopy promieniotwórcze i znajomość ich czasu połowicznego rozpadu?
Izotopy promieniotwórcze są wykorzystywane w wielu dziedzinach, m.in. w medycynie (diagnostyka, radioterapia), energetyce jądrowej (paliwo), przemyśle (sterylizacja, czujki dymu, defektoskopia), a także w nauce (datowanie radiowęglowe, geochronologia) do badania wieku materiałów i Ziemi.
Podsumowanie
Czas połowicznego rozpadu to znacznie więcej niż tylko abstrakcyjna koncepcja fizyczna. To klucz do zrozumienia stabilności materii, potężne narzędzie w rękach naukowców i inżynierów, a także istotny czynnik w ocenie ryzyka radiologicznego. Od datowania starożytnych cywilizacji po nowoczesną medycynę i bezpieczne systemy alarmowe, znajomość i wykorzystanie czasów połowicznego rozpadu izotopów promieniotwórczych odgrywa niezastąpioną rolę w kształtowaniu naszego świata i poszerzaniu naszej wiedzy o nim. Jest to dowód na to, jak subtelne procesy na poziomie atomowym mogą mieć monumentalne konsekwencje dla całej planety i ludzkości.
Zainteresował Cię artykuł Tajemnice Czasu Połowicznego Rozpadu? Zajrzyj też do kategorii Nauka, znajdziesz tam więcej podobnych treści!