03/08/2018
Zrozumienie konfiguracji elektronowej to podstawa w chemii, pozwalająca przewidzieć zachowanie pierwiastków w reakcjach. O ile zapis dla atomów neutralnych jest stosunkowo prosty, o tyle konfiguracja elektronowa jonów, zwłaszcza tych pochodzących od metali przejściowych, może wydawać się bardziej skomplikowana. Ten artykuł rozwieje wszelkie wątpliwości, koncentrując się na konkretnym przykładzie – jonach żelaza Fe2+ i Fe3+ – i wyjaśniając, dlaczego elektrony usuwane są w określonej kolejności.
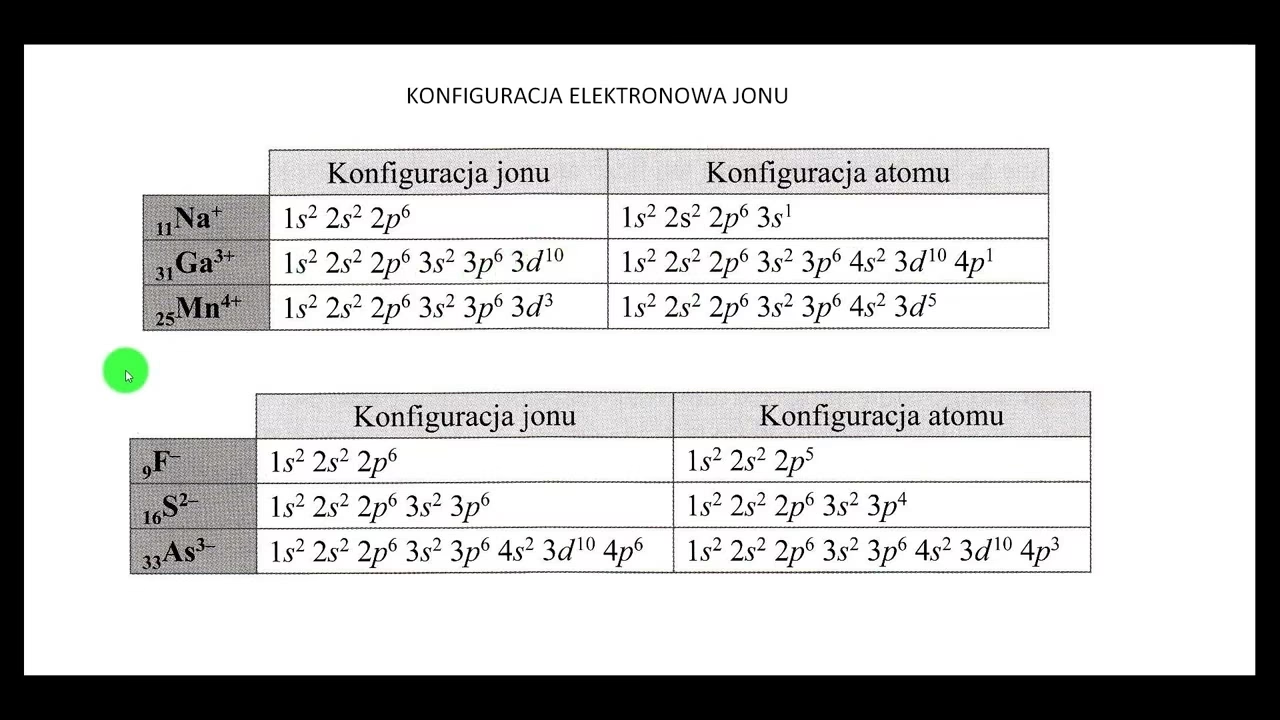
Czym jest Konfiguracja Elektronowa i Dlaczego Jony są Wyjątkowe?
Konfiguracja elektronowa to schemat rozmieszczenia elektronów w orbitalach atomowych wokół jądra atomu. Jest ona unikalna dla każdego pierwiastka i decyduje o jego właściwościach chemicznych. Elektrony zajmujące najbardziej zewnętrzne powłoki, zwane elektronami walencyjnymi, odgrywają kluczową rolę w tworzeniu wiązań chemicznych. To właśnie one są tracone, zyskiwane lub współdzielone, gdy atomy tworzą jony.
Jony to atomy lub grupy atomów, które zyskały lub straciły jeden lub więcej elektronów, uzyskując w ten sposób ładunek elektryczny. Wyróżniamy dwa główne typy jonów:
- Kationy: Jony dodatnie, powstające w wyniku utraty elektronów. Przykładem są jony metali, takie jak Fe2+ i Fe3+.
- Aniony: Jony ujemne, powstające w wyniku przyjęcia elektronów. Przykładem są jony niemetali, takie jak Cl-.
Zapis konfiguracji elektronowej jonów różni się od zapisu dla atomów neutralnych właśnie ze względu na zmienną liczbę elektronów. Kluczową zasadą jest to, że zmiany te dotyczą wyłącznie elektronów walencyjnych, ponieważ to one są najbardziej oddalone od jądra i najsłabiej z nim związane, a przez to najłatwiej dostępne do udziału w reakcjach chemicznych.
Żelazo (Fe): Wprowadzenie do Metalu Przejściowego
Żelazo (symbol Fe, z łacińskiego Ferrum) to pierwiastek chemiczny o liczbie atomowej 26. Jest to metal przejściowy należący do grupy 8. układu okresowego. Żelazo jest niezwykle ważnym pierwiastkiem, będąc najobficiej występującym pierwiastkiem na Ziemi pod względem masy (zaraz po tlenie), stanowiąc dużą część jądra Ziemi. W skorupie ziemskiej jest czwartym co do obfitości pierwiastkiem.
Charakterystyczną cechą żelaza, podobnie jak wielu innych metali przejściowych, jest jego zdolność do tworzenia związków na różnych stopniach utlenienia. Najczęściej spotykane są stopnie utlenienia +2 (żelazo(II), czyli jon żelazawy) i +3 (żelazo(III), czyli jon żelazowy). Rzadziej występują także wyższe stopnie utlenienia, na przykład +6, jak w przypadku żelazianu potasu. Ta zmienność stopni utlenienia jest kluczowa dla jego roli w wielu procesach biologicznych i przemysłowych.
Konfiguracja Elektronowa Atomu Neutralnego Żelaza
Aby zrozumieć konfigurację jonów żelaza, musimy najpierw znać konfigurację atomu neutralnego. Żelazo ma liczbę atomową 26, co oznacza, że neutralny atom żelaza ma 26 protonów i 26 elektronów.
Zgodnie z zasadą Aufbau (regułą zapełniania orbitali od najniższej energii) i regułą Hunda (maksymalizacja liczby elektronów niesparowanych w orbitalach o tej samej energii), pełna konfiguracja elektronowa żelaza wygląda następująco:
1s2 2s2 2p6 3s2 3p6 3d6 4s2
Możemy również użyć skróconego zapisu, wykorzystując konfigurację gazu szlachetnego argonu (Ar), który ma 18 elektronów:
[Ar] 3d6 4s2
W tym zapisie, elektrony 4s2 i 3d6 są elektronami walencyjnymi. Ważne jest, aby pamiętać, że chociaż orbital 4s jest zapełniany przed orbitalem 3d (zgodnie z zasadą Aufbau, ponieważ ma niższą energię w atomie neutralnym), sytuacja zmienia się, gdy atom traci elektrony i tworzy jon.
Jak Zapisać Konfigurację Elektronową Jonów Żelaza (Fe2+ i Fe3+)?
Teraz przejdźmy do sedna – zapisu konfiguracji elektronowej jonów. Dla metali przejściowych, takich jak żelazo, zasada usuwania elektronów jest specyficzna i często bywa źródłem nieporozumień. Kluczowa zasada brzmi: elektrony są zawsze usuwane z orbitali o najwyższej liczbie kwantowej n (głównej liczbie kwantowej) w pierwszej kolejności. Dopiero potem, jeśli jest to konieczne, usuwane są elektrony z orbitali d.
Konfiguracja Elektronowa Jonu Fe2+
Jon Fe2+ powstaje, gdy atom żelaza traci dwa elektrony. Zgodnie z zasadą, te dwa elektrony zostaną usunięte z orbitalu o najwyższej liczbie kwantowej n, czyli z orbitalu 4s. Mimo że orbital 3d jest zapisywany po 3p, a przed 4s w konfiguracji neutralnego atomu (ze względu na kolejność zapełniania), to orbital 4s jest energetycznie wyżej położony w jonach niż 3d, a także leży na bardziej zewnętrznej powłoce. Dlatego to właśnie elektrony 4s są usuwane jako pierwsze.
Konfiguracja atomu neutralnego Fe: [Ar] 3d6 4s2
Po utracie dwóch elektronów z orbitalu 4s, konfiguracja jonu Fe2+ wygląda następująco:
1s2 2s2 2p6 3s2 3p6 3d6 lub w skróconej formie [Ar] 3d6
Jon Fe2+ ma o dwa elektrony mniej niż atom neutralny Fe, co jest zgodne z jego ładunkiem +2.

Konfiguracja Elektronowa Jonu Fe3+
Jon Fe3+ powstaje, gdy atom żelaza traci trzy elektrony. Postępujemy zgodnie z tą samą zasadą. Najpierw usuwamy dwa elektrony z orbitalu 4s. Pozostał nam do usunięcia jeszcze jeden elektron. Ponieważ orbital 4s jest już pusty, następny elektron zostanie usunięty z orbitalu 3d.
Konfiguracja po usunięciu 2 elektronów z 4s (stan Fe2+): [Ar] 3d6
Teraz usuwamy jeden elektron z orbitalu 3d:
1s2 2s2 2p6 3s2 3p6 3d5 lub w skróconej formie [Ar] 3d5
Warto zauważyć, że konfiguracja 3d5 jest szczególnie stabilna. Dzieje się tak, ponieważ orbital d ma pięć podorbitali, a w konfiguracji 3d5 każdy z nich jest zapełniony jednym elektronem (połowicznie zapełniony). Zgodnie z regułą Hunda i zasadą maksymalnej wielokrotności, połowicznie zapełnione lub całkowicie zapełnione podpowłoki są bardziej stabilne ze względu na symetrię i energię wymiany.
Tabela Porównawcza Konfiguracji
Dla lepszego zrozumienia, przedstawiamy tabelę porównującą konfiguracje elektronowe atomu neutralnego żelaza oraz jego jonów:
| Cząstka | Liczba elektronów | Pełna konfiguracja elektronowa | Skrócona konfiguracja elektronowa |
|---|---|---|---|
| Atom Fe | 26 | 1s2 2s2 2p6 3s2 3p6 3d6 4s2 | [Ar] 3d6 4s2 |
| Jon Fe2+ | 24 | 1s2 2s2 2p6 3s2 3p6 3d6 | [Ar] 3d6 |
| Jon Fe3+ | 23 | 1s2 2s2 2p6 3s2 3p6 3d5 | [Ar] 3d5 |
Zastosowania Żelaza i jego Jonów
Zdolność żelaza do tworzenia różnych jonów ma ogromne znaczenie praktyczne. Żelazo jest niezwykle wszechstronnym pierwiastkiem, szeroko stosowanym w wielu gałęziach przemysłu i życia codziennego:
- Budownictwo i przemysł: Żelazo, w postaci stali (stopu żelaza z węglem), jest podstawowym materiałem do produkcji kadłubów dużych statków, samochodów, różnego rodzaju maszyn i części maszyn. Jego wytrzymałość i dostępność sprawiają, że jest niezastąpione w inżynierii.
- Chemia przemysłowa: Azotany i chlorki żelaza są używane jako ważne reagenty w przemyśle. Siarczan żelaza(II) jest stosowany jako fungicyd. Chlorek żelaza jest również wykorzystywany w oczyszczaniu ścieków ze względu na jego zdolność do koagulacji zanieczyszczeń.
- Medycyna: Siarczan żelaza(II) jest powszechnie stosowany w leczeniu niedoborów żelaza (anemii), które są częstym problemem zdrowotnym. Żelazo jest również wykorzystywane w produkcji różnego rodzaju narzędzi chirurgicznych, co podkreśla jego znaczenie w medycynie.
- Biochemia: Jony żelaza, zwłaszcza Fe2+ i Fe3+, odgrywają kluczową rolę w wielu procesach biochemicznych, takich jak transport tlenu (hemoglobina zawiera jon Fe2+), oddychanie komórkowe oraz różne reakcje redoks.
Często Zadawane Pytania (FAQ)
Dlaczego elektrony 4s są usuwane przed 3d w jonach metali przejściowych?
To jedno z najczęstszych pytań i zarazem źródeł błędów. Chociaż w atomie neutralnym orbital 4s jest zapełniany przed 3d (ponieważ ma niższą energię), sytuacja zmienia się, gdy atom traci elektrony i staje się jonem. W jonach, elektrony z orbitali 4s stają się wyżej energetyczne i bardziej zewnętrzne niż elektrony 3d, ze względu na efektywny ładunek jądrowy i wzajemne oddziaływania elektronów. Dlatego to właśnie elektrony z orbitali 4s są usuwane jako pierwsze. Pamiętaj, że elektrony są usuwane z najbardziej zewnętrznej powłoki, a w przypadku jonów metali przejściowych, orbital 4s, mimo niższej energii w atomie neutralnym, staje się „walencyjny” w kontekście usuwania elektronów.
Czy konfiguracja jonów jest zawsze stabilniejsza niż konfiguracja atomu neutralnego?
Nie zawsze. Atomy tworzą jony, aby osiągnąć bardziej stabilną konfigurację elektronową, często naśladując konfigurację gazu szlachetnego (reguła oktetu) lub osiągając stabilne konfiguracje połowicznie lub całkowicie zapełnionych podpowłok (np. 3d5 dla Fe3+). Jednak proces tworzenia jonów wymaga energii (np. energia jonizacji), a stabilność jonu zależy od wielu czynników, w tym od energii sieci krystalicznej w związkach jonowych czy energii solwatacji w roztworach.
Co to jest orbital 4s, a co 3d w kontekście żelaza?
Orbital 4s to orbital s na czwartej powłoce elektronowej (n=4). Może pomieścić maksymalnie dwa elektrony. Orbital 3d to orbital d na trzeciej powłoce elektronowej (n=3). Może pomieścić maksymalnie dziesięć elektronów (pięć podorbitali, każdy z dwoma elektronami). W atomie neutralnym żelaza, elektrony najpierw zapełniają orbital 4s, a dopiero potem orbital 3d. Jednak przy tworzeniu jonów, elektrony z orbitalu 4s są usuwane jako pierwsze, ponieważ w jonach staje się on orbitalem o wyższej energii i większym promieniu niż orbital 3d.
Jak wpływa utrata elektronów na właściwości chemiczne jonów żelaza?
Utrata elektronów radykalnie zmienia właściwości chemiczne żelaza. Atom neutralny Fe jest metalem, który łatwo ulega korozji. Jony Fe2+ i Fe3+ mają zupełnie inne właściwości. Na przykład, Fe2+ jest koloru zielonego w roztworach i jest łatwo utleniane do Fe3+. Fe3+ jest koloru brązowo-żółtego w roztworach i jest bardziej stabilne w obecności tlenu. Różne stopnie utlenienia umożliwiają żelazu pełnienie wielu funkcji, od katalizatora w przemyśle po kluczowy element w biologii (np. w hemoglobinie).
Podsumowanie
Zapis konfiguracji elektronowej jonów, zwłaszcza dla metali przejściowych takich jak żelazo, wymaga zrozumienia specyficznych zasad dotyczących usuwania elektronów. Kluczem jest pamiętanie, że elektrony są usuwane z orbitali o najwyższej głównej liczbie kwantowej (n) w pierwszej kolejności, nawet jeśli były one zapełniane wcześniej. Dla żelaza oznacza to, że elektrony 4s są usuwane przed elektronami 3d.
Poprawne określenie konfiguracji elektronowej jonów jest fundamentalne dla zrozumienia ich reaktywności, właściwości fizycznych i chemicznych oraz ich roli w otaczającym nas świecie. Mamy nadzieję, że ten artykuł pomógł Ci zgłębić tę ważną dziedzinę chemii i zrozumieć, dlaczego jony Fe2+ i Fe3+ mają takie, a nie inne konfiguracje elektronowe.
Zainteresował Cię artykuł Zapis Konfiguracji Elektronowej Jonów Fe2+ i Fe3+? Zajrzyj też do kategorii Chemia, znajdziesz tam więcej podobnych treści!
