07/02/2017
W świecie chemii, gdzie każda cząsteczka ma swoją unikalną tożsamość, zdarzają się fascynujące zjawiska, które wykraczają poza prosty wzór sumaryczny. Jednym z nich jest izomeria, a w szczególności jej intrygująca odmiana – izomeria optyczna. Wyobraź sobie dwie cząsteczki, które na pierwszy rzut oka wyglądają identycznie, mają ten sam skład atomowy i nawet te same połączenia między atomami, a jednak w rzeczywistości są od siebie różne. To tak, jakbyś patrzył na swoje dłonie – są do siebie łudząco podobne, ale nigdy nie nałożysz prawej dłoni idealnie na lewą, chyba że jedną odwrócisz. Właśnie na tej zasadzie opiera się izomeria optyczna, gdzie cząsteczki są swoimi lustrzanymi odbiciami, ale nie dają się na siebie nałożyć. Zrozumienie tego fenomenu jest kluczowe nie tylko dla teoretycznej chemii, ale ma również ogromne znaczenie praktyczne, szczególnie w farmacji i biologii.

Czym jest izomeria optyczna?
Izomeria optyczna, znana również jako enancjomeria, to szczególny przypadek izomerii przestrzennej, czyli stereochemii. Pojawia się, gdy substancje mają ten sam wzór sumaryczny oraz ten sam wzór strukturalny (czyli atomy są połączone w tej samej kolejności), ale ich ułożenie w przestrzeni jest takie, że jedna cząsteczka nie może być nałożona na drugą. Mówiąc prościej, izomery optyczne są swoimi lustrzanymi odbiciami, podobnie jak lewa i prawa ręka. Takie cząsteczki nazywamy chiralnymi (od greckiego „cheir” – ręka), a ich różne formy to enancjomery.
Kluczowym elementem, który często prowadzi do wystąpienia izomerii optycznej, jest obecność asymetrycznego atomu węgla, zwanego również centrum chiralności. Asymetryczny atom węgla to atom, który jest połączony z czterema różnymi grupami atomów. Te grupy mogą być zarówno niezwykle złożonymi fragmentami cząsteczki, jak i prostymi atomami, takimi jak wodór czy chlor. Ważne jest, aby wszystkie cztery podstawniki były różne. Jeśli choć dwa podstawniki są identyczne, cząsteczka nie będzie chiralna (a tym samym nie będzie wykazywać izomerii optycznej), ponieważ będzie posiadała płaszczyznę symetrii, co umożliwi jej nałożenie na swoje lustrzane odbicie.
Enancjomery posiadają identyczne właściwości fizyczne, takie jak temperatura wrzenia, topnienia, gęstość czy rozpuszczalność, z jednym kluczowym wyjątkiem – różnią się sposobem oddziaływania ze światłem spolaryzowanym. Jeden enancjomer skręca płaszczyznę światła spolaryzowanego w prawo (jest prawoskrętny, oznaczany jako (+)), a drugi w lewo (jest lewoskrętny, oznaczany jako (-)). Stąd właśnie nazwa „izomeria optyczna”. Mieszanina równych ilości obu enancjomerów nazywana jest racematem i jest optycznie nieaktywna, ponieważ efekty skręcania płaszczyzny światła wzajemnie się znoszą.
Jak określić typ izomeru? Ścieżka decyzyjna
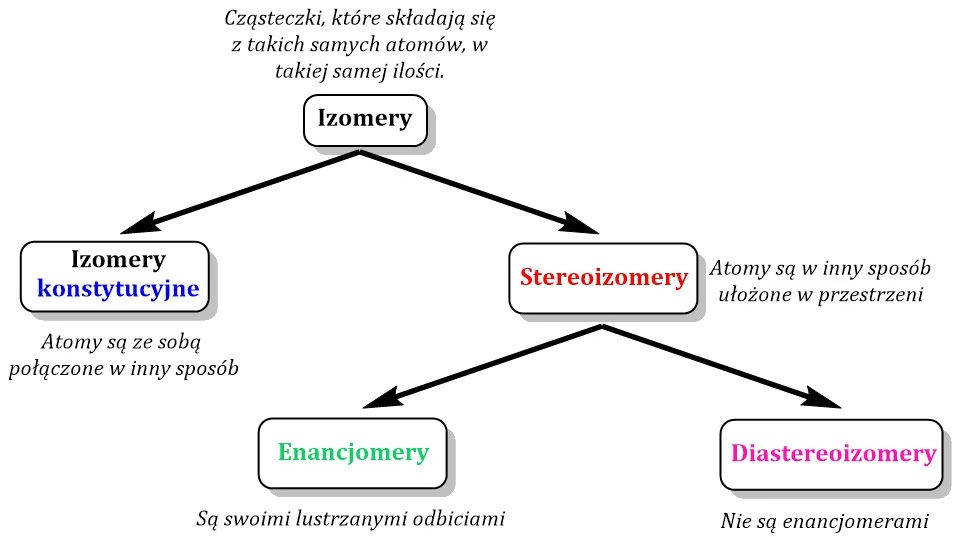
Rozpoznanie i klasyfikacja izomerów w chemii organicznej może być wyzwaniem, ale istnieje logiczna ścieżka, która pozwala na ich prawidłowe zidentyfikowanie. Poniżej przedstawiamy krok po kroku, jak określić, z jakim typem izomeru mamy do czynienia, bazując na kluczowych pytaniach dotyczących struktury i właściwości cząsteczek.
- Czy cząsteczki mają ten sam wzór sumaryczny?
- Tak: Cząsteczki są izomerami. Kontynuuj do kolejnego kroku, aby określić ich typ.
- Nie: Cząsteczki nie są izomerami. Są to po prostu różne związki chemiczne.
Wyjaśnienie: Izomery to cząsteczki składające się z tej samej ilości poszczególnych atomów, a więc mające ten sam wzór sumaryczny (np. C6H12O6). Różnią się jednak układem tych atomów.
- Czy cząsteczki posiadają tę samą nazwę, w której zawierają oznaczenia R lub S, i czy są optycznie czynne?
- Tak: Związki te są stereoizomerami, a dokładniej izomerami optycznymi. Przejdź do następnego pytania, aby precyzyjniej określić ich rodzaj.
- Nie: Związki te są izomerami konstytucyjnymi (strukturalnymi).
Wyjaśnienie: Izomery konstytucyjne (strukturalne) mają ten sam wzór sumaryczny, ale różnią się kolejnością połączeń atomów (np. butan i izobutan). Stereoizomery mają tę samą kolejność połączeń, ale różnią się ułożeniem atomów w przestrzeni. Oznaczenia R i S (Rectus/Sinister) są stosowane do jednoznacznego określenia konfiguracji absolutnej centrum chiralności i są charakterystyczne dla związków optycznie czynnych.
- Czy cząsteczki te są lustrzanymi odbiciami i tworzą parę nienakładalnych na siebie cząsteczek chemicznych?
- Tak: Związki te są enancjomerami.
- Nie: Związki te są diastereoizomerami.
Wyjaśnienie: Enancjomery to para stereoizomerów, które są lustrzanymi odbiciami i nie można ich na siebie nałożyć. Posiadają identyczne właściwości fizyczne (z wyjątkiem skręcalności optycznej) i chemiczne (z wyjątkiem reakcji z innymi chiralnymi substancjami). Diastereoizomery to stereoizomery, które nie są lustrzanymi odbiciami. Posiadają różne właściwości fizyczne i chemiczne.

Geometria molekularna (cz\u0105steczkowa) w\u0119glowodorów jest bezpo\u015brednio zwi\u0105zania z fizycznymi i chemicznymi w\u0142a\u015bciwo\u015bciami tych cz\u0105steczek. Cz\u0105steczki posiadaj\u0105ce ten sam wzór cz\u0105steczkowy, ale inn\u0105 geometri\u0119 nazywane s\u0105 izomerami. Istniej\u0105 dwa g\u0142ówne typy izomerów: izomery strukturalne oraz stereoizomery.
Powyższa ścieżka decyzyjna pozwala na systematyczne podejście do klasyfikacji izomerów, co jest fundamentalne w chemii organicznej.
Główne typy izomerii w chemii
Geometria molekularna węglowodorów i innych związków chemicznych jest bezpośrednio związana z ich fizycznymi i chemicznymi właściwościami. Cząsteczki posiadające ten sam wzór cząsteczkowy, ale inną geometrię lub układ atomów, nazywane są izomerami. Istnieją dwa główne typy izomerów:
1. Izomery strukturalne (konstytucyjne)
Izomery strukturalne to związki, które mają ten sam wzór sumaryczny, ale różnią się kolejnością, w jakiej atomy są ze sobą połączone. Oznacza to, że mają inną budowę (konstytucję) szkieletu węglowego lub inne rozmieszczenie grup funkcyjnych. Przykłady obejmują:
- Izomeria łańcuchowa: Różnice w strukturze szkieletu węglowego (np. n-butan i izobutan).
- Izomeria położeniowa: Różnice w położeniu grupy funkcyjnej lub podstawnika na tym samym szkielecie (np. propan-1-ol i propan-2-ol).
- Izomeria funkcyjna: Różnice w typie grupy funkcyjnej (np. etanol i eter dimetylowy, oba o wzorze C2H6O).
Izomery strukturalne zazwyczaj mają znacząco różne właściwości fizyczne i chemiczne, ponieważ ich fundamentalna struktura połączeń jest odmienna.
2. Stereoizomery
Stereoizomery to związki, które mają ten sam wzór sumaryczny i tę samą kolejność połączeń atomów (tzn. mają tę samą konstytucję), ale różnią się przestrzennym ułożeniem atomów. Są to związki, które nie mogą być na siebie nałożone bez zerwania i ponownego utworzenia wiązań. Stereoizomery dzielimy na dwie główne kategorie:
Izomery optyczne (enancjomery)
Jak już wspomniano, enancjomery to stereoizomery, które są swoimi nienakładalnymi lustrzanymi odbiciami. Ich istnienie jest związane z obecnością centrum chiralności, najczęściej asymetrycznego atomu węgla. Kluczową cechą enancjomerów jest ich zdolność do skręcania płaszczyzny światła spolaryzowanego w przeciwnych kierunkach. Posiadają identyczne właściwości fizyczne (z wyjątkiem skręcalności optycznej) i chemiczne, chyba że wchodzą w reakcję z innym chiralnym reagentem lub oddziałują z chiralnym środowiskiem (np. enzymami w organizmach żywych).
Diastereoizomery
Diastereoizomery to stereoizomery, które nie są lustrzanymi odbiciami siebie nawzajem. Mogą posiadać jedno lub więcej centrów chiralności, ale nie są parą enancjomerów. W przeciwieństwie do enancjomerów, diastereoizomery mają różne właściwości fizyczne (np. temperatury wrzenia i topnienia, rozpuszczalność) oraz chemiczne. Przykładem diastereoizomerów są izomery cis-trans (zwane również izomerami geometrycznymi) w związkach z wiązaniem podwójnym, gdzie obrót wokół wiązania jest ograniczony, a grupy są ułożone po tej samej (cis) lub przeciwnej (trans) stronie płaszczyzny wiązania.
Znaczenie izomerii optycznej w życiu codziennym i nauce
Izomeria optyczna, choć na pierwszy rzut oka wydaje się abstrakcyjnym pojęciem chemicznym, ma ogromne znaczenie praktyczne, zwłaszcza w dziedzinach takich jak farmacja, biochemia, przemysł spożywczy i perfumeryjny. To właśnie subtelne różnice w przestrzennym ułożeniu atomów decydują o aktywności biologicznej cząsteczki.
Farmacja i medycyna
Wiele leków to cząsteczki chiralne, a często tylko jeden z enancjomerów jest aktywny terapeutycznie, podczas gdy drugi może być nieaktywny, a nawet szkodliwy. Klasycznym przykładem jest talidomid, lek stosowany w latach 50. i 60. XX wieku. Jeden enancjomer talidomidu działał uspokajająco, podczas gdy drugi, jego lustrzane odbicie, był teratogenny i powodował poważne wady wrodzone u dzieci. Ten tragiczny przypadek podkreślił kluczowe znaczenie syntezy i separacji czystych enancjomerów w przemyśle farmaceutycznym. Współczesne regulacje wymagają od producentów leków szczegółowych badań nad aktywnością każdego enancjomeru.
Inne przykłady obejmują ibuprofen (lek przeciwbólowy, tylko jeden enancjomer jest aktywny, ale drugi może być w organizmie przekształcony w aktywny) czy lewodopę (stosowaną w leczeniu choroby Parkinsona, tylko L-Dopa jest aktywna, a D-Dopa jest nieaktywna i toksyczna).
Biochemia i biologia
Większość cząsteczek biologicznych, takich jak aminokwasy, białka, cukry i DNA, jest chiralna. Na przykład, wszystkie naturalne aminokwasy występujące w białkach to L-izomery, a cukry to zazwyczaj D-izomery. Enzymy, które są białkami, same są chiralne i potrafią rozróżniać enancjomery substratów, działając specyficznie tylko na jeden z nich. To wyjaśnia, dlaczego tylko jeden enancjomer leku jest często aktywny – pasuje on do „klucza” enzymu lub receptora jak do „zamka”.
Przemysł spożywczy i perfumeryjny
Również w przemyśle spożywczym i perfumeryjnym izomeria optyczna odgrywa rolę. Na przykład, jeden enancjomer limonenu pachnie jak cytryna, podczas gdy drugi pachnie jak pomarańcza. Podobnie, asparaginian (sztuczny słodzik) jest dwoma enancjomerami, z których tylko jeden jest słodki. Te przykłady pokazują, jak subtelne różnice w strukturze przestrzennej mogą prowadzić do odmiennych wrażeń zmysłowych.
Tabela kluczowych pojęć
Aby ułatwić zrozumienie złożoności izomerii optycznej, poniżej przedstawiono tabelę z najważniejszymi terminami i ich krótkimi definicjami:
| Pojęcie | Definicja |
|---|---|
| Izomery optyczne | Cząsteczki o tym samym wzorze sumarycznym i strukturalnym, które są swoimi nienakładalnymi lustrzanymi odbiciami. |
| Chiralność | Właściwość obiektu (np. cząsteczki), polegająca na tym, że nie jest on identyczny ze swoim lustrzanym odbiciem (nie można go na nie nałożyć). |
| Enancjomery | Para izomerów optycznych, które są swoimi nienakładalnymi lustrzanymi odbiciami. Różnią się skręcalnością optyczną. |
| Asymetryczny atom węgla | Atom węgla połączony z czterema różnymi grupami lub atomami. Stanowi centrum chiralności. |
| Diastereoizomery | Stereoizomery, które nie są swoimi lustrzanymi odbiciami. Posiadają różne właściwości fizyczne i chemiczne. |
| Racemat | Mieszanina równych ilości dwóch enancjomerów. Jest optycznie nieaktywny. |
| Optyczna aktywność | Zdolność chiralnej substancji do skręcania płaszczyzny światła spolaryzowanego. |
Często zadawane pytania (FAQ)
1. Czym różnią się enancjomery od diastereoizomerów?
Kluczowa różnica polega na relacji lustrzanego odbicia. Enancjomery to para stereoizomerów, które są swoimi nienakładalnymi lustrzanymi odbiciami (jak lewa i prawa dłoń). Posiadają identyczne właściwości fizyczne (z wyjątkiem skręcalności optycznej) i chemiczne (w środowisku achiralnym). Diastereoizomery to stereoizomery, które NIE są lustrzanymi odbiciami siebie nawzajem. Mają różne właściwości fizyczne i chemiczne. Mogą mieć jedno lub więcej centrów chiralności, ale ich konfiguracja jest inna niż ta, która tworzyłaby lustrzane odbicie.
2. Czy każdy związek z asymetrycznym atomem węgla jest optycznie czynny?
Prawie każdy. Związek zawierający jeden asymetryczny atom węgla zawsze będzie chiralny i optycznie czynny. Jednakże, związki z dwoma lub większą liczbą asymetrycznych atomów węgla mogą być achiralne, jeśli posiadają wewnętrzną płaszczyznę symetrii. Takie związki nazywane są związkami mezo. Mimo posiadania centrów chiralności, cząsteczka jako całość jest achiralna, ponieważ jedna połowa cząsteczki jest lustrzanym odbiciem drugiej, co skutkuje wewnętrzną kompensacją skręcalności optycznej.
3. Jak rozpoznać asymetryczny atom węgla?
Asymetryczny atom węgla (zwany również centrum chiralności) to atom węgla połączony z czterema RÓŻNYMI grupami lub atomami. Aby go rozpoznać, należy systematycznie sprawdzać każdy atom węgla w cząsteczce i analizować podstawniki, które są do niego przyłączone. Jeśli wszystkie cztery podstawniki są unikalne, atom węgla jest asymetryczny. Na przykład, w kwasie mlekowym (CH3CH(OH)COOH), środkowy atom węgla jest asymetryczny, ponieważ jest połączony z grupą metylową (-CH3), grupą hydroksylową (-OH), atomem wodoru (-H) i grupą karboksylową (-COOH) – wszystkie są różne.
4. Czy izomery optyczne mają takie samo działanie biologiczne?
Zazwyczaj nie. Ze względu na chiralną naturę enzymów, receptorów i innych makromolekuł biologicznych, tylko jeden enancjomer zazwyczaj pasuje do miejsca wiążącego jak klucz do zamka. Drugi enancjomer może być nieaktywny, mieć słabsze działanie, wykazywać inne działanie farmakologiczne, a nawet być toksyczny. To dlatego przemysł farmaceutyczny dąży do produkcji leków w formie czystych enancjomerów.
5. Co to jest racemat i dlaczego jest optycznie nieaktywny?
Racemat to mieszanina równych ilości (50:50) dwóch enancjomerów. Jest optycznie nieaktywny, ponieważ skręcanie płaszczyzny światła spolaryzowanego przez jeden enancjomer jest dokładnie kompensowane przez skręcanie w przeciwnym kierunku przez drugi enancjomer. Netto obserwuje się brak skręcania światła, pomimo że każdy enancjomer z osobna jest optycznie czynny. Proces rozdzielania racematów na czyste enancjomery nazywa się rozdzielczością racemiczną.
Zrozumienie izomerii optycznej to klucz do głębszego poznania chemii organicznej i jej wpływu na otaczający nas świat. Subtelne różnice w przestrzennym ułożeniu atomów mogą mieć kolosalne konsekwencje, od zapachu cytrusów po skuteczność i bezpieczeństwo leków. Ta niewidzialna dla oka, ale fundamentalna cecha cząsteczek, nieustannie fascynuje naukowców i stanowi podstawę dla innowacji w wielu dziedzinach.
Zainteresował Cię artykuł Izomeria Optyczna: Lustrzany Świat Chemii? Zajrzyj też do kategorii Chemia, znajdziesz tam więcej podobnych treści!

