31/07/2018
Świat chemii jest pełen fascynujących związków, a wśród nich szczególne miejsce zajmują kwasy. Są one wszechobecne – od soku z cytryny po akumulatory samochodowe. Zrozumienie ich podziału jest kluczowe dla każdego, kto chce zgłębić tajniki tej nauki. Najbardziej fundamentalny podział kwasów opiera się na obecności lub braku atomów tlenu w ich cząsteczkach, co prowadzi do wyróżnienia dwóch głównych kategorii: kwasów tlenowych i beztlenowych. Ta klasyfikacja ma ogromne znaczenie dla przewidywania właściwości chemicznych, reaktywności oraz zastosowań tych związków.
Czym Różnią Się Kwasy Tlenowe od Beztlenowych?
Podstawowa zasada rozróżniania kwasów tlenowych i beztlenowych jest zaskakująco prosta, a jednocześnie fundamentalna dla chemii nieorganicznej. Rozważmy strukturę cząsteczki kwasu.
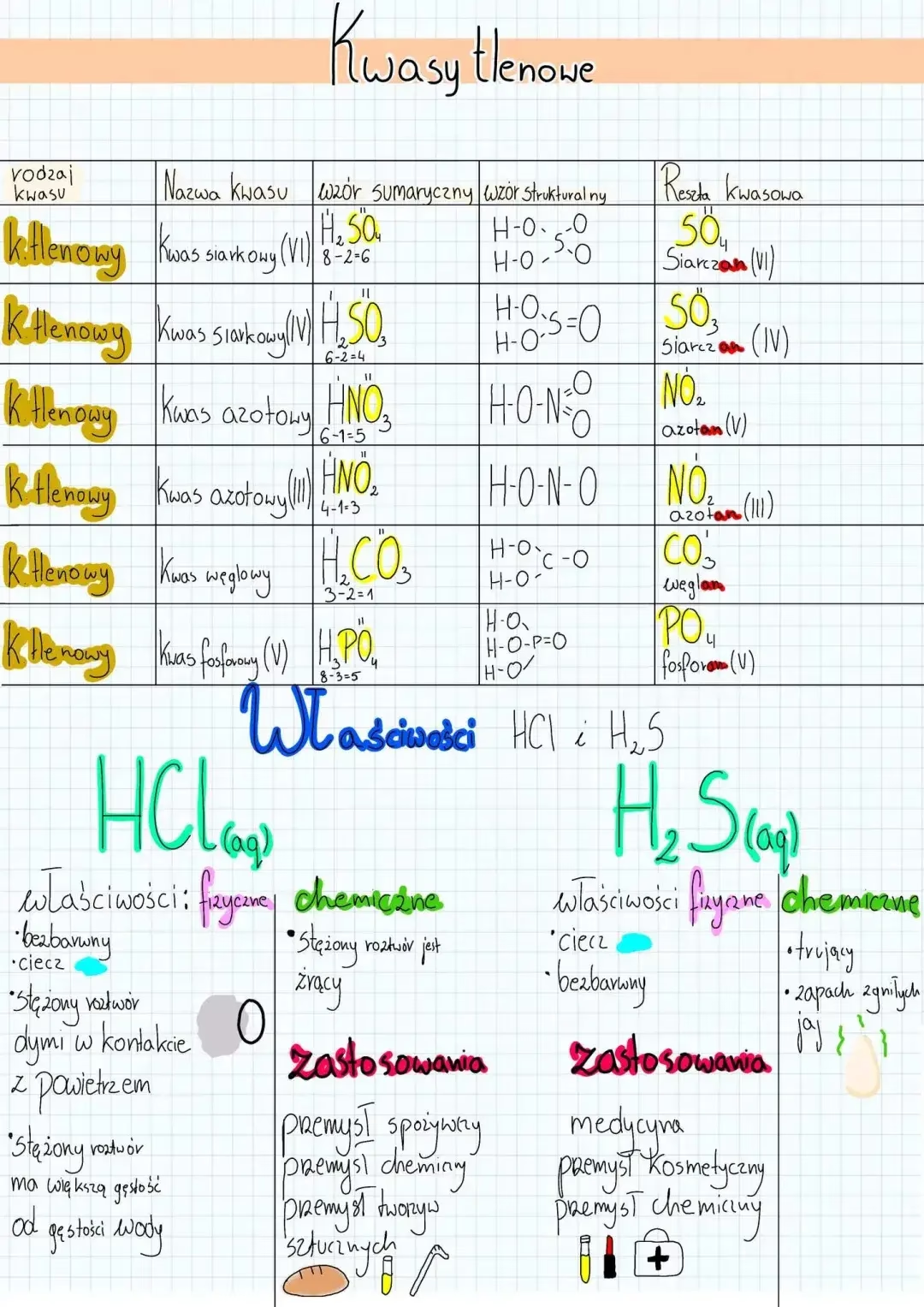
W przypadku, gdy w cząsteczce kwasu, poza atomami wodoru i niemetalu, znajduje się również atom tlenu (lub grupa atomów zawierająca tlen, np. grupa siarczanowa, azotanowa), mówimy o kwasie tlenowym, często nazywanym również oksokwasem. W oksokwasach, kwaśny wodór jest zawsze związany z atomem tlenu. To właśnie obecność tlenu w grupie kwasowej nadaje im specyficzne właściwości. Przykłady obejmują dobrze znany kwas siarkowy (H2SO4), kwas azotowy (HNO3) czy kwas fosforowy (H3PO4).
Z drugiej strony, jeśli cząsteczka kwasu składa się wyłącznie z atomów wodoru i atomu niemetalu (np. chloru, siarki), bez obecności tlenu, wówczas mamy do czynienia z kwasem beztlenowym. W tych kwasach kwaśny wodór jest bezpośrednio związany z atomem niemetalu. Typowe przykłady kwasów beztlenowych to kwas chlorowodorowy (HCl), kwas bromowodorowy (HBr) czy kwas siarkowodorowy (H2S).

Ta prosta definicja ma daleko idące konsekwencje dla zrozumienia zachowania kwasów w roztworach wodnych, ich mocy oraz sposobów reakcji z innymi substancjami. Historia chemii pokazuje, że początkowo sądzono, iż wszystkie kwasy zawierają tlen (stąd nazwa „oxygen” – „tworzący kwasy”, nadana przez Lavoisiera). Dopiero odkrycie kwasów beztlenowych, takich jak kwas chlorowodorowy, wymusiło rozszerzenie definicji i wprowadzenie obecnego podziału.
Jak Ustalić, Czy Kwas Jest Kwasem Tlenowym?
Rozpoznanie kwasu tlenowego wymaga spojrzenia na jego wzór chemiczny i strukturę. Kluczowym elementem jest to, czy kwaśny atom wodoru (lub atomy) jest związany z atomem tlenu, który z kolei jest połączony z atomem centralnym (zazwyczaj niemetalem). W kwasach beztlenowych wodór jest bezpośrednio związany z niemetalem.
Moc kwasów tlenowych zależy od kilku czynników, a przede wszystkim od:
- Elektroujemności atomu centralnego: Im większa elektroujemność atomu centralnego, tym silniejszy kwas. Atom centralny silniej przyciąga elektrony od atomów tlenu, co z kolei powoduje, że wiązanie O-H staje się bardziej spolaryzowane i łatwiej ulega dysocjacji, uwalniając jony H+. Przykład: Kwas siarkowy (H2SO4) jest silniejszy niż kwas selenowy (H2SeO4), ponieważ siarka jest bardziej elektroujemna niż selen.
- Liczby atomów tlenu (zwłaszcza tych niezwiązanych z wodorem): W przypadku kwasów tlenowych o tym samym atomie centralnym, siła kwasu rośnie wraz ze wzrostem liczby atomów tlenu niezwiązanych z wodorem. Te dodatkowe atomy tlenu odciągają gęstość elektronową od atomu centralnego, a tym samym od grup -OH, co ułatwia dysocjację wodoru. Klasycznym przykładem są kwasy chloru: HClO (kwas podchlorawy) jest słaby, HClO2 (kwas chlorawy) jest średnio silny, HClO3 (kwas chlorowy) jest silny, a HClO4 (kwas nadchlorowy) jest jednym z najsilniejszych znanych kwasów. Każdy kolejny atom tlenu zwiększa kwasowość.
To właśnie te czynniki decydują o tym, że kwas nadchlorowy (HClO4), kwas siarkowy (H2SO4) i kwas azotowy (HNO3) są jednymi z najsilniejszych i najczęściej stosowanych kwasów w chemii i przemyśle. Ich struktura z dużą liczbą atomów tlenu wokół atomu centralnego sprzyja efektywnemu oddysocjowaniu protonów.
Właściwości i Stabilność Kwasów Tlenowych
Kwasy tlenowe, mimo swojej wszechstronności, często wykazują mniejszą stabilność niż sole ich zde-protonowanych form (anionów tlenowych). Istnieje kilka ogólnych przyczyn tej niestabilności:
- Kondensacja i tworzenie oligomerów: Niektóre kwasy tlenowe mogą ulegać kondensacji, tworząc większe cząsteczki (oligomery). Na przykład, kwas chromowy (H2CrO4) może kondensować do kwasu dichromowego (H2Cr2O7).
- Dehydratacja do bezwodnika: Wiele kwasów tlenowych może łatwo ulegać dehydratacji (odwodnieniu), tworząc odpowiedni bezwodnik kwasowy. Klasycznym przykładem jest kwas węglowy (H2CO3), który istnieje głównie w roztworze i łatwo rozpada się na dwutlenek węgla (CO2) i wodę. Podobnie, kwas siarkowy(VI) jest bezwodnikiem siarki(VI) (SO3).
- Dysproporcjonowanie: Niektóre kwasy tlenowe są niestabilne i mogą ulegać reakcjom dysproporcjonowania, gdzie atom centralny zmienia swój stopień utlenienia jednocześnie na wyższy i niższy. Przykładem jest kwas chlorawy (HClO2), który może dysproporcjonować do kwasu podchlorawego (HClO) i kwasu chlorowego (HClO3).
- Tautomeria: Czasami kwas może istnieć niemal całkowicie w innej, bardziej stabilnej formie tautomerycznej. Kwas fosforowy (H3PO3), formalnie P(OH)3, występuje niemal wyłącznie jako kwas fosfonowy (HP(=O)(OH)2), gdzie jeden wodór jest bezpośrednio związany z atomem fosforu, a nie tlenu.
Mimo tych wyzwań, wiele kwasów tlenowych, takich jak wspomniane wcześniej kwas nadchlorowy (HClO4), kwas siarkowy (H2SO4) i kwas azotowy (HNO3), można stosunkowo łatwo przygotować jako czyste substancje i są one szeroko wykorzystywane w przemyśle i laboratoriach.

Porównanie Kwasów Tlenowych i Beztlenowych
Aby lepiej zrozumieć różnice między tymi dwoma typami kwasów, warto spojrzeć na nie w formie tabelarycznej:
| Cecha | Kwasy Tlenowe (Oksokwasy) | Kwasy Beztlenowe |
|---|---|---|
| Obecność tlenu | Zawsze zawierają tlen w grupie kwasowej. | Nie zawierają tlenu. |
| Wiązanie H-X | Kwaśny wodór związany z atomem tlenu (H-O-X, gdzie X to atom centralny). | Kwaśny wodór związany bezpośrednio z atomem niemetalu (H-X, gdzie X to niemetal). |
| Przykłady | H2SO4 (kwas siarkowy), HNO3 (kwas azotowy), H3PO4 (kwas fosforowy), HClO4 (kwas nadchlorowy) | HCl (kwas chlorowodorowy), HBr (kwas bromowodorowy), H2S (kwas siarkowodorowy), HF (kwas fluorowodorowy) |
| Nazewnictwo | Zazwyczaj końcówka '-owy' (np. siarkowy, azotowy). Siła kwasu może być oznaczana przedrostkami (np. pod-, -awy, -owy, nad-). | Przedrostek 'wodoro-' i końcówka '-owy' (np. chlorowodorowy, bromowodorowy). |
| Czynniki wpływające na moc | Elektroujemność atomu centralnego, liczba atomów tlenu. | Długość i polarność wiązania H-X (im dłuższe wiązanie, tym słabsze, im większa polarność, tym silniejsze). |
| Stabilność | Wiele jest niestabilnych, ulega kondensacji, dehydratacji, dysproporcjonowaniu lub tautomeryzacji. | Zazwyczaj bardziej stabilne w czystej postaci, ale mogą być lotne. |
Nazewnictwo Kwasów
Systematyczne nazewnictwo kwasów odzwierciedla ich podział i budowę:
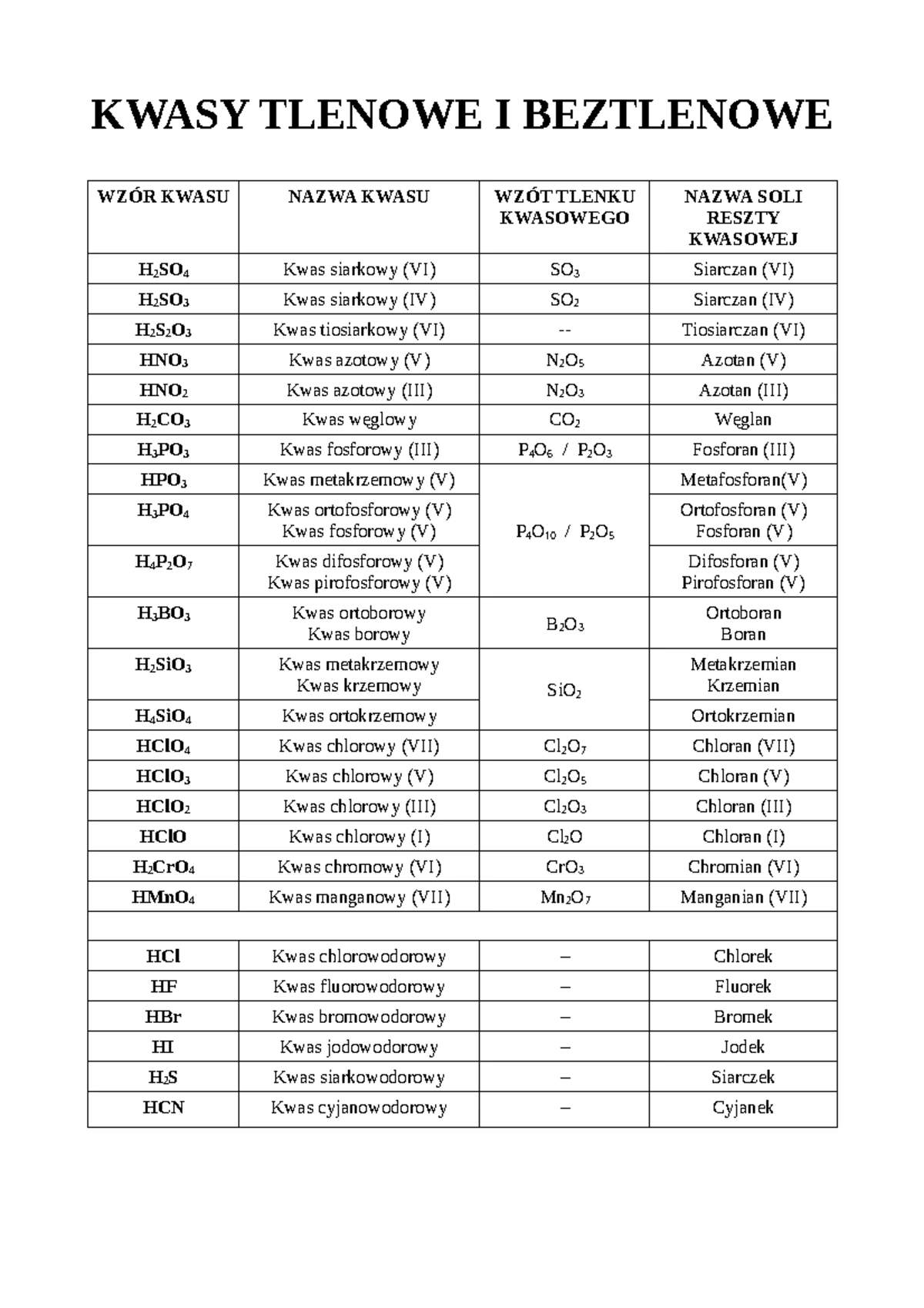
- Kwasy beztlenowe: Nazywamy je dodając przedrostek 'wodoro-' do nazwy niemetalu, a następnie końcówkę '-owy'. Przykłady: kwas chlorowodorowy (HCl), kwas bromowodorowy (HBr), kwas siarkowodorowy (H2S).
- Kwasy tlenowe: Nazwa pochodzi od niemetalu, który jest atomem centralnym, z odpowiednią końcówką '-owy'. Jeśli niemetal tworzy kilka kwasów o różnych stopniach utlenienia, używa się przedrostków i sufiksów, aby je rozróżnić. Na przykład, dla chloru mamy: kwas podchlorawy (HClO, Cl na +I), kwas chlorawy (HClO2, Cl na +III), kwas chlorowy (HClO3, Cl na +V), kwas nadchlorowy (HClO4, Cl na +VII).
Zastosowania Kwasów w Życiu Codziennym i Przemyśle
Kwasy, niezależnie od ich klasyfikacji, odgrywają nieocenioną rolę w naszym życiu i przemyśle:
- Kwas siarkowy (H2SO4): Ten oksokwas jest nazywany „królem chemikaliów” ze względu na swoje wszechstronne zastosowanie. Jest używany do produkcji nawozów sztucznych, akumulatorów, detergentów, barwników, a także w przemyśle naftowym i metalurgicznym.
- Kwas azotowy (HNO3): Kolejny ważny kwas tlenowy, stosowany głównie do produkcji nawozów azotowych, materiałów wybuchowych, barwników i leków.
- Kwas fosforowy (H3PO4): Używany w produkcji nawozów, detergentów, a także jako dodatek do żywności (np. w napojach gazowanych) i w stomatologii.
- Kwas chlorowodorowy (HCl): Ten kwas beztlenowy jest kluczowym składnikiem kwasu solnego, który znajduje się w naszych żołądkach, wspomagając trawienie. W przemyśle jest używany do czyszczenia metali, w produkcji tworzyw sztucznych i farmaceutyków.
- Kwas fluorowodorowy (HF): Wyjątkowy kwas beztlenowy, zdolny do trawienia szkła, co czyni go niezastąpionym w przemyśle optycznym i elektronicznym do trawienia krzemu.
Często Zadawane Pytania
Poniżej przedstawiamy odpowiedzi na najczęściej zadawane pytania dotyczące podziału kwasów:
P: Czy wszystkie kwasy zawierają tlen?
O: Nie, to powszechne błędne przekonanie. Kwasy dzielimy na tlenowe (oksokwasy), które zawierają tlen, oraz beztlenowe, które go nie zawierają. Przykładem kwasu beztlenowego jest kwas chlorowodorowy (HCl).
P: Jakie są najsilniejsze kwasy tlenowe?
O: Do najsilniejszych i najbardziej znanych kwasów tlenowych należą kwas nadchlorowy (HClO4), kwas siarkowy (H2SO4) i kwas azotowy (HNO3).
P: Czym różni się kwas fosforowy od kwasu fosfonowego?
O: Formalnie kwas fosforowy (H3PO3) jest oksokwasem, ale większość jego cząsteczek istnieje w formie tautomerycznej jako kwas fosfonowy (HP(=O)(OH)2), gdzie jeden z atomów wodoru jest bezpośrednio związany z atomem fosforu, a nie tlenu. Ta różnica strukturalna wpływa na liczbę kwaśnych wodorów (kwas fosfonowy jest dwuprotonowy, mimo trzech wodorów w cząsteczce).
P: Dlaczego niektóre kwasy tlenowe są niestabilne?
O: Niestabilność wielu kwasów tlenowych wynika z ich tendencji do ulegania reakcjom takim jak kondensacja (tworzenie większych cząsteczek), dehydratacja (utrata wody i tworzenie bezwodnika kwasowego) lub dysproporcjonowanie (jednoczesna zmiana stopnia utlenienia atomu centralnego na wyższy i niższy). Często istnieją tylko w roztworach wodnych, a nie w czystej postaci.
P: Czy moc kwasu beztlenowego zależy od elektroujemności niemetalu?
O: W przypadku kwasów beztlenowych (np. halogenowodorów HF, HCl, HBr, HI), moc kwasu rośnie wraz ze spadkiem elektroujemności niemetalu i wzrostem rozmiaru atomu niemetalu w grupie. Dzieje się tak, ponieważ wiązanie H-X staje się dłuższe i słabsze, co ułatwia dysocjację protonu. Dlatego HI jest silniejszy niż HCl, a HCl jest silniejszy niż HF.
Podsumowanie
Podział kwasów na tlenowe i beztlenowe jest podstawą zrozumienia ich chemii. Kwasy tlenowe charakteryzują się obecnością atomu tlenu w grupie kwasowej i wiązaniem H-O-X, a ich moc zależy od elektroujemności atomu centralnego i liczby atomów tlenu. Kwasy beztlenowe natomiast nie zawierają tlenu, a wodór jest bezpośrednio związany z niemetalem. Oba typy kwasów odgrywają niezastąpioną rolę w nauce, przemyśle i życiu codziennym. Zrozumienie tych fundamentalnych różnic pozwala na przewidywanie ich zachowań i zastosowań, otwierając drzwi do dalszych odkryć w fascynującym świecie chemii.
Zainteresował Cię artykuł Kwasy Tlenowe i Beztlenowe: Klucz do Zrozumienia? Zajrzyj też do kategorii Chemia, znajdziesz tam więcej podobnych treści!

