22/08/2016
Czy kiedykolwiek zastanawiałeś się nad tym, jak wygląda mikroświat, który nas otacza? Jakie są kształty drobin tworzących materię? Czy można je zobaczyć i czy mają kolory? Odpowiedzi na te pytania, choć na pierwszy rzut oka niewidoczne, stanowią fundament naszego rozumienia wszechświata. Wiemy już, że materia nie jest ciągła, lecz składa się z nieskończenie małych, ale fundamentalnych cząstek. W tym artykule zgłębimy tajniki budowy atomu, nauczymy się nazywać jego poszczególne elementy, określać przestrzeń, w której się znajdują, a także stosować kluczowe pojęcia takie jak nukleony, liczba masowa i liczba atomowa. Przejdziemy przez fascynujące obliczenia z użyciem atomowej jednostki masy, co pozwoli nam lepiej zrozumieć, jak naukowcy opisują ten niewidzialny świat. Przygotuj się na podróż do samego serca materii!
Co to jest atom? Podstawowy budulec materii
Podstawowymi elementami, z których zbudowana jest cała materia we wszechświecie, są atomy. Każda substancja, od powietrza, którym oddychamy, po twarde skały, składa się z atomów. Atomy posiadają masę, objętość i unikalny kształt, który jest zazwyczaj kulisty. Co ważne, każdy pierwiastek chemiczny, taki jak żelazo czy złoto, składa się z atomów tylko jednego rodzaju. Choć atomy żelaza i złota są zbudowane z tych samych fundamentalnych cząstek, różnią się ich liczbą, co nadaje im odmienne właściwości.

Ze względu na swoje niewyobrażalnie małe rozmiary, atomy są niemożliwe do zobaczenia gołym okiem. Przez długi czas uważano je za niepodzielne, twarde kulki. Jednak rozwój technologii, zwłaszcza wynalezienie skaningowego mikroskopu tunelowego (STM) pod koniec XX wieku, pozwolił naukowcom „zobaczyć” atomy w sposób pośredni. Obrazy uzyskane za pomocą STM potwierdziły, że atomy mają kształt kulisty, a ich rozmiary są różne i zależą od rodzaju pierwiastka. Już na początku XIX wieku angielski uczony John Dalton, uważany za twórcę naukowej atomistyki, twierdził, że atomy tworzące różne pierwiastki są kulami różniącymi się między sobą wielkością. Dzięki współczesnym narzędziom możemy potwierdzić jego intuicje i pogłębić naszą wiedzę o ich wewnętrznej strukturze.
W głąb atomu: Jego składowe
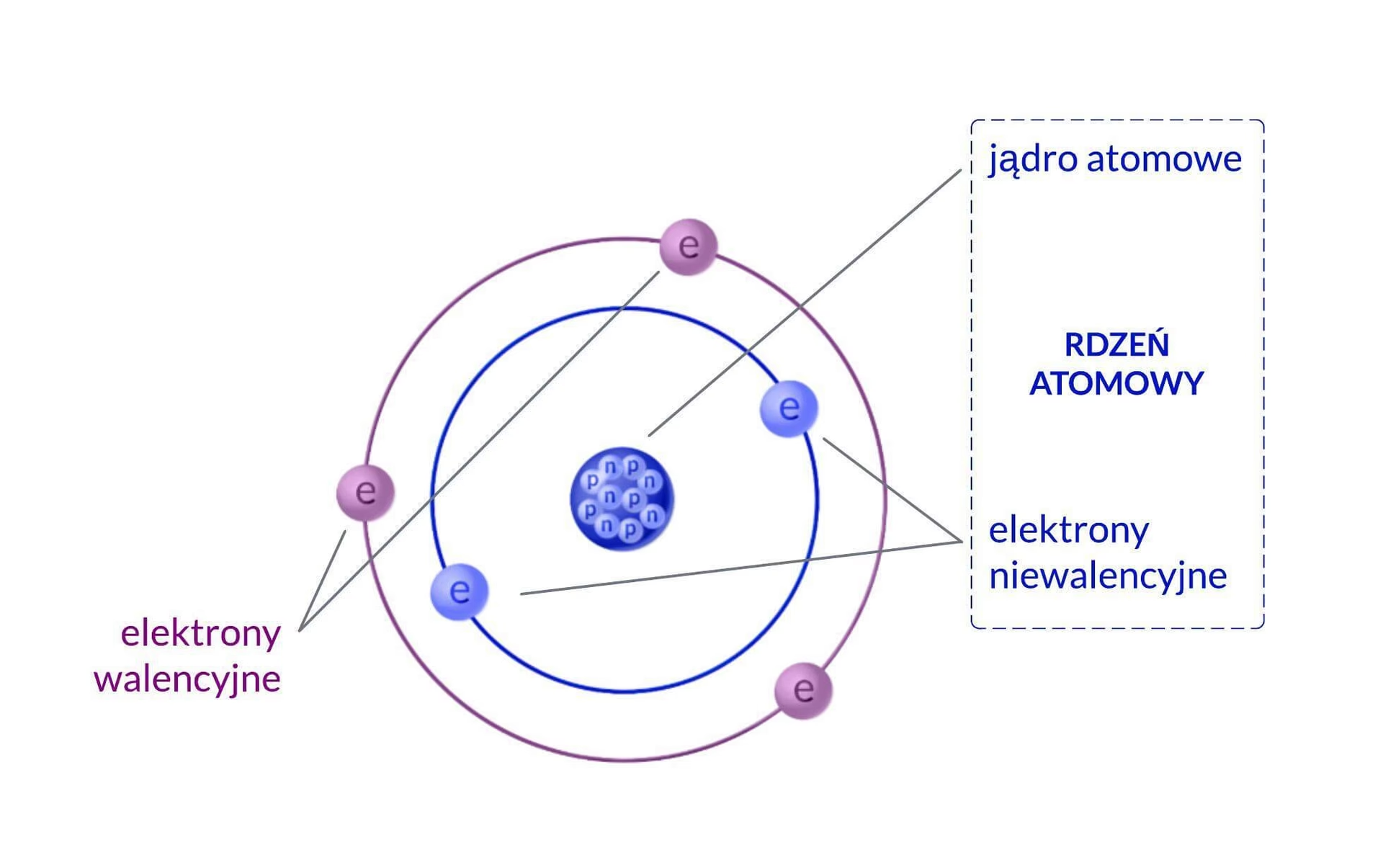
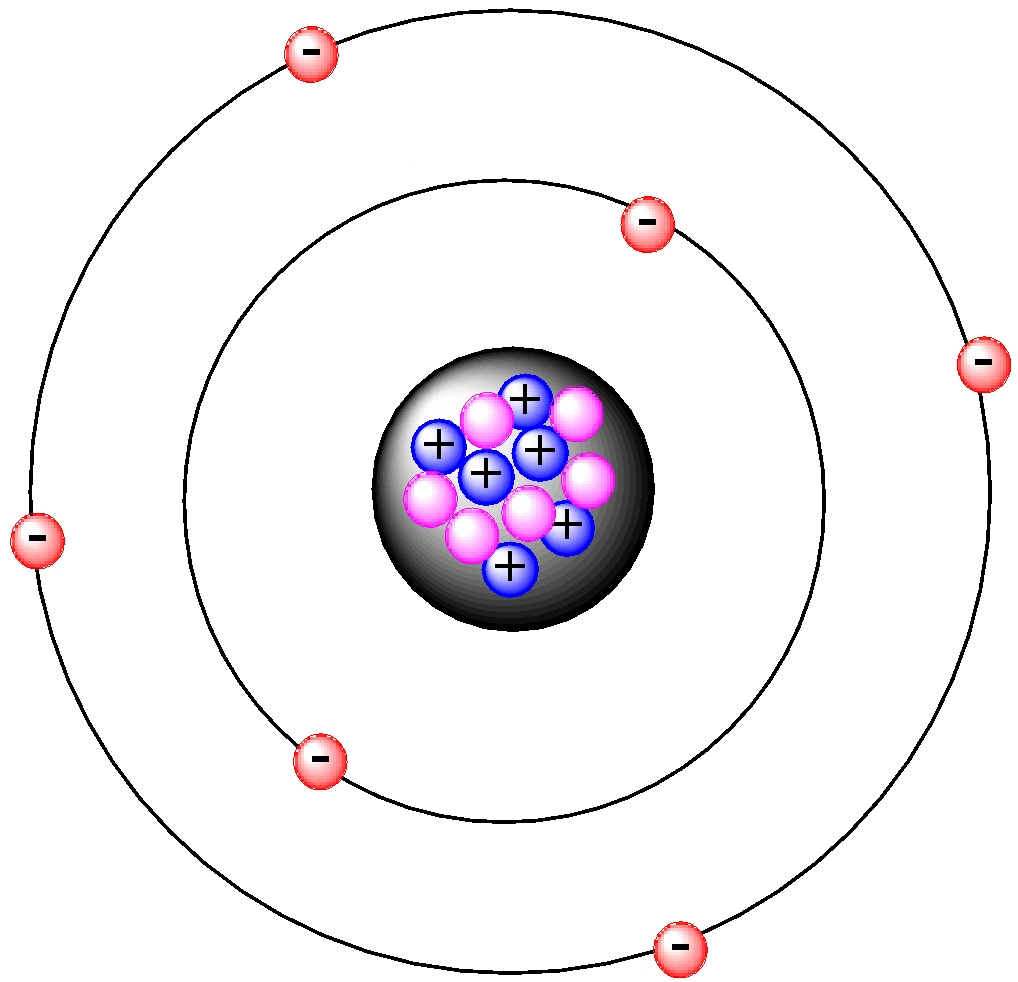
Dziś wiemy, że atomy nie są jednorodne i niepodzielne. Wręcz przeciwnie, posiadają złożoną wewnętrzną budowę. W samym centrum każdego atomu znajduje się niezwykle małe, ale gęste jądro atomowe. Wokół tego jądra, w różnych kierunkach i z ogromną prędkością, poruszają się ujemnie naładowane cząstki, zwane elektronami. Tworzą one coś, co nazywamy chmurą elektronową, która zajmuje znacznie większą przestrzeń niż samo jądro. Aby uświadomić sobie skalę, wyobraźmy sobie, że gdyby jądro powiększyć do rozmiarów małej monety, cały atom miałby przekrój wielkości stadionu sportowego – to pokazuje, jak wiele pustej przestrzeni jest w atomie!
Jądro atomowe: Serce atomu
Samo jądro atomu również ma złożoną budowę. Składa się ono z dwóch rodzajów cząstek: dodatnio naładowanych protonów oraz cząstek pozbawionych ładunku, czyli neutronów. Protony i neutrony, ze względu na to, że znajdują się w jądrze, określa się wspólną nazwą nukleony. To właśnie w jądrze skupiona jest niemal cała masa atomu. Protony i neutrony są utrzymywane razem przez niezwykle silne siły jądrowe, najsilniejsze znane w przyrodzie, które działają na bardzo krótkich dystansach.
Elektrony i chmura elektronowa: Orbity wokół jądra
Elektrony to cząstki o ładunku ujemnym, krążące wokół jądra w określonych obszarach zwanych powłokami elektronowymi. Każdy atom jest elektrycznie obojętną drobiną, co oznacza, że jego ładunki ujemne i dodatnie równoważą się. W praktyce oznacza to, że liczba protonów w jądrze atomu jest zawsze równa liczbie elektronów krążących wokół niego. Liczba neutronów nie wpływa na ładunek atomu ani na jego przynależność do danego pierwiastka.
Poniższa tabela przedstawia podstawowe właściwości cząstek wchodzących w skład atomu:
| Nazwa | Symbol | Ładunek | Miejsce w atomie | Masa [u] |
|---|---|---|---|---|
| Elektron | e- | -1 | Obszar poza jądrem | ~1/1837 |
| Proton | p+ | +1 | Jądro | ~1 |
| Neutron | n | 0 | Jądro | ~1 |
Warto zauważyć, że ujemny ładunek elektronu i dodatni ładunek protonu mają tę samą wartość bezwzględną, różnią się tylko znakiem. Ładunek elektronu jest uznawany za elementarny ładunek ujemny, a protonu za elementarny ładunek dodatni. Masa elektronu jest znikoma w porównaniu do masy protonu i neutronu, dlatego niemal cała masa atomu skupiona jest w jego jądrze.
Ciekawostka: Czy składniki atomu są niepodzielne?
Choć atomy uważano kiedyś za niepodzielne, a następnie odkryto ich składowe (protony, neutrony, elektrony), współczesna fizyka poszła jeszcze dalej. Obecny stan wiedzy mówi nam, że elementarnymi składnikami materii są dwa rodzaje cząstek: leptony i kwarki. Elektron należy do leptonów i jest uważany za cząstkę niepodzielną, bez wewnętrznej struktury. Natomiast protony i neutrony, czyli nukleony, są zbudowane z mniejszych cząstek – kwarków. Naukowcy zidentyfikowali sześć rodzajów kwarków, którym nadano zabawne nazwy: górny (u), dolny (d), dziwny (s), powabny (c), niski (spodni) (b) i wysoki (t). Kwarki nie istnieją samodzielnie w przyrodzie; występują zawsze w grupach, tworząc inne cząstki. Dwa z nich – kwarki górny i dolny – są podstawowymi budulcami protonów i neutronów (proton składa się z dwóch kwarków górnych i jednego dolnego, a neutron z jednego górnego i dwóch dolnych).
Opisywanie atomów: Liczby atomowa i masowa
Aby jednoznacznie opisać atom danego pierwiastka, chemicy używają dwóch kluczowych liczb: liczby atomowej i liczby masowej. Jest to uniwersalny sposób zapisu, który pozwala szybko określić skład jądra atomowego i liczbę elektronów.
- Liczba atomowa (Z): Jest to liczba protonów w jądrze atomu. Ponieważ atom jest elektrycznie obojętny, liczba atomowa Z jest również równa liczbie elektronów krążących wokół jądra. To właśnie liczba atomowa decyduje o tożsamości pierwiastka – każdy pierwiastek ma unikalną liczbę protonów. Na przykład, każdy atom węgla ma Z=6, a każdy atom tlenu Z=8.
- Liczba masowa (A): Jest to suma liczby protonów i liczby neutronów w jądrze atomu (czyli liczba wszystkich nukleonów). Liczba masowa mówi nam o przybliżonej masie atomu, wyrażonej w atomowych jednostkach masy.
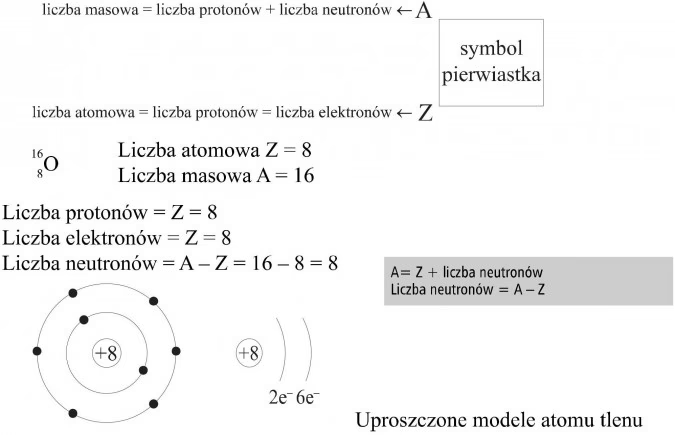
Te dwie liczby umieszcza się w odpowiedniej kolejności i miejscu przy symbolu pierwiastka. Z lewej strony symbolu, w indeksie górnym, umieszcza się liczbę masową A, a w indeksie dolnym – liczbę atomową Z. Ogólny zapis wygląda następująco: AEZ, gdzie E to symbol pierwiastka.
Poniżej przedstawiono przykłady opisu atomów wybranych pierwiastków za pomocą liczb A i Z:
| Nazwa pierwiastka | Symbol pierwiastka | Liczba protonów w jądrze (Z) | Liczba neutronów w jądrze | Liczba elektronów | Liczba masowa (A) | Zapis |
|---|---|---|---|---|---|---|
| Wodór | H | 1 | 0 | 1 | 1 | 1H1 |
| Tlen | O | 8 | 8 | 8 | 16 | 16O8 |
| Wapń | Ca | 20 | 20 | 20 | 40 | 40Ca20 |
| Srebro | Ag | 47 | 60 | 47 | 107 | 107Ag47 |
Dzięki temu zapisowi możemy łatwo obliczyć liczbę neutronów w atomie, odejmując liczbę atomową (Z) od liczby masowej (A). Na przykład, dla atomu srebra (107Ag47): liczba neutronów = A - Z = 107 - 47 = 60.
Masa i rozmiar atomów: Jednostka atomowa masy
Atomy są niewyobrażalnie małe, zarówno pod względem rozmiaru, jak i masy. Ich średnice to wielkości rzędu miliardowej części metra (10-9 m, czyli nanometry), a ich masy stanowią niewyobrażalnie małą część grama (rzędu 10-24 g). Dla porównania, najlżejszy atom wodoru ma masę około 1,66 × 10-24 g, a jego promień wynosi zaledwie 30 pikometrów (pm). Najcięższy z naturalnie występujących na Ziemi atomów, atom uranu, ma masę około 3,95 × 10-22 g i promień równy 138 pm. Manipulowanie tak małymi liczbami w codziennych obliczeniach chemicznych byłoby niezwykle niewygodne i podatne na błędy.
Dlatego chemicy wprowadzili specjalną jednostkę do opisu masy atomów, zwaną atomową jednostką masy lub unitem, oznaczaną symbolem u. Wartość jednego unitu wynosi dokładnie 1,66 × 10-24 g. Masę atomu pierwiastka wyrażoną za pomocą tej jednostki nazywa się masą atomową. Na przykład, masa atomowa wodoru wynosi około 1 u, co oznacza, że jego rzeczywista masa to 1,66 × 10-24 g.
Obliczanie masy atomowej
Przeliczanie mas atomowych między gramami a unitami jest proste i niezbędne w chemii:
- Przeliczanie masy z gramów na unity: Aby wyrazić masę atomu w unitach, należy podzielić jego masę wyrażoną w gramach przez wartość jednego unitu.
Przykład: Wyraź masę atomu helu w atomowych jednostkach masy, jeśli masa atomu helu wynosi 6,644 × 10-24 g.
Masa atomowa helu [u] = (Masa atomu helu [g]) / (1 u [g])
Masa atomowa helu [u] = (6,644 × 10-24 g) / (1,66 × 10-24 g/u) ≈ 4,002 u
Otrzymany wynik, około 4 u, jest masą atomową helu.
- Przeliczanie masy z unitów na gramy: Aby obliczyć rzeczywistą masę atomu w gramach, należy pomnożyć jego masę atomową wyrażoną w unitach przez wartość jednego unitu w gramach.
Przykład: Oblicz, jaka jest masa jednego atomu węgla wyrażona w gramach, jeśli jego masa atomowa wynosi 12 u.
Masa atomu węgla [g] = (Masa atomowa węgla [u]) × (1 u [g])
Masa atomu węgla [g] = 12 u × 1,66 × 10-24 g/u = 19,92 × 10-24 g
Otrzymujemy wynik - masę atomu węgla wyrażoną w gramach.
Masy cząstek subatomowych również można wyrazić w atomowych jednostkach masy. Jak już wspomniano, proton i neutron ważą około 1 u, natomiast masa elektronu jest znacznie, bo około 1837 razy, mniejsza od masy protonu i neutronu, co czyni ją pomijalną w większości obliczeń masy atomu.
Konfiguracja elektronowa i zasady jej ustalania
Zrozumienie, w jaki sposób elektrony rozmieszczają się wokół jądra atomowego, jest kluczowe dla przewidywania właściwości chemicznych pierwiastków. Konfiguracja elektronowa to standardowy zapis opisujący strukturę elektronową atomu lub jonu. Opiera się na koncepcji orbitali, czyli obszarów, w których prawdopodobieństwo znalezienia elektronu jest największe.
Liczby kwantowe: Adres elektronu w atomie
Położenie i energię elektronu w atomie opisuje się za pomocą czterech liczb kwantowych. Można je traktować jako „adres” elektronu w atomie:
- Główna liczba kwantowa (n): Określa powłokę elektronową lub poziom energetyczny, na którym znajduje się elektron. Przyjmuje wartości dodatnie całkowite (1, 2, 3...). Wyższa wartość 'n' oznacza większą odległość od jądra i wyższą energię.
- Poboczna (orbitalna) liczba kwantowa (l): Wskazuje podpowłokę elektronową, a także kształt orbitalu. Przyjmuje wartości od 0 do n-1. Odpowiada typom orbitali: 0 dla orbitalu s (kulisty), 1 dla orbitalu p (kształt hantli), 2 dla orbitalu d, 3 dla orbitalu f itd.
- Magnetyczna liczba kwantowa (ml): Określa orientację przestrzenną orbitalu w danej podpowłoce. Dla danej wartości 'l', ml może przyjmować wartości od -l do +l. Na przykład, dla podpowłoki p (l=1) istnieją trzy orbitale (ml = -1, 0, +1), które odpowiadają orientacjom px, py, pz.
- Magnetyczna spinowa liczba kwantowa (ms): Opisuje spin elektronu, czyli jego wewnętrzny moment pędu. Może przyjmować tylko dwie wartości: +1/2 lub -1/2. Każdy orbital może pomieścić maksymalnie dwa elektrony, ale muszą one mieć przeciwne spiny.
W atomach wieloelektronowych energia elektronu jest determinowana zarówno przez główną liczbę kwantową (n), jak i poboczną liczbę kwantową (l), co odróżnia je od uproszczonego modelu atomu wodoru Bohra.
Ogólne zasady ustalania konfiguracji elektronowej
Istnieją trzy kluczowe zasady, które regulują rozmieszczenie elektronów w orbitalach atomu:
Każdy orbital, niezależnie od typu (s, p, d, f), może być zajęty przez maksymalnie dwa elektrony, pod warunkiem, że mają one przeciwne spiny. Poniższa tabela przedstawia maksymalną liczbę elektronów w poszczególnych podpowłokach:
| Podpowłoka | Liczba orbitali | Maksymalna liczba elektronów |
|---|---|---|
| s | 1 | 2 |
| p | 3 | 6 |
| d | 5 | 10 |
| f | 7 | 14 |
Zasada Aufbau (zasada budowania)
Zasada Aufbau (z niemieckiego „budowanie”) mówi, że elektrony zajmują orbitale w kolejności wzrastającej energii. Oznacza to, że najpierw zapełniane są orbitale o niższej energii, zanim elektrony zaczną zajmować te o wyższej energii. Kolejność zapełniania orbitali jest następująca: 1s < 2s < 2p < 3s < 3p < 4s < 3d < 4p < 5s < 4d < 5p < 6s < 4f < 5d < 6p < 7s < 5f < 6d < 7p. Ta kolejność, choć wydaje się skomplikowana, wynika z minimalizacji energii całego atomu. Istnieją jednak nieliczne wyjątki od tej zasady, np. dla chromu (Cr) i miedzi (Cu), gdzie pełne lub w połowie zapełnione podpowłoki d są bardziej stabilne.
Reguła Hunda (reguła maksymalnej multipletowości)
Reguła Hunda dotyczy orbitali zdegenerowanych, czyli tych, które mają taką samą energię (np. trzy orbitale p: px, py, pz). Mówi ona, że elektrony, zanim zaczną się parować w jednym orbitalu, muszą najpierw pojedynczo zająć wszystkie dostępne orbitale zdegenerowane, a ich spiny muszą być równoległe. Dopiero po pojedynczym zapełnieniu wszystkich orbitali w danej podpowłoce, elektrony zaczynają się parować, zajmując orbitale z przeciwnym spinem. Na przykład, atom azotu (Z=7) ma 3 elektrony walencyjne w podpowłoce 2p. Zgodnie z regułą Hunda, każdy z tych trzech elektronów zajmie inny orbital 2p (2px, 2py, 2pz), zanim jakikolwiek orbital zostanie podwójnie obsadzony.

Zasada wykluczenia Pauliego
Zasada wykluczenia Pauliego, sformułowana przez Wolfganga Pauliego, jest jedną z fundamentalnych zasad mechaniki kwantowej. Stanowi ona, że w jednym atomie nie mogą istnieć dwa elektrony, które miałyby identyczny zestaw wszystkich czterech liczb kwantowych (n, l, ml, ms). Ta zasada ma kluczowe znaczenie dla zrozumienia, dlaczego orbital może pomieścić maksymalnie dwa elektrony: jeśli dwa elektrony zajmują ten sam orbital (mają identyczne n, l i ml), muszą mieć różne wartości spinowej liczby kwantowej (ms), czyli przeciwne spiny (+1/2 i -1/2).
Konfiguracje elektronowe jonów (kationów i anionów)
Konfiguracje elektronowe jonów (atomów naładowanych elektrycznie) ustala się, dodając lub usuwając elektrony z konfiguracji obojętnego atomu, zgodnie z zasadami Aufbau, Hunda i Pauliego.
- Kationy (jony dodatnie): Powstają przez utratę elektronów. Elektrony usuwa się najpierw z orbitali o najwyższej głównej liczbie kwantowej (n), zaczynając od podpowłok p, następnie s, a na końcu d. Na przykład, obojętny atom wapnia (Ca, Z=20) ma konfigurację 1s22s22p63s23p64s2. Jon wapnia Ca2+ powstaje przez utratę dwóch elektronów, które są usuwane z orbitalu 4s (najwyższe n). Konfiguracja Ca2+ to 1s22s22p63s23p6, co jest identyczne z konfiguracją argonu (Ar). Mówimy, że Ca2+ i Ar są izoelektronowe.
- Aniony (jony ujemne): Powstają przez przyjęcie elektronów. Elektrony dodaje się zgodnie z zasadą Aufbau, zapełniając kolejno dostępne orbitale. Na przykład, obojętny atom chloru (Cl, Z=17) ma konfigurację 1s22s22p63s23p5. Jon chlorkowy Cl- powstaje przez przyjęcie jednego elektronu, który zapełnia częściowo obsadzoną podpowłokę 3p. Konfiguracja Cl- to 1s22s22p63s23p6, co również jest izoelektronowe z argonem i jonem Ca2+.
Czym jest dyfuzja?
Atomy i cząsteczki, niezależnie od stanu skupienia materii, są w ciągłym, chaotycznym ruchu. Ten ruch prowadzi do zjawiska zwanego dyfuzją, które definiujemy jako samorzutne mieszanie się cząsteczek. Jest to proces, w którym cząsteczki przemieszczają się z obszaru o wyższym stężeniu do obszaru o niższym stężeniu, aż do osiągnięcia równomiernego rozkładu w całej dostępnej przestrzeni.
Doskonałym przykładem dyfuzji jest rozprzestrzenianie się zapachu perfum w pomieszczeniu. Cząsteczki perfum, początkowo skoncentrowane w butelce, uwalniają się do powietrza i chaotycznie zderzają się z cząsteczkami powietrza, stopniowo rozprzestrzeniając się po całym pokoju. Podobnie, gdy wrzucimy kroplę barwnika do szklanki wody, barwnik powoli, ale nieustannie rozchodzi się po całej objętości wody, aż do momentu, gdy cała woda przyjmie jednolity kolor. Dyfuzja jest procesem ciągłym i zachodzi dopóki istnieją różnice w stężeniu.
Szybkość dyfuzji zależy od kilku czynników, z których najważniejsze to temperatura i stan skupienia substancji:
- Temperatura: Im wyższa temperatura, tym większa energia kinetyczna cząsteczek, co oznacza, że poruszają się one szybciej i częściej zderzają, przyspieszając proces dyfuzji.
- Stan skupienia: Dyfuzja zachodzi najszybciej w gazach, gdzie cząsteczki mają największą swobodę ruchu i duże odległości między sobą. Wolniej zachodzi w cieczach, a najwolniej w ciałach stałych, gdzie cząsteczki są ściśle upakowane i mają ograniczoną możliwość przemieszczania się.
Dyfuzja odgrywa kluczową rolę w wielu procesach naturalnych i codziennych. Dzięki niej tlen z powietrza dostaje się do naszych płuc, a składniki odżywcze z pożywienia są transportowane do komórek. W świecie roślin dyfuzja umożliwia transport wody i soli mineralnych z korzeni do liści. Jest to fundamentalne zjawisko, które choć często niedostrzegane, jest nieodłącznym elementem funkcjonowania materii.
Podsumowanie
Nasza podróż przez mikroświat atomów pozwoliła nam zrozumieć fundamentalne zasady, które rządzą budową materii. Oto kluczowe wnioski:
- Atom to podstawowy element materii, zachowujący właściwości danego pierwiastka chemicznego.
- Atom składa się z centralnego jądra atomowego oraz krążących wokół niego ujemnie naładowanych elektronów.
- Jądro atomowe jest niezwykle gęste i skupia niemal całą masę atomu; składa się z dodatnio naładowanych protonów i elektrycznie obojętnych neutronów, wspólnie nazywanych nukleonami.
- Atom jest elektrycznie obojętny, co oznacza, że liczba protonów jest równa liczbie elektronów.
- Atomy opisuje się za pomocą liczby atomowej (Z), która wskazuje liczbę protonów (i elektronów), oraz liczby masowej (A), będącej sumą protonów i neutronów. Zapis to AEZ.
- Do wyrażania mas atomów używa się atomowej jednostki masy (unit, u), gdzie 1 u = 1,66 × 10-24 g.
- Rozmieszczenie elektronów w atomie opisuje konfiguracja elektronowa, ustalana za pomocą czterech liczb kwantowych (n, l, ml, ms) i trzech zasad: zasady Aufbau, reguły Hunda oraz zasady wykluczenia Pauliego.
- Atomy i cząsteczki są w ciągłym ruchu, co prowadzi do zjawiska dyfuzji – samorzutnego mieszania się cząsteczek, którego szybkość zależy od temperatury i stanu skupienia.
Zrozumienie budowy atomu i praw, które nim rządzą, jest kluczowe dla dalszego zgłębiania tajników chemii i fizyki, otwierając drzwi do fascynującego świata na poziomie molekularnym i subatomowym.
Często zadawane pytania (FAQ)
- Czy atomy można zobaczyć gołym okiem?
- Nie, atomy są zbyt małe, aby zobaczyć je gołym okiem. Ich obserwacja jest możliwa tylko za pomocą bardzo specjalistycznych urządzeń, takich jak skaningowy mikroskop tunelowy (STM) lub mikroskop elektronowy.
- Czy wszystkie atomy są takie same?
- Nie, istnieją różne rodzaje atomów, które nazywamy pierwiastkami chemicznymi. Różnią się one przede wszystkim liczbą protonów w jądrze (liczbą atomową Z). Na przykład atom wodoru ma 1 proton, atom tlenu ma 8 protonów, a atom złota ma 79 protonów. Ta liczba decyduje o tożsamości chemicznej pierwiastka.
- Jak obliczyć liczbę protonów, neutronów i elektronów w atomie?
- Liczbę protonów (Z) odczytujemy z liczby atomowej. Liczba elektronów w obojętnym atomie jest zawsze równa liczbie protonów (Z). Liczbę neutronów obliczamy, odejmując liczbę atomową (Z) od liczby masowej (A): liczba neutronów = A - Z.
- Czym jest nukleon?
- Nukleon to ogólne określenie dla cząstek znajdujących się w jądrze atomowym, czyli protonów i neutronów.
- Czy atomy mogą się łączyć tylko ze sobą?
- Atomy rzadko występują pojedynczo w przyrodzie. Zazwyczaj łączą się ze sobą, tworząc cząsteczki. Mogą łączyć się z atomami tego samego rodzaju (np. dwa atomy tlenu tworzą cząsteczkę tlenu O2) lub z atomami różnych rodzajów (np. dwa atomy wodoru i jeden atom tlenu tworzą cząsteczkę wody H2O). Te połączenia tworzą różnorodność materii, którą obserwujemy.
Zainteresował Cię artykuł Budowa i Obliczanie Atomu: Przewodnik? Zajrzyj też do kategorii Chemia, znajdziesz tam więcej podobnych treści!