11/03/2011
Atom helu, choć wydaje się prosty, stanowi jeden z najbardziej fascynujących obiektów badań w świecie fizyki kwantowej. Jest to najlżejszy z gazów szlachetnych i drugi najpowszechniejszy pierwiastek we wszechświecie. Jego unikalna struktura, będąca pomostem między fundamentalnym atomem wodoru a bardziej złożonymi układami wieloelektronowymi, czyni go idealnym modelem do testowania teorii mechaniki kwantowej. Zrozumienie budowy atomu helu to klucz do pojęcia podstawowych zasad rządzących materią na poziomie subatomowym, a także do wyjaśnienia jego niezwykłych właściwości chemicznych i fizycznych.
Podstawy Budowy Atomu Helu
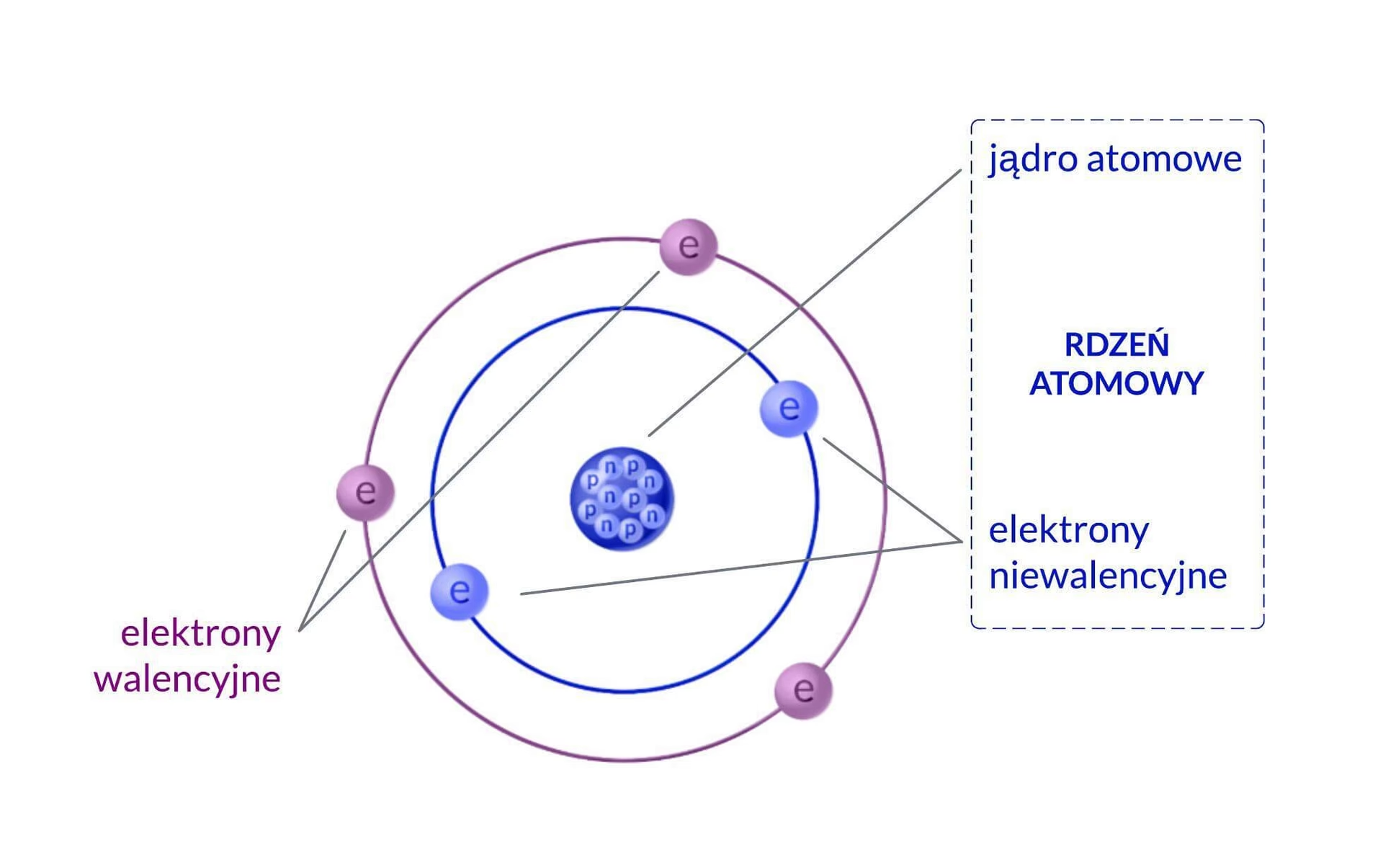
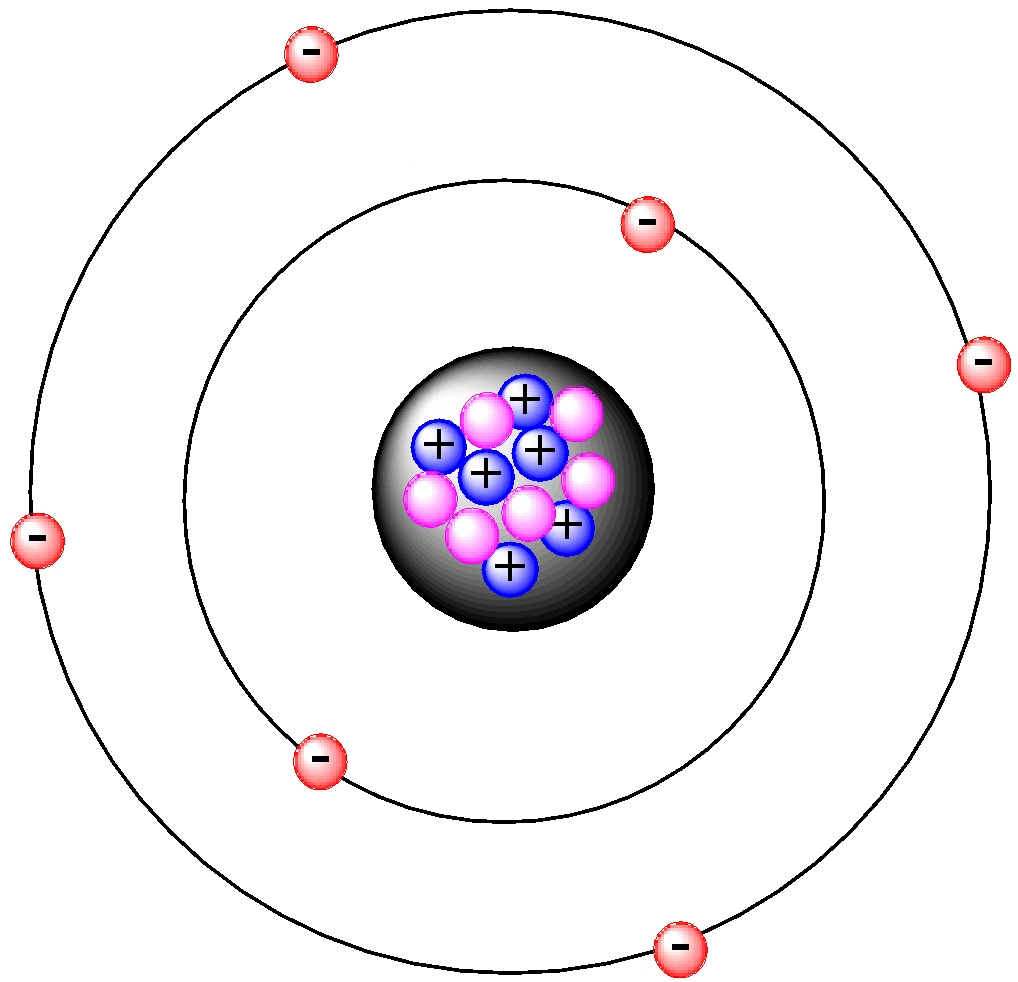
Atom helu (He) jest niezwykle prosty w swojej strukturze. W jego jądrze atomowym, dla najpowszechniejszego izotopu helu-4 (⁴He), znajdują się dwa protony i dwa neutrony. Protony nadają jądru ładunek dodatni (+2e), a neutrony zapewniają stabilność poprzez siły jądrowe, które przezwyciężają odpychanie elektrostatyczne między protonami. Wokół tego dodatnio naładowanego jądra krążą dwa elektrony. To właśnie te dwa elektrony, poruszające się w przestrzeni wokół jądra, decydują o wszystkich chemicznych i wielu fizycznych właściwościach atomu helu.
Elektrony w atomie helu są związane z jądrem siłami elektrostatycznymi, podobnie jak w innych atomach. Jednak ze względu na obecność dwóch elektronów, ich wzajemne oddziaływania (odpychanie elektrostatyczne) komplikują teoretyczny opis systemu, sprawiając, że niemożliwe jest uzyskanie dokładnego analitycznego rozwiązania równania Schrödingera, co jest możliwe dla atomu wodoru. To właśnie ta prostota, połączona z koniecznością uwzględnienia oddziaływań międzyelektronowych, czyni atom helu tak ważnym dla rozwoju metod obliczeniowych w chemii kwantowej i fizyce.
Stan Podstawowy Atomu Helu: Konfiguracja 1s²
Stan podstawowy atomu helu to najbardziej stabilny i najniższy energetycznie stan, w którym elektrony mogą się znajdować. Zgodnie z zasadami mechaniki kwantowej, elektrony zajmują dostępne orbitale w kolejności rosnącej energii. Dla atomu helu, oba elektrony zajmują najniższy dostępny orbital, czyli orbital 1s.
Konfiguracja elektronowa atomu helu w stanie podstawowym jest zapisywana jako 1s². Oznacza to, że:
- Cyfra '1' wskazuje, że elektrony znajdują się na pierwszej powłoce elektronowej (n=1), czyli najbliżej jądra.
- Litera 's' oznacza, że elektrony zajmują orbital s, który ma kształt sferyczny.
- Górny indeks '2' informuje, że na tym orbitalu znajdują się dwa elektrony.
Zgodnie z zasadą Pauliego, dwa elektrony mogą zajmować ten sam orbital tylko wtedy, gdy posiadają przeciwne spiny (jeden spin 'w górę', drugi 'w dół'). Dzięki temu, że oba elektrony w atomie helu zajmują orbital 1s, jego zewnętrzna powłoka elektronowa jest całkowicie zapełniona. Ta pełna powłoka sprawia, że atom helu jest niezwykle stabilny i chemicznie obojętny, co jest charakterystyczne dla gazów szlachetnych. Jest to powód, dla którego hel nie tworzy łatwo wiązań chemicznych z innymi pierwiastkami i występuje w naturze jako pojedyncze atomy, a nie cząsteczki.
Stany Wzbudzone Atomu Helu: Więcej Niż Tylko 1s²
Atom helu, podobnie jak inne atomy, może znajdować się w stanach wzbudzonych. Stany wzbudzone powstają, gdy atom absorbuje energię (na przykład w postaci fotonu lub w wyniku zderzenia) i jeden z jego elektronów przeskakuje na wyższy poziom energetyczny, czyli na orbital o wyższej energii.
Pierwsze stany wzbudzone atomu helu powstają, gdy jeden elektron pozostaje na orbitalu 1s, a drugi przeskakuje na orbital o wyższej energii, np. 2s lub 2p. Przykłady konfiguracji elektronowych dla pierwszych stanów wzbudzonych to:
- 1s2s: Jeden elektron znajduje się na orbitalu 1s, a drugi na orbitalu 2s.
- 1s2p: Jeden elektron znajduje się na orbitalu 1s, a drugi na orbitalu 2p.
Istnieją oczywiście dalsze stany wzbudzone, takie jak 1s3s, 1s3p, 1s3d itd., gdzie elektron przeskakuje na jeszcze wyższe powłoki i podpowłoki. Stany wzbudzone są z natury niestabilne. Elektrony w tych stanach mają tendencję do powrotu na niższe poziomy energetyczne, aż do stanu podstawowego. Kiedy elektron wraca na niższy poziom, emituje nadmiar energii w postaci fotonu o określonej długości fali. To właśnie emisja tych fotonów odpowiada za charakterystyczne linie spektralne helu, które są wykorzystywane w spektroskopii do identyfikacji tego pierwiastka, np. w badaniach gwiazd.
Co ciekawe, stany wzbudzone helu dzielą się na dwie główne serie, zwane stanami singletowymi (parahelium) i tripletowymi (orthohelium), w zależności od orientacji spinów dwóch elektronów. W stanach singletowych spiny elektronów są sparowane (przeciwne), natomiast w stanach tripletowych spiny są niesparowane (równoległe). Przejścia między tymi dwoma typami stanów są zabronione lub bardzo mało prawdopodobne, co prowadzi do odrębnych zestawów linii spektralnych dla każdego typu.
Znaczenie Atomu Helu w Fizyce Kwantowej
Atom helu, ze względu na swoją prostotę (tylko dwa elektrony) i jednocześnie złożoność (konieczność uwzględnienia oddziaływań między tymi dwoma elektronami), stanowi fundamentalne laboratorium dla fizyków kwantowych. Jest to najprostszy układ, dla którego nie można znaleźć dokładnego analitycznego rozwiązania równania Schrödingera, co zmusza do stosowania metod przybliżonych.
Badania nad atomem helu były kluczowe dla rozwoju wielu technik obliczeniowych w chemii kwantowej, takich jak metoda wariacyjna, teoria perturbacji czy metoda Hartree-Focka i późniejsze metody post-Hartree-Focka. Precyzyjne obliczenia energii i funkcji falowych atomu helu, a także jego spektrum, służą jako punkt odniesienia do testowania dokładności tych metod. Zrozumienie, jak elektrony oddziałują ze sobą w tak prostym systemie, jest niezbędne do ekstrapolacji tej wiedzy na bardziej złożone atomy i cząsteczki.
Izotopy Helu
Choć najczęściej mówimy o helu-4 (⁴He) z dwoma protonami i dwoma neutronami, hel posiada również inne izotopy:
- Hel-3 (³He): Posiada dwa protony i tylko jeden neutron w jądrze. Jest to rzadki izotop, ale ma unikalne właściwości fizyczne, takie jak nadciekłość w bardzo niskich temperaturach, co czyni go obiektem intensywnych badań w fizyce materii skondensowanej.
- Hel-5 (⁵He): Bardzo niestabilny izotop z dwoma protonami i trzema neutronami. Rozpada się w ułamku sekundy.
- Hel-6 (⁶He): Również niestabilny, z dwoma protonami i czterema neutronami.
Wszystkie te izotopy posiadają tę samą liczbę elektronów (dwa), co oznacza, że ich konfiguracja elektronowa w stanie podstawowym jest zawsze 1s². Różnice w liczbie neutronów wpływają głównie na masę atomową i stabilność jądra, a w mniejszym stopniu na właściwości chemiczne, które są zdeterminowane przez elektrony.
Porównanie Atomu Helu z Innymi Atomami
Aby lepiej zrozumieć unikalność helu, warto porównać go z sąsiednimi pierwiastkami w układzie okresowym:
| Atom | Liczba protonów | Liczba elektronów | Konfiguracja elektronowa (stan podstawowy) | Właściwości chemiczne |
|---|---|---|---|---|
| Wodór (H) | 1 | 1 | 1s¹ | Bardzo reaktywny, dąży do zapełnienia powłoki (duplet) |
| Hel (He) | 2 | 2 | 1s² | Obojętny chemicznie (pełna powłoka) |
| Lit (Li) | 3 | 3 | 1s²2s¹ | Bardzo reaktywny, dąży do oddania elektronu (oktet) |
Jak widać z tabeli, to właśnie pełna konfiguracja 1s² czyni hel tak wyjątkowym i nieaktywnym chemicznie w porównaniu do wodoru, który dąży do uzyskania konfiguracji helu, czy litu, który łatwo oddaje swój jeden elektron walencyjny, aby uzyskać konfigurację helu.
Często Zadawane Pytania (FAQ)
Ile protonów ma atom helu?
Atom helu zawsze ma dwa protony w swoim jądrze. To liczba protonów (liczba atomowa Z=2) definiuje pierwiastek jako hel.
Dlaczego hel jest gazem szlachetnym?
Hel jest gazem szlachetnym, ponieważ jego zewnętrzna powłoka elektronowa (orbital 1s) jest całkowicie zapełniona dwoma elektronami (konfiguracja 1s²). Ta stabilna konfiguracja sprawia, że atom helu jest chemicznie obojętny i nie ma tendencji do tworzenia wiązań chemicznych z innymi atomami.
Czy atom helu może mieć więcej niż dwa elektrony?
W normalnych warunkach atom helu ma dokładnie dwa elektrony, równoważące ładunek dwóch protonów w jądrze. Teoretycznie można by próbować stworzyć jony helu z dodatkowymi elektronami (np. He⁻), ale byłyby one niezwykle niestabilne i szybko by się rozpadały, ponieważ jądro helu nie jest w stanie stabilnie związać więcej niż dwóch elektronów w stanie podstawowym.
Jak powstają stany wzbudzone atomu helu?
Stany wzbudzone powstają, gdy atom helu absorbuje energię – na przykład poprzez pochłonięcie fotonu o odpowiedniej energii, zderzenie z innym atomem lub cząsteczką, lub w wyniku wyładowania elektrycznego. Ta energia powoduje, że jeden z elektronów przeskakuje na wyższy, niezajęty orbital o wyższej energii.
Jaka jest różnica między stanem 1s2s a 1s2p w atomie helu?
Różnica polega na tym, jaki orbital o wyższej energii zajmuje drugi elektron. W stanie 1s2s, drugi elektron znajduje się na orbitalu 2s, który jest sferyczny. W stanie 1s2p, drugi elektron znajduje się na orbitalu 2p, który ma kształt hantli. Orbitale 2s i 2p mają nieco inne energie, co prowadzi do różnych linii spektralnych podczas deekscytacji.
Podsumowanie
Atom helu, choć pozornie prosty, jest kamieniem węgielnym w zrozumieniu mechaniki kwantowej i budowy materii. Jego budowa, składająca się z jądra z dwoma protonami i dwoma neutronami oraz dwóch elektronów w konfiguracji 1s² w stanie podstawowym, tłumaczy jego niezwykłą stabilność i chemiczną obojętność. Zdolność helu do przechodzenia w stany wzbudzone, takie jak 1s2s czy 1s2p, i emitowania światła podczas powrotu do stanu podstawowego, jest podstawą spektroskopii i pozwala nam badać skład kosmosu.
Jako najprostszy układ wieloelektronowy, hel służy jako kluczowy model do testowania i rozwijania teorii kwantowych. Jego unikalne właściwości fizyczne, takie jak nadciekłość izotopu ³He, dodatkowo podkreślają jego znaczenie w różnych dziedzinach nauki. Zrozumienie atomu helu to nie tylko poznanie pojedynczego pierwiastka, ale także wgląd w fundamentalne zasady, które rządzą całym wszechświatem na poziomie subatomowym.
Zainteresował Cię artykuł Atom Helu: Budowa, Stany i Znaczenie? Zajrzyj też do kategorii Nauka, znajdziesz tam więcej podobnych treści!