07/06/2017
W świecie chemii organicznej, gdzie atomy węgla tworzą niezliczone kombinacje, istnieje szczególna grupa związków znanych jako cykloalkany. Są to molekuły, które zamiast prostych lub rozgałęzionych łańcuchów, układają się w zamknięte pierścienie, nadając im unikalne właściwości i zastosowania. Zrozumienie ich budowy, nazewnictwa i reaktywności jest kluczowe dla każdego, kto zgłębia tajniki chemii. W tym artykule przyjrzymy się cykloalkanom z bliska, odpowiadając na najczęściej zadawane pytania i rozwiewając wszelkie wątpliwości.

Czym są Cykloalkany? Definicja i Charakterystyka
Cykloalkany to rodzaj węglowodorów nasyconych, co oznacza, że w ich cząsteczkach, między atomami węgla w pierścieniu, występują wyłącznie wiązania pojedyncze. Ta cecha odróżnia je od innych węglowodorów, takich jak alkeny czy alkiny, które zawierają wiązania podwójne lub potrójne. Dzięki obecności wyłącznie wiązań pojedynczych, każdy atom węgla w cykloalkanie jest nasycony maksymalną liczbą atomów wodoru, co nadaje im pewną stabilność.
Jedną z kluczowych właściwości cykloalkanów jest ich niska reaktywność. Wynika to z siły wiązań pojedynczych węgiel-węgiel oraz węgiel-wodór. Te silne wiązania sprawiają, że cykloalkany są stosunkowo obojętne chemicznie i rzadko ulegają reakcjom addycji, typowym dla związków nienasyconych. Jednakże, od tej reguły istnieją pewne wyjątki. Mniejsze pierścienie, takie jak cyklopropan (trzy atomy węgla w pierścieniu) czy cyklobutan (cztery atomy węgla), wykazują tak zwane napięcie pierścieniowe. Atomy węgla w tych małych pierścieniach są zmuszone do przyjęcia kątów wiązań znacznie odbiegających od idealnego kąta tetraedrycznego (około 109,5 stopnia), co prowadzi do wewnętrznych naprężeń. To napięcie czyni je bardziej reaktywnymi niż ich większe odpowiedniki, takie jak cykloheksan, który przyjmuje konformację krzesłową, minimalizującą napięcie i sprawiającą, że jest on niezwykle stabilny.
Struktura pierścieniowa cykloalkanów ma również wpływ na ich właściwości fizyczne, takie jak temperatury wrzenia i topnienia, które są zazwyczaj wyższe niż dla odpowiadających im alkanów o otwartym łańcuchu, ze względu na bardziej zwartą budowę i większą powierzchnię kontaktu między cząsteczkami, co prowadzi do silniejszych sił międzycząsteczkowych.
Wzór Ogólny Cykloalkanów i Największy Znany Przedstawiciel
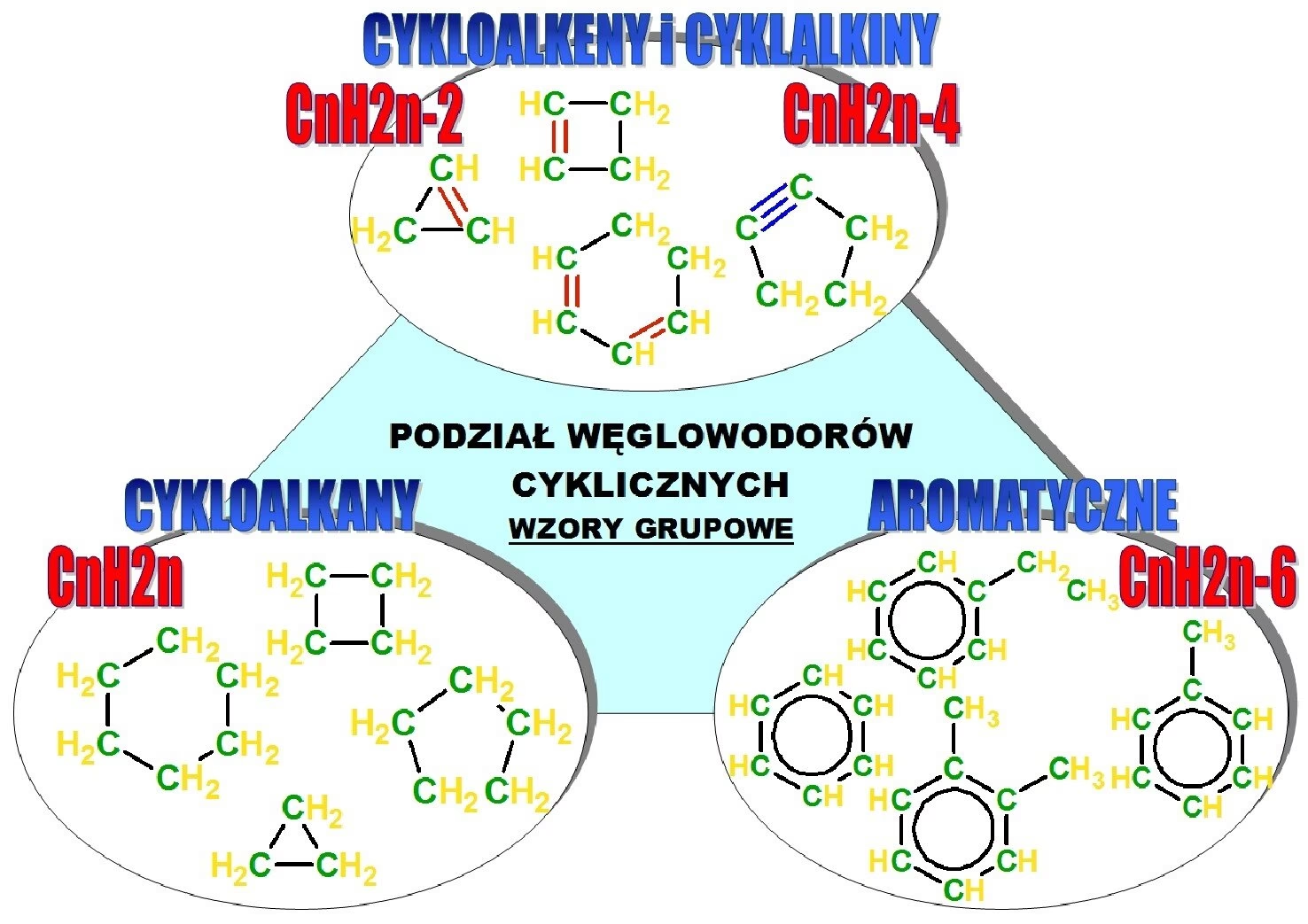
Zrozumienie wzoru sumarycznego jest fundamentalne w chemii organicznej, ponieważ pozwala na szybkie określenie liczby i rodzaju atomów w cząsteczce. Dla cykloalkanów wzór ogólny jest prosty i łatwy do zapamiętania: CnH2n. Wzór ten odzwierciedla cykliczną naturę tych związków.
Dla porównania, alkany (węglowodory nasycone o otwartym łańcuchu) mają wzór ogólny CnH2n+2. Tworzenie jednego pierścienia z łańcucha alkilowego wymaga usunięcia dwóch atomów wodoru (po jednym z każdego końca łańcucha, aby umożliwić zamknięcie pierścienia). Stąd różnica w liczbie atomów wodoru w stosunku do alkanów.
Na przykład:
- Cyklopropan: C3H6 (n=3)
- Cyklobutan: C4H8 (n=4)
- Cyklopentan: C5H10 (n=5)
- Cykloheksan: C6H12 (n=6)
Wzór sumaryczny jest niezwykle przydatny nie tylko do identyfikacji składu związku, ale także, w połączeniu z rozważaniami strukturalnymi, pomaga w zrozumieniu jego właściwości i reakcji. W chemii organicznej, pełne zrozumienie wzorów sumarycznych jest kluczowe do rozwiązywania problemów i klasyfikacji związków.
Jeśli chodzi o największy znany cykloalkan, naukowcy odkryli i scharakteryzowali molekuły o imponujących rozmiarach. Obecnie, największy znany cykloalkan ma wzór sumaryczny C288H576. Ta formuła wskazuje, że w jednej cząsteczce tego cykloalkana znajduje się 288 atomów węgla i 576 atomów wodoru. Jest to przykład niezwykłej zdolności atomów węgla do tworzenia złożonych i rozległych struktur pierścieniowych, co jest podstawą różnorodności związków organicznych.
Nazewnictwo Cykloalkanów: Jak Poprawnie Nazwać Związek?
Systematyczne nazewnictwo związków chemicznych jest kluczowe dla jednoznacznej komunikacji w chemii. Zasady nazewnictwa cykloalkanów opierają się na nomenklaturze IUPAC (International Union of Pure and Applied Chemistry) i są logicznym rozszerzeniem zasad stosowanych dla alkanów. Każdy fragment nazwy dostarcza ważnych informacji o budowie danego związku.
Oto podstawowe zasady nazewnictwa cykloalkanów:
- Podstawa nazwy: Podobnie jak alkany, nazwa cykloalkana zawiera końcówkę „-an”.
- Przedrostek „cyklo-”: Aby wskazać, że atomy węgla są zamknięte w pierścień, dodaje się przedrostek „cyklo-” przed nazwą odpowiadającego mu alkana o tej samej liczbie atomów węgla. Na przykład, sześć atomów węgla w pierścieniu to cykloheksan (od heksanu).
- Wiązania węgiel-węgiel: Przyrostek „-an” oznacza, że między atomami węgla występują wyłącznie wiązania pojedyncze (związek nasycony). Jeśli w pierścieniu pojawiłoby się wiązanie podwójne, przyrostek zmieniłby się na „-en” (cykloalken), a potrójne na „-yn” (cykloalkin).
- Podstawniki alkilowe: Jeśli do pierścienia cykloalkanu są przyłączone grupy alkilowe (np. -CH3, -CH2CH3), ich nazwy otrzymują przyrostek „-ylo” zamiast „-an”. Przykłady:
- -CH3: metylo
- -CH2CH3: etylo
- -CH2CH2CH3: propylo
- -CH2CH2CH2CH3: butylo
- Liczba podstawników: W przypadku wystąpienia więcej niż jednego takiego samego podstawnika, stosuje się przedrostki liczbowe (mnożniki):
Liczba Przedrostek 1 mono- 2 di- 3 tri- 4 tetra- 5 penta- 6 heksa- 7 hepta- 8 okta- 9 nona- 10 deka- - Fluorowce jako podstawniki: Atomy fluorowców (chlor, brom, fluor, jod) również mogą być podstawnikami. Ich nazwy uwzględnia się w nazwie węglowodoru, dodając odpowiedni przedrostek:
- -Br: bromo-
- -Cl: chloro-
- -F: fluoro-
- -I: jodo-
- Numerowanie pierścienia: Jeśli na pierścieniu znajduje się więcej niż jeden podstawnik, należy ponumerować atomy węgla w pierścieniu w taki sposób, aby podstawniki miały jak najniższe numery. Jeśli istnieje kilka możliwości, pierwszeństwo mają podstawniki wymienione alfabetycznie.
Na przykład, 1,2-dimetylocyklopropan to cyklopropan z dwoma grupami metylowymi przyłączonymi do sąsiednich atomów węgla w pierścieniu.
Czy Cykloalkeny Istnieją? Odpowiedź brzmi: Tak!
Tak, cykloalkeny istnieją i są równie ważną klasą związków organicznych jak cykloalkany. Różnica polega na tym, że cykloalkeny zawierają co najmniej jedno wiązanie podwójne w swoim pierścieniu węglowym. Obecność wiązania podwójnego sprawia, że są to węglowodory nienasycone, a ich wzór ogólny dla jednego wiązania podwójnego w pierścieniu to CnH2n-2.
Wiązanie podwójne wprowadza do pierścienia nie tylko dodatkowe nienasycenie, ale także zmienia jego właściwości chemiczne i fizyczne. Cykloalkeny, w przeciwieństwie do cykloalkanów, są znacznie bardziej reaktywne ze względu na możliwość addycji do wiązania podwójnego. Mogą ulegać reakcjom, takim jak uwodornienie (addycja wodoru), halogenowanie (addycja fluorowców) czy hydratacja (addycja wody).

Przykłady cykloalkenów to cyklopropen, cyklobuten, cyklopenten, cykloheksen. Podobnie jak w przypadku cykloalkanów, mniejsze pierścienie cykloalkenów również doświadczają napięcia pierścieniowego, które wpływa na ich stabilność i reaktywność. Na przykład, cyklopropen jest bardzo niestabilny ze względu na duże napięcie pierścienia wynikające z kątów wiązań bliskich 60 stopni, zamiast idealnych 120 stopni dla wiązania podwójnego.
W kontekście elektrochemii, wiązanie alkenowe zazwyczaj nie jest redukowalne w standardowych warunkach. Jednakże, w przypadku, gdy wiązanie alkenowe jest sprzężone z innymi wiązaniami pi (jak w polienach) lub z grupami silnie wyciągającymi elektrony (np. tetrakis(trifluorometylo)eten), ich potencjał redukcyjny może się zmienić, czyniąc je bardziej podatnymi na reakcje redukcji. Konjugacja obniża poziom energetyczny najniższego orbitalu π*, co sprawia, że polieny i fenyleteny stają się redukowalne w dostępnym zakresie potencjałów.
Cykloalkeny typu anty-Hückla, gdzie liczba sprzężonych elektronów π wynosi 4n (gdzie n jest liczbą całkowitą), po redukcji w rozpuszczalnikach aprotycznych przyjmują łącznie dwa elektrony. Powstałe dianiony mają (4n + 2) elektronów π i są stosunkowo stabilne w przypadku braku donorów protonów. Systemy Hückla (4n + 2) są zazwyczaj płaskie, podczas gdy systemy anty-Hückla są zazwyczaj złożone. Przykładem jest cyklooktatetraen, gdzie energia reorganizacji związana ze spłaszczeniem układu pierścieniowego przyczynia się do powolnego transferu elektronów, prowadzącego do powstania rodnika-anionu.
Porównanie Alkanów, Cykloalkanów i Cykloalkenów
Aby lepiej zrozumieć cykloalkany, warto porównać je z innymi, blisko spokrewnionymi grupami węglowodorów. Poniższa tabela przedstawia kluczowe różnice i podobieństwa między alkanami, cykloalkanami i cykloalkenami:
| Cecha | Alkany | Cykloalkany | Cykloalkeny |
|---|---|---|---|
| Struktura | Łańcuchowa (prosta lub rozgałęziona) | Pierścieniowa | Pierścieniowa |
| Wiązania C-C | Wyłącznie pojedyncze | Wyłącznie pojedyncze | Pojedyncze i co najmniej jedno podwójne |
| Nasycenie | Nasycone | Nasycone | Nienasycone |
| Wzór ogólny (dla jednego pierścienia/łańcucha) | CnH2n+2 | CnH2n | CnH2n-2 (dla jednego wiązania podwójnego) |
| Reaktywność | Niska (reakcje substytucji) | Niska (reakcje substytucji, ale małe pierścienie mogą ulegać otwarciu pierścienia) | Wyższa (reakcje addycji do wiązania podwójnego) |
| Przykłady | Metan, etan, propan, butan | Cyklopropan, cyklobutan, cyklopentan, cykloheksan | Cyklopropen, cyklobuten, cyklopenten, cykloheksen |
Najczęściej Zadawane Pytania (FAQ)
Czym różnią się cykloalkany od alkanów?
Główna różnica polega na strukturze: alkany mają otwarte łańcuchy węglowe, podczas gdy cykloalkany mają zamknięte pierścienie. Ta różnica w strukturze prowadzi do odmiennego wzoru ogólnego (alkany CnH2n+2, cykloalkany CnH2n) oraz nieco innych właściwości fizycznych (np. wyższe temperatury wrzenia i topnienia dla cykloalkanów o tej samej liczbie atomów węgla).
Czy cykloalkany są toksyczne?
Większość prostych cykloalkanów, podobnie jak alkanów, jest stosunkowo nietoksyczna. Jednakże, jak w przypadku wszystkich substancji chemicznych, należy zachować ostrożność. Niektóre cykloalkany, zwłaszcza te o mniejszych pierścieniach lub z dodatkowymi grupami funkcyjnymi, mogą wykazywać specyficzne właściwości biologiczne lub toksyczne. Zawsze należy konsultować karty charakterystyki substancji.

Gdzie wykorzystuje się cykloalkany?
Cykloalkany znajdują zastosowanie w wielu dziedzinach. Cykloheksan jest szeroko stosowany jako rozpuszczalnik w przemyśle chemicznym, zwłaszcza do produkcji nylonu. Cyklopentan jest używany jako środek spieniający w produkcji pianek poliuretanowych. Niektóre cykloalkany, w mniejszych ilościach, występują naturalnie w ropie naftowej i są składnikami paliw.
Co to jest napięcie pierścieniowe?
Napięcie pierścieniowe to dodatkowa energia występująca w cyklicznych cząsteczkach, spowodowana odchyleniami od idealnych kątów wiązań i/lub oddziaływań sterycznych między atomami. Jest ono szczególnie wyraźne w małych pierścieniach (cyklopropan, cyklobutan), gdzie atomy węgla są zmuszone do przyjęcia kątów wiązań znacznie mniejszych niż optymalne 109,5° dla sp3 hybrydyzacji, co zwiększa ich reaktywność.
Czy cykloalkany są polarne?
Cykloalkany, podobnie jak alkany, są związkami niepolarnymi. Wiązania węgiel-węgiel i węgiel-wodór są praktycznie niepolarne, a symetryczna struktura pierścienia sprawia, że momenty dipolowe poszczególnych wiązań wzajemnie się znoszą. Dlatego cykloalkany są rozpuszczalne w rozpuszczalnikach niepolarnych (np. benzen, eter), a nierozpuszczalne w wodzie.
Podsumowanie
Cykloalkany to intrygująca i ważna klasa związków organicznych, charakteryzująca się pierścieniową strukturą i nasyconymi wiązaniami. Ich niska reaktywność, z wyjątkiem małych, napiętych pierścieni, oraz specyficzne właściwości fizyczne wynikają bezpośrednio z ich unikalnej budowy. Znajomość wzoru ogólnego CnH2n oraz zasad nazewnictwa pozwala na łatwą identyfikację i klasyfikację tych molekuł.
Co więcej, istnienie cykloalkenów z wiązaniami podwójnymi w pierścieniu otwiera drzwi do świata związków nienasyconych o zwiększonej reaktywności, co podkreśla różnorodność chemii organicznej. Od największych znanych cykloalkanów po najmniejsze, napięte struktury, te pierścieniowe węglowodory odgrywają znaczącą rolę zarówno w naturze, jak i w przemyśle. Ich dalsze badania z pewnością przyniosą nowe odkrycia i zastosowania, pogłębiając naszą wiedzę o podstawowych elementach budulcowych życia.
Zainteresował Cię artykuł Cykloalkany: Zrozumienie Pierścieni Węglowodorów? Zajrzyj też do kategorii Chemia, znajdziesz tam więcej podobnych treści!
