25/10/2024
Czy zastanawiasz się nad tym, jak wygląda mikroświat? Jaki jest kształt drobin, które tworzą materię? Czy można je zobaczyć? Czy są kolorowe? Odpowiedzi na te pytania, choć złożone, leżą u podstaw chemii i fizyki. Zrozumienie budowy atomu to klucz do pojmowania otaczającego nas świata, od najprostszych pierwiastków po złożone związki chemiczne. W tym artykule zgłębimy to, co kiedyś uważano za niepodzielne, a dziś wiemy, że jest niezwykle złożonym i dynamicznym systemem.
Co to jest atom?
Podstawowymi elementami, z których zbudowana jest materia, są atomy. Substancje tworzące świat materialny składają się z różnych atomów. Mają one masę, objętość i kształt. Każdy pierwiastek składa się z atomów tylko jednego rodzaju: żelazo – z atomów żelaza, a złoto – z atomów złota. Choć pojedyncze atomy żelaza i złota są zbudowane z tych samych cząstek, to ich liczba jest inna, co sprawia, że tworzą pierwiastki o odmiennych właściwościach.
Niewielkie rozmiary atomów nie pozwalają nam na oglądanie ich w sposób, w jaki przywykliśmy obserwować otaczający nas świat. Obecnie jednak, dzięki skaningowemu mikroskopowi tunelowemu, możemy dostrzec cienką warstwę atomów unieruchomionych na powierzchni innych ciał stałych. Na otrzymanych za jego pomocą obrazach zobaczyliśmy, że atomy mają kształt kulisty, a ich rozmiary są różne i zależą od rodzaju badanego pierwiastka. Już na początku XIX wieku angielski uczony John Dalton twierdził, że atomy tworzące różne pierwiastki są kulami, które różnią się między sobą wielkością. Co ciekawe, pojęcie „atom” pochodzi z greckiego „átomos”, oznaczającego „niepodzielny”, co odzwierciedlało starożytne przekonanie o ich fundamentalnej, niepodzielnej naturze, choć dziś wiemy, że atomy mają złożoną strukturę wewnętrzną.
W głąb atomu: Jądro i Elektrony
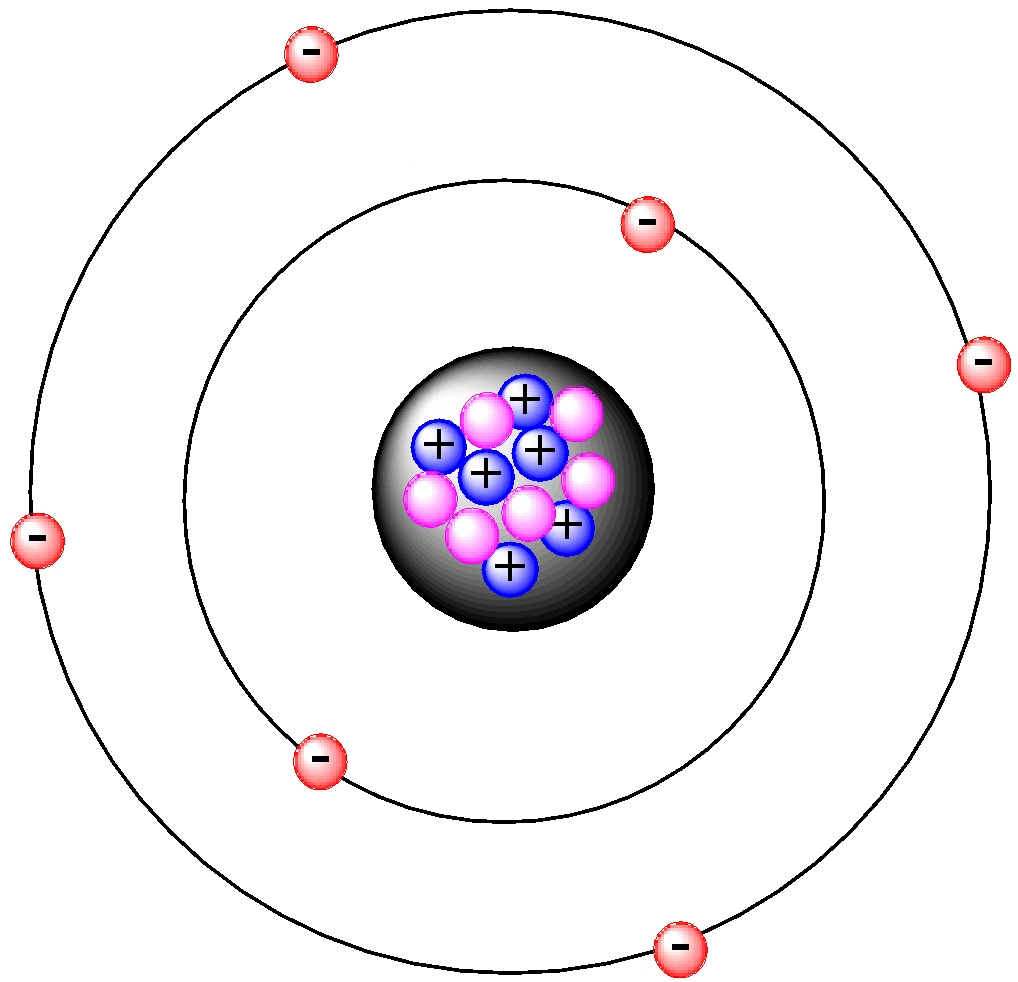
Niemal do końca XIX wieku uważano, że atomy przypominają niewyobrażalnie małe i twarde jak kamień kulki. Dziś już wiemy, że nie są jednorodne i niepodzielne. Okazuje się, że mają złożoną wewnętrzną budowę. W środku każdego atomu, w samym jego centrum, znajduje się jądro atomowe. Poruszające się w różnych kierunkach z dużą szybkością ujemnie naładowane cząstki, zwane elektronami, tworzą chmurę elektronową wokół jądra. Przestrzeń, którą zajmuje jądro atomowe, jest znacznie mniejsza od przestrzeni zajmowanej przez elektrony – średnica atomu jest około 100 000 razy większa od średnicy jądra. Wyobraźmy sobie, że gdyby jądro powiększyć do rozmiarów małej monety, wówczas cały atom byłby kulą o przekroju wielkości stadionu sportowego.
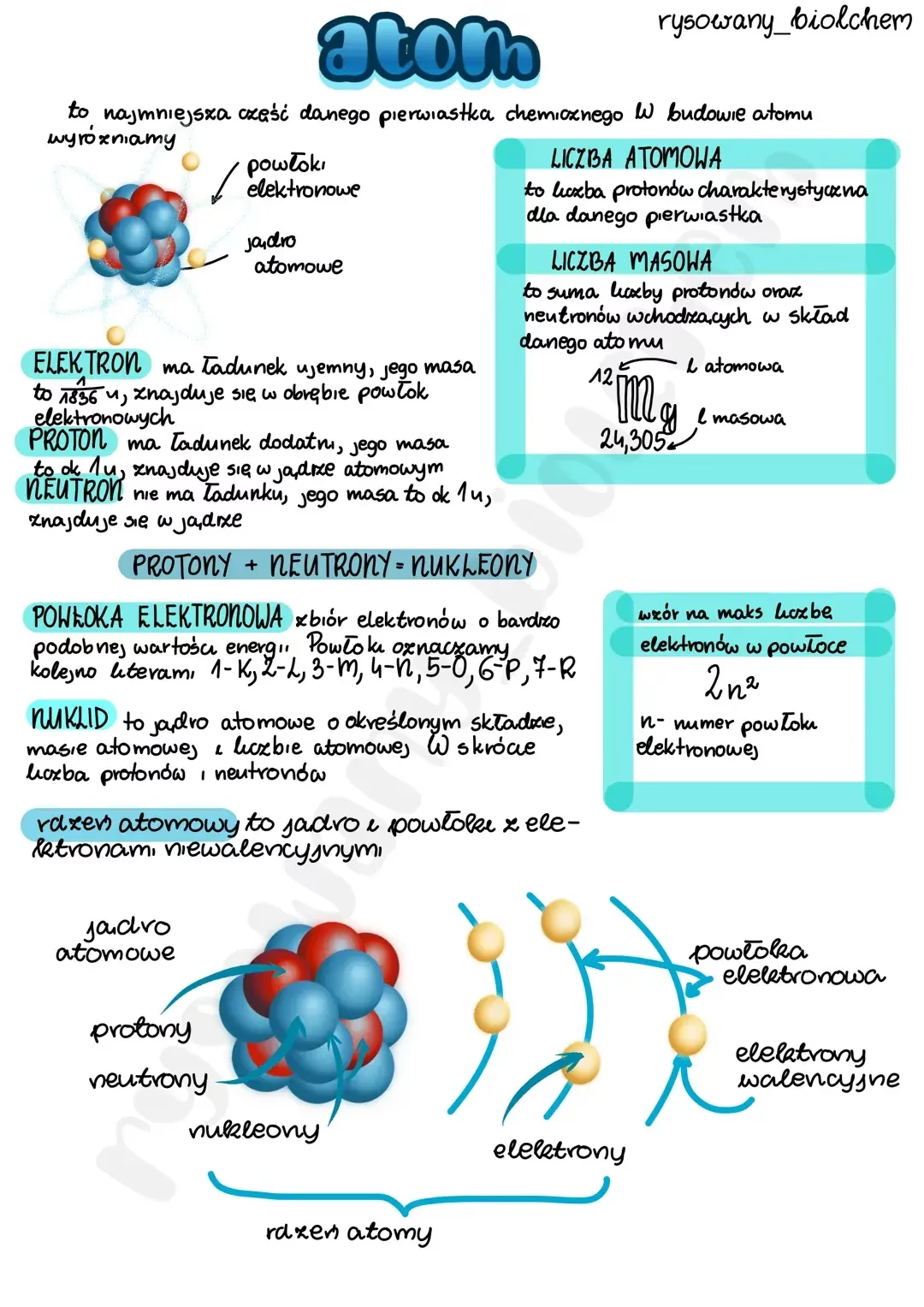
Samo jądro atomu ma również złożoną budowę. W jego skład wchodzą dodatnio naładowane cząstki, nazwane protonami, oraz cząstki pozbawione ładunku – neutrony. Protony i neutrony, jako cząstki znajdujące się w jądrze, określa się wspólnie jako nukleony.
Każdy atom jest elektrycznie obojętną drobiną. Oznacza to, że w jego wnętrzu równoważą się ładunki ujemne i dodatnie, co jest możliwe dzięki temu, że liczba protonów i liczba elektronów w każdym atomie jest jednakowa. Liczba neutronów nie ma wpływu na przynależność atomu do danego pierwiastka, ale ma wpływ na jego masę i stabilność, prowadząc do istnienia izotopów.
Cząstki wchodzące w skład atomów
Poniższa tabela przedstawia podstawowe cząstki subatomowe:
| Nazwa | Symbol | Ładunek* | Miejsce w atomie |
|---|---|---|---|
| elektron | e (e-) | -1 | obszar poza jądrem (powłoki elektronowe) |
| proton | p (p+) | 1 | jądro atomowe |
| neutron | n (n0) | 0 | jądro atomowe |
*Ujemny ładunek elektronu i dodatni ładunek protonu mają tę samą wartość bezwzględną (różnią się tylko znakami). Ustalono, że ładunek ujemny elektronu jest elementarnym ładunkiem ujemnym. Zatem proton ma elementarny ładunek dodatni.
Czy składniki atomu są niepodzielne?
Obecny stan wiedzy pozwala nam powiedzieć, że elementarnymi składnikami materii są dwa rodzaje cząstek: leptony i kwarki. Nie wiemy, czy cząstki te mają strukturę wewnętrzną. Elektron należy do leptonów, czyli zgodnie z obecnym stanem wiedzy jest niepodzielny, nie ma wewnętrznej struktury. Z kolei neutrony i protony są zbudowane z kwarków. Znaleziono dowody na istnienie sześciu rodzajów kwarków: górny (u), dolny (d), dziwny (s), powabny (c), niski (spodni) (b), wysoki (t). Nie istnieją one samodzielnie w przyrodzie, jak tylko w grupie, tworząc inne cząstki. Dwa z nich (górny i dolny) biorą udział w tworzeniu nukleonów. Protony są zbudowane z dwóch kwarków górnych i jednego kwarka dolnego, natomiast neutrony z jednego kwarka górnego i dwóch dolnych. Ta różnica odpowiada za różnicę w masach i ładunku tych dwóch cząstek.
Opisujemy atomy: Liczba Atomowa i Masowa
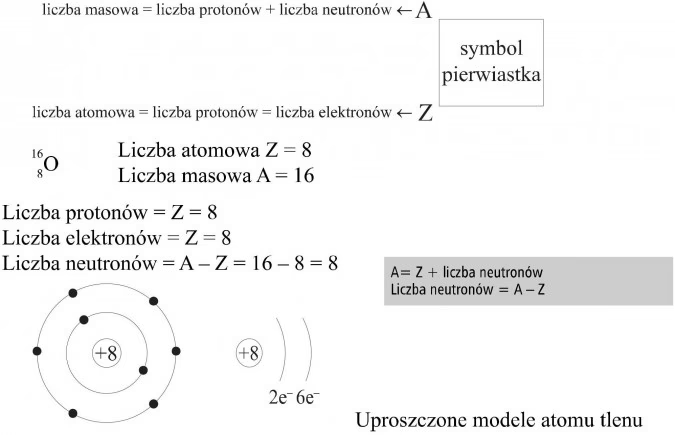
Aby opisać atom, należy podać liczby protonów (lub elektronów) i neutronów, wchodzących w jego skład. Choć istnieje wiele sposobów prezentacji budowy atomu, chemicy wykorzystują tylko jeden – opisują atomy za pomocą dwóch liczb: atomowej i masowej.
- Liczba atomowa (Z) to liczba protonów w jądrze. Określa ona tożsamość pierwiastka.
- Liczba masowa (A) to liczba nukleonów, czyli suma protonów i neutronów w jądrze.
Liczby te umieszcza się w odpowiedniej kolejności i w konkretnym miejscu przy symbolu pierwiastka. Z lewej strony symbolu w indeksie górnym umieszcza się liczbę masową A, a w indeksie dolnym – liczbę atomową Z: EAZ.
Dzięki tym dwóm liczbom można łatwo obliczyć skład atomu:
- Liczba protonów = Z
- Liczba elektronów = Z (w atomie obojętnym)
- Liczba neutronów = A - Z
Historia i Ewolucja Pojęcia Atomu
Pomysł, że materia składa się z mikroskopijnych składników, których nie da się w nieskończoność dzielić na mniejsze części, był znany już w starożytności. Nie opierał się jednak na żadnych danych empirycznych, a jedynie stanowił jedną z filozoficznych koncepcji natury rzeczywistości. Najstarsze odniesienia do atomów można znaleźć w pismach poświęconych dźinizmowi z VI wieku p.n.e. W cywilizacji zachodniej odniesienia do atomów pojawiły się około sto lat później w pismach Leukipposa i zostały usystematyzowane przez jego ucznia Demokryta, który około 450 roku p.n.e. wprowadził słowo átomos (niepodzielny).
W XVII i XVIII wieku chemicy zaczęli potwierdzać te przypuszczenia, identyfikując pierwiastki chemiczne i pokazując, że reagują one ze sobą w ściśle określonych proporcjach. Przełomem było prawo zachowania masy Antoine'a Lavoisiera (1789) i praca Johna Daltona (1803), który skorzystał z koncepcji atomów do wytłumaczenia praw chemii, czyniąc go twórcą współczesnej teorii atomów.
Na początku XX wieku fizycy zbadali wewnętrzną strukturę atomów, pokazując tym samym, że są one podzielne. Odkrycie elektronów przez J.J. Thomsona w 1897 roku obaliło tezę o niepodzielności. Model atomu Rutherforda (1909), w którym dodatni ładunek i większość masy atomu skupione są w niewielkim jądrze, zastąpił wcześniejsze teorie. Niels Bohr w 1913 roku zaproponował wyjaśnienie linii spektralnych przez istnienie dopuszczalnych orbit elektronów. Ostatecznie, w 1926 roku, Erwin Schrödinger stworzył matematyczny model atomu, w którym ruch elektronów został opisany funkcjami fal stojących, co stało się podstawą mechaniki kwantowej i jest obecnie obowiązującym modelem.
Wynalezienie spektrometru mas umożliwiło dokładne zmierzenie bezwzględnych mas atomowych i potwierdziło istnienie izotopów – atomów o tej samej liczbie protonów, ale różniących się liczbą neutronów. Odkrycie neutronu przez Jamesa Chadwicka w 1932 roku dopełniło obraz budowy jądra atomowego.
Właściwości Atomów: Rozmiar, Kształt i Stany Energetyczne
Atomy mają rozmiary rzędu 10-10 m i masę rzędu 10-26 – 10-25 kg. Ponad 99,9% masy atomu jest zawarte w jego jądrze. Atomy nie mają dokładnie określonych granic, ich rozmiary są określane w sposób umowny, na podstawie odległości pomiędzy sąsiednimi jądrami atomów. W układzie okresowym średnice atomów wewnątrz każdej grupy rosną wraz z liczbą obsadzonych powłok, jednak maleją wewnątrz okresu wraz ze zwiększeniem liczby protonów (ponieważ jądro przyciąga elektrony mocniej i rozmiary powłok maleją). Najmniejszą średnicę ma hel – około 62 pm, a największą cez – około 520 pm.
Elektrony w atomie są przyciągane siłami elektrycznymi przez protony w jądrze. To oddziaływanie tworzy studnię potencjału wokół jądra, z której uwolnienie wymaga dostarczenia elektronom energii z zewnątrz. Im bliżej jądra znajduje się elektron, tym silniej jest przyciągany i wzrasta energia konieczna do jego oderwania od atomu. Zgodnie z mechaniką kwantową, elektrony (tak jak wszystkie cząstki) są jednocześnie cząstkami i falami. Każdy elektron można opisać funkcją matematyczną określającą prawdopodobieństwo znalezienia elektronu w określonym obszarze – tak zwany orbital. Zbiór orbitali posiadających podobny poziom energetyczny nazywany jest powłoką elektronową.
Elektron może znaleźć się na wyższym poziomie energetycznym pochłaniając foton o odpowiedniej energii lub otrzymując tę energię ze zderzenia z innym atomem lub cząstką. Odwrotnie – elektron z wyższego poziomu może przenieść się na niższy, emitując foton. Te charakterystyczne wartości energii odpowiadają za występowanie linii spektralnych w widmach liniowych poszczególnych pierwiastków, co jest podstawą spektroskopii i pozwala na badanie składu chemicznego nawet odległych gwiazd.
Wiązania Chemiczne i Stany Skupienia Materii
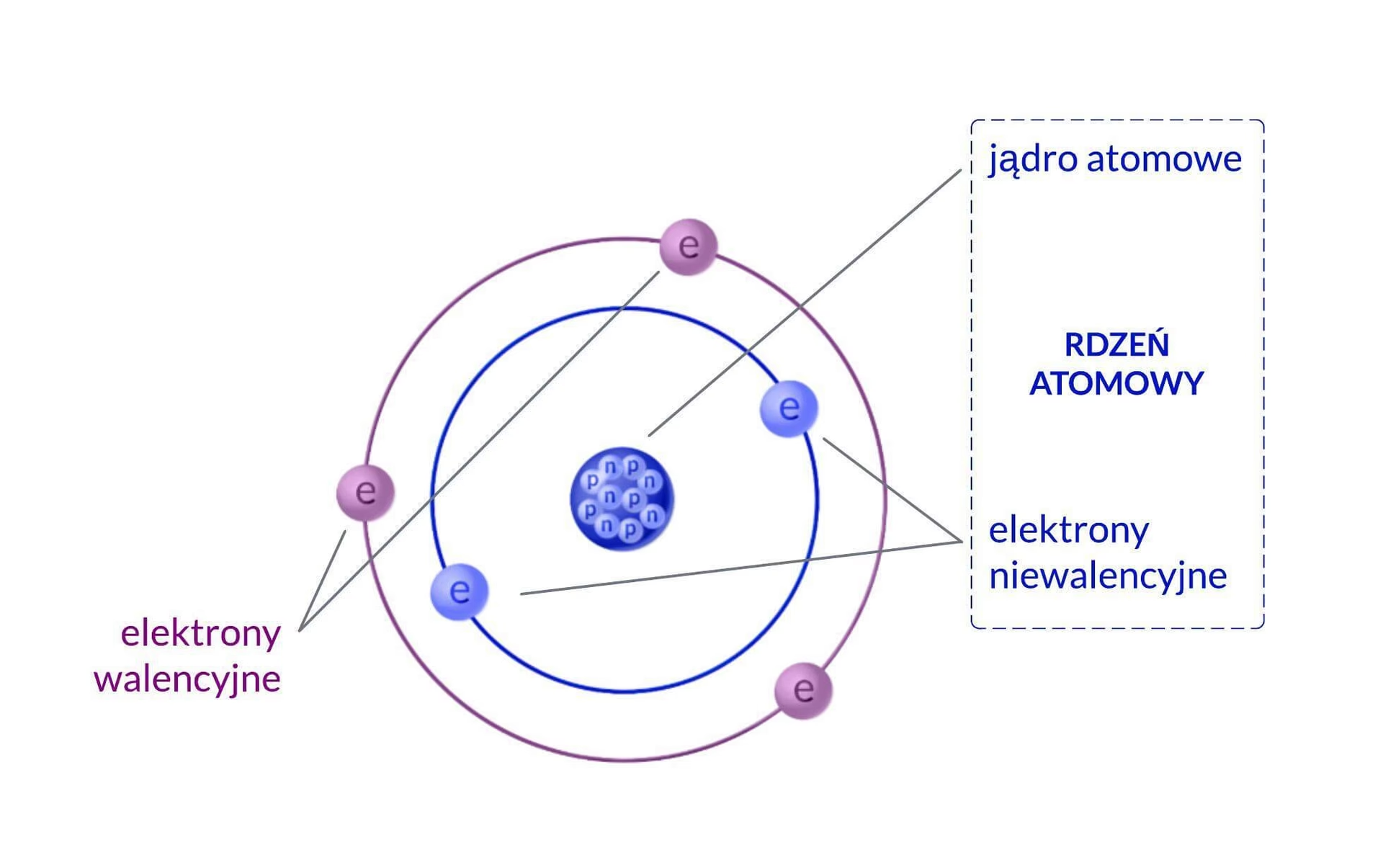
Elektrony znajdujące się na najdalszej powłoce w atomie nazywane są walencyjnymi, a ich powłoka – walencyjną. Liczba takich elektronów determinuje właściwości chemiczne atomów. Atomy, w których powłoka walencyjna nie jest w pełni wypełniona, łatwo oddziałują z innymi atomami, tak aby uzupełnić (lub opróżnić) tę powłokę. Odbywa się to poprzez reakcje chemiczne, czyli procesy tworzenia i zrywania wiązań chemicznych.
Wiązania powstają w efekcie uwspólniania elektronów przez dwa lub więcej atomów (wiązanie kowalencyjne) albo na skutek przeniesienia elektronów z jednego atomu na drugi (wiązanie jonowe). W pierwszym przypadku współdzielone elektrony tworzą jedną, wspólną chmurę wokół połączonych atomów, a w drugim atomy łączą się w pary jonowe, przyciągane do siebie oddziaływaniem elektrostatycznym. O typie wiązania decyduje różnica elektroujemności atomów.
Pierwiastki chemiczne zwykle przedstawia się w układzie okresowym, podkreślającym podobieństwo właściwości chemicznych pierwiastków o tej samej liczbie elektronów walencyjnych (znajdujących się w jednej grupie). Ostatnia grupa zawiera pierwiastki, w których powłoka walencyjna jest całkowicie zapełniona elektronami. Są one niemal całkowicie niereaktywne chemicznie i nazywa się je gazami szlachetnymi.
Grupy atomów mogą znajdować się w różnych stanach skupienia, w zależności od warunków takich jak temperatura i ciśnienie. Zmieniając te warunki, można wywoływać przejścia między stanem stałym, ciekłym, gazowym i plazmą. W temperaturach bliskich zera bezwzględnego niektóre atomy mogą tworzyć kondensat Bosego-Einsteina, w którym wszystkie zachowują się jak jeden superatom, pozwalając na obserwację ich kwantowych własności w skali makroskopowej.
Rozpad Radioaktywny: Niestabilność Jąder
Każdy pierwiastek ma nietrwałe izotopy, które ulegają rozpadowi radioaktywnemu. W trakcie takiego rozpadu jądro emituje cząstki, czemu może towarzyszyć promieniowanie elektromagnetyczne. Szczególnie podatne na taki rozpad są jądra o dużej wielkości w stosunku do zasięgu oddziaływania silnego.
Najbardziej powszechne typy rozpadów radioaktywnych to:
- Rozpad alfa – polegający na emisji cząstki alfa (jądra helu, składającego się z dwóch protonów i dwóch neutronów). W jego wyniku liczba masowa jądra maleje o 4.
- Rozpad beta – wywoływany przez oddziaływanie słabe, polegający na przekształceniu neutronu znajdującego się w jądrze w proton (rozpad β-) lub protonu w neutron (rozpad β+). Taki rozpad zwiększa lub zmniejsza liczbę atomową jądra, nie zmieniając jego liczby masowej.
- Emisja gamma – polegająca na emisji promieniowania gamma w wyniku przejścia nukleonu na niższy poziom energetyczny w jądrze. Taki rozpad nie zmienia liczby atomowej ani masowej jądra i zwykle następuje po rozpadzie alfa albo beta.
Rozpad radioaktywny jest procesem losowym, ale dla każdego nietrwałego jądra można określić charakterystyczny czas połowicznego rozpadu – czas, po jakim połowa jąder z próbki ulegnie rozpadowi.
Techniki Badawcze Atomów
Rozwój technologii umożliwił nam „zobaczenie” i manipulowanie atomami w sposób, który jeszcze kilkadziesiąt lat temu był nie do pomyślenia. Do najważniejszych technik należą:
- Skaningowy mikroskop tunelowy (STM): Umożliwia oglądanie powierzchni w skali atomowej, wykorzystując zjawisko tunelowe elektronów. Pozwala na uzyskanie trójwymiarowego obrazu powierzchni i nawet manipulację pojedynczymi atomami.
- Mikroskopia sił atomowych (AFM): Działa na zasadzie przemiatania ostrza nad powierzchnią próbki i pomiaru sił działających na to ostrze, co w odpowiednich warunkach pozwala na rejestrację pojedynczych atomów.
- Spektrometria mas: Wykorzystuje pole magnetyczne do odchylenia trajektorii jonów, co pozwala na identyfikację izotopów i składów pierwiastkowych cząsteczek na podstawie stosunku masy do ładunku.
- Spektroskopia strat energii elektronów (EELS): Pozwala na uzyskiwanie nanometrowej rozdzielczości i trójwymiarowe obrazowanie przemieszczeń atomów w czasie femtosekund, mierząc straty energii elektronów przechodzących przez próbkę.
- Rentgenografia strukturalna: Umożliwia określenie ułożenia atomów w sieci krystalicznej poprzez analizę dyfrakcji promieniowania rentgenowskiego, co pozwala na ustalenie struktur cząsteczek, długości wiązań i kątów między nimi.
Te i inne techniki, takie jak spektroskopia w podczerwieni, Ramana, UV-Vis, elektronowego rezonansu paramagnetycznego (EPR) czy magnetycznego rezonansu jądrowego (NMR), dostarczają nam bezcennych informacji o właściwościach atomów, ich interakcjach i roli w materii.
Pochodzenie Atomów we Wszechświecie
Atomy stanowią około 4% całkowitej masy-energii obserwowanego Wszechświata. Zgodnie z teorią Wielkiego Wybuchu, protony i neutrony uformowały się około jednej sekundy po powstaniu Wszechświata. W ciągu kolejnych trzech minut w wyniku pierwotnej nukleosyntezy powstała większość helu, litu i deuteru. Pierwsze atomy (ze związanymi elektronami) pojawiły się około 380 tysięcy lat później, w epoce rekombinacji, gdy energia promieniowania zmalała poniżej energii jonizacji atomów.
Cięższe jądra atomowe (do żelaza) zaczęły powstawać w wyniku fuzji jądrowej we wnętrzu gwiazd kilkaset milionów lat później. Pierwiastki cięższe od żelaza powstawały w wyniku eksplozji supernowych (proces r) oraz we wnętrzu gwiazd AGB (proces s), oba procesy polegają na wychwytywaniu neutronów przez jądra atomowe. Większość atomów, z których składa się Ziemia i jej mieszkańcy, nie zmieniła swych jąder od czasu ich powstania, czyli wcześniej niż mgławica, z której powstał Układ Słoneczny, zaczęła się zapadać.
Egzotyczne Atomy i Antyatomy
Poza standardowymi atomami, naukowcy sztucznie wytworzyli również tzw. atomy egzotyczne, w których proton, neutron albo elektron zastąpiono inną cząstką o takim samym ładunku. Przykładem jest atom mionowy, gdzie elektron zastąpiony jest mionem, lub pozytonium, układ złożony z pozytonu i elektronu.
Fascynującym obszarem badań są także antyatomy. Każdy fermion posiada odpowiadającą jej antycząstkę o przeciwnym ładunku. Ponieważ takie antycząstki anihilują w zetknięciu ze zwykłą materią, nie obserwuje się ich w przyrodzie. Jednak w 1996 roku udało się sztucznie wytworzyć kilka atomów antywodoru w laboratorium CERN, a w 2010 roku nawet je uwięzić, otwierając nowe możliwości badań nad antymaterią i jej właściwościami.
Najczęściej Zadawane Pytania (FAQ)
Czy atom jest podzielny?
Tak, atom jest podzielny. Składa się z jądra atomowego (zawierającego protony i neutrony) oraz elektronów krążących wokół jądra. Protony i neutrony są z kolei zbudowane z jeszcze mniejszych cząstek, zwanych kwarkami. Jedynie elektrony i kwarki są uważane za cząstki elementarne, których obecny stan wiedzy nie pozwala dalej podzielić.
Ile waży jeden atom?
Masa atomów jest niezwykle mała, rzędu 10-26 – 10-25 kg. Często wyraża się ją w jednostkach atomowych (u), zdefiniowanych jako 1/12 masy atomu węgla-12 (12C), czyli około 1,66 × 10-27 kg. W tych jednostkach masa każdego atomu jest w przybliżeniu równa jego liczbie masowej. Na przykład masa atomu wodoru (1H) wynosi około 1,007825 u.
Jakie są najmniejsze cząstki w atomie?
Najmniejszymi cząstkami w atomie, które są uważane za elementarne (czyli nie mające znanej wewnętrznej struktury), są elektrony oraz kwarki. Protony i neutrony, choć są częściami atomu, są złożone z kwarków.
Czy atomy można zobaczyć?
Pojedynczych atomów nie można zobaczyć za pomocą tradycyjnego mikroskopu optycznego, ponieważ ich rozmiary są tysiące razy mniejsze od długości fali światła widzialnego. Jednak dzięki zaawansowanym technikom, takim jak skaningowy mikroskop tunelowy (STM) czy mikroskopia sił atomowych (AFM), możliwe jest uzyskanie obrazów pojedynczych atomów i nawet manipulowanie nimi.
Czym różnią się izotopy?
Izotopy to atomy tego samego pierwiastka (czyli mające tę samą liczbę protonów w jądrze, a tym samym tę samą liczbę atomową Z), które różnią się liczbą neutronów w jądrze. W związku z tym mają one różne liczby masowe (A) i różne masy atomowe, ale takie same właściwości chemiczne.
Zrozumienie budowy atomu jest fundamentalne dla całej nauki. Od najmniejszych cząstek po kosmiczne procesy, atomy są wszechobecne i kluczowe dla poznania natury rzeczywistości. Ich złożoność i dynamika wciąż dostarczają nowych fascynujących odkryć, pogłębiając naszą wiedzę o świecie.
Zainteresował Cię artykuł Tajemnice Atomu: Wgłębienie w Mikroświat? Zajrzyj też do kategorii Nauka, znajdziesz tam więcej podobnych treści!