06/05/2022
Czy kiedykolwiek zastanawiałeś się, z czego tak naprawdę składa się wszystko wokół nas? Krzesło, na którym siedzisz, powietrze, którym oddychasz, a nawet Ty sam – wszystko to zbudowane jest z niewyobrażalnie małych cząstek zwanych atomami. Są one fundamentalnymi cegiełkami materii, a ich struktura jest kluczem do zrozumienia całego wszechświata. Wyruszmy w fascynującą podróż do mikroskopijnego świata, aby odkryć, jak te niezwykłe byty są zbudowane i co sprawia, że są tak stabilne i różnorodne.
Co to jest atom?
Atom to najmniejsza cząstka pierwiastka chemicznego, która zachowuje jego właściwości. Przez długi czas uważano, że atomy są niepodzielne – stąd ich nazwa, pochodząca od greckiego słowa „atomos”, oznaczającego „niepodzielny”. Dziś wiemy, że atomy nie tylko są podzielne, ale składają się z jeszcze mniejszych, fascynujących elementów. Pomimo swojej mikroskopijnej natury, atomy są w większości pustą przestrzenią, a ich masa skupiona jest w niezwykle gęstym centrum.
Kluczowe składniki atomu: elektrony, protony, neutrony
Każdy atom składa się z trzech podstawowych typów cząstek subatomowych. Są to: protony, neutrony i elektrony. Każda z tych cząstek odgrywa kluczową rolę w definiowaniu tożsamości i właściwości danego atomu.
- Protony: Są to cząstki posiadające dodatni ładunek elektryczny. Ich liczba w jądrze atomowym determinuje, jakim pierwiastkiem chemicznym jest dany atom. Na przykład, atom z jednym protonem to zawsze wodór, z dwoma – hel, a z ośmioma – tlen.
- Neutrony: Jak sama nazwa wskazuje, neutrony są elektrycznie obojętne, co oznacza, że nie posiadają ładunku elektrycznego. Znajdują się w jądrze atomowym wraz z protonami. Liczba neutronów może się różnić dla atomów tego samego pierwiastka, tworząc tak zwane izotopy.
- Elektrony: To cząstki o ładunku ujemnym, które krążą wokół jądra atomowego. Są znacznie lżejsze od protonów i neutronów – ich masa jest około 1836 razy mniejsza niż masa protonu. Elektrony zajmują „powłoki” lub „orbity” wokół jądra, a ich rozmieszczenie decyduje o chemicznych właściwościach atomu i jego zdolności do tworzenia wiązań.
Jądro atomowe: serce materii
W samym centrum atomu znajduje się jego jądro. To niezwykle mała, ale niewiarygodnie gęsta struktura, w której skupiona jest niemal cała masa atomu. Jądro składa się z protonów i neutronów, które razem nazywane są nukleonami. Pomimo tego, że protony posiadają ładunki dodatnie i naturalnie odpychałyby się wzajemnie, są one utrzymywane razem przez jedną z najsilniejszych sił w naturze – silne oddziaływanie jądrowe. Ta potężna siła jest odpowiedzialna za stabilność jąder atomowych i ma kluczowe znaczenie dla istnienia materii w znanej nam formie.
Rozmiar jądra atomowego jest znikomy w porównaniu do rozmiaru całego atomu. Gdyby atom był wielkości stadionu piłkarskiego, jego jądro byłoby zaledwie ziarenkiem piasku na środku boiska. Ta ogromna dysproporcja w rozmiarach podkreśla, jak dużo pustej przestrzeni znajduje się w atomie.
Elektrony i ich orbity: powłoka atomowa
Wokół gęstego jądra, w stosunkowo dużej odległości, krążą elektrony. Nie poruszają się one po ściśle określonych orbitach, jak planety wokół Słońca, ale raczej zajmują obszary przestrzeni zwane powłokami elektronowymi lub chmurami elektronowymi. Każda powłoka może pomieścić określoną liczbę elektronów, a elektrony na dalszych powłokach posiadają więcej energii. Ruch elektronów wokół jądra jest tak szybki i dynamiczny, że tworzą one rodzaj „chmury” ujemnego ładunku, która otacza dodatnio naładowane jądro.
To właśnie elektrony, a zwłaszcza te znajdujące się na najbardziej zewnętrznej powłoce (zwane elektronami walencyjnymi), decydują o tym, jak atom będzie reagował z innymi atomami. Są one odpowiedzialne za tworzenie wiązań chemicznych, co jest podstawą całej chemii i życia na Ziemi.
Równowaga ładunków: dlaczego atomy są neutralne?
Jedną z najważniejszych cech atomów jest ich elektryczna obojętność w stanie podstawowym. Oznacza to, że całkowity ładunek dodatni protonów w jądrze jest dokładnie równoważony przez całkowity ładunek ujemny elektronów krążących wokół jądra. Na przykład, jeśli atom ma 6 protonów (jak węgiel), będzie miał również 6 elektronów, co sprawia, że jego ładunek netto wynosi zero. Ta równowaga jest kluczowa dla stabilności atomów i ich interakcji ze sobą. Kiedy atom zyskuje lub traci elektrony, staje się jonem – cząstką naładowaną elektrycznie, która dąży do odzyskania neutralności poprzez interakcję z innymi jonami lub atomami.
Przykład helu-4: prosta budowa, głębokie znaczenie
Aby lepiej zrozumieć strukturę atomu, przyjrzyjmy się konkretnemu przykładowi – atomowi helu-4. Jest to najpowszechniejszy izotop helu, drugiego najlżejszego pierwiastka we wszechświecie. Jego budowa jest stosunkowo prosta, co czyni go doskonałym modelem do nauki.
W przypadku atomu helu-4, w jego maleńkim, gęstym jądrze znajdują się dwa protony i dwa neutrony. Protony nadają jądru ładunek +2, a neutrony, będąc obojętnymi, nie wpływają na ładunek. Krążące wokół tego jądra, w jego powłoce elektronowej, znajdują się dwa elektrony. Każdy elektron niesie ładunek -1, więc łącznie dwa elektrony dają ładunek -2. Sumując ładunki: (+2 z protonów) + (-2 z elektronów) = 0. To właśnie sprawia, że atom helu-4 jest elektrycznie obojętny. Ta idealna równowaga ładunków jest cechą charakterystyczną wszystkich atomów w ich naturalnym, stabilnym stanie.
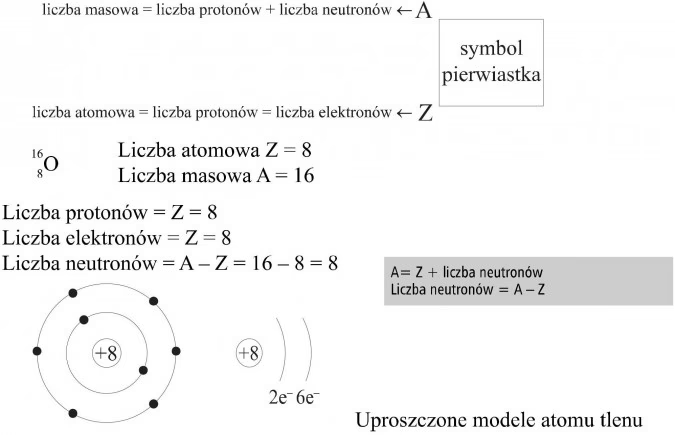
Liczba atomowa i masowa: identyfikatory atomów
Każdy pierwiastek chemiczny jest definiowany przez swoją liczbę atomową (Z). Liczba atomowa to nic innego jak liczba protonów w jądrze atomu. To ona decyduje o miejscu pierwiastka w układzie okresowym i o jego unikalnych właściwościach chemicznych. Na przykład, wszystkie atomy z 6 protonami to atomy węgla, niezależnie od liczby neutronów.
Oprócz liczby atomowej, atomy charakteryzuje także liczba masowa (A), która jest sumą liczby protonów i neutronów w jądrze. Liczba masowa mówi nam o przybliżonej masie atomu. Na przykład, hel-4 ma liczbę atomową 2 (ponieważ ma 2 protony) i liczbę masową 4 (ponieważ ma 2 protony + 2 neutrony).
Izotopy: te same, ale inne
Jak wspomniano wcześniej, atomy tego samego pierwiastka mogą różnić się liczbą neutronów. Takie odmiany nazywane są izotopami. Mają one tę samą liczbę protonów (a więc są tym samym pierwiastkiem), ale różnią się liczbą neutronów, co wpływa na ich masę atomową. Na przykład, wodór ma trzy izotopy: prot (1 proton, 0 neutronów), deuter (1 proton, 1 neutron) i tryt (1 proton, 2 neutrony). Chociaż różnią się masą, ich właściwości chemiczne są bardzo podobne, ponieważ to elektrony (a ich liczba jest taka sama dla danego pierwiastka) decydują o chemii.
Siły w atomie: co trzyma to wszystko razem?
Złożona struktura atomu jest utrzymywana razem przez kilka fundamentalnych sił natury:
- Silne oddziaływanie jądrowe: Jest to najsilniejsza ze wszystkich sił podstawowych. Działa na bardzo krótkich dystansach i jest odpowiedzialna za utrzymywanie protonów i neutronów razem w jądrze, pomimo wzajemnego odpychania się dodatnio naładowanych protonów. Bez tej siły jądra atomowe rozpadłyby się natychmiast.
- Oddziaływanie elektromagnetyczne: Odpowiada za przyciąganie się przeciwnie naładowanych cząstek (protonów i elektronów) oraz odpychanie się cząstek o tym samym ładunku. To właśnie ta siła utrzymuje elektrony na ich orbitach wokół jądra. Jest ona znacznie słabsza od silnego oddziaływania jądrowego, ale działa na większych odległościach.
- Słabe oddziaływanie jądrowe: Odpowiada za pewne rodzaje rozpadów promieniotwórczych i transformacje cząstek, np. przemianę neutronu w proton (rozpad beta).
- Grawitacja: Chociaż jest to siła powszechnie znana, jej wpływ na poziomie subatomowym jest znikomy w porównaniu do pozostałych trzech sił.
Tabela porównawcza cząstek subatomowych
Dla lepszego zrozumienia, przedstawiamy tabelę podsumowującą kluczowe właściwości cząstek subatomowych:
| Cząstka | Ładunek (względem ładunku elementarnego) | Masa względna (względem masy protonu) | Lokalizacja w atomie |
|---|---|---|---|
| Proton | +1 | ~1 | Jądro atomowe |
| Neutron | 0 (neutralny) | ~1 | Jądro atomowe |
| Elektron | -1 | ~1/1836 | Powłoki elektronowe (wokół jądra) |
Często zadawane pytania (FAQ)
Czy atomy są naprawdę puste?
Tak, w przeważającej mierze atomy składają się z pustej przestrzeni. Jądro atomowe, które zawiera prawie całą masę atomu, jest niewyobrażalnie małe w porównaniu do rozmiaru całego atomu. Elektrony krążące wokół jądra również zajmują bardzo małą objętość, a ich ruch tworzy "chmurę" ładunku.
Czy atomy mogą się zmieniać?
Większość atomów jest stabilna, ale niektóre izotopy są niestabilne i podlegają rozpadowi promieniotwórczemu, przekształcając się w inne atomy lub izotopy. Procesy takie jak fuzja jądrowa (łączenie się jąder) i rozszczepienie jądrowe (rozpad jąder) również zmieniają tożsamość atomów, tworząc nowe pierwiastki.
Jakie są największe atomy?
Największe atomy pod względem liczby protonów (liczby atomowej) to pierwiastki superciężkie, które są tworzone sztucznie w laboratoriach, takie jak oganeson (liczba atomowa 118). Są one jednak bardzo niestabilne i istnieją tylko przez ułamki sekund.
Czy atomy są widoczne?
Nie, atomy są zbyt małe, aby zobaczyć je gołym okiem lub nawet za pomocą tradycyjnych mikroskopów optycznych. Do ich "oglądania" używa się specjalistycznych technik, takich jak mikroskopia tunelowa (STM) lub mikroskopia sił atomowych (AFM), które pozwalają na uzyskanie obrazów powierzchni materiałów na poziomie atomowym.
Podsumowanie: atom jako fundament wszechświata
Zrozumienie budowy atomu to klucz do poznania otaczającego nas świata. Od maleńkich, naładowanych protonów i obojętnych neutronów w gęstym jądrze, po szybko krążące elektrony tworzące rozległą powłokę – każdy element odgrywa swoją rolę w kształtowaniu materii. Równowaga ładunków sprawia, że atomy są neutralne, a potężne siły jądrowe i elektromagnetyczne utrzymują je w stabilnej strukturze. Niezależnie od tego, czy mówimy o prostym atomie helu-4, czy o skomplikowanych pierwiastkach, podstawowe zasady ich budowy pozostają niezmienne, stanowiąc fundament dla całej chemii, fizyki i życia. Ta mikroskopijna architektura jest prawdziwym cudem natury, nieustannie inspirującym naukowców do dalszych odkryć.
Zainteresował Cię artykuł Jak zbudowany jest atom? Przewodnik po mikrokosmosie? Zajrzyj też do kategorii Nauka, znajdziesz tam więcej podobnych treści!
