11/03/2023
W świecie chemii, gdzie miliardy atomów łączą się w niezliczone kombinacje, aby tworzyć wszystko, co nas otacza, kluczowe jest precyzyjne ich opisywanie. Jednym z podstawowych narzędzi, które pozwalają nam zrozumieć skład i strukturę związków chemicznych, są wzory chemiczne. Często spotykamy się z różnymi typami wzorów, takimi jak wzór sumaryczny, empiryczny czy rzeczywisty. Choć mogą wydawać się podobne, każdy z nich dostarcza nieco innych, ale równie ważnych informacji. W tym artykule zagłębimy się w różnice między wzorem rzeczywistym a wzorem empirycznym, wyjaśnimy ich znaczenie i pokażemy, jak je wyznaczać, korzystając z podstawowych praw chemii.
Prawo stałości składu – fundament chemii
Zanim przejdziemy do szczegółowych wzorów, warto przypomnieć sobie o fundamentalnej zasadzie, która leży u podstaw chemii – prawie stałości składu. Mówi ono, że każdy związek chemiczny, niezależnie od sposobu jego otrzymywania czy pochodzenia, zawsze ma stały skład jakościowy i ilościowy. Oznacza to, że stosunek mas pierwiastków w danym związku jest zawsze taki sam i charakterystyczny tylko dla niego.
Na przykład, w cząsteczce tlenku węgla(IV) (CO2) zawsze na jeden atom węgla przypadają dwa atomy tlenu. To prawo jest niezwykle ważne, ponieważ pozwala nam na jednoznaczne określenie składu procentowego pierwiastków w związku, co z kolei jest pierwszym krokiem do wyznaczenia jego wzoru empirycznego i rzeczywistego.
Zależność wynikająca z prawa stałości składu dla związku chemicznego o wzorze sumarycznym AxBy przyjmuje postać:
MA · x / MB · y = %A / %B
gdzie:
- MA i MB – masy atomowe pierwiastków;
- x i y – indeksy stechiometryczne;
- %A i %B – procent masowy pierwiastków.
Wzór empiryczny (elementarny) – najprostszy obraz
Wzór empiryczny, nazywany również wzorem elementarnym, to nic innego jak najprostszy stosunek ilościowy atomów wchodzących w skład cząsteczki związku chemicznego. Mówi nam, w jakim najprostszym stosunku liczbowym występują atomy poszczególnych pierwiastków w danym związku. Jest on wyrażony za pomocą najmniejszych liczb całkowitych.
Wyobraź sobie pizzę podzieloną na osiem kawałków. Jeśli zjadłeś cztery kawałki, to zjadłeś 4/8 pizzy. Ale w matematyce, 4/8 zawsze sprowadza się do 1/2. Wzór empiryczny jest jak to uproszczenie do 1/2 – pokazuje najprostszy stosunek, bez względu na to, ile faktycznie było kawałków czy atomów w cząsteczce.
Przykład: Glukoza ma wzór sumaryczny C6H12O6. Jeśli podzielimy wszystkie indeksy (6, 12, 6) przez ich największy wspólny dzielnik (czyli 6), otrzymamy stosunek 1:2:1. Zatem wzór empiryczny glukozy to CH2O.
Jak wyznaczyć wzór empiryczny?
Wyznaczenie wzoru empirycznego zazwyczaj opiera się na znajomości składu procentowego związku. Oto przykład:
Zadanie: Napisz wzór empiryczny związku chemicznego zawierającego 40% siarki i 60% tlenu.

Dane: %S = 40%, %O = 60%
Szukane: wzór empiryczny SxOy
- Założenie masy związku: Przyjmujemy, że masa cząsteczkowa związku wynosi 100 g. Wówczas masy poszczególnych pierwiastków będą równe ich zawartościom procentowym: mS = 40 g, mO = 60 g.
- Obliczenie liczby moli każdego pierwiastka: Dzielimy otrzymane masy przez ich masy molowe (MS = 32 g/mol, MO = 16 g/mol).
- nS = 40 g / 32 g/mol = 1,25 mol
- nO = 60 g / 16 g/mol = 3,75 mol
- Ustalenie stosunku molowego: nS: nO = 1,25 mol: 3,75 mol
- Sprowadzenie do najprostszych liczb całkowitych: Dzielimy obie wartości przez najmniejszą z nich (1,25).
- 1,25 / 1,25 = 1
- 3,75 / 1,25 = 3
- Zapisanie wzoru empirycznego: Stosunek S:O wynosi 1:3, więc wzór empiryczny to SO3.
Wzór rzeczywisty – prawdziwy obraz cząsteczki
Wzór rzeczywisty, zwany także wzorem sumarycznym (choć nie zawsze są tożsame, jak zaraz wyjaśnimy), określa rzeczywiste liczby atomów poszczególnych pierwiastków chemicznych w jednej cząsteczce związku. To dosłowny zapis tego, co „jest w zeszycie”, czyli faktyczny skład molekularny.
Wracając do analogii z pizzą: jeśli wzór empiryczny to 1/2, to wzór rzeczywisty jest jak 4/8. Mówi nam, że zjadłeś cztery kawałki, a było ich osiem – podaje dokładną liczbę. Wzór rzeczywisty jest wielokrotnością wzoru empirycznego.
Przykład: Metanol ma wzór sumaryczny CH4O, ale jego wzór rzeczywisty (strukturalny) to CH3OH, co precyzyjniej oddaje jego strukturę. Z kolei dla kwasu azotowego (HNO3) wzór sumaryczny jest jednoznaczny ze wzorem rzeczywistym.
Kiedy wzór empiryczny jest taki sam jak rzeczywisty?
Tak, jak najbardziej! Wzór empiryczny jest taki sam jak wzór rzeczywisty, gdy stosunek atomów w cząsteczce jest już w swojej najprostszej postaci i nie da się go bardziej uprościć. Przykłady to woda (H2O), tlenek węgla(IV) (CO2) czy kwas solny (HCl). Jak widać na przykładzie N2O4 (ditlenek azotu), jego wzór empiryczny to NO2 (bo 2:4 można uprościć do 1:2), ale wzór rzeczywisty to N2O4. Tutaj widzimy, że wzór rzeczywisty jest dwukrotnością wzoru empirycznego (n=2).
Jak wyznaczyć wzór rzeczywisty?
Wyznaczenie wzoru rzeczywistego wymaga dodatkowej informacji – masy molowej związku. Po ustaleniu wzoru empirycznego, sprawdzamy, ile razy masa molowa wzoru empirycznego mieści się w masie molowej całego związku.
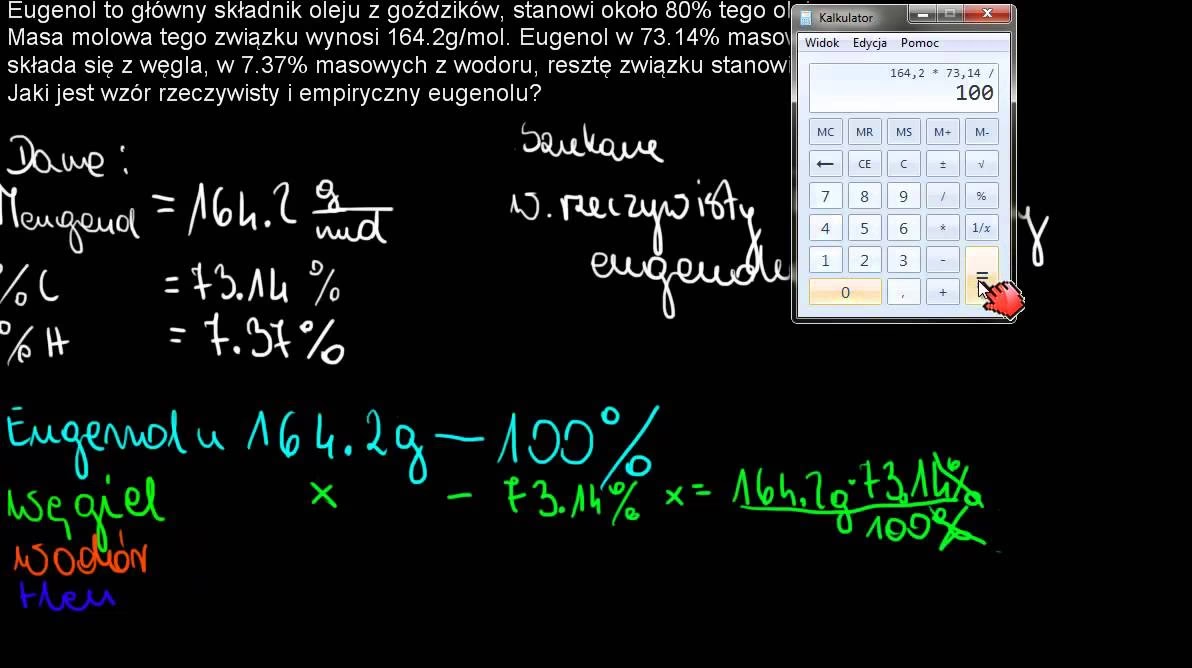
Przykład 1: Pewien związek zawiera wagowo 92,3% węgla oraz 7,7% wodoru. Masa molowa tego związku wynosi 78 g/mol. Ustal wzór rzeczywisty.

- Obliczenie stosunku molowego C:H:
- nC = 92,3 g / 12 g/mol ≈ 7,69 mol
- nH = 7,7 g / 1 g/mol = 7,7 mol
- Stosunek molowy C:H = 7,69: 7,7 ≈ 1:1
- Zapisanie wzoru empirycznego: CH
- Obliczenie masy molowej wzoru empirycznego: MCH = 12 g/mol + 1 g/mol = 13 g/mol
- Ustalenie wielokrotności (n): Dzielimy masę molową związku przez masę molową wzoru empirycznego.
- n = Mrzeczywista / Mempiryczna = 78 g/mol / 13 g/mol = 6
- Zapisanie wzoru rzeczywistego: Wzór rzeczywisty to (CH)n = (CH)6 = C6H6 (benzen).
Przykład 2: Wyznacz wzór rzeczywisty związku chemicznego o masie molowej 130 g/mol, zawierającego 73,85% węgla, 13,85% wodoru i 12,3% tlenu.
- Wyznaczenie stosunku molowego wszystkich pierwiastków:
- nC = 73,85 g / 12 g/mol ≈ 6,15 mol
- nH = 13,85 g / 1 g/mol = 13,85 mol
- nO = 12,3 g / 16 g/mol ≈ 0,77 mol
- Sprowadzenie do najmniejszych liczb całkowitych (dzieląc przez 0,77):
- nC = 6,15 / 0,77 ≈ 8
- nH = 13,85 / 0,77 ≈ 18
- nO = 0,77 / 0,77 = 1
- Zapisanie wzoru empirycznego: C8H18O
- Obliczenie masy molowej wzoru empirycznego: MC8H18O = (8*12) + (18*1) + (1*16) = 96 + 18 + 16 = 130 g/mol
- Ustalenie wielokrotności (n): n = 130 g/mol / 130 g/mol = 1
- Zapisanie wzoru rzeczywistego: Ponieważ n = 1, wzór empiryczny jest taki sam jak wzór rzeczywisty: C8H18O.
Należy pamiętać, że często (zwłaszcza w chemii organicznej) jeden wzór sumaryczny może odpowiadać kilku różnym związkom, które nazywamy izomerami. Mają one ten sam wzór sumaryczny, ale różnią się budową i właściwościami. Przykładowo, dla C8H18O istnieje wiele izomerów, takich jak eter di-tert-butylowy, eter dibutylowy, 2-etyloheksanol, 1-oktanol, 2-oktanol, 3-oktanol, 4-oktanol, 2,2-dimetyloheksan-3-ol i wiele innych.
Porównanie wzorów: Empiryczny vs. Rzeczywisty
Aby lepiej zrozumieć różnice i podobieństwa między wzorami, przyjrzyjmy się im w tabeli:
| Związek | Wzór sumaryczny | Wzór empiryczny | Wzór rzeczywisty | Wyjaśnienie |
|---|---|---|---|---|
| Tlenek węgla(IV) | CO2 | CO2 | CO2 | Najprostszy stosunek jest taki sam jak rzeczywisty skład. |
| Glukoza | C6H12O6 | CH2O | C6H12O6 | Wzór empiryczny to najprostszy stosunek (1:2:1), wzór rzeczywisty to 6-krotność empirycznego. |
| Tlenek azotu(IV) | NO2 | NO2 | NO2 | Najprostszy stosunek jest taki sam jak rzeczywisty skład. |
| Ditlenek azotu | N2O4 | NO2 | N2O4 | Wzór empiryczny to najprostszy stosunek (1:2), wzór rzeczywisty to 2-krotność empirycznego. |
| Eten | C2H4 | CH2 | C2H4 | Wzór empiryczny to najprostszy stosunek (1:2), wzór rzeczywisty to 2-krotność empiricznego. |
| Benzen | C6H6 | CH | C6H6 | Wzór empiryczny to najprostszy stosunek (1:1), wzór rzeczywisty to 6-krotność empirycznego. |
Często Zadawane Pytania (FAQ)
Czy wzór empiryczny może być taki sam jak rzeczywisty?
Tak, jak najbardziej! Wzór empiryczny jest taki sam jak wzór rzeczywisty, gdy stosunek atomów w cząsteczce jest już w swojej najprostszej postaci i nie da się go bardziej uprościć. Przykłady to woda (H2O), tlenek węgla(IV) (CO2) czy kwas solny (HCl).
Do czego służy wzór sumaryczny?
Wzór sumaryczny informuje nas o tym, ile i jakich atomów znajduje się w jednej cząsteczce związku chemicznego. Jest to pierwszy i najbardziej podstawowy sposób zapisu cząsteczek, z którym mamy styczność. Choć jest prosty, może być niewystarczający do pełnego opisu, zwłaszcza w przypadku izomerów, gdzie różne związki mogą mieć ten sam wzór sumaryczny (np. glukoza i fruktoza – oba C6H12O6).
Dlaczego nie zawsze można „skrócić” wzór rzeczywisty do empirycznego?
Wzoru rzeczywistego nie zawsze można „skrócić” do empirycznego, ponieważ wzór rzeczywisty ma za zadanie pokazać faktyczną liczbę atomów w cząsteczce, a nie tylko ich najprostszy stosunek. Przykładem jest cząsteczka etenu (C2H4). Jej wzór empiryczny to CH2. Gdybyśmy jednak „skrócili” wzór rzeczywisty do CH2, stracilibyśmy informację o tym, że cząsteczka etenu zawiera dwa atomy węgla połączone ze sobą, co jest kluczowe dla jej struktury i właściwości. Podobnie jak w analogii z pizzą – zjedzenie 4 z 8 kawałków to nie to samo co zjedzenie 1 z 2 kawałków, nawet jeśli stosunek jest ten sam. Liczba atomów ma znaczenie dla rzeczywistej budowy cząsteczki.
Podsumowanie
Zrozumienie różnic między wzorem empirycznym a rzeczywistym jest kluczowe dla każdego, kto zgłębia tajniki chemii. Wzór empiryczny dostarcza nam najprostszych informacji o proporcjach pierwiastków, podczas gdy wzór rzeczywisty daje nam pełen obraz faktycznej liczby atomów w cząsteczce. Oba są niezbędne do pełnego zrozumienia składu i budowy związków chemicznych. Umiejętność ich wyznaczania na podstawie danych eksperymentalnych, takich jak skład procentowy i masa molowa, to podstawowa umiejętność w laboratorium i na egzaminie. Pamiętaj, chemia to nie tylko wzory, ale przede wszystkim logiczne myślenie i interpretacja danych, które pozwalają nam odkrywać fascynujący świat molekuł.
Zainteresował Cię artykuł Wzór rzeczywisty a elementarny: Różnice? Zajrzyj też do kategorii Chemia, znajdziesz tam więcej podobnych treści!
