29/09/2021
Zwykłe substancje, takie jak sól czy cukier, po wrzuceniu do wody po prostu się rozpuszczają, tworząc roztwór – mieszaninę jednorodną. Ale co się stanie, gdy do wody trafi metal lub jego tlenek? Czy reakcja będzie taka sama? Czy powstanie mieszanina, czy zupełnie nowy związek chemiczny? I co najważniejsze, w jaki sposób możemy to sprawdzić? Odpowiedzi na te pytania prowadzą nas do fascynującego świata wodorotlenków i zasad, związków chemicznych o niezwykłych właściwościach i szerokim zastosowaniu w naszym życiu.

Wodorotlenki to związki o stałym stanie skupienia, zbudowane z kationów metalu i anionów wodorotlenkowych (grupy OH-). Te jony przyciągają się wzajemnie siłami elektrostatycznymi, tworząc uporządkowaną strukturę przestrzenną, zwaną siecią krystaliczną. Wartościowość grupy wodorotlenowej (OH) zawsze wynosi I. To właśnie ta grupa decyduje o charakterze chemicznym wodorotlenku.
Budowa i Nazewnictwo Wodorotlenków
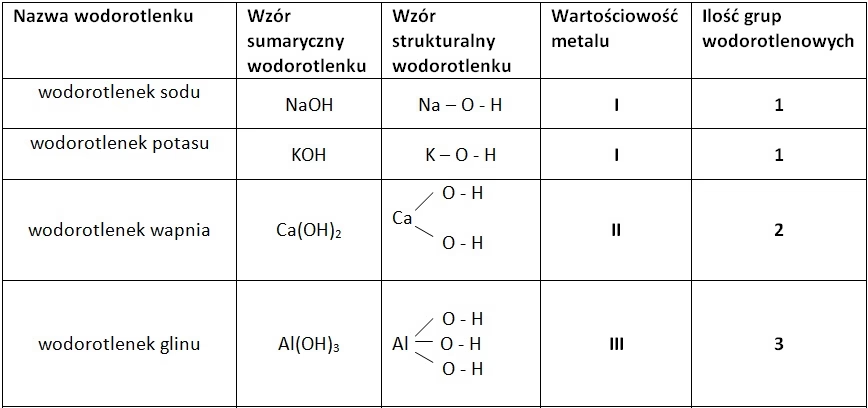
Ogólny wzór wodorotlenków metali jednowartościowych to MOH, gdzie M oznacza metal, a OH to grupa wodorotlenowa. Przykłady takich związków to wodorotlenek litu (LiOH), wodorotlenek sodu (NaOH) oraz wodorotlenek potasu (KOH).
Dla metali o wartościowości większej niż jeden, ogólny wzór przyjmuje postać M(OH)n, gdzie 'n' jest równe wartościowości metalu. Na przykład, wodorotlenek magnezu ma wzór Mg(OH)2, wodorotlenek wapnia to Ca(OH)2, a wodorotlenek glinu to Al(OH)3.
Nazwy wodorotlenków tworzy się, dodając do słowa „wodorotlenek” nazwę pierwiastka tworzącego dany związek w dopełniaczu. Na przykład, NaOH to wodorotlenek sodu. Jeżeli metal tworzy kilka wodorotlenków o różnej wartościowości, do nazwy dodaje się w nawiasie cyfrę rzymską określającą wartościowość metalu. Przykładem może być miedź, która tworzy wodorotlenek miedzi(I) (CuOH) i wodorotlenek miedzi(II) (Cu(OH)2). Jeśli metal tworzy tylko jeden wodorotlenek, wartościowość metalu w nazwie się pomija, tak jak w przypadku wodorotlenku sodu czy wodorotlenku wapnia.
Poniżej przedstawiamy przykłady wzorów i nazw wybranych wodorotlenków:
| Wzór chemiczny | Nazwa wodorotlenku | Wartościowość metalu |
|---|---|---|
| LiOH | Wodorotlenek litu | I |
| NaOH | Wodorotlenek sodu | I |
| KOH | Wodorotlenek potasu | I |
| Mg(OH)2 | Wodorotlenek magnezu | II |
| Ca(OH)2 | Wodorotlenek wapnia | II |
| Al(OH)3 | Wodorotlenek glinu | III |
| Fe(OH)2 | Wodorotlenek żelaza(II) | II |
| Fe(OH)3 | Wodorotlenek żelaza(III) | III |
| CuOH | Wodorotlenek miedzi(I) | I |
| Cu(OH)2 | Wodorotlenek miedzi(II) | II |
Wskaźniki Kwasowo-Zasadowe: Chemia w Kolorach
Aby stwierdzić, czy badany związek ma właściwości zasadowe, używamy specjalnych substancji, zwanych wskaźnikami lub indykatorami. Ich działanie polega na łatwo zauważalnej zmianie barwy pod wpływem różnych substancji, co pozwala nam zidentyfikować obecność interesującego nas związku.
Wskaźniki spotykamy również w życiu codziennym. Klasycznym przykładem jest herbata, która po dodaniu soku z cytryny (kwasu cytrynowego) staje się jaśniejsza. Podobnie, sok z buraków zmienia barwę na intensywnie czerwoną pod wpływem kwasów, takich jak kwas cytrynowy czy ocet.
W chemii, do wykrywania wodorotlenków, czyli środowiska zasadowego, często używa się wywaru z czerwonej kapusty. W wodzie destylowanej ma on fioletowo-niebieskie zabarwienie, natomiast w roztworze zasadowym zmienia kolor na zielony. Inne popularne wskaźniki i ich zmiany barw przedstawia poniższa tabela:
| Wskaźnik | Barwa w wodzie destylowanej | Barwa w środowisku zasadowym (wodny roztwór wodorotlenku) |
|---|---|---|
| Wywar z czerwonej kapusty | Fioletowo-niebieski | Zielony |
| Uniwersalny papierek wskaźnikowy | Żółty | Niebieski |
| Fenoloftaleina | Bezbarwna | Malinowa |
| Oranż metylowy | Żółto-pomarańczowy | Żółty |
| Lakmus | Fioletowy | Niebieski |
Warto zaznaczyć, że fenoloftaleina jest szczególnie często wykorzystywana w laboratoriach ze względu na jej wyraźną zmianę barwy z bezbarwnej na malinową w obecności zasad.
Otrzymywanie Wodorotlenków: Chemia w Akcji
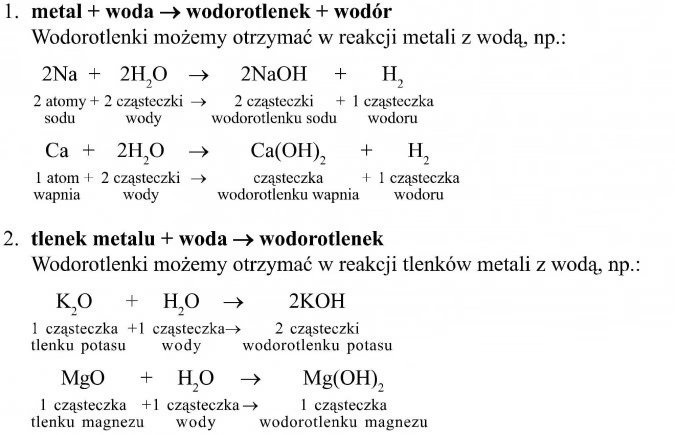
Wodorotlenki można otrzymać na kilka sposobów, zależnie od właściwości metalu. Dwa główne metody to reakcja aktywnych metali z wodą oraz reakcja tlenków metali aktywnych z wodą.
Metoda 1: Reakcja metali aktywnych z wodą
„Aktywny” metal to taki, który jest bardzo reaktywny chemicznie, czyli łatwo wchodzi w reakcje z innymi substancjami. Metalami aktywnymi nazywamy pierwiastki z 1. grupy układu okresowego (litowce, np. sód, potas) oraz z 2. grupy (berylowce, np. wapń, magnez), z wyjątkiem berylu. Ich aktywność rośnie wraz ze wzrostem liczby atomowej w grupie, co jest związane z rosnącą odległością elektronów walencyjnych od jądra atomowego, co ułatwia ich oddawanie.
Gdy kawałek sodu lub potasu umieścimy w wodzie, obserwujemy gwałtowną reakcję. Sód i potas, będące niezwykle aktywnymi metalami, muszą być przechowywane w oleju mineralnym lub nafcie, aby zapobiec ich reakcji z powietrzem i wilgocią. W kontakcie z wodą reagują błyskawicznie, wydzielając bezbarwny gaz (wodór) i tworząc wodorotlenek, który rozpuszcza się w wodzie, tworząc zasadowy roztwór.
Przykład reakcji sodu z wodą:2Na + 2H2O → 2NaOH + H2↑
(sód + woda → wodorotlenek sodu + wodór)
Przykład reakcji potasu z wodą:2K + 2H2O → 2KOH + H2↑
(potas + woda → wodorotlenek potasu + wodór)
Reakcje te są silnie egzotermiczne, co oznacza, że wydzielają dużą ilość ciepła. W przypadku sodu i potasu może dojść nawet do samozapłonu wydzielającego się wodoru, a reakcja jest tak gwałtowna, że może doprowadzić do wybuchu. Powstałe roztwory wodorotlenków sodu i potasu są silnie zasadowe, co można potwierdzić, dodając np. wywar z czerwonej kapusty, który zmieni barwę na zieloną.
Magnez, również metal aktywny z 2. grupy, reaguje z wodą, ale zazwyczaj wymaga podwyższonej temperatury, aby reakcja przebiegła zauważalnie. Powstaje wówczas wodorotlenek magnezu i wodór.
Przykład reakcji magnezu z wodą:Mg + 2H2O → Mg(OH)2 + H2↑
(magnez + woda → wodorotlenek magnezu + wodór)
Metale takie jak miedź są znacznie mniej aktywne i nie reagują z wodą w typowych warunkach.
Metoda 2: Reakcja tlenków metali aktywnych z wodą
Drugim sposobem otrzymywania wodorotlenków jest działanie tlenków metali aktywnych (tzw. tlenków zasadowych, pochodzących z 1. i 2. grupy układu okresowego, z wyjątkiem tlenku berylu) na wodę. W wyniku tych reakcji również powstają zasady, czyli wodne roztwory wodorotlenków.
Ogólny wzór reakcji:tlenek metalu aktywnego + woda → wodorotlenek
Przykład reakcji tlenku wapnia z wodą:CaO + H2O → Ca(OH)2
(tlenek wapnia + woda → wodorotlenek wapnia)
Ta reakcja, nazywana gaszeniem wapna, jest również silnie egzotermiczna i prowadzi do powstania wodorotlenku wapnia, który częściowo rozpuszcza się w wodzie, tworząc wodę wapienną. Pozostała część opada na dno w postaci zawiesiny. Dodanie fenoloftaleiny do tak powstałego roztworu spowoduje zmianę barwy na malinową, potwierdzając zasadowy charakter roztworu.
Przykład reakcji tlenku sodu z wodą:Na2O + H2O → 2NaOH
(tlenek sodu + woda → wodorotlenek sodu)
Metoda 3: Otrzymywanie wodorotlenków nierozpuszczalnych w wodzie
Wodorotlenki metali spoza 1. i 2. grupy układu okresowego, takie jak wodorotlenek żelaza(III) czy wodorotlenek miedzi(II), są zazwyczaj nierozpuszczalne w wodzie. Otrzymuje się je w reakcji mocnej zasady z solą danego metalu. W wyniku tej reakcji wytrąca się osad odpowiedniego wodorotlenku.
Przykład reakcji chlorku żelaza(III) z wodorotlenkiem sodu:FeCl3 + 3NaOH → Fe(OH)3↓ + 3NaCl
(chlorek żelaza(III) + wodorotlenek sodu → wodorotlenek żelaza(III) + chlorek sodu)
Przykład reakcji siarczanu miedzi(II) z wodorotlenkiem sodu:CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4
(siarczan miedzi(II) + wodorotlenek sodu → wodorotlenek miedzi(II) + siarczan sodu)
Właściwości Wodorotlenków: Różnorodność i Zastosowania
Większość wodorotlenków to ciała stałe. Ich rozpuszczalność w wodzie jest zróżnicowana. Wodorotlenki metali z 1. grupy układu okresowego (litowce) oraz niektóre z 2. grupy (np. wodorotlenek wapnia, strontu, baru) są dobrze rozpuszczalne w wodzie i tworzą silnie zasadowe roztwory, które tradycyjnie nazywamy zasadami. Wodne roztwory zasad przewodzą prąd elektryczny, ponieważ dysocjują na kationy metalu i aniony wodorotlenkowe, co czyni je mocnymi elektrolitami. Pozostałe wodorotlenki są słabo rozpuszczalne lub praktycznie nierozpuszczalne w wodzie i są słabymi elektrolitami.
Wodorotlenki są z reguły substancjami aktywnymi chemicznie. Ich najbardziej charakterystyczną reakcją jest reakcja z kwasami, w wyniku której tworzą się sole i woda. Reakcja ta nazywana jest reakcją zobojętniania.
Przykład reakcji zobojętniania:NaOH + HCl → NaCl + H2O
(wodorotlenek sodu + kwas chlorowodorowy → chlorek sodu + woda)
Wodorotlenki zasadowe a amfoteryczne
Wodorotlenki można podzielić na zasadowe i amfoteryczne.
- Wodorotlenki zasadowe (np. NaOH, KOH, Ca(OH)2) reagują z kwasami, tworząc sole, ale nie reagują z zasadami. Są to zazwyczaj krystaliczne ciała stałe, dobrze rozpuszczalne w wodzie (jeśli są zasadami).
- Wodorotlenki amfoteryczne (np. Al(OH)3, Zn(OH)2) wykazują podwójny charakter – mogą reagować zarówno z mocnymi kwasami, jak i z mocnymi zasadami. W obu przypadkach powstają sole, przy czym w reakcji z zasadami tworzą się związki kompleksowe (metal z wodorotlenku amfoterycznego wchodzi w skład anionu soli, np. [Al(OH)4]-). Wodorotlenki amfoteryczne często nie mają budowy krystalicznej, tworzą osady o charakterze koloidalnym i są nierozpuszczalne w wodzie.
Jak odróżnić wodorotlenek od zasady?
To kluczowe pytanie! Zrozumienie różnicy między tymi dwoma pojęciami jest fundamentalne w chemii. Najprościej mówiąc, każda zasada jest wodorotlenkiem, ale nie każdy wodorotlenek jest zasadą. Zasada to specyficzny rodzaj wodorotlenku – mianowicie taki, który dobrze rozpuszcza się w wodzie. Dlatego też, zasady to wodne roztwory rozpuszczalnych wodorotlenków, głównie metali z 1. grupy i niektórych z 2. grupy układu okresowego. Wodorotlenki, które są nierozpuszczalne w wodzie (np. wodorotlenek żelaza(III)), nie są zasadami.
| Cecha | Wodorotlenki rozpuszczalne (Zasady) | Wodorotlenki nierozpuszczalne |
|---|---|---|
| Rozpuszczalność w wodzie | Dobra | Bardzo słaba lub brak |
| Przewodnictwo elektryczne w roztworze | Mocne elektrolity | Słabe elektrolity lub brak |
| Typ metali | Grupa 1, niektóre z Grupy 2 (Ca, Sr, Ba) | Pozostałe metale (np. Fe, Al, Cu, Zn) |
| Reakcja z kwasami | Tak (zobojętnianie) | Tak |
| Reakcja z zasadami (wodorotlenki amfoteryczne) | Nie | Tak |
| Charakter | Zasadowy | Zasadowy lub amfoteryczny |
Przykłady Wodorotlenków w Praktyce
Wodorotlenek sodu (NaOH) – Soda kaustyczna
Wodorotlenek sodu, znany również jako soda kaustyczna lub soda żrąca, to białe, stałe ciało. Jest silnie higroskopijny, co oznacza, że pochłania wilgoć i dwutlenek węgla z powietrza, rozpuszczając się i pokrywając kruchą warstwą węglanu sodu. Rozpuszcza się w wodzie z wydzieleniem dużej ilości ciepła (reakcja egzotermiczna). Jest substancją silnie żrącą, niszczy bibułę, działa drażniąco na skórę, a w stanie stopionym niszczy szkło i porcelanę.
Otrzymywanie:
- Reakcja metalicznego sodu z wodą:
2Na + 2H2O → 2NaOH + H2↑ - Reakcja tlenku sodu z wodą:
Na2O + H2O → 2NaOH - Metoda kaustyfikacji sody:
Ca(OH)2 + Na2CO3 → 2NaOH + CaCO3↓ - Elektroliza wodnych roztworów chlorku sodu (metoda przemysłowa).
Zastosowanie: Wodorotlenek sodu jest szeroko wykorzystywany w przemyśle do produkcji mydła, środków piorących, celulozy, papieru, jedwabiu wiskozowego, barwników, detergentów. Znajduje zastosowanie w przemyśle włókienniczym, do wyrobu szkła wodnego, regeneracji kauczuku, w przemyśle petrochemicznym oraz do produkcji gumy. Jest również ważnym odczynnikiem laboratoryjnym i składnikiem wielu płynów czyszczących i wybielaczy (np. Domestos).
Wodorotlenek potasu (KOH) – Zasada potasowa
Wodorotlenek potasu, zwany zasadą potasową, wykazuje duże podobieństwo do wodorotlenku sodu. Jest białą, stałą substancją, higroskopijną, dobrze rozpuszczalną w wodzie z wydzieleniem ciepła. Jest substancją żrącą.
Otrzymywanie:
- Reakcja metalicznego potasu z wodą:
2K + 2H2O → 2KOH + H2↑ - Reakcja tlenku potasu z wodą:
K2O + H2O → 2KOH
Zastosowanie: Służy do produkcji mydła potasowego (miękkiego), wykorzystywany jest jako środek suszący, odczynnik laboratoryjny, w litografii, grawernictwie i rytownictwie.
Wodorotlenek wapnia (Ca(OH)2) – Wapno gaszone
Wodorotlenek wapnia, potocznie nazywany wapnem gaszonym, jest substancją, która niezbyt dobrze rozpuszcza się w wodzie. Zawiesina Ca(OH)2 opada na dno, a przezroczysta ciecz nad osadem to woda wapienna, wykorzystywana do wykrywania obecności dwutlenku węgla (zmętnienie wody wapiennej). Jest to mocna i tania zasada.
Otrzymywanie:
- Reakcja wapnia z wodą:
Ca + 2H2O → Ca(OH)2 + H2↑ - Reakcja tlenku wapnia (wapna palonego) z wodą:
CaO + H2O → Ca(OH)2(tzw. gaszenie wapna, reakcja silnie egzotermiczna).
Zastosowanie: Wapno gaszone po zmieszaniu z piaskiem i wodą tworzy zaprawę wapienną stosowaną w budownictwie. Mleko wapienne (zawiesina Ca(OH)2 w wodzie) służy jako środek dezynfekcyjny do bielenia wnętrz, budynków gospodarczych oraz zwalczania szkodników w sadownictwie. Stosowany jest również w przemyśle garbarskim, cukrowniczym, do zmiękczania wody, w procesie produkcji sody oraz jako sztuczny nawóz do gleb kwaśnych (wapnowanie).
Zasada amonowa (NH3·H2O lub NH4OH)
Zasada amonowa to wodny roztwór amoniaku. Choć często zapisywana jako NH4OH, w rzeczywistości jest to roztwór gazowego amoniaku (NH3) w wodzie, który reaguje z wodą, tworząc jony amonowe (NH4+) i wodorotlenkowe (OH-). Jest to słaba zasada, co oznacza, że tylko niewielka część cząsteczek amoniaku reaguje z wodą.
Zastosowanie: Wykorzystywana w przemyśle farmaceutycznym, do produkcji nawozów sztucznych, środków czyszczących oraz jako odczynnik laboratoryjny.
Najczęściej Zadawane Pytania (FAQ)
Czym różni się wodorotlenek od zasady?
Wodorotlenek to związek chemiczny zawierający grupę wodorotlenową (OH-) i kation metalu. Zasada to wodny roztwór wodorotlenku, który jest dobrze rozpuszczalny w wodzie. Oznacza to, że każda zasada jest wodorotlenkiem, ale nie każdy wodorotlenek jest zasadą (ponieważ wiele wodorotlenków jest nierozpuszczalnych w wodzie).
Dlaczego sód reaguje z wodą gwałtowniej niż magnez?
Sód jest metalem z 1. grupy układu okresowego (litowcem), a magnez z 2. grupy (berylowcem). Litowce mają tylko jeden elektron walencyjny, który łatwo oddają, co czyni je niezwykle reaktywnymi. Berylowce mają dwa elektrony walencyjne, które również oddają, ale proces ten jest mniej gwałtowny niż w przypadku litowców. Aktywność metali rośnie w dół grupy układu okresowego, ponieważ elektrony walencyjne są coraz dalej od jądra i słabiej przez nie przyciągane.
Jakie są główne metody otrzymywania wodorotlenków?
Główne metody to: 1) reakcja aktywnych metali (z 1. i 2. grupy układu okresowego, z wyjątkiem berylu) z wodą, 2) reakcja tlenków metali aktywnych (tlenków zasadowych) z wodą, oraz 3) reakcja mocnej zasady z solą metalu (dla wodorotlenków nierozpuszczalnych w wodzie).
Jak sprawdzić, czy roztwór jest zasadowy?
Aby sprawdzić, czy roztwór jest zasadowy, używa się wskaźników kwasowo-zasadowych. Najpopularniejsze to fenoloftaleina (zmienia barwę z bezbarwnej na malinową w zasadach), oranż metylowy (z pomarańczowego na żółty), lakmus (z fioletowego na niebieski) lub uniwersalny papierek wskaźnikowy (z żółtego na niebieski).
Czym różni się wodorotlenek amfoteryczny od zasadowego?
Wodorotlenki zasadowe reagują tylko z kwasami, tworząc sole. Wodorotlenki amfoteryczne wykazują podwójny charakter – reagują zarówno z mocnymi kwasami, jak i z mocnymi zasadami, tworząc w obu przypadkach sole (w reakcji z zasadami sole kompleksowe). Wodorotlenki amfoteryczne są zazwyczaj nierozpuszczalne w wodzie.
Podsumowanie
Wodorotlenki i zasady to fundamentalne związki chemiczne, zbudowane z kationów metali i anionów wodorotlenkowych. Ich budowa, nazewnictwo i właściwości są kluczowe dla zrozumienia wielu procesów chemicznych. Otrzymuje się je głównie w wyniku reakcji aktywnych metali z wodą lub tlenków metali aktywnych z wodą. Wodorotlenki rozpuszczalne w wodzie nazywamy zasadami, które są silnymi elektrolitami i odgrywają ogromną rolę w przemyśle, budownictwie, rolnictwie oraz w życiu codziennym. Poznanie tych związków pozwala nie tylko zrozumieć podstawy chemii, ale także dostrzec, jak wszechobecne są one w otaczającym nas świecie.
Zainteresował Cię artykuł Wodorotlenki i Zasady: Klucz do Chemii", "kategoria": "Chemia? Zajrzyj też do kategorii Edukacja, znajdziesz tam więcej podobnych treści!