27/11/2007
W świecie chemii nieorganicznej tlenki i sole stanowią dwie z najbardziej fundamentalnych i wszechstronnych grup związków. Zrozumienie ich właściwości, reakcji i zastosowań jest kluczowe dla każdego, kto zgłębia tajniki tej nauki, zwłaszcza w kontekście przygotowań do egzaminów maturalnych. Artykuł ten kompleksowo omówi charakter chemiczny tlenków, ich typowe reakcje, a także właściwości, rozpuszczalność, dysocjację i szerokie zastosowania soli, odpowiadając na najczęściej zadawane pytania.

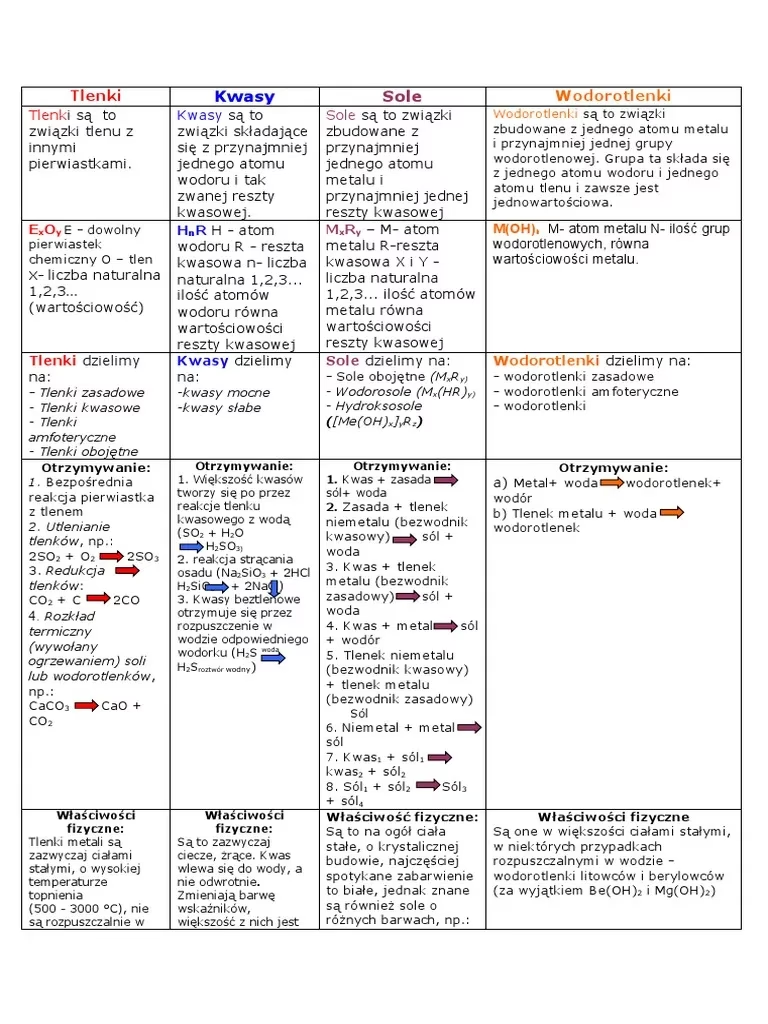
Charakter Chemiczny Tlenków – Co To Właściwie Znaczy?
Charakter chemiczny tlenków to zagadnienie o fundamentalnym znaczeniu w chemii. Określa on, w jaki sposób dany tlenek będzie zachowywał się w obecności kwasów i zasad. Choć często wspomina się również o jego zachowaniu w wodzie, należy pamiętać, że nie zawsze jest to czynnik decydujący. Istnieją tlenki nierozpuszczalne w wodzie, które mimo to zaliczamy do tlenków kwasowych lub zasadowych. Dlatego też, aby prawidłowo określić charakter chemiczny tlenku, zawsze badamy jego reaktywność względem kwasów i zasad.
Wyróżniamy cztery główne typy tlenków, każdy o specyficznym charakterze i reaktywności:
- Tlenki kwasowe: Zazwyczaj są to tlenki niemetali (np. SO3, SiO2), ale mogą to być również tlenki metali z bloku d na najwyższych stopniach utlenienia (np. CrO3). Reagują z zasadami, tworząc sole i wodę, ale nie reagują z kwasami. Jeśli są rozpuszczalne w wodzie, tworzą kwasy (wyjątkiem jest SiO2, który nie reaguje z wodą).
- Tlenki zasadowe: Są to tlenki metali bloku s (z wyjątkiem berylu, np. Na2O, CaO) oraz tlenki metali z bloku d na niskich stopniach utlenienia (np. CrO). Reagują z kwasami, tworząc sole i wodę, ale nie reagują z zasadami. Jeśli są rozpuszczalne w wodzie, tworzą zasady (wodorotlenki).
- Tlenki amfoteryczne: To tlenki pierwiastków bloku d na pośrednich stopniach utlenienia, a także tlenki berylu (BeO) i glinu (Al2O3). Są wyjątkowe, ponieważ reagują zarówno z kwasami, jak i z mocnymi zasadami, tworząc w obu przypadkach sole. Co istotne, zazwyczaj nie reagują z wodą.
- Tlenki obojętne: To tlenki, które nie reagują ani z kwasami, ani z zasadami. Przykładami są tlenek azotu (NO), tlenek węgla (CO) i podtlenek azotu (N2O). Mimo to, mogą one ulegać innym reakcjom, np. NO reaguje z tlenem atmosferycznym, tworząc NO2.
Tabela Porównawcza Charakteru Tlenków
| Typ Tlenku | Typowe Pierwiastki | Reakcja z Wodą (jeśli rozpuszczalny) | Reakcja z Kwasami | Reakcja z Zasadami | Przykłady |
|---|---|---|---|---|---|
| Kwasowy | Niemetale, metale bloku d (wysokie st. utl.) | Tworzą kwasy (oprócz SiO2) | NIE reagują | Reagują | SO3, SiO2, CrO3 |
| Zasadowy | Metale bloku s (bez Be), metale bloku d (niskie st. utl.) | Tworzą zasady | Reagują | NIE reagują | Na2O, CaO, MgO, CrO |
| Amfoteryczny | Pierwiastki bloku d (pośrednie st. utl.), Be, Al | NIE reagują | Reagują | Reagują z mocnymi zasadami | Al2O3, ZnO, Cr2O3 |
| Obojętny | Wybrane niemetale | NIE reagują | NIE reagują | NIE reagują | NO, CO, N2O |
Typowe Reakcje Tlenków
W chemii nieorganicznej wiele reakcji opiera się na zasadzie „przeciwieństwa się przyciągają”. Kwasowość i zasadowość można traktować jako przeciwne bieguny skali, co oznacza, że związki o charakterze kwasowym chętnie reagują ze związkami o charakterze zasadowym i odwrotnie. Związki amfoteryczne natomiast leżą „pośrodku” i reagują z obiema grupami. Ważne jest, że w tego typu reakcjach zwykle nie zmienia się stopień utlenienia atomów.
Reakcje Tlenków Kwasowych
Tlenki kwasowe, zgodnie z zasadą przeciwieństw, reagują z substancjami o charakterze zasadowym. Będą zatem chętnie reagować z zasadami oraz z tlenkami zasadowymi:
- SO3 + 2NaOH → Na2SO4 + H2O
- SO3 + Na2O → Na2SO4
Nie będą natomiast reagować z substancjami o charakterze kwasowym, takimi jak kwasy czy inne tlenki kwasowe:
- SO3 + HCl → nie zachodzi
- SO3 + N2O5 → nie zachodzi
Jeśli tlenek kwasowy jest rozpuszczalny w wodzie, będzie z nią reagował, tworząc kwas. Należy jednak pamiętać o ważnym wyjątku – SiO2 nie reaguje z wodą:
- SO3 + H2O → H2SO4
- SiO2 + H2O → nie zachodzi
Reakcje Tlenków Zasadowych
Tlenki zasadowe są przeciwieństwem tlenków kwasowych i reagują z substancjami o charakterze kwasowym, czyli z kwasami i tlenkami kwasowymi:
- Na2O + 2HCl → 2NaCl + H2O
- Na2O + H2SO4 → Na2SO4 + H2O
Analogicznie, tlenki zasadowe nie będą reagować z zasadami ani z innymi tlenkami zasadowymi:
- Na2O + KOH → nie zachodzi
- Na2O + K2O → nie zachodzi
Jeśli tlenek zasadowy jest rozpuszczalny w wodzie, będzie z nią reagował, tworząc roztwór wodorotlenku, czyli zasadę:
- Na2O + H2O → 2NaOH
Reakcje Tlenków Amfoterycznych
Tlenki amfoteryczne stanowią grupę pośrednią, reagującą zarówno z kwasami, jak i z mocnymi zasadami. W przeciwieństwie do większości tlenków kwasowych i zasadowych, tlenki amfoteryczne zazwyczaj nie reagują z wodą:
- Al2O3 + H2O → nie zachodzi
W reakcjach z kwasami, tlenki amfoteryczne zachowują się jak tlenki zasadowe, tworząc sole:
- Al2O3 + 6HCl → 2AlCl3 + 3H2O
Z mocnymi zasadami tworzą związki kompleksowe, zwane solami kompleksowymi. Najczęściej mają one liczbę koordynacyjną 4 lub 6:
- Al2O3 + 3H2O + 4NaOH → 2Na3[Al(OH)6]
Czasami spotyka się również uproszczoną formę tej reakcji bez wody jako substratu, np. Al2O3 + 6NaOH → 2Na3AlO3 + 3H2O. Jednak w kontekście reakcji w roztworach wodnych, pierwsza forma jest bardziej prawidłowa.
Reakcje Tlenków Obojętnych
Tlenki obojętne charakteryzują się tym, że nie reagują ani z kwasami, ani z zasadami:
- CO + NaOH → nie zachodzi
- CO + HCl → nie zachodzi
Pamiętaj jednak, że brak reakcji z kwasami i zasadami nie oznacza, że tlenki te nie ulegają żadnym innym reakcjom. Na przykład, tlenek azotu (NO) reaguje z tlenem atmosferycznym, tworząc NO2.
Tlenki Pierwiastków na Różnych Stopniach Utlenienia
Niektóre pierwiastki, zwłaszcza te z bloku d, mogą tworzyć tlenki na różnych stopniach utlenienia. Co ciekawe, charakter chemiczny tych tlenków zależy od stopnia utlenienia metalu. Ogólna zasada jest taka, że wraz ze wzrostem stopnia utlenienia pierwiastka, zwiększa się udział właściwości kwasowych tlenku, a zmniejsza udział właściwości zasadowych. Jest to ważna reguła, która pozwala przewidzieć zachowanie tlenków.
Sole: Budowa, Właściwości i Zastosowanie
Sole to rozległa grupa związków chemicznych, zbudowanych z kationów metali (lub kationu amonu NH4+) i anionów reszt kwasowych. Większość z nich ma budowę krystaliczną, choć istnieją wyjątki, takie jak difosforan cyny (niekrystaliczny) czy fluorek antymonu (ciekły). Sole są związkami jonowymi, a ich kryształy składają się z naprzemiennie ułożonych kationów i anionów. Warto podkreślić, że sole zawierają elementy pochodzące zarówno od wodorotlenków, jak i od kwasów.
Nazwy soli są dwuczłonowe: pierwszy człon pochodzi od reszty kwasowej, a drugi od metalu. Sole kwasów tlenowych mają końcówkę „-an” (np. siarczan, azotan), natomiast sole kwasów beztlenowych końcówkę „-ek” (np. siarczek, chlorek, jodek). Przy tworzeniu nazwy zawsze uwzględnia się wartościowość reszty kwasowej i metalu, często podając ją w nawiasie rzymską cyfrą, zwłaszcza gdy pierwiastek może występować na różnych stopniach utlenienia (np. siarczan(VI) miedzi(II)).
Najważniejsze Właściwości Soli
Kryształy soli zazwyczaj są bezbarwne, a biały kolor, który czasem obserwujemy, jest efektem ich rozdrobnienia. Istnieją jednak sole o wyraźnym zabarwieniu, które zależy od obecności jonów metali przejściowych. Przykładowo:
- Zielony lub niebieski – sole z kationami miedzi.
- Zielony – sole niklu.
- Żółty, brązowy, zielony – sole zawierające żelazo.
Ciekawą właściwością jest zmiana zabarwienia soli bezwodnych w procesie przechodzenia w sole uwodnione (hydraty). Na przykład, bezwodny chlorek kobaltu jest niebieski, ale po połączeniu z cząsteczkami wody zmienia kolor na różowy.

Jedną z kluczowych właściwości soli jest ich rozpuszczalność w wodzie. Większość soli rozpuszczalnych ulega w wodzie dysocjacji elektrolitycznej, czyli rozpadowi na swobodnie poruszające się jony. Rozpuszczalność związków zazwyczaj rośnie wraz ze wzrostem temperatury. Istnieje również spora grupa soli, które są trudno rozpuszczalne lub praktycznie nierozpuszczalne w wodzie, tworząc osady. Informacje o rozpuszczalności soli można znaleźć w specjalnych tablicach rozpuszczalności.
Wodne roztwory soli rozpuszczalnych są elektrolitami, co oznacza, że przewodzą prąd elektryczny. Jest to bezpośredni wynik obecności swobodnie poruszających się jonów w roztworze.
Budowa i Podział Soli
Sole zazwyczaj mają budowę jonową, będąc połączeniem metalu (lub grupy amonowej) i reszty kwasowej. W zależności od budowy wyróżniamy:
- Sole kwasów tlenowych: Aniony pochodzą od kwasów zawierających tlen, np. azotowy, siarkowy, węglowy, fosforowy. Nazwy kończą się na „-an”.
- Sole kwasów beztlenowych: Pochodne kwasów beztlenowych, ich nazwa kończy się na „-ek”, np. chlorek, bromek, siarczek.
- Wodorosole (sole kwaśne): Powstają z kwasów, w których nie wszystkie atomy wodoru zostały zastąpione kationami metali, np. wodorosiarczan(VI) sodu (NaHSO4).
- Hydroksosole (sole zasadowe): Sole, w których nie wszystkie aniony wodorotlenkowe zostały zastąpione anionami reszt kwasowych, np. chlorek hydroksowapnia (CaOHCl).
- Hydraty (sole uwodnione): Sole, które są dodatkowo związane z cząsteczkami wody.
- Sole podwójne i potrójne: Zawierają dwa lub trzy różne kationy połączone z jedną resztą kwasową.
Inny podział, oparty na charakterze kwasowo-zasadowym, wyróżnia:
- Sole obojętne: Zawierają jeden rodzaj kationu i jeden rodzaj anionu, np. NaCl.
- Sole kwaśne (wodorosole): Np. NaHSO4.
- Sole zasadowe (hydroksosole): Np. Mg(OH)Cl.
Reakcje, w Których Otrzymuje się Sole
Sole można otrzymać w wyniku wielu różnych reakcji chemicznych:
- Reakcja zobojętniania: Kwas reaguje z zasadą, tworząc sól i wodę. Aniony wodorotlenkowe z kationami wodoru tworzą obojętne cząsteczki wody.
NaOH + HCl → NaCl + H2O - Reakcja tlenku metalu z kwasem: Powstaje sól i woda.
CaO + 2HCl → CaCl2 + H2O - Reakcja tlenku niemetalu z zasadą: Powstaje sól i woda.
SO2 + 2KOH → K2SO3 + H2O - Reakcja kwasów z metalami (aktywnymi): Powstaje sól i wodór.
Mg + 2HCl → MgCl2 + H2↑ - Reakcja metalu z niemetalem: Powstaje sól.
Cu + Cl2 → CuCl2 - Reakcja dwóch wodnych roztworów soli: Jeśli jeden roztwór zawiera anion, a drugi kation soli trudno rozpuszczalnej, powstaje osad (nowa sól) i druga sól rozpuszczalna.
AgNO3 + KCl → AgCl↓ + KNO3 - Reakcja tlenku zasadowego z tlenkiem kwasowym: Powstaje sól.
BaO + CO2 → BaCO3
Dysocjacja Elektrolityczna Soli
Sole, podobnie jak wiele kwasów i wodorotlenków, ulegają w wodzie procesowi dysocjacji elektrolitycznej, o ile są w niej rozpuszczalne. Ten proces polega na rozpadzie związku na swobodnie poruszające się jony. Sole są związkami jonowymi, a ich sieć krystaliczna zbudowana jest z kationów metali i anionów reszt kwasowych. Pod wpływem polarnych cząsteczek wody, siły elektrostatyczne powodują uwolnienie tych jonów z sieci krystalicznej do roztworu.
Zapis opisujący proces dysocjacji przykładowych soli:
| Nazwa soli | Wzór sumaryczny soli | Dysocjacja soli |
|---|---|---|
| Chlorek sodu | NaCl | NaCl →H2O Na+ + Cl– |
| Azotan(V) potasu | KNO3 | KNO3 →H2O K+ + NO3– |
| Siarczan(VI) miedzi(II) | CuSO4 | CuSO4 →H2O Cu2+ + SO42– |
| Fosforan(V) potasu | K3PO4 | K3PO4 →H2O 3K+ + PO43– |
| Azotan(V) ołowiu(II) | Pb(NO3)2 | Pb(NO3)2 →H2O Pb2+ + 2NO3– |
| Siarczan(VI) żelaza(III) | Fe2(SO4)3 | Fe2(SO4)3 →H2O 2Fe3+ + 3SO42– |
Czy Sole Przewodzą Prąd Elektryczny?
Sole w stanie stałym zazwyczaj nie przewodzą prądu elektrycznego, ponieważ jony w ich sieci krystalicznej są unieruchomione. Dopiero pod wpływem wody, ulegając dysocjacji, jony stają się ruchliwe i mogą przenosić ładunki elektryczne. Dlatego wodne roztwory soli rozpuszczalnych są doskonałymi przewodnikami prądu elektrycznego – sole są elektrolitami.

Zastosowanie Soli w Życiu Codziennym i Przemyśle
Zastosowanie soli jest niezwykle szerokie i towarzyszy człowiekowi na każdym kroku. Ich unikalne właściwości znalazły zastosowanie w wielu dziedzinach, od kuchni po przemysł zaawansowany.
Sole w Przemyśle Farmaceutycznym i Medycynie
- Węglan magnezu: Stosowany jako suplement diety uzupełniający poziom magnezu, a także składnik leków zobojętniających kwas solny w żołądku.
- Azotan srebra: Aktywny składnik preparatów wspomagających gojenie się skóry i leczenie wirusowych zmian skórnych.
- Siarczan magnezu (sól gorzka): Znany środek przeczyszczający.
- Sól fizjologiczna (roztwór NaCl): Niezastąpiona w medycynie do przemywania ran, błon śluzowych, a także do wlewów dożylnych w celu uzupełnienia elektrolitów lub podawania leków.
Sole w Przemyśle Spożywczym
- Wodorowęglan sodu (soda oczyszczona): Składnik proszków do pieczenia, stosowany również jako regulator pH w produktach spożywczych.
- Azotany: Wykorzystywane do peklowania mięsa – zapobiegają jego psuciu się i pomagają zachować naturalną barwę.
- Chlorek sodu (sól kuchenna): Najpopularniejsza przyprawa, niezbędna w każdej kuchni.
Sole w Chemii Domowej i Innych Dziedzinach
- Proszki do prania: Sole zmiękczają wodę, poprawiając efektywność prania.
- Sole do kąpieli: Wykorzystywane w kosmetyce dla relaksu i pielęgnacji skóry.
- Nawozy roślinne: Wiele soli, np. azotany, fosforany, siarczany, to kluczowe składniki nawozów dostarczających roślinom niezbędne pierwiastki.
- Impregnaty do drewna: Chronią drewno przed szkodnikami i wilgocią.
- Produkcja luster, zaprawy gipsowej, ceramiki: Sole są surowcami w wielu procesach produkcyjnych.
Często Zadawane Pytania (FAQ)
Czy sole reagują z tlenkami?
Tak, sole mogą reagować z tlenkami, ale zależy to od charakteru chemicznego tlenków i samej soli. Najczęściej obserwuje się reakcje:
- Tlenki kwasowe z tlenkami zasadowymi: Reagują ze sobą, tworząc sól. Jest to jedna z metod otrzymywania soli. Na przykład: BaO (tlenek zasadowy) + CO2 (tlenek kwasowy) → BaCO3 (sól).
- Tlenki amfoteryczne: Mogą reagować z tlenkami kwasowymi (zachowując się jak tlenki zasadowe) oraz z tlenkami zasadowymi (zachowując się jak tlenki kwasowe), choć częściej spotyka się ich reakcje z kwasami i zasadami.
Warto pamiętać, że sole same w sobie nie reagują z każdym tlenkiem, a ich reakcje z tlenkami zazwyczaj wymagają specyficznych warunków, np. wysokiej temperatury lub obecności wody.
Czy wszystkie sole rozpuszczają się w wodzie?
Nie, nie wszystkie sole rozpuszczają się w wodzie w jednakowym stopniu. Istnieją sole bardzo dobrze rozpuszczalne (np. chlorek sodu, azotan(V) potasu), sole trudno rozpuszczalne (np. siarczan(VI) wapnia) oraz sole praktycznie nierozpuszczalne, które tworzą osady (np. węglan wapnia, siarczan(VI) baru). Informacje o rozpuszczalności soli w wodzie są zawarte w tablicy rozpuszczalności.
Jak rozpoznać sole od kwasów?
Sole i kwasy to różne grupy związków chemicznych, które można rozpoznać po ich budowie i właściwościach:
- Kwasy: W ich cząsteczkach zawsze występują atomy wodoru, które mogą być odszczepiane w postaci kationów H+ (protonów). Kwasy dysocjują na kationy wodoru i aniony reszty kwasowej. Wzory kwasów często zaczynają się od H, np. HCl, H2SO4. Ich wodne roztwory zazwyczaj mają kwaśny odczyn.
- Sole: Są to związki jonowe, zbudowane z kationów metali (lub kationu amonu NH4+) i anionów reszt kwasowych. Sole nie zawierają odszczepialnych kationów H+. Ich wzory sumaryczne zazwyczaj zaczynają się od symbolu metalu, np. NaCl, CuSO4. Wodne roztwory soli mogą mieć odczyn obojętny, kwasowy lub zasadowy, w zależności od hydrolizy.
Podsumowując, zarówno tlenki, jak i sole są niezmiernie ważnymi grupami związków w chemii, posiadającymi szerokie spektrum właściwości i zastosowań. Zrozumienie ich charakteru, reakcji i zachowania w roztworach wodnych jest kluczowe dla pełnego zrozumienia zasad chemii nieorganicznej.
Zainteresował Cię artykuł Sole i Tlenki: Podstawy Chemii Nieorganicznej", "kategoria": "Chemia? Zajrzyj też do kategorii Edukacja, znajdziesz tam więcej podobnych treści!

