10/02/2011
Czy zastanawiałeś się kiedyś, jak prosta zmiana chemiczna może mieć ogromny wpływ na działanie leków, a nawet na to, jak twoje geny są włączane i wyłączane? Kluczem do zrozumienia wielu takich procesów jest acetylacja – fundamentalna reakcja chemiczna, która odgrywa zaskakująco wszechstronną rolę zarówno w laboratorium, jak i w złożonym świecie biologii. Od produkcji popularnych leków, przez zabezpieczanie grup funkcyjnych w syntezie organicznej, aż po precyzyjną kontrolę ekspresji genów w każdej komórce naszego ciała – acetylacja jest wszechobecna i niezwykle ważna. W tym artykule zagłębimy się w świat tej fascynującej reakcji, wyjaśniając jej mechanizmy, zastosowania i biologiczne znaczenie, tak abyś mógł w pełni zrozumieć jej kluczową rolę w nauce i życiu.
Czym jest Acetylacja?
Acetylacja to nic innego jak reakcja chemiczna, w której do związku chemicznego zostaje przyłączona grupa acetylowa (CH3C=O). Proces ten polega na zastąpieniu aktywnego atomu wodoru (najczęściej w grupie hydroksylowej -OH lub aminowej -NH2) właśnie tą grupą acetylową. W wyniku acetylacji powstają związki, które często zawierają grupę funkcyjną acetoksy (-OCOCH3) lub są estrami octowymi, jeśli grupa acetylowa zastąpiła wodór z grupy alkoholowej. Reakcja ta jest specyficznym rodzajem acylowania, czyli ogólnego procesu wprowadzania grupy acylowej (R-C=O) do cząsteczki. W przypadku acetylacji, grupa acylowa to konkretnie grupa acetylowa, pochodząca zazwyczaj od kwasu octowego lub jego pochodnych.
Przeciwieństwem acetylacji jest deacetylacja, czyli proces usuwania grupy acetylowej z cząsteczki. Ta odwracalność jest niezwykle ważna, zwłaszcza w kontekście biologicznym, gdzie precyzyjna kontrola nad dodawaniem i usuwaniem grup acetylowych decyduje o aktywności wielu białek i regulacji procesów komórkowych.
Główne Czynniki Acetylujące
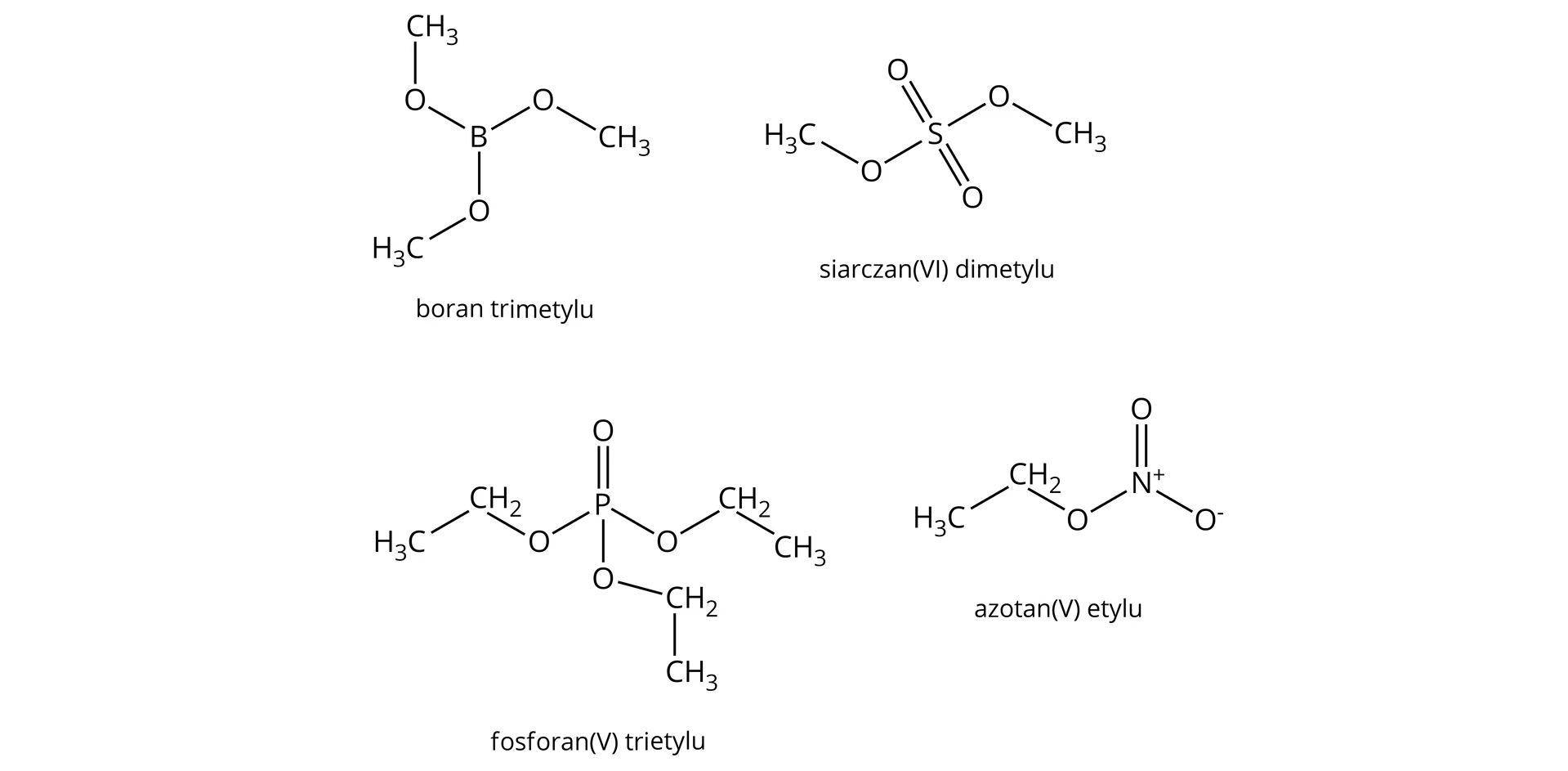
W chemii organicznej, do przeprowadzenia acetylacji wykorzystuje się różne związki, które są źródłem grupy acetylowej. Najczęściej stosowane czynniki acetylujące to:
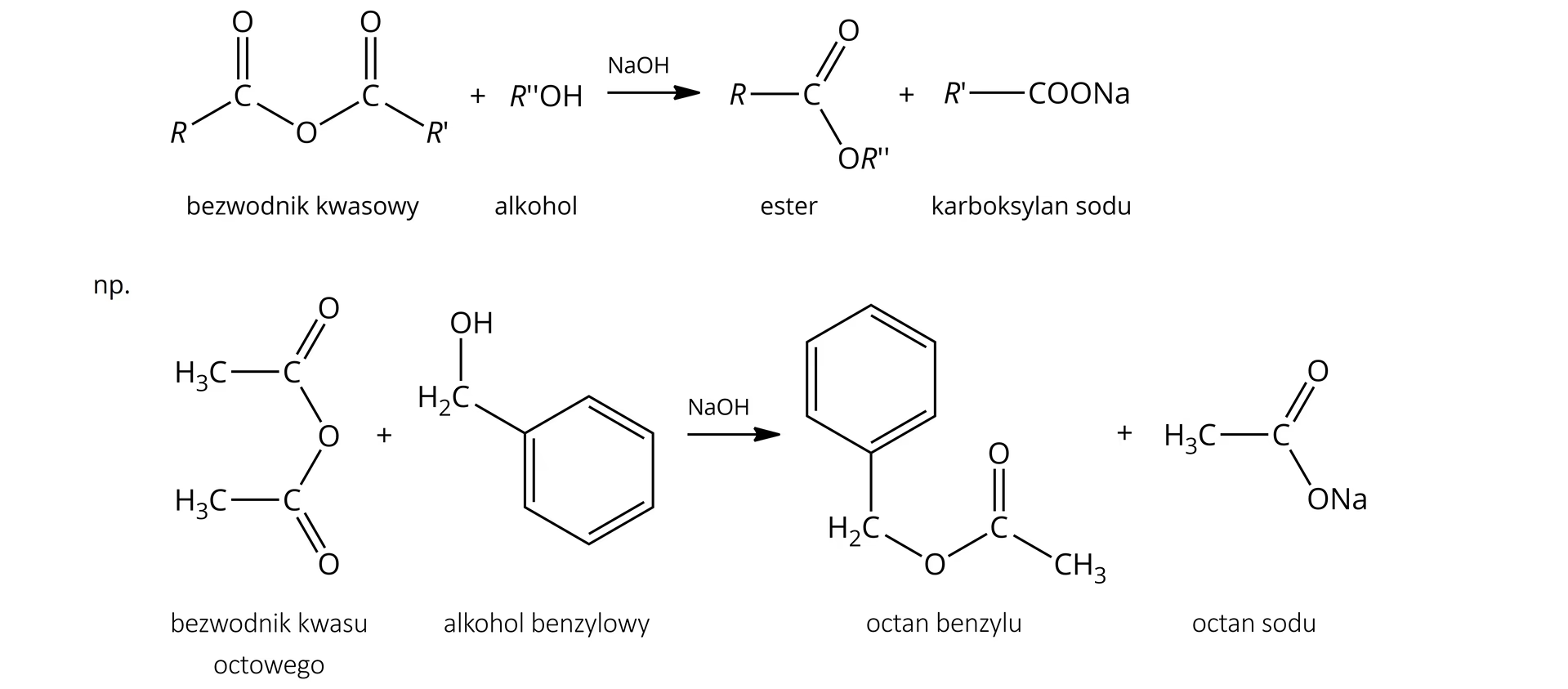
- Bezwodnik octowy ((CH3CO)2O): Jest to bardzo popularny i skuteczny czynnik acetylujący ze względu na swoją wysoką reaktywność i stosunkowo łatwą dostępność. Jest często używany w syntezach laboratoryjnych i przemysłowych.
- Chlorek acetylu (CH3COCl): To kolejny silnie reaktywny czynnik acetylujący, który jest jednak bardziej lotny i trudniejszy w obsłudze niż bezwodnik octowy ze względu na swoją korozyjność.
- Kwas octowy (CH3COOH): Może być używany jako czynnik acetylujący, choć jest mniej reaktywny niż bezwodnik octowy czy chlorek acetylu i często wymaga zastosowania katalizatora kwasowego, aby reakcja przebiegała efektywnie.
- Acetylo-CoA: W systemach biologicznych, głównym donorem grupy acetylowej jest acetylo-koenzym A (acetylo-CoA), który jest kluczowym metabolitem w wielu szlakach metabolicznych.
Zastosowanie Acetylacji w Syntezie Organicznej
W chemii organicznej, acetylacja jest nie tylko metodą tworzenia nowych związków, ale także strategicznym narzędziem w wieloetapowych syntezach. Jednym z kluczowych zastosowań jest zabezpieczanie grup funkcyjnych. Reaktywne grupy, takie jak grupy hydroksylowe (-OH) w alkoholach i fenolach, czy grupy aminowe (-NH2) w aminach, mogą ulegać niepożądanym reakcjom w trakcie kolejnych etapów syntezy. Poprzez ich acetylację, na przykład do postaci estrów octowych (dla -OH) lub amidów (dla -NH2), ich reaktywność jest tymczasowo „wyłączana”.
Po zakończeniu wymaganych reakcji na innych częściach cząsteczki, grupa acetylowa może zostać usunięta, czyli następuje proces deacetylacji, który przywraca oryginalną grupę funkcyjną. Deacetylacja może być przeprowadzona w stosunkowo łagodnych warunkach, na przykład poprzez hydrolizę (kwasową lub zasadową) lub amonolizę (reakcję z amoniakiem). Dzięki temu chemicy mogą precyzyjnie kontrolować przebieg syntezy, izolując tylko pożądane reakcje i chroniąc wrażliwe fragmenty cząsteczki.
Acetylacja w Systemach Biologicznych: Klucz do Regulacji Życia
Jednak prawdziwa magia acetylacji objawia się w systemach biologicznych, gdzie odgrywa ona kluczową rolę w regulacji funkcji białek i ekspresji genów. Jest to przykład modyfikacji potranslacyjnej, czyli chemicznej zmiany białka po jego syntezie, która wpływa na jego aktywność, stabilność, lokalizację czy interakcje z innymi cząsteczkami.
Acetylacja Białek – Ogólne Zasady
W biologii, acetylacja białek polega na przyłączeniu reszty acetylowej, pochodzącej z acetylo-CoA, do białka w miejscu aktywnego atomu wodoru w bocznej grupie funkcyjnej reszty aminokwasowej białka. Najczęściej acetylacji ulegają reszty lizynowe, ale inne reszty aminokwasowe również mogą być acetylowane. Ta z pozoru niewielka zmiana chemiczna może mieć dalekosiężne konsekwencje dla funkcji białka.
N-końcowa Acetylacja Białek
Jednym z bardzo powszechnych typów acetylacji białek jest N-końcowa acetylacja. Jest to modyfikacja kowalencyjna, która często zachodzi już podczas syntezy białka (ko-translacyjnie), szczególnie u eukariotów (organizmów z jądrem komórkowym, w tym ludzi). Polega ona na przyłączeniu grupy acetylowej do wolnej grupy aminowej na N-końcu białka. Ta modyfikacja może wpływać na stabilność białka, jego oddziaływania z innymi cząsteczkami, a nawet na jego transport w komórce.
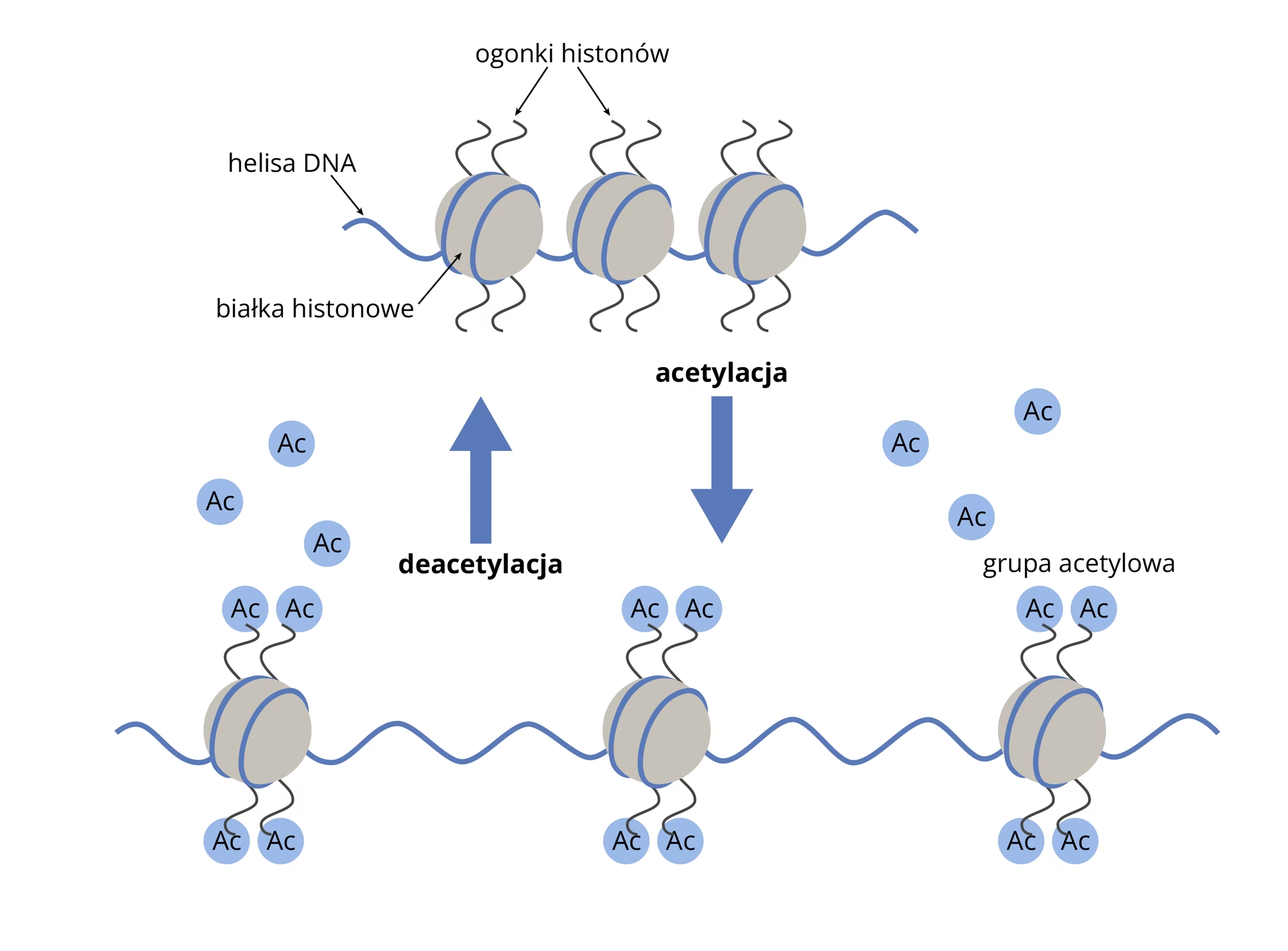
Acetylacja Histonów: Włącznik/Wyłącznik Genów
Aby zrozumieć najbardziej spektakularne znaczenie acetylacji w biologii, musimy najpierw przyjrzeć się histonom – białkom, wokół których nawinięte jest DNA w jądrze komórkowym, tworząc strukturę zwaną chromatyną. Chromatyna jest niczym skomplikowany system upakowania, który pozwala na zmieszczenie gigantycznej długości DNA w mikroskopijnym jądrze komórkowym. To upakowanie nie jest jednak statyczne; jest dynamicznie regulowane, a od jego stopnia zależy, czy geny są dostępne do odczytu (transkrypcji).
Acetylacja i deacetylacja histonów to kluczowe modyfikacje potranslacyjne, które stanowią fundamentalny mechanizm epigenetyczny kontroli ekspresji genów. „Epigenetyka” odnosi się do zmian w aktywności genów, które nie wynikają ze zmian w sekwencji DNA, ale są dziedziczone i regulują, które geny są aktywne, a które nie.
Mechanizm Działania
W histonach, to głównie reszty lizynowe, obecne w tzw. ogonach N-końcowych wystających z rdzenia nukleosomu (podstawowej jednostki chromatyny), ulegają acetylacji lub deacetylacji. Proces ten jest ściśle kontrolowany przez dwa typy enzymów:
- Acetylotransferazy histonowe (HATs): Enzymy te dodają grupy acetylowe do grup ε-aminowych reszt lizyny.
- Deacetylazy histonowe (HDACs): Enzymy te usuwają grupy acetylowe z reszt lizyny.
Jak to działa? Reszty lizyny w histonach posiadają dodatni ładunek elektryczny. Gdy HATs przyłączają grupę acetylową do lizyny, neutralizują jej dodatni ładunek. Ta neutralizacja ładunku zmniejsza siłę oddziaływań elektrostatycznych między histonami a ujemnie naładowanym DNA. W rezultacie struktura chromatyny staje się luźniejsza, bardziej „otwarta” (tworzy się euchromatyna), co ułatwia dostęp maszynerii transkrypcyjnej do DNA i zwiększa poziom ekspresji genów – geny są „włączane”.
Z drugiej strony, gdy HDACs usuwają grupy acetylowe, lizyna odzyskuje swój dodatni ładunek. Powoduje to silniejsze oddziaływania elektrostatyczne między histonami a DNA, co prowadzi do ściślejszego upakowania chromatyny (tworzy się heterochromatyna). Ta skondensowana struktura utrudnia dostęp do DNA, hamując transkrypcję i „wyłączając” geny.
Równowaga między acetylacją a deacetylacją histonów jest kluczowa dla prawidłowego funkcjonowania komórek i organizmu. Zaburzenia w tym procesie mogą prowadzić do wielu chorób, w tym nowotworów, dlatego inhibitory deacetylazy histonowej (HDACis) są przedmiotem intensywnych badań w terapii przeciwnowotworowej.
Poniższa tabela porównuje efekty acetylacji i deacetylacji histonów:
| Cecha | Acetylacja Histonów | Deacetylacja Histonów |
|---|---|---|
| Wpływ na ładunek lizyny | Neutralizuje dodatni ładunek | Zwiększa dodatni ładunek (protonacja) |
| Wpływ na oddziaływania z DNA | Osłabia oddziaływania elektrostatyczne | Wzmacnia oddziaływania elektrostatyczne |
| Struktura chromatyny | Rozluźnienie (euchromatyna) | Kondensacja (heterochromatyna) |
| Dostępność DNA do transkrypcji | Ułatwiony dostęp | Utrudniony dostęp |
| Ekspresja genów | Zwiększona (geny "włączone") | Zahamowana (geny "wyłączone") |
Acetylacja Białek Niehistonowych
Warto podkreślić, że acetylacja nie ogranicza się wyłącznie do histonów. Wiele innych białek niehistonowych, w tym czynniki transkrypcyjne (białka regulujące transkrypcję), enzymy metaboliczne, białka cytoszkieletu, a nawet białka związane z naprawą DNA, również ulega acetylacji i deacetylacji. Te modyfikacje mogą wpływać na ich aktywność enzymatyczną, stabilność, lokalizację w komórce, a także na interakcje z innymi cząsteczkami. Oznacza to, że acetylacja jest wszechobecnym mechanizmem regulacyjnym, wpływającym na niemal każdy aspekt funkcjonowania komórki.
Przykłady Reakcji Acetylacji
Synteza Aspiryny (Kwasu Acetylosalicylowego)
Najbardziej znanym przykładem acetylacji w codziennym życiu jest synteza kwasu acetylosalicylowego, powszechnie znanego jako aspiryna. Aspiryna to popularny lek przeciwbólowy, przeciwzapalny i przeciwgorączkowy, który jest syntetyzowany z kwasu salicylowego poprzez reakcję acetylacji z bezwodnikiem octowym.
Reakcja ta zachodzi w środowisku kwasowym (zazwyczaj z użyciem stężonego kwasu siarkowego jako katalizatora). W jej trakcie grupa hydroksylowa (-OH) kwasu salicylowego ulega acetylacji, a w jej miejsce wchodzi grupa acetylowa, tworząc ester. Jednocześnie powstaje kwas octowy jako produkt uboczny. Mechanizm reakcji polega na tym, że kwas siarkowy protonuje jeden z atomów tlenu w bezwodniku octowym, co zwiększa jego reaktywność. Następnie, grupa hydroksylowa kwasu salicylowego atakuje węgiel karbonylowy bezwodnika, prowadząc do powstania związku pośredniego. Po dalszych przekształceniach i utracie cząsteczki kwasu octowego, powstaje pożądany kwas acetylosalicylowy. To klasyczny przykład, jak prosta reakcja chemiczna może prowadzić do powstania leku o tak szerokim zastosowaniu.
Acetylacja Aniliny do Acetanilidu
Innym przykładem acetylacji w chemii organicznej jest reakcja aniliny (amina aromatyczna) z bezwodnikiem octowym (w obecności lodowatego kwasu octowego) w celu otrzymania acetanilidu. W tej reakcji grupa aminowa (-NH2) aniliny ulega acetylacji, tworząc amid. Acetanilid jest ważnym półproduktem w syntezie wielu innych związków organicznych i był kiedyś stosowany jako środek przeciwgorączkowy i przeciwbólowy, zanim został zastąpiony bezpieczniejszymi alternatywami.
Często Zadawane Pytania (FAQ)
Czy acetylacja jest odwracalna?
Tak, acetylacja jest procesem odwracalnym. Reakcja odwrotna, czyli usunięcie grupy acetylowej, nazywana jest deacetylacją. W chemii organicznej deacetylacja może być przeprowadzona poprzez hydrolizę (kwasową lub zasadową) lub amonolizę. W systemach biologicznych deacetylacja jest katalizowana przez specyficzne enzymy, takie jak deacetylazy histonowe (HDACs).

Jakie są główne czynniki acetylujące w laboratorium?
W laboratorium najczęściej stosowanymi czynnikami acetylującymi są bezwodnik octowy ((CH3CO)2O) oraz chlorek acetylu (CH3COCl). Kwas octowy (CH3COOH) również może być używany, ale jest mniej reaktywny i często wymaga katalizatora.
Dlaczego acetylacja białek jest tak ważna w biologii?
Acetylacja białek, zwłaszcza histonów, jest kluczowa dla regulacji ekspresji genów. Poprzez zmianę upakowania chromatyny, acetylacja wpływa na to, czy geny są „włączane” czy „wyłączane”. Ma to fundamentalne znaczenie dla rozwoju, funkcjonowania komórek, a także dla odpowiedzi na stres i choroby. Acetylacja wpływa również na aktywność i stabilność wielu innych białek niehistonowych, regulując szeroki zakres procesów komórkowych.
Czym różni się acetylacja od acylowania?
Acylowanie to ogólny termin oznaczający reakcję chemiczną, w której grupa acylowa (R-C=O, gdzie R to dowolna grupa organiczna) jest wprowadzana do cząsteczki. Acetylacja jest specyficznym rodzajem acylowania, w którym wprowadzaną grupą acylową jest konkretnie grupa acetylowa (CH3C=O). Zatem każda acetylacja jest acylowaniem, ale nie każde acylowanie jest acetylacją.
Czy acetylacja ma zastosowanie w medycynie poza aspiryną?
Tak, acetylacja ma szerokie zastosowanie w medycynie. Poza aspiryną, procesy acetylacji i deacetylacji są celami dla wielu leków, zwłaszcza w dziedzinie onkologii. Inhibitory deacetylazy histonowej (HDACis) są badane i stosowane w leczeniu niektórych nowotworów, ponieważ mogą one zmieniać ekspresję genów w komórkach rakowych, prowadząc do ich śmierci lub zahamowania wzrostu. Ponadto, wiele innych leków i związków aktywnych biologicznie może być modyfikowanych przez acetylację w celu poprawy ich właściwości farmakologicznych.
Podsumowanie
Acetylacja to znacznie więcej niż tylko prosta reakcja chemiczna. To wszechstronny mechanizm, który ma fundamentalne znaczenie zarówno w przemyśle farmaceutycznym, jak i w skomplikowanych procesach biologicznych, takich jak regulacja ekspresji genów. Od syntezy aspiryny, przez ochronę grup funkcyjnych w zaawansowanej chemii, aż po precyzyjne sterowanie aktywnością genów poprzez modyfikację histonów – acetylacja jest kluczowym elementem, który pomaga nam zrozumieć, jak działa świat chemii i biologii. Jej głębokie zrozumienie otwiera drzwi do dalszych odkryć w medycynie, biotechnologii i naukach podstawowych, podkreślając, jak potężne mogą być nawet najmniejsze zmiany na poziomie molekularnym.
Zainteresował Cię artykuł Acetylacja: Klucz do Zrozumienia Procesów Życia", "kategoria": "Chemia? Zajrzyj też do kategorii Edukacja, znajdziesz tam więcej podobnych treści!
