09/12/2023
W świecie chemii organicznej, gdzie różnorodność związków jest niemal nieograniczona, kluczowe jest posiadanie narzędzi pozwalających na ich precyzyjną identyfikację. Wśród nich wyróżniają się dwie niezwykle ważne reakcje: próba Tollensa i próba Trommera. Oba te testy stanowią fundament w laboratoryjnym wykrywaniu aldehydów oraz odróżnianiu ich od ketonów, a także w identyfikacji specyficznych rodzajów cukrów. Uczniowie klasy IV LO o profilu medycznym mieli okazję przekonać się o ich praktycznym zastosowaniu, wykonując obie te próby na zajęciach chemii. Zapraszamy do zgłębienia tajników tych fascynujących reakcji chemicznych.
Próba Tollensa: Lustro Srebra w Praktyce
Próba Tollensa, znana również jako próba lustra srebrowego, to klasyczna reakcja chemiczna wykorzystywana do wykrywania obecności aldehydów. Nazwa "lustro srebrowe" doskonale oddaje jej najbardziej charakterystyczny efekt – podczas pozytywnego wyniku reakcji na wewnętrznej powierzchni naczynia reakcyjnego osadza się metaliczne srebro w postaci błyszczącej, lustrzanej powłoki. Jest to efekt wizualny, który nie tylko świadczy o obecności grupy aldehydowej, ale także znalazł zastosowanie w praktyce, np. do posrebrzania szklanych bombek choinkowych, choć współcześnie jest to zastosowanie historyczne.
Odczynnik Tollensa i jego przygotowanie
Kluczowym elementem tej próby jest odczynnik Tollensa – świeżo sporządzony roztwór azotanu srebra z wodą amoniakalną. W rzeczywistości jest to amoniakalny roztwór wodorotlenku diaminasrebra(I), o wzorze [Ag(NH3)2]OH, często określany mianem "srebra amoniakalnego". Proces jego przygotowania jest dwuetapowy i wymaga precyzji: najpierw do roztworu azotanu(V) srebra dodaje się wodę amoniakalną, co prowadzi do wytrącenia czarnobrunatnego osadu tlenku srebra(I) (Ag2O). Następnie, w miarę dodawania kolejnych porcji wody amoniakalnej, osad ten ulega roztworzeniu, tworząc wspomniany kompleksowy wodorotlenek diaminasrebra(I). Należy pamiętać, że odczynnik ten jest nietrwały i musi być przygotowany bezpośrednio przed użyciem. Długotrwałe przechowywanie takich roztworów jest niebezpieczne, ponieważ może prowadzić do powstania substancji o właściwościach wybuchowych, takich jak azotek srebra(I) (Ag3N).
Mechanizm reakcji Tollensa
Próba Tollensa to klasyczny przykład reakcji redoks, czyli reakcji utleniania-redukcji. W tym procesie aldehydy, zawierające redukującą grupę aldehydową (-CHO), ulegają utlenieniu do odpowiednich kwasów karboksylowych (RCOOH). Jednocześnie jon kompleksowy srebra z odczynnika Tollensa (gdzie srebro występuje na I stopniu utlenienia) ulega redukcji do metalicznego srebra (Ag0). To właśnie to zredukowane srebro osadza się na ściankach naczynia, tworząc charakterystyczne lustro. Reakcja ta jest zazwyczaj przeprowadzana w podwyższonej temperaturze i w lekko zasadowym środowisku, co sprzyja jej przebiegowi. Brak pojawienia się srebrnej powłoki oznacza negatywny wynik próby.
Próba Trommera: Miedź w Służbie Chemii Organicznej
Podobnie jak próba Tollensa, próba Trommera jest reakcją chemiczną stosowaną do jakościowego oznaczania aldehydów. Wykorzystuje ona również redukujące właściwości grupy aldehydowej, ale w odróżnieniu od próby Tollensa, jej odczynnikiem jest związek miedzi.
Odczynnik Trommera i jego właściwości
Odczynnikiem Trommera jest świeżo strącony wodorotlenek miedzi(II) (Cu(OH)2). Przybiera on postać niebieskiego, galaretowatego osadu. Jest to kluczowe, aby odczynnik był świeżo strącony, gdyż tylko wtedy jest on wystarczająco reaktywny. W podwyższonej temperaturze wodorotlenek miedzi(II) pełni rolę utleniacza.

Mechanizm reakcji Trommera
W próbie Trommera aldehyd (RCHO) ulega utlenieniu do kwasu karboksylowego (RCOOH), tak samo jak w próbie Tollensa. Wodorotlenek miedzi(II) natomiast, ulegnie redukcji. Miedź z II stopnia utlenienia (w Cu(OH)2) redukuje się do miedzi(I), tworząc ceglastoczerwony osad tlenku miedzi(I) (Cu2O). Jest to wizualny sygnał pozytywnego wyniku próby Trommera. Reakcja również wymaga ogrzewania.
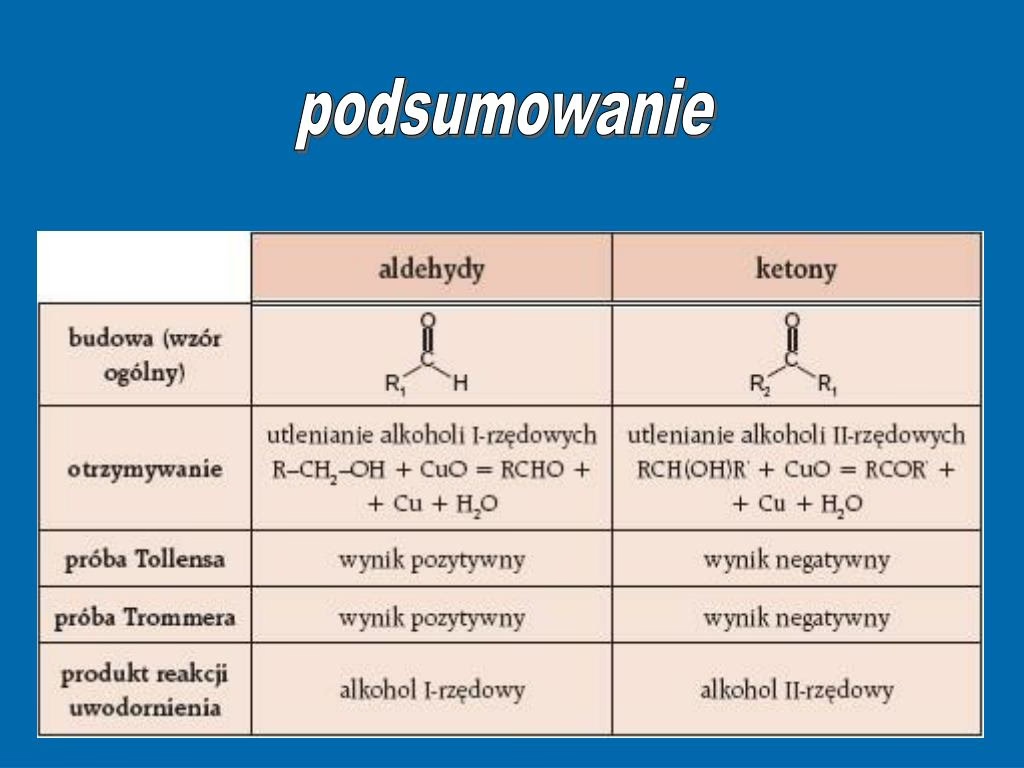
Aldehydy a Ketony: Klucz do Rozróżnienia
Obie próby – Trommera i Tollensa – są niezastąpionymi narzędziami w chemii organicznej, pozwalającymi na identyfikację grupy aldehydowej (-CHO) oraz, co równie ważne, na rozróżnienie aldehydów od ketonów. Dlaczego tak się dzieje?
Różnica w zachowaniu aldehydów i ketonów w tych próbach wynika bezpośrednio z ich struktury chemicznej. Aldehydy posiadają w swojej grupie funkcyjnej (-CHO) atom wodoru przyłączony bezpośrednio do atomu węgla grupy karbonylowej. Ten atom wodoru jest łatwo usuwalny podczas reakcji utleniania, co sprawia, że aldehydy są związkami łatwo utlenialnymi do kwasów karboksylowych. To właśnie ta łatwość utleniania jest podstawą pozytywnych wyników w próbach Tollensa i Trommera.
Ketony natomiast, choć na pierwszy rzut oka wydają się bardzo podobne do aldehydów (również zawierają grupę karbonylową -CO-), różnią się tym, że zamiast atomu wodoru przy węglu karbonylowym, mają dwie grupy alkilowe (lub arylowe). Brak tego atomu wodoru sprawia, że ketony są znacznie trudniejsze do utlenienia w łagodnych warunkach. W rezultacie, ketony dają negatywne wyniki w próbach Tollensa i Trommera. W przypadku próby Trommera z ketonami, często obserwuje się pojawienie się czarnego osadu tlenku miedzi(II) (CuO), który powstaje w wyniku termicznego rozkładu wodorotlenku miedzi(II) w podwyższonej temperaturze, a nie w wyniku reakcji redoks z ketonem.
Kwas Mrówkowy i Jego Wyjątkowe Właściwości Redukujące
Choć próby Tollensa i Trommera są przede wszystkim testami na aldehydy, istnieje jeden wyjątkowy kwas karboksylowy, który również wykazuje właściwości redukujące i może dawać pozytywne (lub częściowo pozytywne) wyniki w tych testach. Mowa o kwasie mrówkowym (metanowym).
Kwas mrówkowy jest jedynym spośród kwasów karboksylowych, który posiada właściwości redukujące. Ta unikalna cecha wynika z obecności w jego strukturze zarówno grupy karboksylowej (-COOH), jak i, co kluczowe, aldehydopodobnej grupy (-CHO) wbudowanej w strukturę. Atom wodoru jest przyłączony bezpośrednio do węgla karbonylowego, co umożliwia mu pełnienie roli reduktora.
Wynik próby Tollensa dla kwasu mrówkowego
W przypadku próby Tollensa z kwasem mrówkowym, jej efekt można uznać za pozytywny – wytrąca się srebrnoczarny osad, świadczący o redukcji jonów srebra. Należy jednak zaznaczyć, że w przeciwieństwie do aldehydów, nie powstaje typowe lustro srebrowe. Anion mrówczanowy (pochodzący od kwasu mrówkowego) podczas próby Tollensa jest utleniany do anionu węglanowego (CO32-).
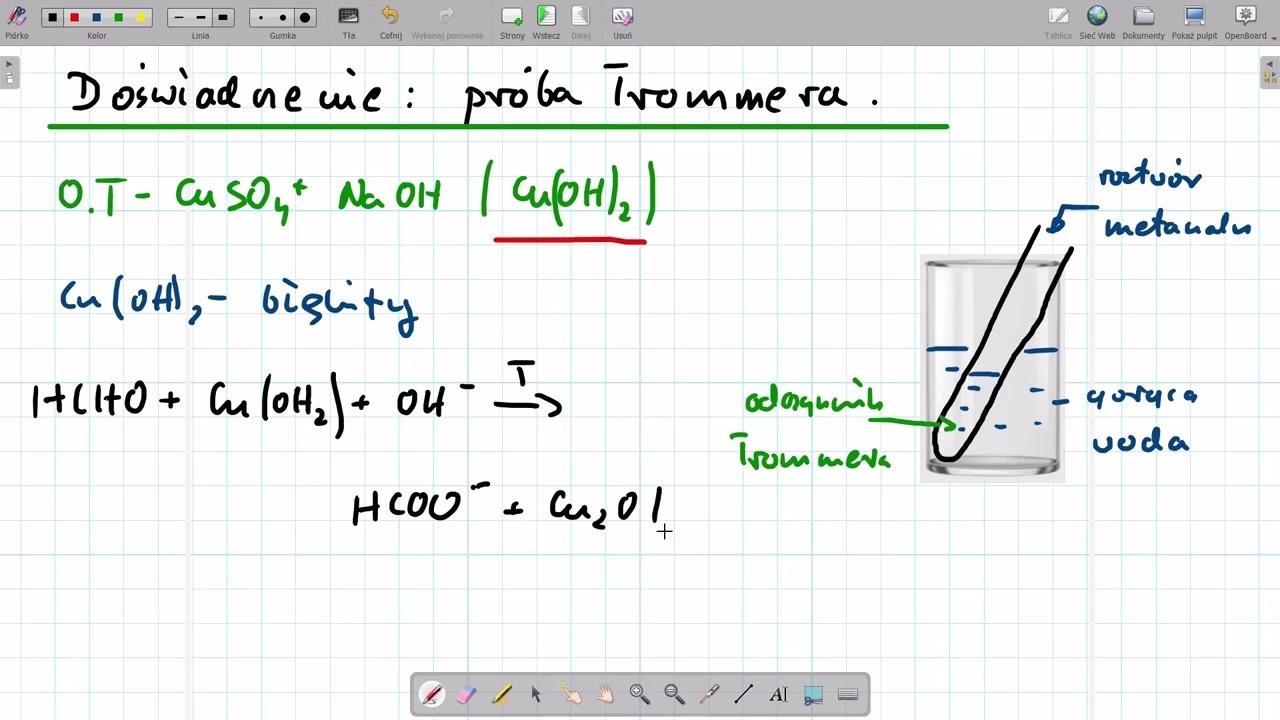
Wynik próby Trommera dla kwasu mrówkowego
Co ciekawe, mimo swoich właściwości redukujących, kwas mrówkowy daje negatywny wynik próby Trommera. Po dodaniu go do świeżo strąconej zawiesiny wodorotlenku miedzi(II) o odczynie zasadowym i ogrzaniu naczynia reakcyjnego, zamiast ceglastoczerwonego osadu tlenku miedzi(I), obserwuje się powstanie czarnego osadu. Dzieje się tak, ponieważ w warunkach próby Trommera kwas mrówkowy przechodzi w anion mrówczanowy, natomiast osad wodorotlenku miedzi(II) nie roztwarza się i ulega termicznemu rozkładowi do czarnego tlenku miedzi(II) (CuO). Oznacza to, że kwas mrówkowy nie jest w stanie zredukować jonów miedzi(II) do miedzi(I) w tych konkretnych warunkach.
Cukry Redukujące: Słodkie Wykrywanie
Zarówno próba Trommera, jak i Tollensa są również wykorzystywane jako narzędzia pozwalające na identyfikację cukrów redukujących. Cukry redukujące to takie, które posiadają wolną grupę aldehydową lub ketonową, która może izomeryzować do grupy aldehydowej.
Wszystkie aldozy (cukry zawierające grupę aldehydową, np. glukoza) są cukrami redukującymi. Dają one pozytywny wynik w obu próbach, ponieważ posiadają aldehydową grupę karbonylową, która łatwo ulega utlenieniu.
Należy jednak pamiętać, że niektóre ketozy (cukry zawierające grupę ketonową, np. fruktoza) również są cukrami redukującymi, mimo że nie zawierają grupy aldehydowej w swojej podstawowej formie. Dzieje się tak, ponieważ w warunkach zasadowych (w jakich przeprowadzane są obie próby) fruktoza łatwo izomeryzuje do aldolozy poprzez szereg tautomerycznych przesunięć keto-enolowych. Po izomeryzacji do formy aldehydowej, może ona zredukować odczynnik Tollensa lub Trommera, dając pozytywny wynik.
Tabela Porównawcza: Próba Tollensa vs. Próba Trommera
Aby ułatwić zrozumienie różnic i podobieństw między tymi dwoma ważnymi próbami, przedstawiamy tabelę porównawczą:
| Cecha | Próba Tollensa | Próba Trommera |
|---|---|---|
| Główny cel | Wykrywanie aldehydów, rozróżnianie aldehydów od ketonów, wykrywanie cukrów redukujących | Wykrywanie aldehydów, rozróżnianie aldehydów od ketonów, wykrywanie cukrów redukujących |
| Odczynnik | Amoniakalny roztwór azotanu srebra ([Ag(NH3)2]OH) | Świeżo strącony wodorotlenek miedzi(II) (Cu(OH)2) |
| Kolor/Forma odczynnika | Bezbarwny roztwór (po rozpuszczeniu Ag2O) | Niebieski, galaretowaty osad |
| Obserwowany pozytywny wynik | Lustro srebrowe (metaliczne srebro) na ściankach naczynia | Ceglastoczerwony osad (tlenek miedzi(I), Cu2O) |
| Stopień utlenienia metalu (przed → po) | Ag+ → Ag0 | Cu2+ → Cu+ |
| Wynik dla ketonów | Negatywny | Negatywny (czarny osad CuO z rozkładu Cu(OH)2) |
| Wynik dla kwasu mrówkowego | Pozytywny (srebrnoczarny osad, brak lustra) | Negatywny (czarny osad CuO) |
| Wymagane warunki | Ogrzewanie, środowisko zasadowe | Ogrzewanie, środowisko zasadowe |
Często Zadawane Pytania (FAQ)
Do czego służą próby Tollensa i Trommera?
Służą przede wszystkim do jakościowego wykrywania aldehydów w próbkach chemicznych. Pozwalają również na rozróżnienie aldehydów od ketonów oraz na identyfikację cukrów redukujących.

Czy ketony dają pozytywny wynik w tych próbach?
Nie, ketony z reguły dają negatywny wynik w obu próbach. Wynika to z ich budowy chemicznej – brak atomu wodoru przyłączonego bezpośrednio do węgla karbonylowego sprawia, że są one znacznie trudniejsze do utlenienia niż aldehydy w łagodnych warunkach tych testów.
Czy kwasy karboksylowe ulegają próbie Trommera lub Tollensa?
Zazwyczaj nie. Większość kwasów karboksylowych nie posiada właściwości redukujących i nie reaguje z odczynnikami Tollensa ani Trommera. Wyjątkiem jest kwas mrówkowy (metanowy), który jako jedyny z kwasów karboksylowych posiada właściwości redukujące. W próbie Tollensa daje pozytywny wynik (srebrnoczarny osad, ale bez lustra), natomiast w próbie Trommera wynik jest negatywny (powstaje czarny osad CuO).
Jak zapamiętać różnice między próbą Tollensa a Trommera?
Łatwo zapamiętać różnicę, kojarząc metale użyte w odczynnikach z nazwami i wynikami:
- Tollens: "T" jak "To srebro", srebro daje lustro srebrowe. Srebro jest cenne, więc daje "piękne" lustro.
- Trommer: "Tr" jak "Trudna miedź" lub "Tradycyjna miedź", miedź daje ceglastoczerwony osad.
Pamiętaj też, że oba testy opierają się na utlenianiu aldehydów i redukcji jonów metalu, ale w przypadku Tollensa jest to srebro, a w Trommera – miedź.
Czy cukry nieredukujące (np. sacharoza) dają pozytywny wynik?
Nie, cukry nieredukujące, takie jak sacharoza, nie posiadają wolnej grupy aldehydowej ani ketonowej, która mogłaby izomeryzować do aldehydowej. W związku z tym, nie dają one pozytywnych wyników w próbach Tollensa ani Trommera.
Podsumowanie
Próby Tollensa i Trommera są podstawowymi i niezwykle użytecznymi narzędziami w chemii organicznej. Pozwalają one szybko i wizualnie zidentyfikować obecność grupy aldehydowej, odróżnić aldehydy od ketonów, a także wykryć obecność cukrów redukujących. Zrozumienie mechanizmów tych reakcji, właściwości używanych odczynników oraz interpretacja wyników jest kluczowa dla każdego, kto zgłębia świat chemii. Pamiętajmy o wyjątkowych właściwościach kwasu mrówkowego i o tym, że nawet z pozoru podobne związki mogą zachowywać się zupełnie inaczej w obliczu tych specyficznych testów.
Zainteresował Cię artykuł Próby Tollensa i Trommera: Wykrywanie Aldehydów? Zajrzyj też do kategorii Chemia, znajdziesz tam więcej podobnych treści!
