08/01/2024
W fascynującym świecie chemii nieorganicznej, gdzie każdy związek odgrywa kluczową rolę, kwasy stanowią jedną z najbardziej intrygujących i wszechobecnych grup substancji. Odgrywają one fundamentalne znaczenie zarówno w procesach naturalnych, jak i w niezliczonych zastosowaniach przemysłowych oraz codziennym życiu. Zrozumienie ich budowy, właściwości i reakcji jest niezbędne dla każdego, kto chce zgłębić tajniki tej nauki. Wraz z wodorotlenkami i tlenkami, kwasy tworzą trzon związków nieorganicznych, a ich wzajemne oddziaływania kształtują świat wokół nas. W tym artykule zanurzymy się głębiej w świat kwasów, odkrywając ich różnorodność i wyjaśniając, dlaczego są tak ważne.

Chemia nieorganiczna to dziedzina zajmująca się badaniem związków chemicznych, które zazwyczaj nie zawierają wiązań węgiel-wodór, choć istnieją pewne wyjątki. W ramach tej szerokiej kategorii wyróżniamy tlenki, wodorotlenki, kwasy i sole. Każda z tych grup charakteryzuje się specyficzną budową i właściwościami, które decydują o ich zastosowaniach. Chociaż wodorotlenki, jako związki chemiczne zbudowane z kationów metalu i anionów wodorotlenkowych, mają swoje unikalne cechy, takie jak higroskopijność w przypadku wodorotlenku sodu i potasu, to właśnie kwasy często wzbudzają największe zainteresowanie ze względu na swoją reaktywność i wszechstronność.
Czym są Kwasy w Chemii?
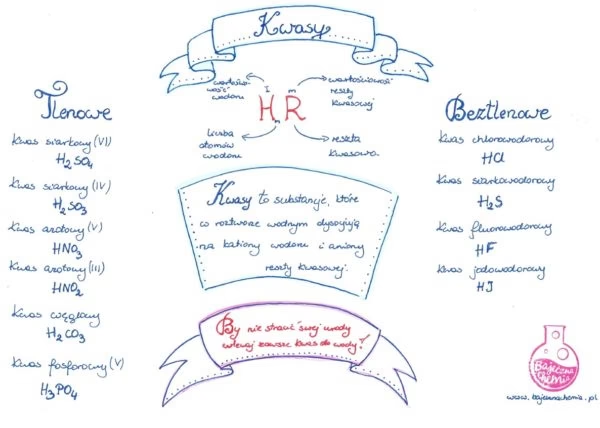
Zgodnie z klasyczną teorią Arrheniusa, kwasy to związki chemiczne, których cząsteczki są zbudowane z atomów wodoru i tak zwanej reszty kwasowej. W roztworach wodnych, kwasy dysocjują, czyli rozpadają się na kationy wodoru (H+) i aniony reszt kwasowych. To właśnie obecność kationów wodoru jest odpowiedzialna za charakterystyczne właściwości kwasowe roztworów, takie jak kwaśny smak (choć nigdy nie należy próbować kwasów!) czy zdolność do zmiany barwy wskaźników.
Ogólny wzór kwasów można przedstawić jako HnR, gdzie 'n' oznacza liczbę atomów wodoru w cząsteczce kwasu, a 'R' to reszta kwasowa. Ładunek anionu reszty kwasowej jest zawsze równy liczbie kationów wodoru, które uwalniają się podczas dysocjacji. To podstawowe zrozumienie budowy pozwala nam klasyfikować kwasy i przewidywać ich zachowanie w różnych reakcjach chemicznych.
Rodzaje Kwasów: Tlenowe i Beztlenowe
Kwasy można podzielić na dwie główne kategorie, bazując na obecności lub braku atomów tlenu w ich cząsteczkach: kwasy beztlenowe i kwasy tlenowe. Każda z tych grup ma swoje specyficzne metody otrzymywania i charakterystyczne zastosowania.
Kwasy Beztlenowe
W cząsteczkach kwasów beztlenowych atomy wodoru łączą się bezpośrednio z atomem niemetalu. Są to zazwyczaj proste związki, ale ich roztwory wodne wykazują silne właściwości kwasowe. Otrzymuje się je zazwyczaj przez rozpuszczenie w wodzie związku chemicznego powstałego podczas reakcji wodoru z niektórymi niemetalami. Przykładowo, popularny kwas chlorowodorowy, znany również jako kwas solny, powstaje w wyniku reakcji wodoru z chlorem, a następnie rozpuszczenia powstałego chlorowodoru w wodzie:
H2 (g) + Cl2 (g) → 2 HCl (g)
HCl (g) → H2O HCl (aq)
Innym ważnym kwasem beztlenowym jest kwas siarkowodorowy (H2S), często kojarzony z zapachem zgniłych jaj.
Zastosowanie Kwasów Beztlenowych
Mimo swojej prostoty, kwasy beztlenowe mają szerokie zastosowanie:
- Kwas chlorowodorowy (solny): Jest to jeden z najważniejszych kwasów w przemyśle i laboratorium. Wykorzystuje się go do produkcji leków (np. w syntezie niektórych substancji czynnych), barwników, tworzyw sztucznych (np. do produkcji bidonów sportowych), a także w przemyśle tekstylnym do obróbki tkanin. Ma również kluczowe znaczenie w hutnictwie do trawienia metali oraz jako odczynnik w laboratoriach chemicznych. Nawet w przemyśle spożywczym, w niewielkich ilościach, jest używany do regulacji kwasowości, np. w słodkich żelkach.
- Kwas siarkowodorowy: Mimo swojego nieprzyjemnego zapachu, jest stosowany jako odczynnik laboratoryjny do wykrywania niektórych jonów metali. Występuje również naturalnie w wodach mineralnych o specyficznych właściwościach zdrowotnych.
Kwasy Tlenowe
Kwasy tlenowe to związki, w których reszta kwasowa zawiera atomy tlenu. Są one zazwyczaj otrzymywane w wyniku reakcji tlenku niemetalu z wodą. Na przykład, kwas siarkowy(VI), jeden z najsilniejszych i najbardziej wszechstronnych kwasów, powstaje z tlenku siarki(VI) i wody:
SO3 + H2O → H2SO4
Nazewnictwo kwasów tlenowych często zawiera rzymską cyfrę w nawiasie po nazwie niemetalu, która informuje o wartościowości tego niemetalu w danym kwasie, np. kwas siarkowy(VI).
Zastosowanie Kwasów Tlenowych
Kwasy tlenowe odgrywają ogromną rolę w przemyśle i życiu codziennym:
- Kwas siarkowy(VI): Nazywany „królem kwasów” ze względu na swoje wszechstronne zastosowanie. Jest kluczowym składnikiem nawozów sztucznych, akumulatorów samochodowych, a także wykorzystywany jest do produkcji leków, detergentów, barwników i w przemyśle tekstylnym. Pełni funkcję odczynnika laboratoryjnego i środka suszącego.
- Kwas siarkowy(IV): Stosowany jest głównie w przemyśle papierniczym do produkcji papieru oraz jako środek konserwujący, np. do beczek drewnianych.
- Kwas azotowy(V): Ważny w produkcji nawozów sztucznych, barwników, a także w przemyśle farmaceutycznym (do produkcji nitrogliceryny) i wojskowym (do produkcji materiałów wybuchowych).
- Kwas fosforowy(V): Wykorzystywany do produkcji nawozów sztucznych, jako środek do polerowania stali, a także jako regulator kwasowości w napojach gazowanych.
- Kwas węglowy: Choć jest to kwas nietrwały, obecny jest w wodach gazowanych i odgrywa rolę w procesach biologicznych.
Właściwości Kwasów: Od Higroskopijności po Reakcje z Białkami
Kwasy wykazują szereg charakterystycznych właściwości, które decydują o ich zastosowaniach i wymagają ostrożności w obchodzeniu się z nimi. Jedną z najważniejszych cech wielu stężonych kwasów jest ich żrący charakter. Oznacza to, że mogą one powodować poważne uszkodzenia skóry, tkanek i wielu materiałów. Dlatego zawsze należy przestrzegać podstawowej zasady bezpieczeństwa podczas pracy z kwasami, zwłaszcza przy ich rozcieńczaniu: „Pamiętaj chemiku młody, wlewaj zawsze kwas do wody!” Dodawanie wody do stężonego kwasu może prowadzić do gwałtownego wydzielania ciepła i niebezpiecznego rozpryskiwania substancji.
Niektóre kwasy, jak na przykład stężony kwas siarkowy(VI), posiadają silne właściwości higroskopijne, co oznacza, że bardzo chętnie pochłaniają wodę z otoczenia. Ta cecha sprawia, że kwas siarkowy(VI) jest wykorzystywany jako środek suszący w laboratoriach. Inną ciekawą właściwością jest zdolność stężonego kwasu azotowego(V) do wykrywania białek. Reakcja ksantoproteinowa, polegająca na działaniu kwasem azotowym(V) na substancje zawierające białko, powoduje ich zabarwienie na żółto, co jest często wykorzystywane w analizach chemicznych.
Wskaźniki Chemiczne i Skala pH: Jak Rozpoznać Kwas?
W laboratorium i w życiu codziennym często zachodzi potrzeba określenia, czy dana substancja ma odczyn kwasowy, zasadowy czy obojętny. W tym celu wykorzystuje się specjalne substancje zwane wskaźnikami. Ich działanie polega na łatwo zauważalnej zmianie barwy pod wpływem różnych odczynów roztworu.

Najbardziej popularnym narzędziem do szybkiej oceny odczynu jest uniwersalny papierek wskaźnikowy. W środowisku kwasowym barwi się on na czerwono, natomiast w zasadowym na zielono lub niebiesko. Bardziej precyzyjną miarą kwasowości i zasadowości roztworu jest skala pH. Skala ta przyjmuje wartości od 0 do 14. Roztwory o pH poniżej 7 są kwasowe, o pH równym 7 są obojętne, a o pH powyżej 7 są zasadowe.
Oto tabela prezentująca zachowanie wybranych wskaźników w różnych środowiskach:
| Wskaźnik | Barwa w środowisku kwasowym (pH < 7) | Barwa w środowisku obojętnym (pH = 7) | Barwa w środowisku zasadowym (pH > 7) |
|---|---|---|---|
| Oranż metylowy | Czerwony | Pomarańczowy | Żółty |
| Fenoloftaleina | Bezbarwna | Bezbarwna | Malinowa |
| Papierek uniwersalny | Czerwony | Żółty | Zielony/Niebieski |
| Wywar z czerwonej kapusty | Czerwony | Fioletowy | Zielony |
Zastosowania Kwasów w Życiu Codziennym i Przemyśle
Kwasy, ze względu na swoje unikalne właściwości, są niezastąpione w wielu gałęziach przemysłu i w życiu codziennym. Stanowią podstawę produkcji nawozów sztucznych, które są niezbędne dla rolnictwa i zapewnienia bezpieczeństwa żywnościowego. Kwas siarkowy(VI) jest nieodzowny w produkcji akumulatorów, a kwas azotowy(V) i fosforowy(V) są kluczowe w przemyśle chemicznym, farmaceutycznym i spożywczym.
W przemyśle tekstylnym kwasy są wykorzystywane do barwienia tkanin i ich obróbki. W metalurgii służą do oczyszczania powierzchni metali przed dalszą obróbką. Nawet w naszych domach spotykamy kwasy – na przykład w środkach czyszczących, odkamieniaczach (często zawierających kwas cytrynowy lub octowy) czy nawet w napojach gazowanych (kwas węglowy, kwas fosforowy). Są również obecne w naszym organizmie, np. kwas solny w żołądku, niezbędny do trawienia.
Ważne Zasady Bezpieczeństwa
Praca z kwasami wymaga szczególnej ostrożności ze względu na ich żrące właściwości. Zawsze należy używać odpowiedniego sprzętu ochronnego, takiego jak rękawice, okulary ochronne i fartuch laboratoryjny. W przypadku kontaktu kwasu ze skórą lub oczami, należy natychmiast przemyć to miejsce dużą ilością wody i zasięgnąć pomocy medycznej. Rozcieńczanie kwasów powinno odbywać się zawsze poprzez powolne dolewanie kwasu do wody, nigdy odwrotnie, aby uniknąć gwałtownego wydzielania ciepła i rozprysków. Odpowiednie wentylowanie pomieszczeń jest również kluczowe, ponieważ opary niektórych kwasów mogą być drażniące lub toksyczne.
Często Zadawane Pytania
Czym różni się kwas od zasady?
Główna różnica leży w ich budowie i sposobie dysocjacji w wodzie. Kwasy (np. HCl, H2SO4) w roztworze wodnym dysocjują na kationy wodoru (H+) i aniony reszt kwasowych. To kationy H+ nadają roztworowi charakter kwasowy. Zasady (czyli rozpuszczalne w wodzie wodorotlenki, np. NaOH, KOH) dysocjują na kationy metalu (np. Na+, K+) i aniony wodorotlenkowe (OH-). To aniony OH- są odpowiedzialne za charakter zasadowy roztworu. Kwasy i zasady reagują ze sobą w procesie neutralizacji, tworząc sole i wodę.
Dlaczego fenoloftaleina nie nadaje się do wykrywania kwasów?
Fenoloftaleina jest wskaźnikiem, który zmienia barwę z bezbarwnej na malinową w środowisku zasadowym (pH powyżej 8,2). W środowisku kwasowym (pH poniżej 8,2) pozostaje bezbarwna. Oznacza to, że jeśli dodamy fenoloftaleinę do roztworu kwasowego, nie zaobserwujemy żadnej zmiany barwy, co uniemożliwia nam stwierdzenie obecności kwasu. Jest ona natomiast bardzo skuteczna do wykrywania zasad.
Czy kwasy są zawsze niebezpieczne?
Nie wszystkie kwasy są równie niebezpieczne. Stężone mocne kwasy, takie jak kwas siarkowy(VI), azotowy(V) czy chlorowodorowy, są bardzo żrące i mogą powodować poważne oparzenia. Istnieją jednak również kwasy słabe, takie jak kwas octowy (składnik octu) czy kwas cytrynowy (obecny w cytrynach), które są znacznie mniej niebezpieczne w rozcieńczonych roztworach i są powszechnie stosowane w kuchni czy przemyśle spożywczym. Stopień niebezpieczeństwa zależy od stężenia, mocy kwasu oraz sposobu jego użycia.
Jak sprawdzić odczyn roztworu mydła?
Roztwór mydła ma zazwyczaj odczyn zasadowy. Można to sprawdzić na kilka sposobów: najprostszym jest użycie uniwersalnego papierka wskaźnikowego – powinien zmienić barwę na zieloną lub niebieską. Innym sposobem jest dodanie kilku kropli fenoloftaleiny do roztworu mydła; jeśli roztwór zmieni barwę na malinową, potwierdzi to jego zasadowy charakter. Można również użyć wywaru z czerwonej kapusty, który w roztworze mydła zabarwi się na zielono.
Czym są kwaśne opady?
Kwaśne opady to opady atmosferyczne (deszcz, śnieg, mgła), które mają niższe pH niż normalne opady (pH około 5,6). Są one spowodowane emisją do atmosfery tlenków siarki (głównie SO2) i tlenków azotu (głównie NOx), pochodzących głównie ze spalania paliw kopalnych w przemyśle i transporcie. Te tlenki reagują z parą wodną w atmosferze, tworząc kwas siarkowy i kwas azotowy, które następnie opadają na ziemię. Kwaśne opady mają szkodliwy wpływ na środowisko, powodując zakwaszenie gleb i wód, niszczenie lasów, uszkodzenia budynków i pomników oraz negatywny wpływ na zdrowie ludzi i zwierząt.
Podsumowanie
Kwasy są niezwykle ważną i różnorodną grupą związków chemicznych, które otaczają nas w każdym aspekcie życia. Od prostych kwasów beztlenowych, takich jak kwas chlorowodorowy, po złożone kwasy tlenowe, jak kwas siarkowy(VI), ich rola w przemyśle, nauce i naturze jest nie do przecenienia. Zrozumienie ich budowy, właściwości, metod otrzymywania i zastosowań jest kluczowe dla każdego, kto chce pogłębiać wiedzę chemiczną. Pamiętajmy jednak, że z ich mocą wiąże się odpowiedzialność – zawsze należy obchodzić się z nimi z należytą ostrożnością i przestrzegać zasad bezpieczeństwa. Mamy nadzieję, że ten artykuł rozjaśnił Państwu świat kwasów i zachęcił do dalszych chemicznych odkryć!
Zainteresował Cię artykuł Kwasy w Chemii: Rodzaje, Właściwości i Zastosowania", "kategoria": "Chemia? Zajrzyj też do kategorii Edukacja, znajdziesz tam więcej podobnych treści!