08/08/2017
Zrozumienie kształtu cząsteczek to jeden z najbardziej fascynujących i fundamentalnych aspektów chemii. To nie tylko abstrakcyjna koncepcja; trójwymiarowa struktura cząsteczki ma kluczowe znaczenie dla jej właściwości fizycznych i chemicznych, w tym reaktywności, polarności, temperatury topnienia i wrzenia, a nawet funkcji biologicznych, takich jak zdolność leku do wiązania się z receptorem w organizmie. Wyobraź sobie, że każda cząsteczka ma swój unikalny „odcisk palca” w przestrzeni, który decyduje o tym, jak oddziałuje z innymi cząsteczkami i środowiskiem. Ale jak naukowcy są w stanie określić te niewidzialne kształty? W tym artykule zanurkujemy w świat geometrii molekularnej, ze szczególnym uwzględnieniem potężnej Teorii VSEPR, która pozwala przewidzieć te kształty z zadziwiającą precyzją, bazując na prostych zasadach odpychania elektronów.
Czym jest Geometria Cząsteczkowa?
Geometria cząsteczkowa, zwana również geometrią molekularną, to dziedzina chemii zajmująca się badaniem trójwymiarowego rozmieszczenia atomów tworzących cząsteczkę. Jest to klucz do zrozumienia, jak atomy są ze sobą połączone i w jaki sposób te połączenia wpływają na ogólny kształt cząsteczki. Geometria molekularna dostarcza informacji nie tylko o ogólnym kształcie cząsteczki, ale także o długościach wiązań (odległościach między jądrami atomów), kątach wiązań (kątach między dwoma wiązaniami wychodzącymi z tego samego atomu centralnego), kątach torsyjnych (kątach obrotu wokół wiązania) oraz wszelkich innych parametrach geometrycznych, które precyzyjnie określają pozycję każdego atomu w przestrzeni. W cząsteczkach kowalencyjnych, gdzie atomy dzielą się elektronów, wiązania mają charakter kierunkowy. Oznacza to, że wspólne pary elektronów pozostają zlokalizowane w określonej przestrzeni między jądrami uczestniczących atomów. Model przestrzenny, który uzyskujemy poprzez połączenie punktów reprezentujących różne wiązania w cząsteczce kowalencyjnej, odzwierciedla jej rzeczywisty kształt. To właśnie ten kształt decyduje o tym, czy dana substancja będzie gazem, cieczą czy ciałem stałym, jak będzie rozpuszczać się w innych substancjach, a nawet jak będzie reagować w skomplikowanych procesach chemicznych i biologicznych. Na przykład, różnica w kształcie między dwutlenkiem węgla (liniowy) a wodą (kątowy) jest fundamentalna dla ich odmiennych właściwości i roli w naturze.
Jak Określić Kształty Cząsteczek?
Określanie geometrii molekularnej odbywa się za pomocą różnych metod, zarówno eksperymentalnych, jak i teoretycznych. Eksperymentalne techniki pozwalają na bezpośrednie pomiary odległości i kątów w cząsteczkach:
- Metody spektroskopowe: Spektroskopia IR (podczerwieni), mikrofalowa i Ramana to potężne narzędzia, które analizują interakcję cząsteczek ze światłem. Mogą one dostarczyć informacji o geometrii cząsteczki na podstawie szczegółów absorpcji wibracyjnej i rotacyjnej wykrywanej przez te techniki. Każda cząsteczka ma unikalny "odcisk palca" w widmie, który zależy od jej kształtu.
- Metody dyfrakcyjne: Krystalografia rentgenowska, dyfrakcja neutronów i dyfrakcja elektronów są stosowane do badania struktury krystalicznych ciał stałych (krystalografia rentgenowska) lub cząsteczek w fazie gazowej (dyfrakcja elektronów). Te metody dostarczają precyzyjnych danych o odległościach między jądrami atomów i koncentracji gęstości elektronowej, co pozwala na rekonstrukcję trójwymiarowej struktury molekularnej.
Jednakże, geometrie i obserwowane kształty cząsteczek kowalencyjnych można również przewidzieć teoretycznie za pomocą niezwykle użytecznej i powszechnie stosowanej Teorii Odpychania Par Elektronów Walencyjnych (VSEPR). Ta teoria, choć prosta w założeniach, jest niezwykle skuteczna w przewidywaniu trójwymiarowych struktur cząsteczek, co czyni ją podstawowym narzędziem dla każdego chemika. Jej siła tkwi w intuicyjnym podejściu do problemu, bazującym na podstawowych prawach fizyki i chemii.
Teoria VSEPR: Klucz do Zrozumienia Kształtów
Teoria VSEPR (Valence Shell Electron Pair Repulsion Theory) opiera się na prostym, ale potężnym założeniu: pary elektronów w powłoce walencyjnej atomu centralnego odpychają się wzajemnie, ponieważ ich chmury elektronowe są ujemnie naładowane. Aby zminimalizować to odpychanie i osiągnąć jak największą stabilność, pary elektronów (zarówno te tworzące wiązania, jak i te niewiążące, czyli wolne pary) układają się w przestrzeni w taki sposób, aby znajdować się jak najdalej od siebie. Teoria ta traktuje każdą parę elektronów, niezależnie od tego, czy jest to para wiążąca (pojedyncze, podwójne czy potrójne wiązanie liczy się jako jedna domena elektronowa), czy wolna para, jako "domenę elektronową". Kształt cząsteczki jest następnie określany przez rozmieszczenie tych domen w przestrzeni.
Główne założenia Teorii VSEPR:
- Kształt cząsteczki zależy od liczby domen elektronowych (par wiązanych lub niewiązanych) wokół atomu centralnego. Liczba tych domen determinuje geometrię domen elektronowych.
- Pary elektronów w powłoce walencyjnej odpychają się wzajemnie, ponieważ ich chmury elektronowe są ujemnie naładowane. Im bliżej są siebie, tym silniejsze odpychanie.
- Pozycje domen elektronowych w przestrzeni wokół atomu centralnego są takie, aby zminimalizować odpychanie i tym samym zmaksymalizować odległość między nimi. To prowadzi do najbardziej stabilnej konfiguracji.
- Wielkości różnych typów odpychania elektronowego podążają za następującą kolejnością, co jest kluczowe dla przewidywania zniekształconych kształtów:
- Para niewiążąca – Para niewiążąca (LP-LP) > Para niewiążąca – Para wiążąca (LP-BP) > Para wiążąca – Para wiążąca (BP-BP)
To oznacza, że wolne pary elektronowe zajmują więcej miejsca wokół atomu centralnego i silniej odpychają inne pary (zarówno wiążące, jak i niewiążące) niż pary wiążące. W rezultacie, obecność wolnych par elektronowych często prowadzi do zniekształcenia idealnych kątów wiązań i nieregularnego kształtu molekuły.
- Odpychanie elektronowe między dwiema parami elektronów będzie minimalne, jeśli są one od siebie jak najdalej. Na tej podstawie, dla danej liczby domen elektronowych, można przewidzieć najbardziej odpowiednie układy geometryczne. Geometria cząsteczki jest następnie określana przez położenie samych atomów (z pominięciem wolnych par elektronowych, które jednak wpływają na ten układ).
Podstawowe Typy Geometrii Cząsteczkowej (Gdy Brak Wolnych Par Elektronowych)
Kiedy wokół atomu centralnego występują tylko pary wiążące (bez wolnych par elektronowych), geometria domen elektronowych jest taka sama jak geometria cząsteczki. Istnieje pięć podstawowych geometrii molekularnych, które stanowią fundament dla zrozumienia bardziej złożonych struktur. Te kształty wynikają z minimalizacji odpychania między parami elektronów walencyjnych wokół atomu centralnego.
1. Liniowa geometria molekularna (2 domeny elektronowe)
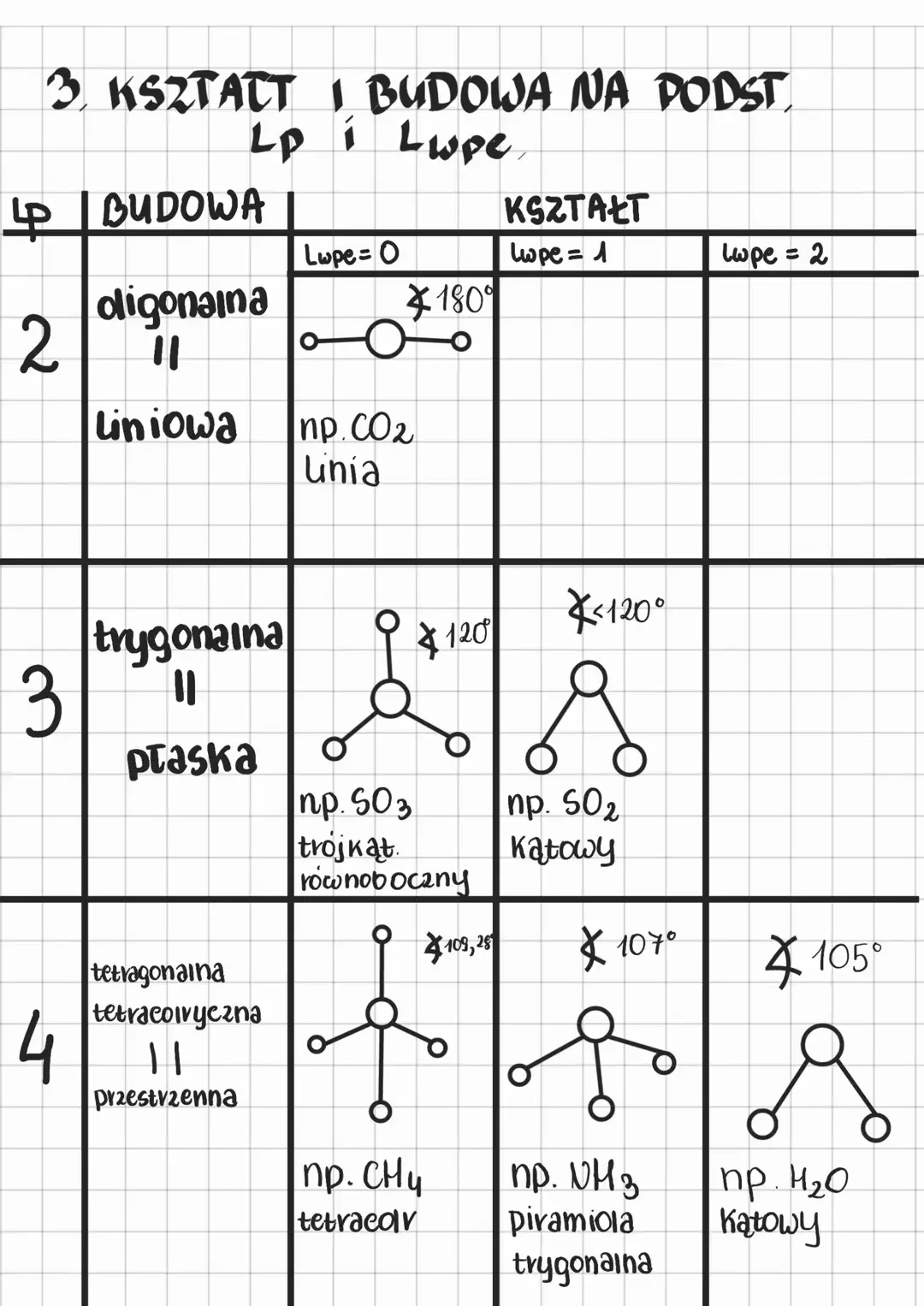
W tej strukturze atom centralny jest połączony z dwoma innymi atomami. Aby zminimalizować odpychanie, te dwie domeny elektronowe (pary wiążące) układają się w przeciwnych kierunkach, tworząc prostą linię. Kąt wiązania w tej strukturze wynosi idealnie 180°. Jest to najbardziej efektywny sposób na maksymalizację odległości między dwoma obszarami gęstości elektronowej. Przykłady: BeCl2, MgCl2, CO2 (gdzie każde podwójne wiązanie liczy się jako jedna domena).
2. Trójkątna płaska geometria molekularna (3 domeny elektronowe)
W tym typie cząsteczki trzy atomy są przyłączone do atomu centralnego. Trzy domeny elektronowe (pary wiążące) układają się w kierunku wierzchołków trójkąta równobocznego, aby zminimalizować odpychanie. Wszystkie atomy leżą w jednej płaszczyźnie. Kąt wiązania w tej strukturze wynosi 120°. Przykłady: BF3, BCl3, AlF3.
3. Czworościenna geometria molekularna (4 domeny elektronowe)
W czworościennej geometrii molekularnej atom centralny znajduje się w środku, a cztery podstawniki (atomy) są rozmieszczone w wierzchołkach czworościanu. Jest to najbardziej symetryczny układ dla czterech par elektronów, zapewniający największą odległość między nimi. Kąt wiązania w tej strukturze wynosi 109°28' (około 109,5°). Przykłady: CH4, CCl4, SiH4.
4. Trójkątna bipiramidalna geometria molekularna (5 domen elektronowych)
Rozważmy przykład PF5. W tej cząsteczce pięć par elektronów walencyjnych wokół atomu fosforu minimalizuje odpychanie poprzez równomierne rozmieszczenie w kierunku wierzchołków trójkątnej bipiramidy. W trójkątnej bipiramidzie, trzy pozycje leżą wzdłuż równika cząsteczki (pozycje równikowe) i są od siebie oddalone o 120°, a dwie pozycje leżą wzdłuż osi prostopadłej do płaszczyzny równikowej (pozycje osiowe). Kąty wiązań wynoszą 90° (między osiowymi a równikowymi) i 120° (między równikowymi). Pozycje osiowe są bardziej zatłoczone niż równikowe, co ma znaczenie, gdy pojawiają się wolne pary elektronowe. Przykłady: PF5, PCl5.

5. Oktaedryczna geometria molekularna (6 domen elektronowych)
Oktaedryczna geometria molekularna opisuje kształt związków z sześcioma atomami lub grupami atomów (ligandami) symetrycznie rozmieszczonymi wokół atomu centralnego, definiującymi wierzchołki oktaedru. Wszystkie pozycje są równoważne, a kąty wiązań wynoszą idealnie 90°. Jest to bardzo symetryczna struktura. Przykłady: SF6, TeF6.
Geometria Regularna a Nieregularna (Zniekształcona)
Na podstawie Teorii VSEPR, cząsteczki kowalencyjne mogą mieć dwa typy geometrii molekularnych: regularne i nieregularne (zniekształcone). Rozróżnienie to jest kluczowe dla zrozumienia, dlaczego niektóre cząsteczki mają idealnie symetryczne kształty, podczas gdy inne są wyraźnie zniekształcone.
Geometria Regularna:
Geometria cząsteczek kowalencyjnych jest regularna, jeśli atom centralny jest otoczony wyłącznie parami wiążącymi elektronów i wszystkie te wiązania są z takimi samymi atomami (lub grupami atomów). W takim przypadku, oddziaływania odpychające między parami wiążącymi wzajemnie się równoważą, co prowadzi do idealnie symetrycznego kształtu, zgodnego z podstawową geometrią domen elektronowych. Przykładem jest metan (CH4), gdzie atom węgla jest otoczony czterema identycznymi wiązaniami C-H. Wszystkie cztery domeny elektronowe są parami wiążącymi, co skutkuje idealnym kształtem czworościanu z kątami wiązań 109,5°.
Geometria Nieregularna (Zniekształcona):
W tym przypadku atom centralny jest otoczony albo parami wiążącymi z różnymi atomami (np. CHCl3, gdzie choć geometria domen jest tetraedryczna, to różna wielkość atomów H i Cl może powodować drobne odchylenia), albo co ważniejsze, zarówno parami wiążącymi, jak i wolnymi parami elektronów (np. H2O, NH3). W takich warunkach, oddziaływania odpychające nie równoważą się wzajemnie, ponieważ wolne pary elektronowe (LP) zajmują więcej miejsca wokół atomu centralnego i silniej odpychają inne pary (zarówno wiążące, jak i niewiążące) niż pary wiążące (BP). Prowadzi to do zniekształcenia geometrii cząsteczek, która jest wówczas nazywana nieregularną lub zniekształconą.
- Amoniak (NH3): Atom azotu w amoniaku ma cztery domeny elektronowe: trzy pary wiążące (z wodorem) i jedną wolną parę elektronów. Geometria domen elektronowych jest tetraedryczna. Jednakże, ze względu na silniejsze odpychanie wolnej pary elektronów (LP-BP > BP-BP), wolna para „spycha” pary wiążące bliżej siebie. To powoduje zmniejszenie kątów wiązań H-N-H z idealnych 109,5° do około 107°, a kształt molekuły, rozpatrywany tylko w kontekście pozycji atomów, jest piramidalny trójkątny.
- Woda (H2O): Atom tlenu w wodzie ma również cztery domeny elektronowe: dwie pary wiążące (z wodorem) i dwie wolne pary elektronów. Podobnie jak w amoniaku, geometria domen elektronowych jest tetraedryczna. Jednak obecność dwóch wolnych par elektronów (LP-LP > LP-BP > BP-BP) powoduje jeszcze większe zniekształcenie. Wolne pary bardzo silnie odpychają pary wiążące, co skutkuje znacznym zmniejszeniem kąta wiązania H-O-H do około 104,5°, nadając cząsteczce kształt kątowy (wygięty).
- Dwutlenek siarki (SO2): Atom siarki ma trzy domeny elektronowe: dwa wiązania (jedno podwójne z tlenem, jedno pojedyncze z tlenem, ale liczone jako dwie domeny wiążące) i jedną wolną parę. Geometria domen jest trójkątna płaska. Wolna para odpycha wiązania, nadając cząsteczce kształt kątowy.
Przykłady Geometrii Cząsteczek Opisane Teorią VSEPR
Poniżej przedstawiono tabelę podsumowującą różne typy geometrii cząsteczkowej, wraz z liczbą par wiążących i wolnych par elektronów, które je determinują. Notacja ABxLy oznacza A jako atom centralny, B jako atom związany, a L jako wolną parę elektronów. Ta tabela jest niezwykle przydatnym narzędziem do szybkiego przewidywania kształtów molekuł.
| Typ Cząsteczki | Liczba par wiążących (x) | Liczba wolnych par (y) | Suma domen elektronowych | Geometria par elektronowych | Kształt cząsteczki | Przykłady |
|---|---|---|---|---|---|---|
| AB2 | 2 | 0 | 2 | Liniowa | Liniowa | BeF2, BeCl2, CO2 |
| AB3 | 3 | 0 | 3 | Trójkątna płaska | Trójkątna płaska | BF3, BCl3 |
| AB2L | 2 | 1 | 3 | Trójkątna płaska | Kątowa (wygięta) | SO2, O3 |
| AB4 | 4 | 0 | 4 | Czworościenna | Czworościenna | CH4, CCl4 |
| AB3L | 3 | 1 | 4 | Czworościenna | Piramidalna trójkątna | NH3, PCl3 |
| AB2L2 | 2 | 2 | 4 | Czworościenna | Kątowa (wygięta) | H2O, OF2 |
| AB5 | 5 | 0 | 5 | Trójkątna bipiramidalna | Trójkątna bipiramidalna | PF5, PCl5 |
| AB4L | 4 | 1 | 5 | Trójkątna bipiramidalna | Huśtawka | SF4 |
| AB3L2 | 3 | 2 | 5 | Trójkątna bipiramidalna | W kształcie litery T | ClF3 |
| AB2L3 | 2 | 3 | 5 | Trójkątna bipiramidalna | Liniowa | XeF2 |
| AB6 | 6 | 0 | 6 | Oktaedryczna | Oktaedryczna | SF6, TeF6 |
| AB5L | 5 | 1 | 6 | Oktaedryczna | Piramidalna kwadratowa | ClF5 |
| AB4L2 | 4 | 2 | 6 | Oktaedryczna | Kwadratowa płaska | XeF4 |
Często Zadawane Pytania (FAQ)
Jak znaleźć kształty cząsteczek?
Kształty cząsteczek można znaleźć na kilka sposobów. Eksperymentalnie, wykorzystuje się techniki takie jak spektroskopia (IR, mikrofalowa, Ramana) oraz metody dyfrakcyjne (rentgenowska, neutronowa, elektronowa), które dostarczają danych o odległościach i kątach wiązań w cząsteczkach. Teoretycznie, najpopularniejszą i najłatwiej dostępną metodą jest Teoria VSEPR, która pozwala przewidzieć kształt na podstawie liczby par elektronów walencyjnych (wiązanych i niewiązanych, czyli wolnych par) wokół atomu centralnego. Na przykład, jeśli wokół atomu centralnego istnieje jedna wolna para elektronów i trzy pary wiązań (czyli łącznie cztery domeny elektronowe), geometria domen elektronowych jest tetraedryczna, ale wynikająca z tego geometria cząsteczki jest piramidą trójkątną (np. NH3), ponieważ wolna para zniekształca kształt. Jeśli istnieją dwie pary wiązań i dwie wolne pary elektronów (łącznie cztery domeny), geometria domen również jest tetraedryczna, ale geometria cząsteczki jest kątowa lub wygięta (np. H2O).
Jakie są 5 podstawowych kształtów cząsteczek?
Pięć podstawowych kształtów cząsteczek, które wynikają z minimalizacji odpychania między parami elektronów wokół atomu centralnego (w przypadkach, gdy nie ma wolnych par elektronowych lub gdy ich wpływ jest symetryczny), to:
- Liniowa (gdy atom centralny ma 2 domeny elektronowe, np. BeCl2)
- Trójkątna płaska (gdy atom centralny ma 3 domeny elektronowe, np. BF3)
- Czworościenna (gdy atom centralny ma 4 domeny elektronowe, np. CH4)
- Trójkątna bipiramidalna (gdy atom centralny ma 5 domen elektronowych, np. PF5)
- Oktaedryczna (gdy atom centralny ma 6 domen elektronowych, np. SF6)
Jakie są 13 kształtów cząsteczek?
Oprócz pięciu podstawowych kształtów, uwzględniając obecność wolnych par elektronów, Teoria VSEPR pozwala zidentyfikować wiele bardziej złożonych, a często zniekształconych geometrii molekularnych. Lista 13 typowych kształtów cząsteczek, które można spotkać w chemii, obejmuje:
- Liniowy (np. CO2, XeF2)
- Trójkątny płaski (np. BF3)
- Wygięty (kątowy) (np. SO2, H2O)
- Czworościenny (np. CH4)
- Piramidalny trójkątny (np. NH3)
- Trójkątny bipiramidalny (np. PF5)
- Huśtawka (np. SF4)
- W kształcie litery T (np. ClF3)
- Oktaedryczny (np. SF6)
- Piramidalny kwadratowy (np. ClF5)
- Kwadratowa płaska (np. XeF4)
- Piramidalny (często jako piramidalny trójkątny lub kwadratowy)
- Liniowy (także jako liniowy z trzema wolnymi parami, np. XeF2, który jest liniowy pomimo 5 domen elektronowych, ze względu na trzy wolne pary w płaszczyźnie równikowej)
Warto zauważyć, że niektóre kształty, takie jak "liniowy" czy "wygięty", mogą pojawić się w różnych kontekstach, w zależności od liczby domen elektronowych i obecności wolnych par. Na przykład, liniowy kształt może wynikać z 2 domen elektronowych (BeCl2) lub z 5 domen, w tym 3 wolnych par (XeF2).
Jaki jest kształt CH4 według teorii VSEPR?
Według Teorii VSEPR, cząsteczka metanu (CH4) posiada kształt czworościanu foremnego (tetraedru). Atom węgla jest atomem centralnym, do którego przyłączone są cztery atomy wodoru. Węgiel w metanie tworzy cztery pojedyncze wiązania kowalencyjne i nie posiada żadnych wolnych par elektronów w swojej powłoce walencyjnej. Oznacza to, że wokół atomu centralnego (węgla) znajdują się cztery domeny elektronowe, z których wszystkie są parami wiążącymi. Aby zminimalizować odpychanie między tymi czterema parami wiążącymi, układają się one w przestrzeni w wierzchołkach czworościanu. Kąty wiązań H-C-H wynoszą idealnie 109,5°, co jest charakterystyczne dla tej symetrycznej i stabilnej geometrii. Jest to klasyczny przykład cząsteczki o regularnej geometrii, gdzie geometria domen elektronowych jest identyczna z geometrią molekularną.
Zainteresował Cię artykuł Kształty Cząsteczek: Tajemnice Geometrii Molekularnej? Zajrzyj też do kategorii Chemia, znajdziesz tam więcej podobnych treści!

