27/07/2024
Nauka konfiguracji elektronowej to często jeden z pierwszych momentów w chemii ogólnej, który sprawia, że studenci czują się zagubieni. Wyobraź sobie scenę: właśnie wyjaśniłeś bloki s, p, d, f, a uczniowie kiwają głowami z pełnym zrozumieniem. Potem zaczynasz tłumaczyć, jak odczytywać to wszystko z układu okresowego i nagle... SCREEECH! Dźwięk zdartych płyt winylowych. Trzydzieści dwie twarze wpatrują się w ciebie, jakbyś stracił rozum, a oni dają za wygraną. Wiesz, że pod koniec zajęć odzyskasz 70% z nich, bo jesteś świetnym nauczycielem. Ale co, gdybyś w ogóle nie musiał ich tracić na początku? Co, gdyby istniał łatwiejszy sposób?
W tym artykule odkryjesz metodę, która nie tylko uprości proces nauki, ale także sprawi, że zapamiętywanie i stosowanie konfiguracji elektronowej stanie się drugą naturą. Przygotuj się na chemiczną rewolucję w Twoim podręczniku!
Czym jest konfiguracja elektronowa i dlaczego jest tak ważna?
Zacznijmy od podstaw. Protony i neutrony znajdują się w jądrze atomowym, które jest centralną częścią atomu i zajmuje bardzo małą przestrzeń. Elektrony natomiast nie znajdują się w jądrze; mogą być dosłownie wszędzie wokół niego, co sprawia, że ich lokalizacja może być dość trudna. To trochę jak szukanie igły w stogu siana. Dlaczego w ogóle obchodzi nas znajdowanie elektronów? Ponieważ elektrony są absolutnymi MVP chemii. W skrócie, to one są powodem, dla którego atomy są w stanie wchodzić w interakcje z innymi atomami, tworząc wiązania i substancje, które nas otaczają.

Elektrony można znaleźć w orbitalach – obszarach w przestrzeni wokół jądra, gdzie istnieje wysokie (około 90%) prawdopodobieństwo znalezienia elektronu. Orbitale nie są dokładnym miejscem, lecz raczej obszarem, który to dokładne miejsce obejmuje. Powłoka elektronowa, zwana również poziomem energetycznym, to zbiór orbitali znajdujących się w tej samej prawdopodobnej odległości od jądra. Każda powłoka zawiera jedną lub więcej podpowłok, a każda podpowłoka zawiera jeden lub więcej orbitali. Ważne jest, aby pamiętać, że każdy orbital może pomieścić maksymalnie dwa elektrony.
Układ okresowy składa się z pierwiastków, z których wszystkie są atomami wieloelektronowymi (z wyjątkiem oczywiście wodoru). Konfiguracja elektronowa mówi nam, jak te elektrony są rozmieszczone wśród różnych orbitali atomowych. To zagadnienie pojawia się na egzaminach z chemii ogólnej bez wyjątku, więc opanowanie go jest kluczowe dla sukcesu.
Konwencjonalna metoda określania konfiguracji elektronowej
Jak już wspomniano, konfiguracja elektronowa to specyficzne rozmieszczenie elektronów w dostępnych orbitalach. Wymienia ona symbole orbitali sekwencyjnie z indeksem górnym wskazującym liczbę elektronów zajmujących ten orbital. W obojętnym pierwiastku liczba protonów jest równa liczbie elektronów. Im więcej elektronów ma pierwiastek, tym więcej orbitali będzie musiał wypełnić.
Istnieje kilka zasad, których należy przestrzegać podczas pisania konfiguracji elektronowych, takich jak zasada Aufbau, zasada wykluczenia Pauliego i reguła Hunda. Nie będziemy ich tutaj szczegółowo omawiać, ale wspomnę o nich, aby podkreślić fakt, że istnieje specyficzna kolejność, w jakiej wypełniamy orbitale.

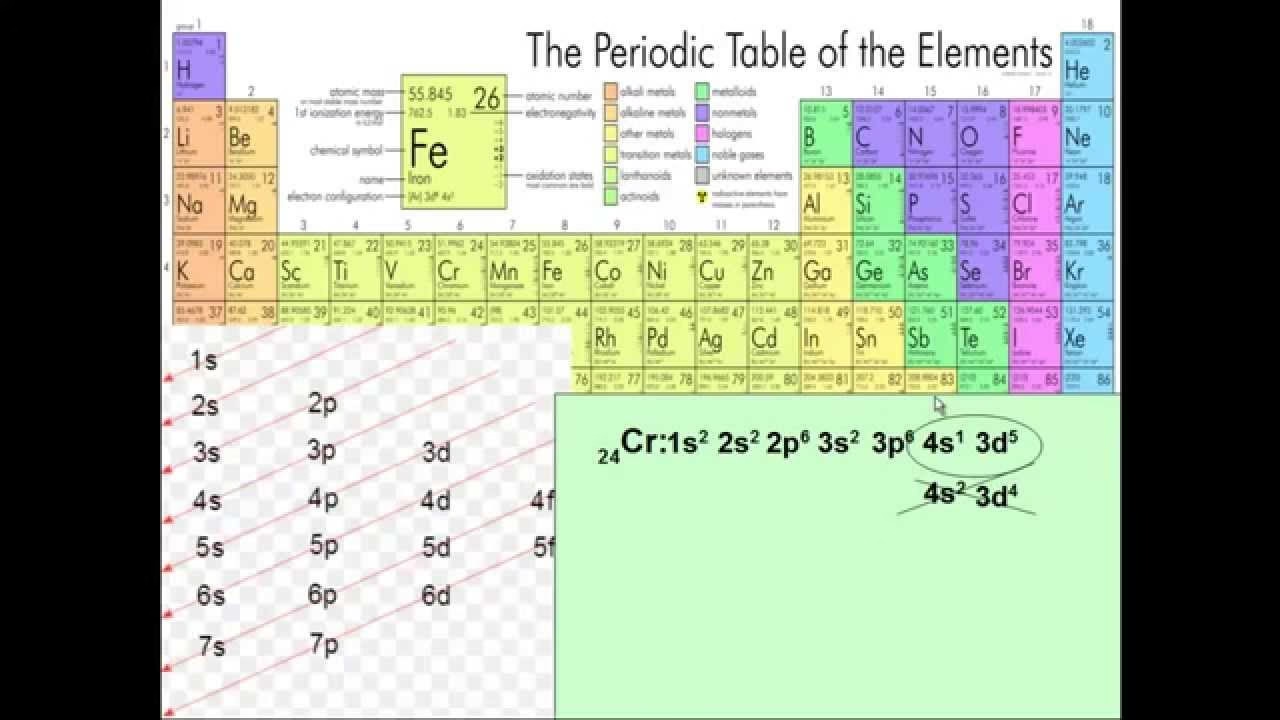
Tradycyjnie, aby określić konfigurację elektronową, wielu z nas uczyło się diagramu, który wygląda jak labirynt strzałek. Jest to popularna pomoc pamięciowa, którą widział każdy, kto kiedykolwiek brał udział w zajęciach z chemii ogólnej. Należy podążać za strzałkami po przekątnych, od ogona do głowy. Trzeba też pamiętać, że podpowłoka s mieści dwa elektrony, p – sześć elektronów, d – dziesięć elektronów, a f – czternaście elektronów. Ale nie jestem tu po to, żeby uczyć cię, jak używać tej konwencjonalnej metody. Jestem tu, żeby powiedzieć ci, co jest z nią nie tak:
- Musisz zapamiętać ten diagram, wszystkie przekątne i kolejność.
- Musisz na bieżąco śledzić liczbę elektronów, które już wykorzystałeś, aby nie przekroczyć liczby elektronów w pierwiastku, nad którym pracujesz.
- Musisz pamiętać, ile elektronów mieści się w każdej podpowłoce (s, p, d, f).
- Zajmuje to dużo czasu, zwłaszcza gdy pierwiastek ma więcej niż 20 elektronów.
Rewolucyjna metoda blokowa: Twoja tajna broń
Rozwiązaniem wszystkich twoich problemów z konfiguracją elektronową jest odpowiednie wykorzystanie tabeli okresowej. To, co widzisz, to układ okresowy oznaczony blokami. Zauważ, że dla bloku d współczynnik, czyli liczba z przodu, jest zawsze o jeden mniejszy niż numer okresu, w którym się znajduje. Dla bloku f współczynnik jest zawsze o dwa mniejszy niż numer okresu, w którym się znajduje. Będziesz musiał to zapamiętać. Jeśli chodzi o chemię ogólną, zawsze będą rzeczy, które po prostu musisz zapamiętać. Nawet „haki” wymagają pewnej pracy mózgu. Ale poza oznaczeniem czystego układu okresowego w dniu testu, tak jak to widzisz powyżej, to dosłownie wszystko. Jak więc tego używać?
Jak krok po kroku używać metody blokowej?
Ta metoda przekształca układ okresowy w intuicyjną mapę elektronów. Oto pięć prostych kroków:
Krok 1: Oznacz swoją tabelę okresową blokami.
Na swojej kopii układu okresowego (na egzaminie, jeśli dozwolone) oznacz bloki: po lewej stronie blok s, po prawej blok p, w środku blok d, a na dole blok f. Pamiętaj o zasadach dla współczynników: dla bloku d to (n-1), dla bloku f to (n-2), gdzie n to numer okresu.
Krok 2: Zidentyfikuj pierwiastek, którego konfigurację chcesz określić, i zaznacz go.
Znajdź pierwiastek na układzie okresowym i otocz go kółkiem lub zaznacz w inny sposób, aby był twoim punktem docelowym.
Krok 3: Zlokalizuj wodór jako swój punkt startowy.
Zawsze zaczynaj od wodoru, który jest pierwszym pierwiastkiem w bloku s. To twój punkt wyjścia.
Krok 4: Przejdź przez każdy okres (wiersz), od lewej do prawej i od góry do dołu, zapisując konfigurację elektronową, aż dotrzesz do swojego pierwiastka.
- Nie przechodź do następnego okresu, dopóki nie ukończysz okresu powyżej.
- Policz liczbę pierwiastków, które mijasz w każdym bloku. Ta liczba będzie twoim indeksem górnym (liczbą elektronów).
- Gdy w końcu pojawi się blok d, pamiętaj, że jego współczynnik jest o jeden mniejszy niż numer okresu, w którym się znajduje. Jeśli oznaczyłeś to wcześniej, będzie to oczywiste.
- Przykład: Określmy konfigurację elektronową dla Germanu (Ge).
- Zaczynamy od wodoru (okres 1): Przechodzimy przez 1s (2 pierwiastki: H, He) → 1s2
- Okres 2: Przechodzimy przez 2s (2 pierwiastki: Li, Be) → 2s2. Następnie przez 2p (6 pierwiastków: B do Ne) → 2p6.
- Okres 3: Przechodzimy przez 3s (2 pierwiastki: Na, Mg) → 3s2. Następnie przez 3p (6 pierwiastków: Al do Ar) → 3p6.
- Okres 4: Przechodzimy przez 4s (2 pierwiastki: K, Ca) → 4s2. Teraz wchodzimy w blok d. Pamiętaj, że to 3d (4-1=3), a nie 4d. Przechodzimy przez 3d (10 pierwiastków: Sc do Zn) → 3d10. Kontynuujemy w bloku p w tym samym okresie. Ge znajduje się w 4p. Przechodzimy przez 4p (pierwiastki Ga i Ge to 2) → 4p2.
- Pełna konfiguracja dla Ge: 1s22s22p63s23p64s23d104p2.
Krok 5: Sprawdź swoją pracę, sumując wszystkie indeksy górne i sprawdzając, czy suma odpowiada całkowitej liczbie elektronów w twoim pierwiastku.
Dla Ge: 2 + 2 + 6 + 2 + 6 + 2 + 10 + 2 = 32. Liczba atomowa Germanu (liczba elektronów w obojętnym atomie) to 32. Wynik się zgadza!
Dlaczego metoda blokowa jest lepsza?
Oto lista rzeczy, które sprawiają, że ta metoda jest znacznie lepsza:
- Nie musisz pamiętać, ile elektronów mieści się w każdej podpowłoce (s, p, d, f) – rozmiary bloków na układzie okresowym same ci to mówią!
- Nie musisz pamiętać tego irytującego diagramu z przekątnymi.
- Nie musisz na bieżąco śledzić liczby elektronów, które już wykorzystałeś, aby nie przekroczyć liczby elektronów w pierwiastku, nad którym pracujesz.
- Zajmuje to znacznie mniej czasu, a pierwiastki z więcej niż 20 elektronami nie są już problemem.
- To metoda, która minimalizuje ryzyko błędu, ponieważ opiera się na wizualnym odczycie z narzędzia, które zawsze masz pod ręką – układu okresowego.
Nie wierzysz, że jest bezbłędna? Jeśli nie jesteś przekonany, wypróbuj metodę blokową na kilku pierwiastkach i sprawdź swoją pracę za pomocą metody konwencjonalnej. Szybko przekonasz się o jej skuteczności.
Tabela porównawcza: Metoda Konwencjonalna vs. Metoda Blokowa
Aby jeszcze lepiej zobrazować przewagę metody blokowej, przyjrzyjmy się krótkiej tabeli porównawczej:
| Cecha | Metoda Konwencjonalna (Diagram) | Metoda Blokowa (Układ Okresowy) |
|---|---|---|
| Wymagana pamięć | Wysoka (diagram, kolejność, pojemności podpowłok) | Niska (zasady n-1 dla d i n-2 dla f) |
| Szybkość | Umiarkowana do wolnej, zwłaszcza dla dużych atomów | Bardzo szybka, nawet dla dużych atomów |
| Złożoność | Wymaga przestrzegania wielu zasad i śledzenia elektronów | Intuicyjne czytanie układu okresowego |
| Prawdopodobieństwo błędu | Wyższe (pomyłki w liczeniu, zapamiętywaniu) | Bardzo niskie (wizualne potwierdzenie) |
| Narzędzia | Diagram (często trzeba rysować lub pamiętać) | Układ okresowy (zazwyczaj dostępny) |
Często Zadawane Pytania (FAQ)
1. Czy metoda blokowa działa dla wszystkich pierwiastków?
Tak, metoda blokowa jest uniwersalna i działa dla wszystkich pierwiastków w układzie okresowym. Jest szczególnie przydatna dla tych z dużą liczbą elektronów, gdzie tradycyjne metody stają się uciążliwe. Pamiętaj jednak o wyjątkach od reguły Aufbau (np. chrom, miedź), które wynikają ze stabilności zapełnionych lub w połowie zapełnionych podpowłok d i f. Te wyjątki i tak wymagają indywidualnego zapamiętania, ale metoda blokowa dostarcza solidną podstawę, od której można wyjść.

2. Co z wodorem i helem? Czy są jakieś specjalne uwagi?
Wodór (1s1) i hel (1s2) są proste. Hel, choć znajduje się w bloku p (grupa 18), ma konfigurację 1s2 i często jest traktowany jako część bloku s, ponieważ jego powłoka walencyjna jest zapełniona jak w bloku s. W kontekście metody blokowej po prostu „przechodzisz” przez te dwa pierwiastki w pierwszym okresie.
3. Czy muszę znać układ okresowy na pamięć, aby używać tej metody?
Absolutnie nie! Wystarczy, że będziesz potrafił odczytywać układ okresowy i oznaczyć na nim bloki s, p, d, f. Na większości egzaminów dostajesz kopię układu okresowego, co czyni tę metodę niezwykle praktyczną.
4. Czy ta metoda jest akceptowana przez nauczycieli?
Metoda blokowa jest logicznym i poprawnym sposobem określania konfiguracji elektronowej, ponieważ opiera się na strukturze układu okresowego. Wielu nauczycieli docenia jej efektywność i zrozumienie leżących u jej podstaw zasad. Zawsze warto jednak zapytać swojego nauczyciela, czy możesz używać tej techniki na egzaminie, zwłaszcza jeśli wymaga to pisania po układzie okresowym.
5. Jakie są najważniejsze rzeczy do zapamiętania w metodzie blokowej?
Kluczowe jest zapamiętanie zasad dotyczących współczynników dla bloków d i f: dla bloku d współczynnik jest zawsze o jeden mniejszy niż numer okresu (n-1), a dla bloku f – o dwa mniejszy (n-2). Reszta to po prostu „czytanie” układu okresowego od lewej do prawej i od góry do dołu, zliczając elektrony w każdym bloku.
Podsumowanie
Wróćmy do twojego kolokwium. Gdzie byliśmy? Ach tak, dwie minuty na zrobienie 10 konfiguracji elektronowych. Kończysz zaledwie kilka sekund przed końcem. Dobrze, że użyłeś metody blokowej. Bez potu na czole, bez paniki i bez błędów. Opanowanie konfiguracji elektronowej nigdy nie było prostsze!
Zainteresował Cię artykuł Konfiguracja Elektronowa: Prostsza Niż Myślisz!? Zajrzyj też do kategorii Chemia, znajdziesz tam więcej podobnych treści!