09/05/2009
Zrozumienie budowy atomu jest fundamentem chemii, a jednym z najważniejszych aspektów tej budowy jest konfiguracja elektronowa. To nic innego jak opis rozmieszczenia elektronów wokół jądra atomowego na poszczególnych poziomach energetycznych i w orbitalach. Wiedza ta pozwala przewidywać właściwości chemiczne pierwiastków, ich reaktywność oraz sposób, w jaki tworzą wiązania. Bez opanowania zasad rządzących konfiguracją elektronową, trudno jest w pełni pojąć fascynujący świat reakcji chemicznych i różnorodności materii.
W tym artykule zagłębimy się w metody zapisu konfiguracji elektronowej, wykorzystując jako główne narzędzie układ okresowy pierwiastków. Poznasz proste kroki, które pozwolą Ci samodzielnie określać rozkład elektronów dla dowolnego atomu, a także zrozumiesz, dlaczego liczba powłok elektronowych jest tak ważna i jak ją odczytać. Przygotuj się na podróż do mikroskopijnego świata atomów, która rozjaśni wiele chemicznych zagadek!
Czym jest Konfiguracja Elektronowa i Dlaczego Jest Ważna?
Konfiguracja elektronowa to specyficzny układ elektronów w atomie. Elektrony nie krążą wokół jądra w dowolny sposób; zajmują ściśle określone obszary przestrzeni, nazywane orbitalami, które z kolei należą do różnych poziomów energetycznych, czyli powłok. Każdy atom dąży do osiągnięcia jak najniższego stanu energetycznego, co oznacza, że elektrony zajmują orbitale w określonej kolejności, zaczynając od tych o najniższej energii.
Dlaczego ta wiedza jest tak kluczowa? Przede wszystkim dlatego, że to właśnie elektrony, a zwłaszcza te znajdujące się na najbardziej zewnętrznej powłoce (tzw. powłoka walencyjna), decydują o chemicznych właściwościach pierwiastka. To one biorą udział w tworzeniu wiązań chemicznych, a ich liczba i rozmieszczenie wpływają na to, czy atom będzie łatwo oddawał, przyjmował czy uwspólniał elektrony. Zrozumienie konfiguracji elektronowej to pierwszy krok do przewidywania, jak pierwiastki będą ze sobą reagować.
Podstawowe Zasady Wypełniania Orbitali
Zapisywanie konfiguracji elektronowej opiera się na trzech głównych zasadach, które określają kolejność i sposób obsadzania orbitali przez elektrony:
Zasada Aufbau (zasada budowania)
Zasada Aufbau mówi, że elektrony obsadzają orbitale atomowe w kolejności wzrastającej energii. Oznacza to, że najpierw wypełniane są orbitale o najniższej energii, a dopiero potem te o wyższej. Kolejność ta nie zawsze jest intuicyjna (np. orbital 4s ma niższą energię niż 3d), dlatego układ okresowy jest tak pomocny w jej zapamiętaniu.
Zasada Pauliego (zakaz Pauliego)
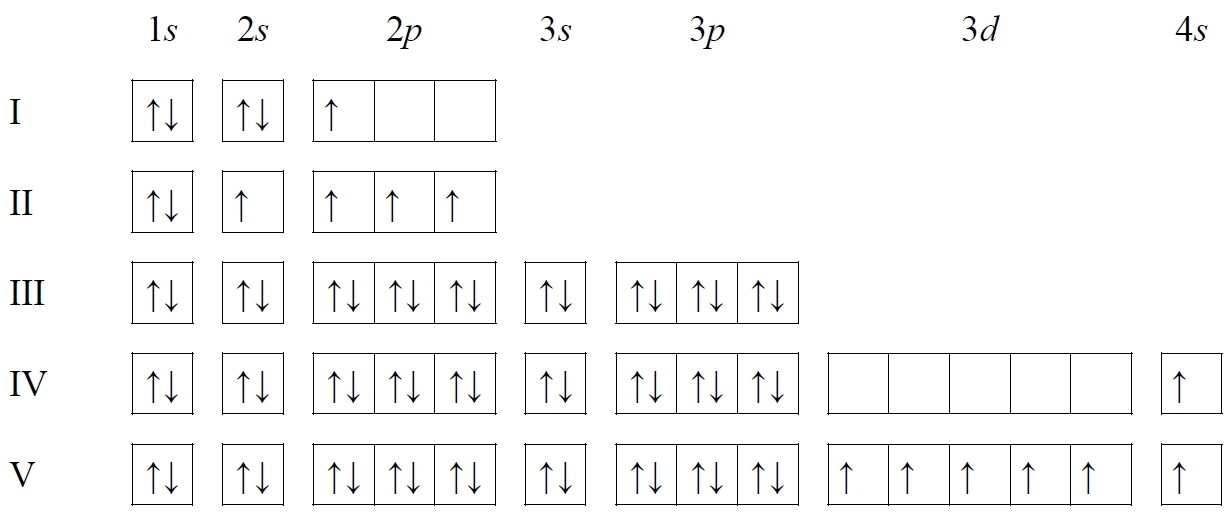
Zgodnie z zakazem Pauliego, w jednym orbitalu mogą znajdować się maksymalnie dwa elektrony, pod warunkiem, że mają przeciwne spiny (czyli orientację momentu magnetycznego). Spiny te są często przedstawiane jako strzałki skierowane w górę i w dół (↑↓).
Reguła Hunda
Reguła Hunda dotyczy orbitali o tej samej energii (tzw. orbitale zdegenerowane, np. trzy orbitale 2p, pięć orbitali 3d). Mówi ona, że elektrony w pierwszej kolejności zajmują pojedynczo każdy z zdegenerowanych orbitali, zachowując ten sam kierunek spinu. Dopiero po obsadzeniu wszystkich orbitali pojedynczo, elektrony zaczynają się parować, zajmując puste miejsca i przyjmując spin przeciwny do już obecnego elektronu.
Zapisywanie Konfiguracji Elektronowej Krok po Kroku z Układem Okresowym
Układ okresowy pierwiastków to nie tylko tabela, ale mapa, która znacznie ułatwia zapisywanie konfiguracji elektronowej. Oto jak go użyć:
Krok 1: Zidentyfikuj Pierwiastek i Jego Liczbę Atomową
Pierwszym i najważniejszym krokiem jest zlokalizowanie danego pierwiastka w układzie okresowym. Kluczową informacją jest jego liczba atomowa (Z), która zazwyczaj znajduje się w lewym dolnym rogu symbolu pierwiastka lub nad nim. W przypadku atomu obojętnego elektrycznie (niejonowego), liczba atomowa jest równa liczbie protonów w jądrze, a co za tym idzie, również liczbie elektronów. To właśnie tę liczbę elektronów musimy rozmieścić w orbitalach.
Przykład: Dla tlenu (O), liczba atomowa Z=8. Oznacza to, że neutralny atom tlenu ma 8 elektronów.
Krok 2: Użyj Układu Okresowego jako Mapy Orbitali
Układ okresowy jest podzielony na bloki, które odpowiadają typom orbitali (s, p, d, f) wypełnianych w danym okresie (rzędzie):
- Blok s: Grupy 1 i 2 (oraz hel). Każdy okres wypełnia dwa elektrony w orbitalu s.
- Blok p: Grupy 13-18. Każdy okres wypełnia sześć elektronów w orbitalach p.
- Blok d: Metale przejściowe (Grupy 3-12). Pamiętaj, że dla bloku d numer okresu jest o jeden wyższy niż numer powłoki d (np. 4. okres wypełnia orbitale 3d). Wypełnia dziesięć elektronów.
- Blok f: Lantanowce i aktynowce. Numer okresu jest o dwa wyższy niż numer powłoki f (np. 6. okres wypełnia orbitale 4f). Wypełnia czternaście elektronów.
Aby zapisać konfigurację, "przechodź" przez układ okresowy, rzędami, od wodoru aż do pierwiastka, dla którego chcesz zapisać konfigurację. Z każdym kolejnym pierwiastkiem dodajesz jeden elektron do odpowiedniego orbitalu. Liczba elektronów na danym orbitalu jest oznaczana w indeksie górnym.
Schemat wypełniania orbitali:
| Okres (Rząd) | Wypełniane orbitale | Maks. liczba elektronów |
|---|---|---|
| 1 | 1s | 2 |
| 2 | 2s, 2p | 2 + 6 = 8 |
| 3 | 3s, 3p | 2 + 6 = 8 |
| 4 | 4s, 3d, 4p | 2 + 10 + 6 = 18 |
| 5 | 5s, 4d, 5p | 2 + 10 + 6 = 18 |
| 6 | 6s, 4f, 5d, 6p | 2 + 14 + 10 + 6 = 32 |
| 7 | 7s, 5f, 6d, 7p | 2 + 14 + 10 + 6 = 32 |
Zapisz konfigurację elektronową najpierw według poziomu energetycznego i rodzaju orbitalu, a następnie liczbę elektronów obecnych na orbitalu w indeksie górnym.
Przykłady Zapisu Konfiguracji Elektronowej:
1. Węgiel (C) - Z=6
- Przechodzimy przez 1. okres: wypełniamy 1s2 (2 elektrony). Zostało 4 elektrony.
- Przechodzimy przez 2. okres: zaczynamy od 2s. Wypełniamy 2s2 (2 elektrony). Zostało 2 elektrony.
- Kontynuujemy w 2. okresie w bloku p: wypełniamy 2p2 (2 elektrony).
- Suma elektronów: 2 + 2 + 2 = 6.
Konfiguracja: 1s2 2s2 2p2
2. Sód (Na) - Z=11
- 1. okres: 1s2 (2 elektrony). Zostało 9.
- 2. okres: 2s2 (2 elektrony), 2p6 (6 elektronów). Razem 2+6 = 8 elektronów w 2. okresie. Został 1.
- 3. okres: 3s1 (1 elektron).
- Suma elektronów: 2 + 2 + 6 + 1 = 11.
Konfiguracja: 1s2 2s2 2p6 3s1
3. Wapń (Ca) - Z=20
- 1. okres: 1s2
- 2. okres: 2s2 2p6
- 3. okres: 3s2 3p6
- 4. okres: 4s2 (Pamiętaj, że po 3p6 następuje 4s2, a dopiero potem 3d).
- Suma elektronów: 2 + 8 + 8 + 2 = 20.
Konfiguracja: 1s2 2s2 2p6 3s2 3p6 4s2
Skrócona Konfiguracja Elektronowa (Zapis z Gazem Szlachetnym)
Dla większych atomów zapis pełnej konfiguracji może być długi. W takich przypadkach często stosuje się skrócony zapis, używając symbolu gazu szlachetnego z poprzedniego okresu. Konfiguracja gazu szlachetnego reprezentuje w pełni wypełnione powłoki wewnętrzne.
Przykład: Sód (Na), Z=11. Najbliższy gaz szlachetny z poprzedniego okresu to Neon (Ne), Z=10, którego konfiguracja to 1s2 2s2 2p6. Zatem konfigurację sodu można zapisać jako:
[Ne] 3s1
Przykład: Wapń (Ca), Z=20. Najbliższy gaz szlachetny z poprzedniego okresu to Argon (Ar), Z=18, którego konfiguracja to 1s2 2s2 2p6 3s2 3p6. Zatem konfigurację wapnia można zapisać jako:
[Ar] 4s2
Skąd Wiedzieć, Ile Atom Ma Powłok?
Kolejną ważną informacją, którą możemy łatwo odczytać z układu okresowego, jest liczba powłok elektronowych w atomie. Numer okresu (rzędu), w którym leży dany atom, bezpośrednio wskazuje, ile atom ma powłok elektronowych.
Na przykład:
- Wodór (H) i Hel (He) leżą w 1. okresie, co oznacza, że mają 1 powłokę elektronową.
- Lit (Li) i Neon (Ne) leżą w 2. okresie, co oznacza, że mają 2 powłoki elektronowe.
- Sód (Na) i Argon (Ar) leżą w 3. okresie, co oznacza, że mają 3 powłoki elektronowe.
- Potas (K) i Krypton (Kr) leżą w 4. okresie, co oznacza, że mają 4 powłoki elektronowe.
Ostatnia powłoka elektronowa, na której znajdują się elektrony, nazywana jest powłoką walencyjną. To właśnie elektrony na tej powłoce (elektrony walencyjne) są odpowiedzialne za właściwości chemiczne pierwiastka i jego zdolność do tworzenia wiązań. Numer okresu wskazuje więc nie tylko liczbę wszystkich powłok, ale także numer powłoki walencyjnej.
Wyjątki od Reguł Wypełniania Orbitali
Chociaż zasady Aufbau, Pauliego i Hunda są bardzo pomocne, istnieją pewne wyjątki, szczególnie wśród metali przejściowych. Najbardziej znane to chrom (Cr) i miedź (Cu). Wyjątki te wynikają z dodatkowej stabilizacji, jaką daje całkowite lub częściowe wypełnienie orbitali d lub f.

Chrom (Cr, Z=24):Oczekiwana konfiguracja: [Ar] 3d4 4s2Faktyczna konfiguracja: [Ar] 3d5 4s1Jeden elektron z orbitalu 4s przechodzi na orbital 3d, tworząc półpełny i stabilny podpoziom 3d.
Miedź (Cu, Z=29):Oczekiwana konfiguracja: [Ar] 3d9 4s2Faktyczna konfiguracja: [Ar] 3d10 4s1Jeden elektron z orbitalu 4s przechodzi na orbital 3d, tworząc całkowicie wypełniony i stabilny podpoziom 3d.
Te wyjątki podkreślają, że natura dąży do jak największej stabilności energetycznej, a w pełni lub w połowie wypełnione podpowłoki są bardziej stabilne.
Często Zadawane Pytania (FAQ)
1. Co to są elektrony walencyjne i dlaczego są ważne?
Elektrony walencyjne to elektrony znajdujące się na najbardziej zewnętrznej powłoce atomu (powłoce walencyjnej). Są one kluczowe, ponieważ to właśnie one biorą udział w tworzeniu wiązań chemicznych. Ich liczba i rozmieszczenie decydują o reaktywności pierwiastka, jego zdolności do tworzenia jonów oraz rodzaju wiązań, jakie będzie tworzył.
2. Czy konfiguracja elektronowa zmienia się, gdy atom staje się jonem?
Tak, konfiguracja elektronowa zmienia się, gdy atom traci lub zyskuje elektrony, stając się jonem. Kationy (jony dodatnie) powstają przez utratę elektronów, zazwyczaj z najbardziej zewnętrznej powłoki. Aniony (jony ujemne) powstają przez zyskanie elektronów, które zajmują dostępne miejsca w orbitalach.
Przykład: Na (1s2 2s2 2p6 3s1) traci 1 elektron, tworząc Na+ (1s2 2s2 2p6, czyli [Ne]).
3. Jaka jest różnica między powłoką a orbitalem?
Powłoka elektronowa (poziom energetyczny) to ogólny obszar wokół jądra, charakteryzujący się główną liczbą kwantową (n = 1, 2, 3...). Im większy numer powłoki, tym dalej od jądra i tym wyższa energia elektronów na tej powłoce. Każda powłoka składa się z jednego lub więcej orbitali.
Orbital to konkretny obszar przestrzeni, w którym istnieje największe prawdopodobieństwo znalezienia elektronu. Orbitale mają różne kształty (sferyczne s, hantlowate p, bardziej złożone d i f) i różne orientacje w przestrzeni. Każdy orbital może pomieścić maksymalnie dwa elektrony o przeciwnych spinach.
4. Czy wszystkie pierwiastki mają taką samą konfigurację elektronową?
Nie, każdy pierwiastek ma unikalną liczbę atomową, a co za tym idzie, unikalną liczbę elektronów, co prowadzi do unikalnej konfiguracji elektronowej. Pierwiastki w tej samej grupie (kolumnie) układu okresowego mają jednak podobną konfigurację elektronową na swojej powłoce walencyjnej, co wyjaśnia ich podobne właściwości chemiczne.
Podsumowanie
Opanowanie zasad zapisu konfiguracji elektronowej jest niezbędne dla każdego, kto chce zrozumieć podstawy chemii. Dzięki liczbie atomowej i sprytnemu wykorzystaniu układu okresowego jako mapy, możesz łatwo określić rozmieszczenie elektronów w dowolnym atomie. Pamiętaj o zasadzie Aufbau, zakazie Pauliego i regule Hunda, które kierują wypełnianiem orbitali. Zrozumienie, że numer okresu wskazuje liczbę powłok, a tym samym powłokę walencyjną, otwiera drzwi do przewidywania reaktywności pierwiastków.
Konfiguracja elektronowa to nie tylko suchy zapis, ale potężne narzędzie, które pozwala zaglądać w głąb materii i przewidywać jej zachowanie. Im lepiej ją zrozumiesz, tym łatwiej będzie Ci poruszać się po świecie chemii, od prostych reakcji po złożone procesy biologiczne i przemysłowe.
Zainteresował Cię artykuł Konfiguracja Elektronowa: Klucz do Chemii? Zajrzyj też do kategorii Chemia, znajdziesz tam więcej podobnych treści!

