19/02/2010
Klonowanie, słowo, które często wywołuje skojarzenia z fantastyką naukową i etycznymi dylematami, jest w rzeczywistości fundamentalnym procesem w biologii, zarówno naturalnym, jak i laboratoryjnym. W swoim najszerszym rozumieniu, klonowanie odnosi się do tworzenia identycznej kopii czegoś, co już istnieje. W świecie nauki termin ten nabiera wielu odcieni, obejmując zarówno powstawanie genetycznie identycznych organizmów, jak i precyzyjne manipulacje na poziomie molekularnym. Ten artykuł ma na celu rozjaśnienie złożoności klonowania, przedstawiając jego różnorodne typy, szczegółowe procesy, kluczową nomenklaturę oraz najnowsze osiągnięcia, które rewolucjonizują dziedziny od medycyny po rolnictwo.

Co to jest klonowanie?
W potocznym rozumieniu, klonowanie określa proces tworzenia identycznej kopii z oryginału. W biologii mianem klonu określa się organizmy mające identyczny lub prawie identyczny materiał genetyczny. Klonami są więc organizmy powstałe w procesie rozmnażania wegetatywnego, takie jak kolonie bakterii, jednokomórkowców, odrośla i rozmnóżki roślin.
Termin klonowanie jest używany w kilku znaczeniach, co często prowadzi do nieporozumień. Warto je sobie uporządkować:
- Klonowanie organizmów: To procedura otrzymywania organizmów o takiej samej informacji genetycznej, z reguły poprzez procedurę transferu jądra z komórki somatycznej do komórki jajowej pozbawionej uprzednio jądra. Szczególnym przypadkiem jest tzw. twinning, czyli powstawanie lub otrzymywanie bliźniąt monozygotycznych, gdzie nie można wyróżnić dawcy. W przypadku klonowania roślin stosuje się procedurę odróżnicowania komórek dawcy do komórek merystematycznych.
- Klonowanie genów (molekularne): W genetyce i biologii molekularnej to proces wyosobniania genu. Polega na łączeniu fragmentów materiału genetycznego z wektorem molekularnym i ich namnażaniu w innym organizmie. Otrzymuje się w ten sposób wiele kopii tego samego genu. Termin klonowanie genów odnosi się też do identyfikacji genów poprzez wykorzystanie procedury klonowania genów. Jeśli pojedynczy fragment genomu jest przenoszony z jednego wektora do drugiego, taki proces określa się mianem subklonowania.
- Klonowanie komórkowe: Tworzenie populacji identycznych komórek z jednej komórki macierzystej.
Opanowano obecnie metody klonowania wielu gatunków roślin i zwierząt. W przypadku zwierząt zazwyczaj stosuje się technikę polegającą na przeniesieniu jądra komórki somatycznej pobranej z klonowanego osobnika, do komórki jajowej pozbawionej jądra. Proces ten tworzy funkcjonalną zygotę, która może rozwinąć się w żywego osobnika. Dawca komórki jajowej z reguły pochodzi z tego samego gatunku, ponieważ transfer jądra do komórki jajowej innego gatunku rzadko jest skuteczny. Warto pamiętać, że klony otrzymane w procesie transferu jądrowego nie są w 100% genetycznie identyczne z dawcami, ponieważ wymienia się tylko materiał genetyczny zawarty w jądrze komórkowym, pozostawiając DNA mitochondrialny biorcy, który jednak ma minimalny wkład w dziedziczenie cech genetycznych.
Rodzaje klonowania organizmów
Obecnie stosowane metody klonowania organizmów, głównie na etapie embrionalnym, obejmują kilka kluczowych podejść:
Metoda podziału bliźniaczego (podział wczesnego embrionu)
Jest to jedna z najprostszych technik, w wyniku której powstają dwa embriony identyczne genetycznie. Polega ona na mikrochirurgicznym przecięciu zarodka, gdy znajduje się on w stadium od dwóch do ośmiu komórek. Na początku rozwoju embrionalnego komórki posiadają zdolności multipotencjalne, to znaczy, że mogą przejmować i zastępować funkcje brakujących komórek, włącznie z odbudowaniem brakujących. W ten sposób można otrzymać jednojajowe bliźniaki, które posiadają identyczną strukturę białkową oraz te same cechy dziedziczenia. W tym przypadku bliźnięta są dla siebie klonami.
Metoda izolacji blastomerów
Ta technika polega na wyizolowywaniu komórek embrionu (blastomerów) dających początek nowym organizmom. Została opracowana pod koniec lat 60. XX wieku dla klonowania zarodków zwierzęcych. Przy jej wykorzystaniu uzyskiwano bliźnięta, trojaczki, a nawet czasami czworaczki i pięcioraczki. Mimo możliwości uzyskania identycznych genetycznie wieloraczków, metoda ta nie zyskała jednak praktycznego znaczenia i nie wyszła poza stadium eksperymentalne.
Metoda agregacji blastomerów
W tej technice wyizolowane komórki embrionu (blastomery) są umieszczane w otoczeniu blastomerów pochodzących z innych osobników. Celem jest stworzenie chimerycznego zarodka, który może rozwijać się w organizm. Podobnie jak izolacja blastomerów, metoda ta ma ograniczone zastosowanie praktyczne i jest głównie wykorzystywana w badaniach.
Metoda transferu jąder komórkowych (SCNT - Somatic Cell Nuclear Transfer)
Jest to najbardziej znana i rewolucyjna metoda klonowania, pozwalająca na uzyskanie u ssaków klonów liczących znacznie więcej osobników niż przy wykorzystaniu poprzednich metod. Polega na umieszczeniu w niezapłodnionej komórce jajowej jądra komórkowego pochodzącego z embrionu lub, co bardziej przełomowe, z komórki ciała dorosłego osobnika. Proces ten odbywa się w następujących fazach:
- Przygotowanie jądra komórki somatycznej, które będzie sterowało rozwojem komórki jajowej.
- Przygotowanie komórki jajowej – wypreparowanie jądra komórkowego (tzw. enukleacja).
- Wszczepienie jądra komórki somatycznej w miejsce jądra komórki jajowej (rozpoczyna się rozwój powstałej w ten sposób zygoty, często stymulowany impulsem elektrycznym).
- Przeniesienie rozwijającego się embrionu do narządów rodnych matki zastępczej.
Innym wariantem klonowania, na drodze transplantacji jąder komórkowych, jest klonowanie z zastosowaniem pierwotnych komórek zarodkowych. Jest to metoda, która, przynajmniej teoretycznie, może prowadzić do masowej produkcji identycznych zarodków ssaków. Jak dotąd udało się ją zastosować tylko w odniesieniu do myszy. W chwili obecnej nie są jeszcze jasne możliwości produkcji pierwotnych komórek zarodkowych w odniesieniu do innych zwierząt, mimo że notuje się na tym polu pewne osiągnięcia.
Klonowanie owcy Dolly – kamień milowy w biotechnologii
Zazwyczaj słowo klonowanie kojarzy nam się ze słynną owcą Dolly. Procedura ta jednak różniła się znacznie od tej, którą zwykle określamy mianem klonowania molekularnego. Wspomniany eksperyment klonowania był o tyle wyjątkowy, że po raz pierwszy pokazano, iż ssak może zostać „odtworzony” (sklonowany) z komórki somatycznej organizmu. Zespół naukowców z Roslin Institute, pod przewodnictwem Iana Wilmuta i Keitha Campbella, dokonał transferu jądra komórkowego diploidalnej (2n) komórki gruczołu mlekowego dorosłej owcy (SCNT) do komórki jajowej (haploidalnej, 1n) pozbawionej jądra komórkowego (0n). Po tej manipulacji zaindukowano komórkę do podziałów, w wyniku czego powstał zarodek, który następnie został wszczepiony do macicy owcy zastępczej. Tam rozwijał się aż do narodzin owieczki Dolly w 1996 roku. Sklonowanie owcy Dolly stanowiło niezaprzeczalnie kamień milowy w biotechnologii oraz wpłynęło na dalszy rozwój genetyki i medycyny regeneracyjnej.
Klonowanie molekularne – serce inżynierii genetycznej
Klonowanie molekularne (molecular cloning) jest podstawową techniką inżynierii genetycznej, ułatwiającą manipulację i analizę cząsteczek DNA, prowadzenie replikacji elementów genetycznych oraz wprowadzanie egzogennej ekspresji. Proces ten, zapoczątkowany w latach 70. ubiegłego wieku, zrewolucjonizował różne dziedziny, od badań podstawowych po biotechnologię i medycynę. W swojej istocie klonowanie molekularne polega na replikacji, powieleniu fragmentów DNA w celu wygenerowania wielu jego identycznych kopii. Następnie w wyniku podziałów zmodyfikowanego organizmu jednokomórkowego dochodzi do powstania wielu identycznych klonów (np. szczepów bakteryjnych). Takie manipulacje umożliwiają naukowcom precyzyjne badania i analizy genetyczne.
Proces klonowania molekularnego – krok po kroku
Proces klonowania molekularnego jest złożony, ale powtarzalny. Obejmuje kilka kluczowych etapów:
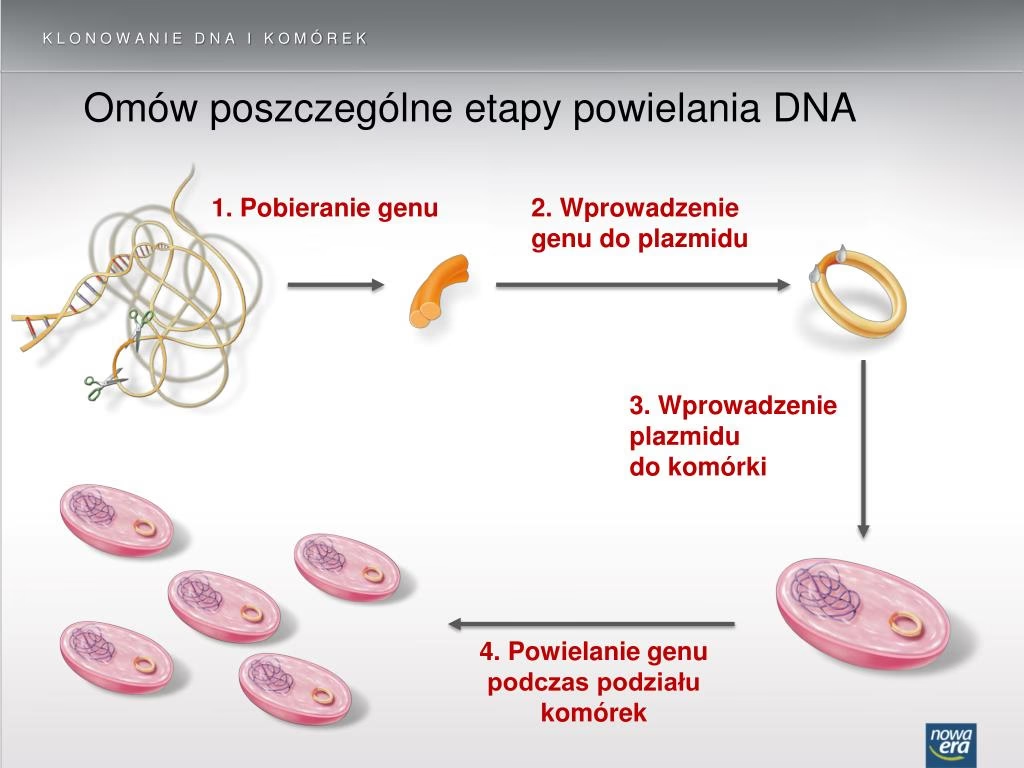
- Otrzymanie fragmentu DNA zawierającego pożądany gen (Izolacja DNA): Proces rozpoczyna się od przygotowania i izolacji interesującego fragmentu DNA. Często odbywa się to poprzez PCR (odczynniki PCR i qPCR) sekwencji z organizmu dawcy, takiego jak bakterie, rośliny lub zwierzęta. Fragment ten zawiera gen lub sekwencję, którą naukowcy chcą manipulować lub badać. Techniki izolacji DNA różnią się w zależności od źródła i złożoności materiału genetycznego, ale zazwyczaj obejmują trawienie enzymatyczne i etapy oczyszczania.
- Łączenie pozyskanych fragmentów z cząsteczkami wektorowymi (Wstawianie do wektora): Po wyizolowaniu, fragment DNA jest wstawiany do wektora, cząsteczki DNA zdolnej do samoreplikacji w organizmie gospodarza. Wektory służą jako nośniki do przenoszenia obcego DNA do organizmu gospodarza, umożliwiając jego propagację i ekspresję. Powszechnie stosowane wektory obejmują plazmidy, które są kolistymi cząsteczkami DNA występującymi w bakteriach.
- Ligacja: Kolejnym kluczowym etapem klonowania molekularnego jest ligacja fragmentu DNA do wektora. W procesie tym zazwyczaj pośredniczy ligaza DNA, enzym katalizujący tworzenie wiązań fosfodiestrowych między fragmentami DNA, tworząc rekombinowaną cząsteczkę DNA. Powstały konstrukt, znany jako rekombinowany wektor, zawiera obcy fragment DNA zintegrowany z jego genomem.
- Wprowadzenie zrekombinowanych wektorów do komórek (Transformacja): Po utworzeniu rekombinowanego wektora jest on wprowadzany do organizmu gospodarza w procesie zwanym transformacją. W przypadku bakterii, na przykład, często wiąże się to z wystawieniem komórek bakteryjnych na działanie roztworu zawierającego rekombinowany wektor, a następnie inkubacją w określonych warunkach, aby umożliwić pobranie obcego DNA.
- Identyfikację i selekcję organizmów z pożądaną sekwencją genetyczną (Selekcja): Po transformacji naukowcy stosują różne techniki selekcji w celu identyfikacji komórek zawierających pożądane rekombinowane DNA. Mogą one obejmować markery oporności na antybiotyki lub inne geny reporterowe zintegrowane z wektorem, co pozwala na identyfikację i izolację transformowanych komórek. Po wyizolowaniu, komórki te mogą być hodowane w celu wygenerowania populacji klonów zawierających rekombinowane DNA.
W badaniach podstawowych klonowanie molekularne umożliwia badanie funkcji, regulacji i ekspresji genów. W biotechnologii klonowanie molekularne służy jako istotne narzędzie do produkcji rekombinowanych białek, szczepionek i innych biofarmaceutyków. W medycynie klonowanie molekularne ułatwiło rozwój technik terapii genowej w leczeniu zaburzeń genetycznych i nowotworów.
Klonowanie klasyczne z użyciem restryktaz i ligaz
Klonowanie za pomocą enzymów restrykcyjnych jest podstawową techniką stosowaną w biologii molekularnej. Procedura opiera się na wykorzystaniu enzymów restrykcyjnych (restriction enzymes), znanych również jako restryktazy lub endonukleazy restrykcyjne, które są białkami rozpoznającymi i tnącymi obie nici DNA w określonych krótkich sekwencjach (ok. 6-8 nt) znanych jako miejsca restrykcyjne. Przecinając DNA w tych precyzyjnych miejscach, enzymy restrykcyjne generują fragmenty z tzw. „lepkimi końcami” (sticky ends) lub „tępymi końcami” (blunt ends), w zależności od użytego enzymu. Końce te mogą następnie łączyć się w pary zasad z komplementarnymi sekwencjami na innych fragmentach DNA, czyli w plazmidzie.
Kolejnym krokiem jest ligacja (ligation) lub łączenie tych fragmentów DNA. Zazwyczaj odbywa się to przy użyciu ligazy DNA (ligase), enzymu, który ułatwia tworzenie wiązań fosfodiestrowych między sąsiednimi nukleotydami fragmentów DNA, skutecznie „sklejając” kawałki razem. Nowo utworzoną cząsteczkę rekombinowanego DNA można następnie wprowadzić do organizmu gospodarza, w procesie zwanym transformacją. Zwykle wykorzystuje się komórki bakterii szczepów E. coli tzw. kompetentnych (competent cells), czyli tak modyfikowanych, aby z łatwością pobierały elementy genetyczne. W organizmie gospodarza rekombinowane DNA może być replikowane lub eksprymowane w celu zbadania funkcji genu lub wytworzenia interesujących białek.
Ograniczenia klonowania klasycznego
Mimo swojej wszechstronności i roli w rozwoju genetyki, biotechnologii i medycyny, klonowanie z użyciem enzymów restrykcyjnych niesie ze sobą szereg ograniczeń:
- Zależność od enzymów: Jesteśmy zależni od działania enzymów – restryktaz i ligazy.
- Miejsca cięcia: Przed i za naszą sekwencją (insertem) musimy umieścić miejsca cięcia dla restryktaz. Zazwyczaj wykonuje się to za pomocą PCR. Miejsca te ponadto muszą być zbieżne do tych występujących w MCS plazmidu. Jednocześnie sama wstawka nie może w swojej strukturze zawierać takiego miejsca, aby podczas trawienia końców insertu sama nie została zdeintegrowana.
- Przesunięcie ramki odczytu: Musimy zadbać o odpowiednią liczbę nukleotydów pomiędzy promotorem, pozostałością po miejscu restrykcyjnym i insertem, aby nie doszło do przesunięcia ramki odczytu.
- Nukleotydy szwowe: Praca z enzymami restrykcyjnymi pozostawia tzw. szwowe nukleotydy (scar nucleotides), których nie możemy usunąć, a które nie mają sensu biologicznego.
- Trudny dobór enzymów: Wszystko to sprawia, że niekiedy bardzo trudno jest dobrać odpowiednie enzymy restrykcyjne do naszych warunków.
- Fałszywie pozytywne kolonie: Często zdarza się, że po wysianiu transformantów bez końca testujemy dziesiątki kolonii w poszukiwaniu pozytywnego klonu. Dzieje się tak, ponieważ większość plazmidów zostało zamkniętych enzymatycznie bez insertu.
- Długi czas: Przygotowanie insertu i plazmidu poddanych obróbce enzymami restrykcyjnymi, duże prawdopodobieństwo powstania fałszywie pozytywnych kolonii, które następnie należy poddać testom, sprawia, że metoda ta trwa bardzo długo – od 2 dni do kilku tygodni.
Nomenklatura klonowania molekularnego
Zazwyczaj w procesie klonowania sekwencja nowo wprowadzana nazywa się insertem (insert) lub wstawką, a element genetyczny pozwalający na replikację, ekspresję i często z elementem reporterowym to plazmid lub wektor. Te ostatnie elementy to zazwyczaj koliste cząsteczki DNA, zdolne do autoreplikacji, występujące w bakteriach.
Wspomniane miejsca na plazmidzie to:
- Ori (origin of replication): specyficzne dla organizmu, do którego klonowany jest plazmid; miejsce początku replikacji.
- Promotor: jeśli plazmid jest ekspresyjny, zapoczątkowuje transkrypcję.
- MCS (Multi Cloning Site): fragment zazwyczaj za promotorem, koncentracja miejsc cięcia dla enzymów restrykcyjnych, pozwalający na wstawienie insertu.
- Kaseta oporności na dany antybiotyk (np. Ampicylinę) lub kaseta dla β-galaktozydazy (jako reporter).
Kaseta dla β-galaktozydazy pozwala na tzw. blue-white screening kolonii. Enzym jest elementem operonu laktozowego (gen lacZ) i w naturalnych warunkach umożliwia metabolizm laktozy. Natomiast ma także zdolność do rozkładania bezbarwnego związku X-gal (analogu laktozy). Rozkład ten powoduje powstawanie niebieskiego zabarwienia (w procesie powstaje 5-bromo-4-chloro-indoksyl, który następnie spontanicznie dimeryzuje i utlenia się, tworząc jasnoniebieski nierozpuszczalny pigment 5,5′-dibromo-4,4′-dichloro-indigo).
Także komórki poprawnie transformowane plazmidem z nieprzerwaną kasetą dla β-galaktozydazy będą barwiły się na niebiesko. A komórki, które nie uległy transformacji, będą po dodaniu X-gal białe (tj. naturalnego koloru).
Czym jest α-komplementacja?
W tym miejscu warto wspomnieć o procesie zwanym α-komplementacją. Gen lacZ (dla β-galaktozydazy) można podzielić na dwie funkcjonalne części: peptyd α (część N-końcowa) i fragment ω (część C-końcowa). Gdy obie części są obecne w tej samej komórce, mogą się wzajemnie uzupełniać, tworząc funkcjonalny enzym β-galaktozydazy, nawet jeśli są wytwarzane z oddzielnych łańcuchów polipeptydowych. Proces ten znany jest jako α-komplementacja.
W praktyce α-komplementacja jest szeroko stosowana we wspomnianych wyżej analizach przesiewowych wyrośniętych kolonii, tj. blue-white screening. Metoda ta pozwala na rozróżnienie rekombinowanych i nierekombinowanych plazmidów w eksperymentach klonowania. Jak się to dzieje?
Konieczne są dwa warunki:
- Szczep transformowany E. coli musi mieć mutację w swoim własnym genie lacZ (lacZΔM15), co czyni go niezdolnym do samodzielnego wytwarzania funkcjonalnej β-galaktozydazy (może jednak wytwarzać fragment ω β-galaktozydazy). Warunki takie spełniają komórki JM109, DH5α i XL1-Blue.
- Plazmid musi być odpowiednio przysposobiony do metody. Musi zawierać gen lacZ, jednak jego region α musi być przecięty sekwencją MCS – czyli miejscem wstawiania insertu, np. pUC19 i pBluescript.
Podczas klonowania insert zostanie wstawiony w MCS w środek regionu α, genu lacZ plazmidu. Powoduje to błędy w komplementacji β-galaktozydazy. W rezultacie komórki zawierające rekombinowane plazmidy nie wybarwiają się na niebiesko, ponieważ nie wytwarzają funkcjonalnego enzymu. Komórki zaś z pustym plazmidem są niebieskie. Czyli odwrotnie do sytuacji, gdy kaseta dla β-galaktozydazy służy jako reporter (np. drożdże).
Klonowanie "Seamless" – przyszłość precyzji
Pomimo swojego ogromnego znaczenia, klonowanie molekularne nie jest pozbawione wyzwań, o kilku wspomnieliśmy omawiając klasyczną technikę klonowania. Proces ten może być wymagający technicznie i czasochłonny, wymagając starannej optymalizacji warunków eksperymentalnych. Co więcej, wybór wektora i organizmu gospodarza może mieć wpływ na wydajność i powodzenie eksperymentów klonowania, dlatego przez długi czas starano się opracować technikę klonowania bardziej przyjazną dla użytkowników i efektywniejszą.
Tak powstały systemy do klonowania „seamless”, czyli takie nie pozostawiające nukleotydów szwowych (pozostałości po działaniu restryktazami). Ponadto ten rodzaj klonowania umożliwia badaczom uniezależnienie od sekwencji restrykcyjnych, a w konsekwencji swobodny dobór wektorów i wstawek, a nawet tworzenie fuzyjnych sekwencji (fuzyjnych białek rekombinantów). Poniżej zostaną omówione trzy metody seamless.

Gibson Assembly
Metoda Gibsona wykorzystuje mieszaninę trzech enzymów (egzonukleazy, ligazy i polimerazy DNA) do przejścia od liniowych fragmentów DNA do gotowego plazmidu. Podobnie jak w przypadku innych metod klonowania bezszwowego (seamless), wstawki są amplifikowane metodą PCR, tak aby zawierały homologiczne flanki ze zlinearyzowanym plazmidem lub innymi sąsiednimi fragmentami. Zaleca się, aby długość tych elementów zawierała się pomiędzy 15-25 nt i aby ją dobrać eksperymentalnie. Po złożeniu reakcji, 5′ egzonukleaza hydrolizuje DNA w celu utworzenia lepkich końców. Po odnalezieniu przez insert i plazmid komplementarnych końców, polimeraza DNA (o ograniczonej aktywności proofreading) uzupełnia luki pomiędzy elementami konstruktu, a ligaza scala wszystko w jedność (in vitro). Nowsza wersja metody, NEBuilder HiFi DNA Assembly, wykorzystuje tę samą technologię, ale znajdująca się w premiksie polimeraza jest wysokiej wierności, przez co powstaje mniej mismatchy w odcinkach przed i za insertem. W przypadku obu wersji metody Gibsona, do ostatecznego scalenia wykorzystywana jest aktywność ligazy będącej w mieszaninie od początku. Obecność ta sprawia, że dochodzi do zamykania pustych plazmidów i powstawania kolonii fałszywie pozytywnych, które musimy odrzucić podczas kolonijnego PCR. Sprawia to, że metoda jest mniej efektywna przy wysokoprzepustowym klonowaniu i tworzeniu fuzyjnych konstruktów.
Klonowanie z użyciem enzymów restrykcyjnych typu IIS (RE)
Enzymy restrykcyjne typu IIS (RE) tną DNA poza swoimi miejscami restrykcyjnymi, co sprawia, że nie tworzą się tzw. szwowe nukleotydy jak w przypadku klasycznego klonowania. Niemniej etapy metody są bardzo podobne do klonowania z użyciem zwykłych enzymów restrykcyjnych. Wstawki i wektory są zaprojektowane w taki sposób, że miejsce restrykcyjne jest usuwane przez sam enzym. Flanki mogą być specjalnie zaprojektowane, aby zapewnić kierunkowe (sensowne) wstawienie jednego insertu lub wielu fragmentów w tej samej reakcji. Takie wykorzystanie metody jest jednak mało wydajne i może wymagać dodatkowych manipulacji i wstawiania lub usuwania miejsc restrykcyjnych w obrębie plazmidu i insertów. Ten rodzaj klonowania wykorzystuje dostępny na rynku Golden Gate Assembly, który zawiera mieszaninę enzymów restrykcyjnych typu IIS RE oraz ligazę DNA T4.
Klonowanie In-Fusion®
Technologia klonowania In-Fusion® w odróżnieniu od omówionych metod seamless zapewnia klonowanie produktów PCR bez ligacji in vitro. System umożliwia klonowanie dowolnego insertu w każdy zlinearyzowany plazmid, niezależnie od locus. Ponieważ metoda ta nie wykorzystuje restryktaz, nie ma potrzeby enzymatycznej obróbki fragmentu PCR (np. trawienie restrykcyjne, fosforylacja), a ponieważ w mieszaninie nie ma ligazy, obecność kolonii „tła” (fałszywie pozytywnych) jest niezwykle niska (tj. powstawanie pustych wektorów). Typowe problemy wynikające z nieefektywności ligacji są również wyeliminowane, umożliwiając pominięcie etapów subklonowania, nawet w przypadku dużych wektorów i wstawek (plazmidy adenowirusowe, inserty do 34 kb).
Wektory liniowe mogą być przygotowywane za pomocą trawienia restrykcyjnego lub w wyniku PCRu, oferując możliwości prawdziwego klonowania niezależnego od sekwencji. Reakcja In-Fusion® jest jednoetapowa i trwa jedynie 15 minut. Podobnie jak metoda Gibsona opiera się na homologii fragmentów między plazmidem a wstawką. W przeciwieństwie jednak do niej, wspomniane odcinki zawsze mają długość 15 nt, nie trzeba zatem optymalizować warunków reakcji, a każda reakcja jest kierunkowa i dokładna. W mieszaninie działa egzonukleaza 3′, hydrolizująca fragmenty DNA i tworząca przez to kompatybilne ze sobą końce na zasadzie komplementarności. W takiej formie materiał jest transformowany do komórek kompetentnych, które ligują konstrukt (in vivo) chroniąc przed wprowadzeniem jakichkolwiek błędów sekwencji lub niedopasowaniem nukleotydów. Takie rozwiązanie zapewnia wysoką dokładność i efektywność na poziomie 95% usprawniając pracę. Metoda sprawdza się także w klonowaniu wysokoprzepustowym i tworzeniu fuzyjnych konstruktów (multiklonowanie).
Porównanie metod klonowania "Seamless"
| Cecha | Gibson Assembly | Klonowanie RE typu IIS (np. Golden Gate) | In-Fusion® |
|---|---|---|---|
| Zasada działania | Homologia końców, działanie 3 enzymów (egzonukleaza, polimeraza, ligaza) | Enzymy tnące poza miejscem rozpoznania | Homologia końców (15 nt), egzonukleaza 3', ligacja in vivo |
| Nukleotydy szwowe | Brak | Brak | Brak |
| Zależność od sekwencji restrykcyjnych | Niezależne (ale wymaga homologicznych flanek) | Zależne od miejsc rozpoznania RE typu IIS | Niezależne (homologiczne flanki 15 nt) |
| Fałszywie pozytywne klony | Możliwe (ligaza w mieszaninie) | Możliwe | Niezwykle niskie (brak ligazy in vitro) |
| Czas reakcji in vitro | Zależny od protokołu, zazwyczaj dłuższy | Zależny od protokołu | 15 minut |
| Efektywność | Dobra, ale niższa przy wysokoprzepustowym | Umiarkowana, może wymagać optymalizacji | Wysoka (~95%), idealna do wysokoprzepustowego |
| Wszechstronność | Duża | Duża, ale z ograniczeniami | Bardzo duża (dowolny insert, dowolny wektor) |
Etyczne i praktyczne aspekty klonowania
Naturalną konsekwencją sukcesów w klonowaniu ssaków jest idea sklonowania człowieka. Budzi ono jednak głębokie kontrowersje natury etycznej. Wiadomości o sklonowaniu ssaków wywołały panikę wśród prawodawców wielu krajów, którzy zabronili klonowania ludzi, szczególnie w celach reprodukcyjnych.
Klonowanie ludzi w celach reprodukcyjnych ma niewielki sens praktyczny, dodatkowo niedoskonałości natury technicznej i mutacje somatyczne w komórkach będącymi donorami materiału genetycznego, powodują, że przy obecnym stanie technologii, ludzki klon najprawdopodobniej cierpiałby na zaburzenia natury genetycznej. Tak więc klonowanie ludzi, przynajmniej na razie, z medycznego punktu widzenia jest nieetyczne, ze względu na zasadę primum non nocere (po pierwsze nie szkodzić).
Odmiennie przedstawia się sprawa klonowania w celu pozyskania komórek macierzystych (tzw. klonowanie terapeutyczne). Ponieważ komórki macierzyste mogą się różnicować do wszystkich typów komórek ciała, komórki macierzyste otrzymane w wyniku klonowania mogą mieć potencjalne zastosowanie terapeutyczne, a procedura taka nie wiąże się z otrzymywaniem organizmu. Dodatkowo, komórki macierzyste sklonowane z dawców obarczonych ciężką chorobą dziedziczną mogą służyć jako model badań nad takimi chorobami. Ogólna zgoda środowiska naukowego jest taka, że klonowanie w celu pozyskania komórek macierzystych jest zgodne z etyką badawczą, choć mimo to nadal wzbudza kontrowersje.
Klonowanie wymarłych gatunków zwierząt
Klonowanie wymarłych gatunków zwierząt budzi zrozumiałe zainteresowanie, zwłaszcza w świetle filmów fantastycznych, takich jak Jurassic Park. Procedury takie pozostają jak na razie w sferze fantastyki, choć niektóre ośrodki rozpoczęły badania nad możliwością takiej procedury. Główne trudności ze zrealizowaniem projektu sklonowania wymarłego organizmu to:
- Brak odpowiedniego DNA: DNA dostępny ze źródeł kopalnych bądź to muzealnych jest bardzo fragmentaryczny i dostępny w znikomych ilościach. Nie jest jasne, czy możliwe jest otrzymanie wystarczającej ilości i jakości, by odtworzyć sekwencję kompletnego genomu.
- Transfer jądra: Obecne metody klonowania wykorzystują transfer jądra. Nie jest jasne, czy nagi DNA mógłby być wystarczający. Paradoksalnie, nagi DNA może być lepszym substratem do klonowania, gdyż może łatwiej ulegać reprogramowaniu epigenetycznemu.
- Wybór donora komórki jajowej: Większość transferu jądrowego pomiędzy różnymi gatunkami się nie powodzi.
Mimo tych wyzwań, badania nad klonowaniem wymarłych gatunków, a także zagrożonych gatunków, są kontynuowane, otwierając nowe perspektywy dla ochrony różnorodności biologicznej.
Często zadawane pytania (FAQ)
- Czy klony są identyczne?
- Klony organizmów są genetycznie identyczne z dawcą, ale nie są to dokładne kopie pod każdym względem. Czynniki środowiskowe, doświadczenia życiowe i subtelne różnice w DNA mitochondrialnym (w przypadku klonowania transferem jądrowym) mogą prowadzić do odmienności w wyglądzie, zachowaniu czy nawet zdrowiu. W przypadku klonowania molekularnego, uzyskane kopie DNA są praktycznie identyczne.
- Czy klonowanie jest bezpieczne?
- Klonowanie organizmów, szczególnie ssaków, jest procesem o niskiej efektywności i wysokim ryzyku. Wiele sklonowanych zwierząt cierpi na wady rozwojowe, choroby lub przedwczesną śmierć. Z tego powodu klonowanie reprodukcyjne ludzi jest powszechnie uznawane za nieetyczne i zabronione. Klonowanie molekularne, stosowane w badaniach i produkcji białek, jest bezpieczne i rutynowo wykorzystywane w laboratoriach na całym świecie.
- Jakie są zastosowania klonowania?
- Zastosowania klonowania są różnorodne:
- Klonowanie molekularne: produkcja białek (np. insuliny, szczepionek), terapia genowa, badania nad funkcjami genów, diagnostyka chorób genetycznych.
- Klonowanie organizmów (zwierząt): rolnictwo (replikacja zwierząt o pożądanych cechach), ochrona zagrożonych gatunków, modelowanie chorób ludzkich.
- Klonowanie terapeutyczne: pozyskiwanie komórek macierzystych do leczenia chorób degeneracyjnych, tworzenie modeli chorobowych.
- Czym różni się klonowanie molekularne od klonowania organizmów?
- Klonowanie molekularne to proces tworzenia wielu identycznych kopii konkretnego fragmentu DNA (np. genu) w laboratorium, zazwyczaj w bakteriach. Służy do badania i manipulowania DNA. Klonowanie organizmów (reprodukcyjne) to proces tworzenia genetycznie identycznej kopii całego organizmu, najczęściej poprzez transfer jądra komórki somatycznej do komórki jajowej. Są to fundamentalnie różne techniki o odmiennych celach i implikacjach.
Klonowanie, w swoich wielu formach, jest potężnym narzędziem w rękach naukowców. Od zrozumienia podstawowych procesów biologicznych po rewolucyjne zastosowania w medycynie i biotechnologii, jego wpływ na naukę i społeczeństwo jest niezaprzeczalny. Ciągły rozwój technik, takich jak klonowanie "seamless", otwiera nowe możliwości, jednocześnie stawiając przed nami wyzwania etyczne, które wymagają ciągłej refleksji i dialogu.
Zainteresował Cię artykuł Rodzaje i Procesy Klonowania: Przewodnik? Zajrzyj też do kategorii Edukacja, znajdziesz tam więcej podobnych treści!
