15/07/2023
Chemia to nauka o przemianach materii, ale równie ważne, jak co się zmienia, jest jak szybko to się dzieje. Właśnie tym zajmuje się kinetyka chemiczna – dziedzina chemii fizycznej, która bada przebieg reakcji chemicznych w czasie. Jej twórcą był Ludwig Ferdinand Wilhelmy, a dzięki jego pionierskim pracom dziś możemy dogłębnie analizować dynamikę procesów chemicznych. Kinetyka koncentruje się na szybkości reakcji, wpływie różnorodnych czynników na tę szybkość, a także na ogólnym przebiegu całego procesu. Zrozumienie kinetyki jest fundamentalne nie tylko dla teoretyków, ale przede wszystkim dla praktyków, zwłaszcza w przemyśle, gdzie optymalizacja procesów reakcyjnych ma kluczowe znaczenie.
Czym jest kinetyka chemiczna i co bada?
Kinetyka chemiczna to gałąź chemii fizycznej, która bada, jak szybko reakcje chemiczne zachodzą i co dzieje się z nimi w czasie. Jej głównym celem jest ustalenie zależności szybkości powstawania produktów (i ubytku substratów) od wielu czynników. Do tych czynników należą między innymi:
- początkowe stężenia substratów,
- temperatura,
- ciśnienie,
- rodzaj rozpuszczalnika,
- rodzaj i stężenie katalizatora.
Zebrane dane pozwalają na określenie postaci równania kinetycznego reakcji chemicznej, wyznaczenie wartości jego współczynników, a nawet na poznanie mechanizmu reakcji, czyli szczegółowego przebiegu na poziomie molekularnym. Chociaż badanie kinetyki reakcji rzadko jest niezbędne do preparatyki na skalę laboratoryjną, staje się absolutną koniecznością, gdy dana reakcja ma być stosowana przemysłowo. W skali przemysłowej kontrola szybkości i warunków reakcji przekłada się bezpośrednio na wydajność i bezpieczeństwo procesu.
Czy kinetyka jest trudna? Przystępne spojrzenie na wyzwania
Często zadawane pytanie brzmi: czy kinetyka chemiczna jest trudna? Odpowiedź brzmi: bywa trudna, ale absolutnie nie jest niemożliwa do opanowania. Jednym z głównych wyzwań może być matematyka, która bywa nieco skomplikowana z powodu równań różniczkowych i złożonych praw szybkości reakcji. Niektórym studentom początkowo trudno jest zrozumieć abstrakcyjne koncepcje leżące u podstaw kinetyki. Jednakże, kiedy już oswoisz się z podstawami i zaczniesz dostrzegać zależności, zrozumienie, jak reakcje zachodzą na poziomie molekularnym, staje się niezwykle fascynujące. Z odpowiednim podejściem i cierpliwością, kinetyka staje się pasjonującym obszarem wiedzy.
Szybkość reakcji: Podstawowe pojęcie kinetyki
Jednym z najważniejszych pojęć w kinetyce jest szybkość reakcji. Najprościej mówiąc, średnia szybkość reakcji jest to zmiana stężenia substratu lub produktu w danym przedziale czasowym. Aby to lepiej zrozumieć, posłużmy się analogią z codziennego życia. Wyobraź sobie samochód pokonujący drogę 280 km w ciągu 2 godzin. Aby obliczyć średnią prędkość, z jaką porusza się pojazd, wystarczy podzielić drogę przez czas. Otrzymamy wówczas wynik równy 140 km/h. Można zatem powiedzieć, że samochód w ciągu 1 godziny średnio pokonał trasę o długości 140 km.
Średnia szybkość w odniesieniu do reakcji chemicznych jest analogiczna, jednakże przy jej obliczaniu zamiast długości drogi będziemy używać różnicy stężeń molowych. Jednostką szybkości reakcji jest mol/(dm3∙s). Wzór na średnią szybkość reakcji (V) przedstawia się następująco:
V = | ΔC / Δt |
gdzie:
- ΔC – delta stężeń dla substratów lub produktów,
- Δt – czas reakcji.
Aby lepiej zrozumieć wprowadzone pojęcie średniej szybkości reakcji, rozwiążmy zadanie:
Zadanie: Stężenie produktu A w czasie 60-sekundowej reakcji chemicznej zwiększyło się z 0,02 mol/dm3 do 0,05 mol/dm3. Oblicz średnią szybkość reakcji powstawania produktu.
Rozwiązanie:
- Wypisujemy dane:
- Stężenie początkowe = 0,02 mol/dm3
- Stężenie końcowe = 0,05 mol/dm3
- ΔC = 0,05 - 0,02 = 0,03 mol/dm3
- Δt = 60 s (gdyby w zadaniu podany był czas w innej jednostce, należałoby dokonać zamiany na sekundy lub minuty w zależności od polecenia).
- Podstawiamy dane pod wzór w celu obliczenia szybkości „V”:
- V = 0,03 / 60 = 0,0005 mol/(dm3∙s)
Uwaga! Gdyby zadanie dotyczyło średniej szybkości ubytku substratu, wówczas otrzymana różnica stężeń byłaby wartością ujemną. Aby uniknąć wyniku na minusie, we wzorze należy uwzględnić znak „-”. Na przykład, jeśli stężenie substratu zmalało z 0,05 mol/dm3 do 0,02 mol/dm3:
- ΔC = 0,02 - 0,05 = -0,03 mol/dm3
- Δt = 60 s
- V = -(-0,03) / 60 = 0,0005 mol/(dm3∙s)
Rodzaje reakcji chemicznych z perspektywy kinetycznej
Aby zrozumieć pojęcie rzędowości reakcji, najpierw przypomnijmy podstawy podziału reakcji chemicznych:
- Reakcje proste (elementarne): Do ich zajścia wymagane jest efektywne zderzenie cząsteczek, jonów lub atomów, lub też przekształcenie jednych drobin w drugie. W przebiegu reakcji prostych można wyróżnić tylko jeden etap.
- Reakcje złożone: Zachodzą w kilku etapach, a w trakcie ich przebiegu dochodzi do powstania produktów pośrednich. Wśród nich można wyróżnić:
- Reakcje następcze: Zachodzące jedna po drugiej. Przykładem może być przemiana promieniotwórcza, np. rozpad uranu, gdzie etapy kolejnych rozpadów zachodzą sekwencyjnie.
- Reakcje współbieżne (konkurencyjne): Zachodzące w tym samym czasie, konkurujące o substrat. Przykładem jest nitrowanie fenolu, w wyniku którego powstają izomeryczne produkty z różną wydajnością.
Cząsteczkowość i rzędowość reakcji – kluczowe rozróżnienia
Po ustaleniu równania stechiometrycznego danej reakcji prostej możemy określić jej cząsteczkowość oraz rzędowość.
Cząsteczkowość
Zgodnie z definicją, cząsteczkowość jest to liczba cząsteczek, atomów lub jonów, które biorą udział w danej reakcji chemicznej. Aby ją określić, należy zsumować wszystkie współczynniki stojące przed substratami w równaniu. Rozważmy reakcję syntezy związku C:
D + B → C
W tym przykładzie cząsteczkowość będzie równa 2 (1 cząsteczka D + 1 cząsteczka B), zatem mamy do czynienia z reakcją dwucząsteczkową.
Rzędowość reakcji
Rzędowość reakcji jest sumą wykładników potęg, do których podniesione są stężenia substratów w równaniu kinetycznym. Jego postać dla rozważanego przykładu (D + B → C) zapiszemy w sposób następujący:
v = k ∙ CD ∙ CB
gdzie:
- v - szybkość reakcji,
- CB, CD - stężenia substratów, które biorą udział w reakcji,
- k - stała szybkości reakcji, inaczej współczynnik proporcjonalności zależny od temperatury.
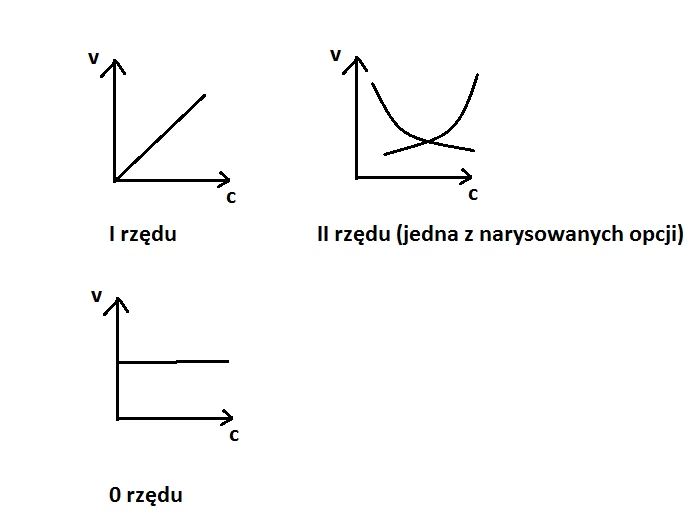
Zgodnie z powyższą definicją, rzędowość reakcji syntezy związku C jest równa 2 (1 dla CD + 1 dla CB). Możemy zatem powiedzieć, że jest ona przemianą drugorzędową. Wykres dla reakcji II-rzędowej przedstawiający zależność szybkości reakcji od stężenia substratu D ma kształt fragmentu paraboli.
Reakcja pierwszorzędowa
Przeanalizujmy teraz przemianę, której szybkość zależy jedynie od stężenia substratu A:
A → B + C
Przy założeniu, że jest to reakcja prosta, jej równanie kinetyczne przyjmuje postać:
v = k ∙ CA
Zależność stężenia substratu od szybkości jest wprost proporcjonalna i przedstawia ją linia prosta, inaczej fragment funkcji liniowej.
Reakcja zerowego rzędu
W reakcjach zerowego rzędu szybkość reakcji jest stała w czasie i nie zależy od stężenia substratu. Równanie kinetyczne takiej przemiany możemy zapisać jako równość:
v = k
Wykres ilustrujący zależność stężenia od czasu jest linią prostą, której wartości na osi Y nie ulegają zmianie, gdyż zmiana stężenia substratu nie ma wpływu na szybkość reakcji zerowego rzędu.
Ważna uwaga! Wszystkie rozważane dotąd przemiany były reakcjami prostymi. Dlatego też postać równania stechiometrycznego przekładała się na równanie kinetyczne. Jeżeli jednak będziemy mieć do czynienia z reakcją złożoną, wówczas równanie kinetyczne może się zupełnie różnić od równania reakcji. Współczynniki stechiometryczne wcale nie muszą być równe rzędom, do których podniesione są stężenia odpowiednich substratów! W przypadku reakcji złożonych postać równania kinetycznego uzależniona jest od najwolniejszego etapu i wyznacza się ją doświadczalnie.
Jak wyznaczyć równanie kinetyczne? Praktyczne podejście
Wyznaczanie równania kinetycznego na podstawie danych doświadczalnych jest kluczową umiejętnością w kinetyce. Przeanalizujmy poniższe zadanie, aby to zilustrować:
Zadanie: Na podstawie danych z tabeli, wyznacz równanie kinetyczne reakcji:
| Pomiar | Stężenie A [mol/dm3] | Stężenie B [mol/dm3] | Szybkość reakcji [mol/(dm3∙s)] |
|---|---|---|---|
| 1 | 0,1 | 0,1 | 0,01 |
| 2 | 0,2 | 0,1 | 0,02 |
| 3 | 0,1 | 0,2 | 0,04 |
Rozwiązanie:
- Wyznaczenie rzędu względem substratu A: Znajdźmy dwa wiersze, w których szybkość reakcji zależy jedynie od stężenia A, czyli stężenie B pozostaje stałe. Będzie to pomiar 1 i 2.
- Stosunek stężeń A: 0,2 / 0,1 = 2
- Stosunek szybkości: 0,02 / 0,01 = 2
Widzimy, że dwukrotny wzrost stężenia substratu A przy niezmienionym stężeniu B spowodował dwukrotny wzrost szybkości reakcji. Zatem oznacza to, że mamy do czynienia z rzędem pierwszym względem substratu A.
- Wyznaczenie rzędu względem reagenta B: Powtarzamy czynności. Szukamy dwóch wierszy, w których szybkość reakcji zależy jedynie od zmiany stężenia substratu B, a stężenie A pozostaje stałe. Będzie to pomiar 1 i 3.
- Stosunek stężeń B: 0,2 / 0,1 = 2
- Stosunek szybkości: 0,04 / 0,01 = 4
Widzimy, że dwukrotny wzrost stężenia reagenta B przy niezmienionym stężeniu substratu A powoduje czterokrotny wzrost szybkości reakcji. Zatem rząd względem B jest równy 2.
- Ostateczna postać równania kinetycznego:
v = k ∙ CA ∙ CB2
Wskazówka: Aby dojść do wyniku, można również zapisać otrzymaną wartość ilorazu szybkości w postaci potęgi o tej samej podstawie co liczba otrzymana z dzielenia stężeń: 4 = 22. Wykładnik potęgi równy 2 jest rzędem względem substratu B.
Czynniki wpływające na szybkość reakcji chemicznych
Po zapoznaniu się z pojęciem szybkości reakcji chemicznej i wzorami, za pomocą których możemy ją obliczyć, przychodzi pora na omówienie najważniejszych czynników mających wpływ na szybkość jej przebiegu. Należą do nich:
- Stężenie substratu: Im jest ono większe, tym zachodzi więcej zderzeń drobin w jednostce czasu lub aktów reakcyjnych, zatem szybkość reakcji wzrasta.
- Stopień rozdrobnienia substratu (dotyczy ciał stałych): Oprócz stężenia kluczową rolę odgrywa również powierzchnia reakcyjna. Co to oznacza? Wyobraźmy sobie dwa naczynia, w których znajduje się roztwór kwasu solnego. Do jednego z nich dodajemy pył magnezowy, do drugiego zaś wstążkę z magnezu. W której probówce reakcja zajdzie szybciej? Oczywiście w pierwszej! Ponieważ tam powierzchnia kontaktu magnezu z kwasem solnym jest większa niż w naczyniu drugim. Pył magnezowy ma zatem większą powierzchnię reakcyjną niż wstążka z uwagi na większe rozdrobnienie.
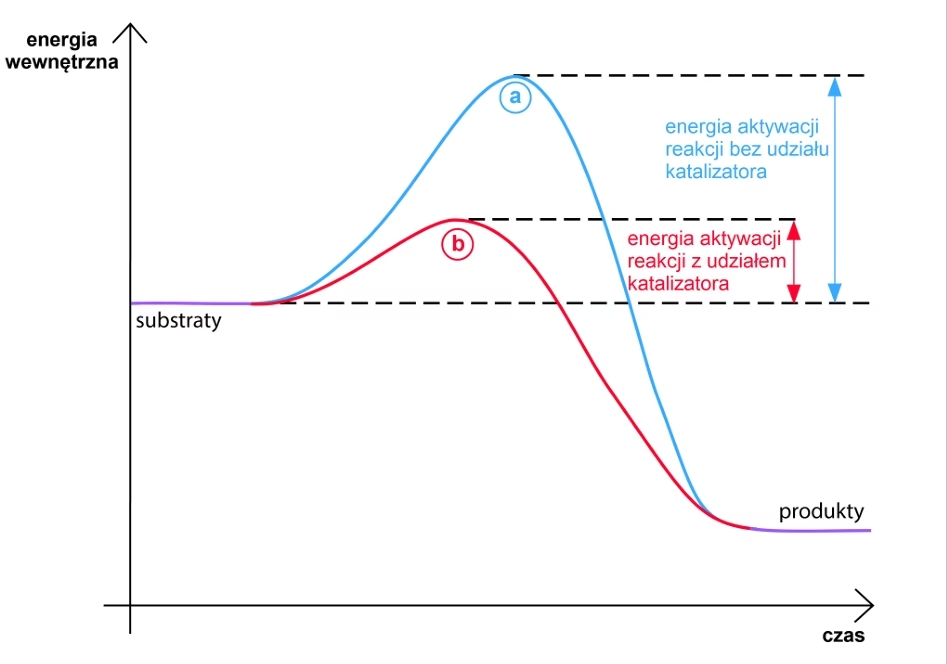
- Katalizator: Jego obecność powoduje przyspieszenie reakcji chemicznych poprzez obniżenie energii aktywacji (najmniejszej porcji energii potrzebnej do zajścia reakcji). Warto jednak pamiętać, że nie wpływa on na wydajność reakcji, a jedynie na jej kinetykę.
- Obecność inhibitora: Spowalnia reakcje chemiczne.
- Temperatura: Jej wzrost powoduje wzrost energii drobin w danym układzie, przyspiesza to ich ruch i przekłada się na większą liczbę zderzeń lub aktów reakcyjnych w jednostce czasu. Podwyższenie temperatury zwiększa również liczbę drobin o energii większej lub równej energii aktywacji (niezbędnej do zajścia reakcji), w związku z czym większa ich ilość ulega przemianie.
- Ciśnienie (dotyczy gazów): Wzrost ciśnienia powoduje zwiększenie szybkości reakcji, wtedy kiedy razem z nim rośnie stężenie substratu (warunki izotermiczne) lub jest on efektem podniesienia temperatury.
Uwaga! Podwyższenie temperatury powoduje wzrost szybkości reakcji chemicznej niezależnie od jej efektu energetycznego!
Warto wiedzieć: Jeżeli do układu zostałby wprowadzony gaz niebiorący udziału w reakcji chemicznej (tzw. gaz obojętny), wówczas zwiększyłoby się jedynie ciśnienie sumaryczne w naczyniu, a ciśnienie parcjalne (stężenie) substratu pozostałoby stałe, a co za tym idzie, szybkość reakcji również nie uległaby zmianie.
Powszechny błąd w zadaniach z kinetyki: Czas a stężenie
W niektórych zbiorach zadań można spotkać dość powszechny typ zadań, który wymaga obliczenia stężenia substratu na podstawie równania kinetycznego. Czy na pewno jest to prawidłowy sposób? Absolutnie NIE! Aby sprawdzić, ile moli substancji A pozostało po danym czasie, nie możemy skorzystać z równania kinetycznego. Dlaczego? Ponieważ w równaniu kinetycznym nie pojawia się czas. Równania kinetyczne dla reakcji I i II rzędu przedstawiają zależność szybkości od stężenia, a nie stężenia od czasu. Stężenie substratu przecież spada w czasie trwania reakcji, co z kolei pociąga za sobą spadek szybkości reakcji.
Aby policzyć ilość substancji po danym czasie, potrzebujemy odpowiedniego wzoru, w którym czas się pojawia. Dla reakcji I rzędu wygląda on następująco:
C = C0 ⋅ e-kt
gdzie:
- C0 – stężenie początkowe substratu,
- C – stężenie końcowe substratu,
- k – stała szybkości reakcji,
- t – czas,
- e – podstawa logarytmu naturalnego równa w przybliżeniu 2,71828.
Przykład: Oblicz stężenie substancji A po 1 s, jeśli C0 = 1 mol/dm3, a k = 0,1 1/s.
C = 1 ⋅ 2,71828-0,1⋅1
C = 0,90484 mol/dm3
Mając stężenie końcowe, możemy obliczyć, jak dużo substancji A przereagowało po czasie 1 s:
1 - 0,90484 = 0,09516 mol/dm3
Jak należałoby obliczyć zadanie, jeśli podana reakcja byłaby II rzędu?
Jeśli zamiast pierwszorzędowej przemiany zostałaby podana reakcja drugorzędowa, wówczas sposób rozwiązania byłby analogiczny. Musielibyśmy skorzystać z odpowiedniego wzoru (a nie równania kinetycznego!) o następującej postaci:
1/C = 1/C0 + kt
Uwaga! Jedynie wtedy, kiedy podana reakcja miałaby rząd zerowy, moglibyśmy użyć postaci równania kinetycznego w celu obliczenia stężenia substratu A po czasie trwania reakcji i zapisać, że np. 0,1 mol/dm3 substratu ulega reakcji w ciągu 1s. Ponieważ w przemianie zerowego rzędu mimo spadku stężenia, szybkość reakcji pozostaje stała. Zatem po 3s stężenie substancji A byłoby równe 0,7 mol/dm3 (jeśli początkowe było 1 mol/dm3 i szybkość 0,1 mol/dm3⋅s).
Ważne: Znajomość powyższych wzorów nie jest wymagana na egzaminie maturalnym. Jeżeli zadanie będzie wymagało ich użycia, wówczas zostaną podane w treści polecenia!
Kinetyka w zadaniach maturalnych: Przykłady z egzaminów
W celu utrwalenia poznanego tematu oraz nowo wprowadzonych pojęć przeanalizujmy parę zadań maturalnych, które w ostatnich latach pojawiły się w arkuszach egzaminacyjnych.
Matura Czerwiec 2023, poziom rozszerzony (Formuła 2023) - zadanie 6
W roztworze alkoholowo-wodnym zawierającym bromometan oraz wodorotlenek sodu przebiega reakcja opisana równaniem:
CH3Br + OH− → CH3OH + Br−
Zależność szybkości tej reakcji od stężeń reagentów przedstawia równanie kinetyczne:
v = k ⋅ cCH3Br ⋅ cOH−
W temperaturze 55 °C wartość k jest równa 2,14 ⋅ 10-2 mol/(dm3⋅s).
Reakcję CH3Br z NaOH prowadzono w temperaturze 55 °C. Po pewnym czasie stężenie jonów OH− wskutek przebiegu reakcji chemicznej zmalało z 0,06 mol/dm3 do wartości 0,05 mol/dm3, a szybkość reakcji wynosiła 1,07 ⋅ 10-5 mol/(dm3⋅s). Oblicz początkowe stężenie molowe bromometanu.

Wyjaśnienie i rozwiązanie:
- Jeżeli stężenie OH− zmalało z 0,06 mol/dm3 do 0,05 mol/dm3, to oznacza, że reakcji uległo 0,01 mol/dm3 jonów OH−. Z równania reakcji wynika, że substraty reagują w stosunku molowym 1:1, zatem ilość bromometanu, który przereagował, także musi być równa 0,01 mol/dm3.
- Oznaczmy stężenia: początkowe i końcowe bromometanu jako x oraz y.
| cCH3Br | cOH− | |
|---|---|---|
| Stężenia początkowe | x | 0,06 |
| Δ Stężeń | -0,01 | -0,01 |
| Stężenia końcowe | y | 0,05 |
- Wiemy, ile wynosiła szybkość reakcji po czasie, kiedy stężenie OH− zmalało do wartości 0,05 mol/dm3. Na tej podstawie możemy obliczyć końcowe stężenie bromometanu (y), używając do tego równania kinetycznego podanego w treści zadania:
v = k ⋅ cCH3Br ⋅ cOH−
1,07 ⋅ 10-5 = 2,14 ⋅ 10-2 ⋅ y ⋅ 0,05
1,07 ⋅ 10-5 = 0,00107 ⋅ y
y = 1,07 ⋅ 10-5 / 0,00107 = 0,01 mol/dm3
Zatem cCH3Br (końcowe) = 0,01 mol/dm3.
- Teraz, znając stężenie końcowe bromometanu, możemy policzyć jego stężenie początkowe (x), dodając do powyższego wyniku stężenie, które uległo reakcji:
x = 0,01 + 0,01 = 0,02 mol/dm3
Odpowiedź: Stężenie początkowe bromometanu wynosiło 0,02 mol/dm3.
Matura Maj 2023, poziom rozszerzony (Formuła 2023) - zadanie 6
Pewna reakcja chemiczna:
2A (g) + B (g) ↔ 2C (g)
przebiega w temperaturze 298 K według równania kinetycznego:
v = k ⋅ cA2 ⋅ cB
Stała szybkości k opisanej przemiany w temperaturze 298 K jest równa 6,7 ⋅ 103 dm6/(mol2⋅s). Początkowe stężenie substancji A wynosiło 4 mol/dm3, a początkowe stężenie substancji B było równe 3 mol/dm3. Oblicz szybkość opisanej reakcji w momencie, w którym przereagowało 50 % początkowej ilości substancji B.
Wyjaśnienie i rozwiązanie:
- W zadaniu podane mamy jedynie stężenia substratów oraz stałą szybkość reakcji, która wynosi 6,7 ⋅ 103 dm6/(mol2⋅s). Wiemy też, że 50 % początkowej ilości substancji B przereagowało.
50 % z 3 mol/dm3 to 1,5 mol/dm3.
Zgodnie z równaniem reakcji (2A + B), substraty A i B reagują ze sobą w stosunku molowym 2:1. Oznacza to, że jeśli 1,5 mol/dm3 substancji B przereagowało, to substancji A przereagowało dwukrotnie więcej, czyli 2 ⋅ 1,5 mol/dm3 = 3 mol/dm3.
| cA | cB | |
|---|---|---|
| Stężenia początkowe | 4 | 3 |
| Δ Stężeń (przereagowało) | -3 | -1,5 |
| Stężenia końcowe | 4 - 3 = 1 | 3 - 1,5 = 1,5 |
- Teraz możemy przejść do obliczenia szybkości reakcji, korzystając z końcowych stężeń substratów oraz podanego równania kinetycznego:
v = k ⋅ cA2 ⋅ cB
v = 6,7 ⋅ 103 ⋅ (1)2 ⋅ 1,5
v = 10050 mol/(dm3⋅s)
Odpowiedź: Szybkość reakcji w momencie przereagowania 50% początkowej ilości substancji B wynosi 10050 mol/(dm3⋅s).
Reguła van’t Hoffa: Wpływ temperatury na szybkość reakcji
Jedną z ważniejszych reguł w kinetyce, o której należy pamiętać, jest reguła van’t Hoffa. Informuje nas ona, że szybkość reakcji chemicznej przyspiesza lub spowalnia od 2 do 4 razy w momencie spadku lub wzrostu temperatury o 10 °C lub 10 K. Z regułą tą nierozerwalnie łączy się współczynnik van’t Hoffa (γ), który zazwyczaj przyjmuje wartość od 2 do 4. Wzór łączący wspomnianą regułę wraz z współczynnikiem wyrażony jest zależnością:
v2 / v1 = γ(T2-T1):10
gdzie:
- v1 – szybkość reakcji chemicznej w temperaturze początkowej,
- v2 – szybkość reakcji chemicznej w temperaturze końcowej,
- T1 – temperatura początkowa,
- T2 – temperatura końcowa,
- γ – temperaturowy współczynnik van’t Hoffa.
Reguła van’t Hoffa w praktyce
Zadanie: Wiadomo, że wzrost temperatury o 10 °C powoduje mniej więcej dwukrotne zwiększenie szybkości reakcji. Określ, w jakiej temperaturze reakcja, która w temperaturze 100 K trwa 100 minut, mogła być przeprowadzona w czasie 25 minut.
Wyjaśnienie i rozwiązanie:
- Zacznijmy od wypisania danych:
- T1 = 100 K
- T2 = x (szukana)
- t1 = 100 minut (czas trwania reakcji w T1)
- t2 = 25 minut (czas trwania reakcji w T2)
- Jeżeli reakcja po podwyższeniu temperatury przebiega na przykład dwa razy szybciej niż druga reakcja, wówczas czas trwania reakcji I będzie dwa razy mniejszy niż drugiej. Stosunek szybkości możemy więc wyznaczyć ze stosunku czasów trwania obydwu przemian (szybkość jest odwrotnie proporcjonalna do czasu, jeśli ilość substancji jest stała):
v2 / v1 = t1 / t2 = 100 / 25 = 4
Współczynnik γ jest równy 2 (zgodnie z informacją w zadaniu o dwukrotnym zwiększeniu szybkości na każde 10 °C/K).
- Podstawmy teraz dane pod wzór i obliczmy niewiadomą T2:
v2 / v1 = γ(T2-T1):10
4 = 2(T2-100):10
22 = 2(T2-100):10
2 = (T2 - 100) / 10
20 = T2 - 100
T2 = 120 K
Odpowiedź: W temperaturze równej 120 K reakcja, która w temperaturze 100 K trwa 100 minut, mogła być przeprowadzona w czasie 25 minut.
Najczęściej zadawane pytania (FAQ)
- Czym jest kinetyka chemiczna?
- Kinetyka chemiczna to dział chemii fizycznej badający szybkość reakcji chemicznych i czynniki wpływające na ich przebieg w czasie, takie jak stężenie, temperatura czy katalizatory.
- Dlaczego kinetyka jest ważna?
- Kinetyka jest kluczowa dla optymalizacji procesów przemysłowych, ponieważ pozwala kontrolować szybkość produkcji, minimalizować koszty i zwiększać bezpieczeństwo reakcji.
- Jakie czynniki wpływają na szybkość reakcji?
- Główne czynniki to: stężenie substratów, stopień rozdrobnienia (dla ciał stałych), temperatura, obecność katalizatorów (przyspieszają) lub inhibitorów (spowalniają) oraz ciśnienie (dla reakcji z udziałem gazów).
- Czym różni się rzędowość od cząsteczkowości?
- Cząsteczkowość to liczba cząsteczek biorących udział w elementarnym etapie reakcji. Rzędowość to suma wykładników potęg stężeń w równaniu kinetycznym, określająca faktyczną zależność szybkości od stężeń, wyznaczana doświadczalnie.
- Czy kinetyka jest trudna do nauki?
- Kinetyka może być wyzwaniem ze względu na aspekty matematyczne i abstrakcyjne koncepcje, ale z odpowiednim podejściem i praktyką staje się zrozumiała i fascynująca, otwierając drogę do głębszego zrozumienia procesów chemicznych.
Zainteresował Cię artykuł Kinetyka Chemiczna: Klucz do Zrozumienia Reakcji? Zajrzyj też do kategorii Chemia, znajdziesz tam więcej podobnych treści!