14/02/2013
Ketony to niezwykle ważna i wszechstronna grupa związków organicznych, szeroko wykorzystywanych zarówno w przemyśle, jak i w codziennym życiu. Od prostego acetonu, będącego popularnym rozpuszczalnikiem, po złożone struktury występujące w naturze, ketony odgrywają kluczową rolę w wielu procesach. Ich unikalna budowa, charakteryzująca się obecnością grupy karbonylowej, nadaje im specyficzne właściwości fizykochemiczne oraz decyduje o ich reaktywności. W niniejszym artykule zagłębimy się w świat ketonów, analizując ich budowę, metody otrzymywania, różnorodne reakcje chemiczne oraz praktyczne zastosowania, ze szczególnym uwzględnieniem najważniejszego przedstawiciela tej grupy – acetonu. Dowiemy się również, jak skutecznie odróżnić ketony od pokrewnych im aldehydów.
Co to są Ketony? Budowa i Nazewnictwo
Ketony to związki organiczne zawierające grupę ketonową, czyli grupę karbonylową (C=O) połączoną z dwoma atomami węgla. W odróżnieniu od aldehydów, gdzie grupa karbonylowa jest połączona z co najmniej jednym atomem wodoru, w ketonach oba wiązania węgla karbonylowego są z atomami węgla. Mogą to być grupy alkilowe lub arylowe, jednakowe lub różne. Proste ketony, będące monokarbonylowymi pochodnymi alkanów, nazywane są alkanonami i mają wzór ogólny CnH2n+2CO.
Budowa
Węgiel w grupie karbonylowej ketonu ma hybrydyzację sp2, co nadaje tej grupie płaski kształt. Silnie elektroujemny atom tlenu w grupie karbonylowej sprawia, że jest ona polarna. Ta polarność wpływa na właściwości fizykochemiczne ketonów oraz na ich reaktywność. Ketony mogą zawierać jedną grupę ketonową (monoketony) lub dwie (diketony), a także być częścią bardziej złożonych struktur cyklicznych czy aromatycznych. Najprostszym ketonem jest propanon (aceton), w którym grupa karbonylowa jest połączona z dwiema grupami metylowymi.
Nazewnictwo
Nazewnictwo ketonów opiera się na systematycznych zasadach IUPAC, choć często stosuje się również nazwy zwyczajowe. W nazewnictwie systematycznym, do nazwy odpowiedniego węglowodoru dodaje się sufiks „-on”, a położenie grupy karbonylowej oznacza się numerem, jeśli jest to konieczne. Numeracja łańcucha głównego rozpoczyna się od końca najbliżej grupy karbonylowej. Przykładowo, propanon jest najprostszym ketonem i nie wymaga numeru. Butanon to keton, w którym grupa karbonylowa znajduje się przy drugim atomie węgla (butan-2-on). W nazewnictwie zwyczajowym często wymienia się nazwy grup alkilowych połączonych z grupą karbonylową, np. propanon to keton dimetylowy, a butanon to keton metylowo-etylowy. Ketony tworzą szereg homologiczny, podobnie jak inne klasy związków organicznych, takie jak węglowodory czy alkohole.
Właściwości Fizykochemiczne Ketonów
Ketony o niewielkich grupach alkilowych, takie jak propanon, są cieczami, które dobrze mieszają się zarówno z wodą, jak i z rozpuszczalnikami organicznymi. Są związkami umiarkowanie polarnymi, ale w przeciwieństwie do alkoholi, nie tworzą wiązań wodorowych między swoimi cząsteczkami, ponieważ nie posiadają atomu wodoru bezpośrednio połączonego z atomem tlenu. Mogą jednak tworzyć wiązania wodorowe z cząsteczkami wody, co odpowiada za ich rozpuszczalność w wodzie.
Temperatury wrzenia ketonów są wyższe niż analogicznych alkanów czy alkenów o podobnej masie cząsteczkowej, co jest wynikiem polarności grupy karbonylowej i wynikających z niej sił dipol-dipol. Jednakże, są one niższe niż temperatury wrzenia odpowiednich alkoholi, które tworzą silne wiązania wodorowe. Ketony są stosunkowo niereaktywne w porównaniu do aldehydów, co sprawia, że często znajdują zastosowanie jako rozpuszczalniki i dodatki do zmywaczy farb.

Charakterystyczną cechą ketonów jest ich negatywna reakcja w próbach Tollensa i Trommera, które są używane do odróżniania ich od aldehydów. Natomiast dla ketonów metylowych charakterystyczna jest pozytywna próba jodoformowa.
Metody Otrzymywania Ketonów
Ketony można otrzymać na kilka sposobów, wykorzystując różne reakcje chemiczne. Poniżej przedstawiono najważniejsze z nich:
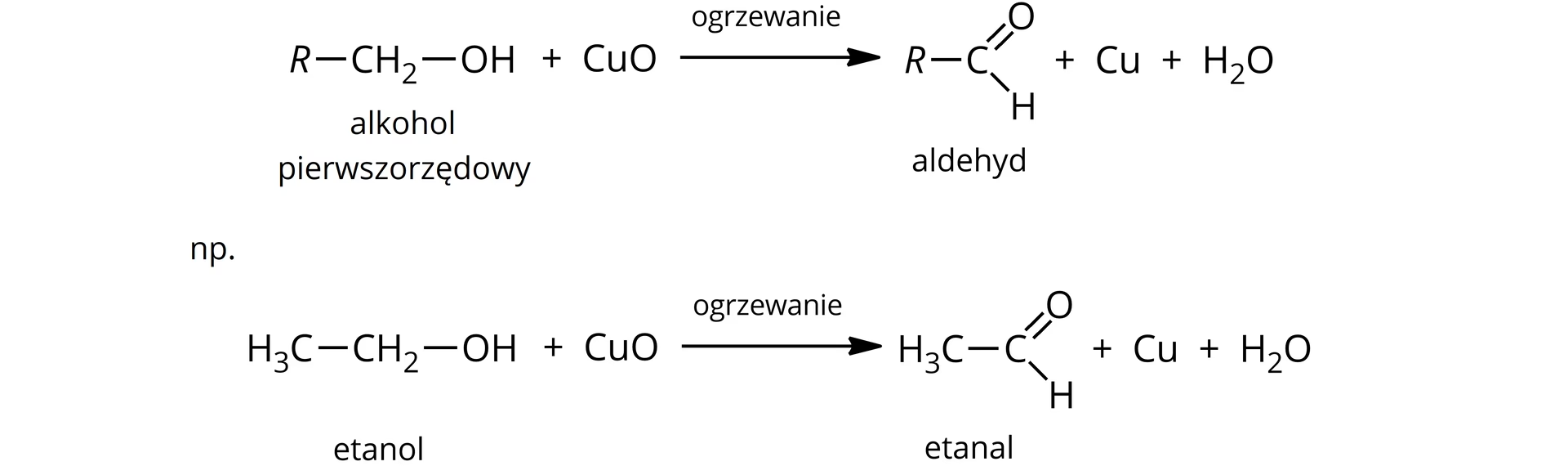
- Utlenianie alkoholi drugorzędowych: Jest to jedna z najczęściej stosowanych metod. Alkohole drugorzędowe poddane utlenianiu (np. za pomocą dwuchromianu potasu lub nadmanganianu potasu w środowisku kwasowym) przekształcają się w ketony.
- Hydroliza dwuchlorowcopochodnych: Dwuchlorowcopochodne, w których oba atomy chloru są przyłączone do tego samego atomu węgla (geminalne dihalogenki), mogą być hydrolizowane, prowadząc do powstania ketonów.
- Hydratacja alkinów: Alkiny, szczególnie te z potrójnym wiązaniem na końcu łańcucha, mogą ulegać hydratacji (przyłączaniu wody) w obecności katalizatorów (np. soli rtęci), tworząc enole, które następnie tautomerizują do ketonów.
- Reakcja Friedla-Craftsa: Jest to metoda syntezy ketonów aromatycznych. Acylacja Friedla-Craftsa polega na reakcji chlorków acylowych lub bezwodników kwasowych z arenami w obecności kwasu Lewisa (np. AlCl3), prowadząca do powstania ketonów.
- Piroliza soli kwasów karboksylowych: Specyficzne metody, takie jak prażenie soli wapniowych kwasów karboksylowych (np. etanianu wapnia), mogą prowadzić do otrzymywania ketonów.
Poniższa tabela przedstawia porównanie wybranych metod otrzymywania ketonów:
| Metoda | Substrat | Warunki/Katalizator | Charakterystyka |
|---|---|---|---|
| Utlenianie alkoholi 2° | Alkohol drugorzędowy | KMnO4, K2Cr2O7, odczynniki chromowe | Czyste produkty, wysoka wydajność. |
| Hydratacja alkinów | Alkin | HgSO4/H2SO4 | Tworzenie enoli, które tautomerizują do ketonów. |
| Reakcja Friedla-Craftsa | Aren + chlorek acylowy/bezwodnik | AlCl3 (kwas Lewisa) | Dla ketonów aromatycznych. |
Reakcje Ketonów – Rdzeń Aktywności Chemicznej
Reakcje chemiczne ketonów są w dużej mierze związane z obecnością grupy karbonylowej. Mimo że są stosunkowo niereaktywne w porównaniu do aldehydów, ulegają wielu ważnym przemianom.
Addycja Nukleofilowa
Najbardziej charakterystycznymi reakcjami dla ketonów są reakcje addycji nukleofilowej do grupy karbonylowej. Jest to możliwe dzięki płaskiej budowie grupy karbonylowej (atom węgla sp2) oraz zdolności silnie elektroujemnego atomu tlenu do przyjmowania ładunku ujemnego. W wyniku ataku nukleofila na elektrofilowy atom węgla grupy karbonylowej następuje jego przyłączenie. Ketony są mniej reaktywne od aldehydów w tych reakcjach, często wymagając ostrzejszych warunków.
Przykłady addycji nukleofilowej:
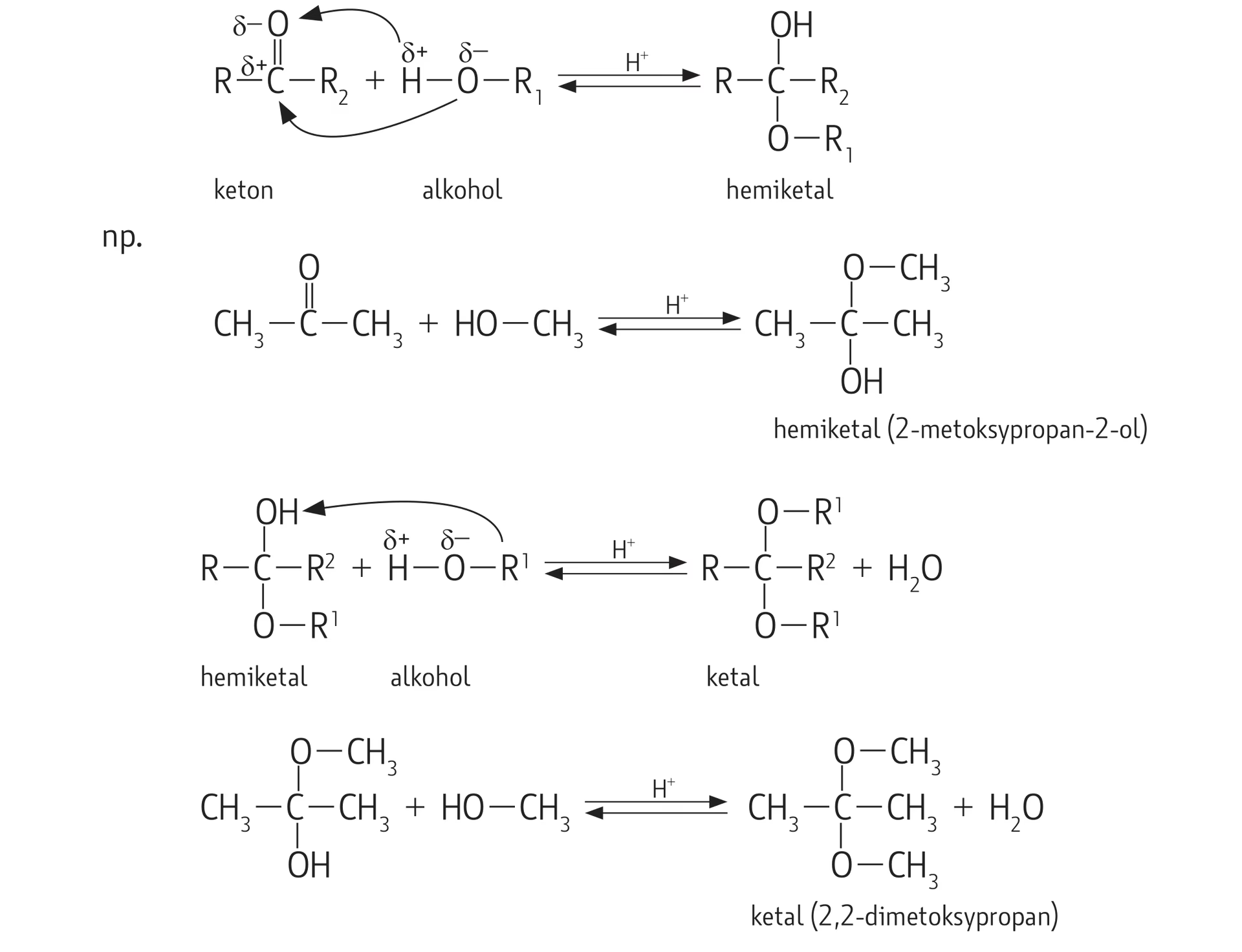
- Przyłączenie alkoholi: Prowadzi do powstania nietrwałych hemiacetali, a w obecności katalizatora kwasowego i nadmiaru alkoholu, do stabilnych acetali. Acetylowanie jest procesem odwracalnym, a acetale są często używane jako grupy ochronne dla grup karbonylowych.
- Przyłączenie cyjanowodoru (HCN): Tworzy cyjanohydryny. Reakcja ta jest katalizowana zasadami i jest ważna w syntezie organicznej, ponieważ wprowadza grupę hydroksylową i nitrylową.
- Reakcje z pochodnymi amoniaku: Ketony reagują z hydrazyną, hydroksyloaminą, fenylohydrazyną czy semikarbazydem, tworząc odpowiednio hydrazony, oksymy, fenylohydrazony czy semikarbazony. Te produkty często są stabilnymi, krystalicznymi związkami, używanymi do identyfikacji ketonów.
- Przyłączenie wodorosiarczynu sodu (NaHSO3): Tworzy krystaliczne sole addycyjne, które mogą być wykorzystane do oczyszczania ketonów.
Reakcje Utleniania Ketonów
Ketony są zazwyczaj odporne na utlenianie i do ich zajścia wymagana jest wysoka temperatura lub silne utleniacze, co prowadzi do rozerwania wiązania węgiel–węgiel. Takiej reakcji z silnymi utleniaczami, np. KMnO4 czy K2Cr2O7, ulegają w rzeczywistości nietrwałe formy enolowe, pozostające w stanie równowagi z ketonem. W wyniku takiego utleniania powstają złożone mieszaniny kwasów karboksylowych.
- Utlenianie ketonów zawierających grupę hydroksylową lub karbonylową w pozycji α: Ulegają reakcji z kwasem nadjodowym (HIO4) i jego solami (np. NaIO4), co prowadzi do rozerwania wiązania węgiel-węgiel i powstania mieszaniny kwasów karboksylowych i aldehydów.
- Reakcja haloformowa: Ketony metylowe (posiadające grupę CH3 przy grupie karbonylowej) ulegają utlenianiu w wyniku reakcji z solami kwasów podchlorawego, podbromawego lub podjodawego (NaOX). Powstaje wtedy odpowiedni haloform (chloroform, bromoform lub jodoform) oraz sól kwasu karboksylowego. Jest to ważna reakcja diagnostyczna.
- Utlenianie Baeyera-Villigera: Ketony można utlenić za pomocą nadtlenku wodoru lub kwasów nadtlenowych (np. kwasu nadmrówkowego, mCPBA). W środowisku lekko kwasowym lub zasadowym zachodzi wtedy reakcja prowadząca do otrzymania estru. W przypadku utleniania ketonu cyklicznego produktem reakcji jest lakton.
Redukcja Ketonów
Ketony mogą być redukowane do alkoholi drugorzędowych lub bezpośrednio do węglowodorów.

Redukcja do alkoholi drugorzędowych:
- Hydrogenacja katalityczna: Na katalizatorach takich jak pallad (Pd) czy nikiel (Ni).
- Reduktory chemiczne: Stosuje się łagodniejsze reduktory, takie jak glinowodorek litu (LiAlH4) lub tetraboran sodu (NaBH4). Zaletą tych związków jest to, że nie redukują one podwójnych wiązań węgiel–węgiel, co pozwala na selektywną redukcję grupy karbonylowej.
Poniższa tabela porównuje właściwości i zastosowania dwóch popularnych reduktorów:
| Reduktor | Preferowane rozpuszczalniki | Redukowane grupy funkcyjne | Charakterystyka |
|---|---|---|---|
| Tetraboran sodu (NaBH4) | Etanol, wodny etanol, 15% NaOH | Aldehydy (do alkoholi 1°), ketony (do alkoholi 2°); większość innych grup jest obojętna. | Łagodny, bezpieczny, selektywny, łatwe warunki reakcji. |
| Glinowodorek litu (LiAlH4) | Eter, THF | Aldehydy (do alkoholi 1°), ketony (do alkoholi 2°), kwasy karboksylowe (do alkoholi 1°), estry, epoksydy, nitryle, amidy. | Bardzo silny, reaktywny z wodą i alkoholami, mniej selektywny. |
Redukcja do węglowodorów:
- Redukcja Clemmensena: Prowadzi do otrzymania węglowodoru bezpośrednio z ketonu. Reduktorem tej reakcji jest amalgamat cynku (Zn(Hg)) w stężonym kwasie solnym. Metoda ta jest odpowiednia dla związków stabilnych w środowisku kwasowym.
- Redukcja Wolffa-Kiżnera: Bezpośrednia redukcja do węglowodoru następuje w reakcji z hydrazyną (H2NNH2) w mocno zasadowym środowisku (zazwyczaj wodorotlenek potasu lub tert-butanolan potasu). Jest to metoda preferowana dla związków wrażliwych na środowisko kwasowe.
Dzięki identycznym produktom redukcji Clemmensena i Wolffa-Kiżnera można dobrać odpowiednią metodę redukcji w zależności od odporności redukowanego ketonu na środowisko kwasowe lub zasadowe. Obie metody są często stosowane do otrzymywania węglowodorów aromatycznych jako kolejny etap po acylowaniu Friedla-Craftsa.
Reakcje z Azotowymi Związkami Organicznymi (Aminy i Amoniak)
- Aminowanie redukcyjne: Ketony mogą być redukowane za pomocą amoniaku lub amin pierwszorzędowych na drodze aminowania redukcyjnego. Pośrednim etapem tej reakcji jest wytworzenie iminy (R1R2C=NR3).
- Tworzenie enamin: W przypadku zastosowania aminy drugorzędowej produktem reakcji jest enamina. Reakcja zachodzi tylko wtedy, gdy keton zawiera atom wodoru α (czyli węgiel w pozycji alfa do grupy karbonylowej ma atom wodoru). Taki atom wodoru zostaje odszczepiony, co umożliwia powstanie wiązania podwójnego. Enaminy są ważne w syntezie organicznej, np. jako półprodukty do reakcji C-alkilowania (synteza Storka), prowadzące do ketonów z grupą alkilową w pozycji α.
Reakcje z Odczynnikami Metalorganicznymi (Grignarda i Reformatskiego)
- Związki Grignarda (RMgX): Ulegają addycji do grupy karbonylowej ketonów. W wyniku reakcji do atomu tlenu przyłącza się grupa MgX, zaś reszta alkilowa R przyłącza się do atomu węgla grupy karbonylowej. Po hydrolizie produktu pośredniego otrzymuje się alkohole trzeciorzędowe.
- Reakcja Reformatskiego: Ketony reagują z α-bromoestrami w obecności metalicznego cynku (zazwyczaj w eterze). Powstaje in situ związek cynkoorganiczny, który przyłącza się do grupy karbonylowej. Po hydrolizie produktu przejściowego powstaje β-hydroksyketon, który w środowisku kwasowym może ulec dehydratacji, dając związek α,β-nienasycony.
Reakcje w Położeniu Alfa (Kwasowość Wodorów α)
Atom tlenu grupy karbonylowej zwiększa kwasowość atomów wodoru w pozycji α (czyli przy węglu sąsiadującym z grupą karbonylową). Dlatego ketony posiadające takie atomy wodoru mogą w środowisku zasadowym przekształcać się w karboaniony (enolanowe jony), które są silnymi nukleofilami i szybko wchodzą w dalsze reakcje.
- Kondensacja aldolowa: W lekko zasadowym środowisku ketony posiadające atomy wodoru α ulegają kondensacji aldolowej. W jej wyniku powstaje związek posiadający w pozycji β względem grupy karbonylowej grupę hydroksylową, tzw. aldol. Tak powstałe β-hydroksyketony stosunkowo łatwo ulegają dehydratacji w środowisku lekko kwasowym, co prowadzi do otrzymania związków α,β-nienasyconych, posiadających sprzężone wiązania podwójne. Możliwa jest również krzyżowa kondensacja aldolowa między dwoma różnymi ketonami, pod warunkiem, że jeden z nich nie posiada atomów wodoru α, aby uniknąć mieszaniny produktów.
- Reakcja Wittiga: Ketony reagują z ylidami fosforowymi. W wyniku tej przemiany najpierw powstaje produkt pośredni – betaina – który natychmiast samorzutnie ulega eliminacji z wytworzeniem tlenku trifenylofosfiny i alkenu. Jest to cenna metoda syntezy alkenów.
Reakcje Ketonów α,β-Nienasyconych
Ketony, które posiadają wiązanie podwójne w pozycji α,β względem grupy karbonylowej, wykazują specyficzną reaktywność:
- Addycja nukleofilowa (Addycja Michaela): W przypadku addycji nukleofilowej do związków α,β-nienasyconych, czynnik nukleofilowy przyłączany jest zawsze w pozycji β względem grupy karbonylowej. W silnie zasadowym środowisku (np. etanolan sodu) związki posiadające kwasowe atomy wodoru (np. estry kwasu malonowego) reagują ze związkami α,β-nienasyconymi. Reakcja ta nazywana jest addycją Michaela i prowadzi do utworzenia wiązania węgiel-węgiel i przyłączenia nowej grupy w pozycję β.
- Reakcja Dielsa-Aldera (cykloaddycja [4+2]): Ketony α,β-nienasycone ulegają reakcji Dielsa-Aldera z dienami o sprzężonych wiązaniach. W jej trakcie powstają dwa nowe wiązania węgiel-węgiel, tworząc związek cykliczny.
Aceton – Najważniejszy Przedstawiciel Ketonów
Najprostszy z ketonów, propanon, powszechnie znany jako aceton, jest bez wątpienia najważniejszym przedstawicielem tej grupy związków. Jest to bezbarwna, łatwopalna ciecz o charakterystycznym zapachu, doskonale mieszalna z wodą, alkoholami i wieloma rozpuszczalnikami organicznymi. Sam aceton jest również doskonałym rozpuszczalnikiem dla wielu substancji organicznych, takich jak oleje, żywice, tłuszcze czy tworzywa sztuczne.
Otrzymywanie przemysłowe acetonu
Aceton jest produkowany na dużą skalę w przemyśle chemicznym różnymi metodami:
- Metoda kumenowa: Najczęściej stosowana metoda, polegająca na utlenianiu kumenu (izopropylobenzenu) do wodoronadtlenku kumenu, który następnie rozkłada się na aceton i fenol.
- Z propylenu: Przeróbka propylenu na alkohol izopropylowy, który następnie jest poddawany katalitycznemu odwodornieniu do acetonu.
- Fermentacja: Historycznie, aceton był również produkowany w procesach fermentacji roztworów zawierających cukry (np. melasę) przez bakterie (fermentacja butanolowo-acetonowa).
Zastosowanie acetonu
Znaczenie acetonu wynika z jego unikalnych właściwości fizykochemicznych. Jest on szeroko stosowany jako:
- Rozpuszczalnik: W przemyśle farb i lakierów, do produkcji tworzyw sztucznych (np. pleksi), w przemyśle gumowym, do produkcji leków i kosmetyków (np. zmywacze do paznokci).
- Surowiec chemiczny: Do syntezy innych związków organicznych, np. bisfenolu A, który jest używany do produkcji żywic epoksydowych i poliwęglanów.
- Środek czyszczący: W laboratoriach do mycia sprzętu szklanego.
Należy pamiętać, że aceton jest związkiem lotnym i łatwopalnym, a jego pary z powietrzem tworzą mieszaniny wybuchowe. Wdychanie acetonu w dużych stężeniach może być szkodliwe dla zdrowia, dlatego podczas pracy z nim należy zachować szczególną ostrożność i zapewnić odpowiednią wentylację.
Jak Odróżnić Ketony od Aldehydów?
Odróżnienie ketonów od aldehydów jest kluczowe w chemii organicznej, zwłaszcza w analizie jakościowej. Podstawowa różnica polega na tym, że aldehydy posiadają właściwości redukujące (dzięki obecności atomu wodoru przy grupie karbonylowej), natomiast ketony ich nie wykazują. Do ich rozróżnienia stosuje się specjalne próby chemiczne:
1. Próba Tollensa (Próba lustra srebrnego)
Próba Tollensa wykorzystuje roztwór azotanu(V) srebra(I) w amoniaku, który jest kompleksem diamino srebra(I) [Ag(NH3)2]+, zwanym odczynnikiem Tollensa. W obecności aldehydu, jon srebra(I) ulega redukcji do metalicznego srebra, które osadza się na ściankach probówki w postaci charakterystycznego, błyszczącego lustra. Aldehyd natomiast utlenia się do odpowiedniego kwasu karboksylowego (lub jego soli). Ketony nie reagują z odczynnikiem Tollensa, co oznacza brak zmian w probówce.
Uproszczona reakcja:
RCHO + 2[Ag(NH3)2]+ + 2OH- → RCOO- + 2Ag↓ + 4NH3 + H2O
2. Próba Trommera
Próba Trommera polega na zastosowaniu wodorotlenku miedzi(II) (Cu(OH)2) w środowisku zasadowym. Wodorotlenek miedzi(II) jest niebieskim osadem. W obecności aldehydu, jon miedzi(II) (Cu2+) ulega redukcji do tlenku miedzi(I) (Cu2O), który jest ceglastoczerwonym osadem. Aldehyd, podobnie jak w próbie Tollensa, utlenia się do kwasu karboksylowego. Ketony nie reagują z wodorotlenkiem miedzi(II) i osad pozostaje niebieski.
Uproszczona reakcja:
RCHO + 2Cu(OH)2 → RCOOH + Cu2O↓ + 2H2O
Poniższa tabela podsumowuje różnice w reakcjach aldehydów i ketonów z odczynnikami diagnostycznymi:
| Odczynnik | Aldehydy | Ketony |
|---|---|---|
| Odczynnik Tollensa | Tworzy lustro srebrne | Brak reakcji |
| Odczynnik Trommera | Tworzy ceglastoczerwony osad Cu2O | Brak reakcji |
| Reakcja haloformowa (dla ketonów metylowych) | Brak reakcji (z wyjątkiem aldehydu octowego) | Tworzy haloform (np. jodoform - żółty osad) |
Często Zadawane Pytania (FAQ)
1. Dlaczego ketony są mniej reaktywne niż aldehydy w reakcjach addycji nukleofilowej?
Ketony są mniej reaktywne niż aldehydy z dwóch głównych powodów: zawada steryczna i efekty elektroniczne. Grupa karbonylowa w ketonach jest połączona z dwoma grupami alkilowymi, które są większe niż atomy wodoru w aldehydach. Te większe grupy alkilowe utrudniają dostęp nukleofilowi do elektrofilowego atomu węgla grupy karbonylowej (zawada steryczna). Dodatkowo, grupy alkilowe są grupami oddającymi elektrony (efekt indukcyjny), co stabilizuje częściowy ładunek dodatni na atomie węgla karbonylowego, zmniejszając jego elektrofilowość i tym samym reaktywność na atak nukleofilowy.
2. Czy ketony tworzą wiązania wodorowe?
Ketony nie tworzą wiązań wodorowych między swoimi własnymi cząsteczkami, ponieważ nie posiadają atomu wodoru bezpośrednio połączonego z atomem tlenu (tak jak w alkoholach czy kwasach karboksylowych). Jednakże, dzięki obecności silnie elektroujemnego atomu tlenu, ketony mogą działać jako akceptory wiązań wodorowych i tworzyć je z cząsteczkami wody lub alkoholi, co wpływa na ich rozpuszczalność w tych rozpuszczalnikach.
3. Do czego wykorzystuje się ketony w przemyśle?
Ketony, zwłaszcza aceton i metyloetyloketon (butan-2-on), są szeroko wykorzystywane jako rozpuszczalniki w przemyśle chemicznym, farmaceutycznym, kosmetycznym oraz w produkcji farb, lakierów, żywic i tworzyw sztucznych. Ich zdolność do rozpuszczania szerokiej gamy substancji organicznych oraz stosunkowo niska reaktywność sprawiają, że są idealnymi środkami do czyszczenia, odtłuszczania i syntezy chemicznej. Są także ważnymi półproduktami w syntezie wielu innych związków organicznych.
4. Co to jest próba jodoformowa i do czego służy?
Próba jodoformowa to test chemiczny służący do wykrywania obecności grupy metylowo-ketonowej (-COCH3) lub grupy α-hydroksylowej (-CH(OH)CH3). Reakcja polega na potraktowaniu próbki jodem (I2) w środowisku zasadowym. Jeśli test jest pozytywny, obserwuje się wytrącanie żółtego osadu jodoformu (CHI3), który ma charakterystyczny zapach. Jest to szczególnie przydatne do identyfikacji ketonów metylowych, ale również aldehydu octowego i alkoholi zawierających grupę -CH(OH)CH3.
Zainteresował Cię artykuł Ketony: Reakcje, Otrzymywanie i Właściwości", "kategoria": "Chemia? Zajrzyj też do kategorii Edukacja, znajdziesz tam więcej podobnych treści!
