15/02/2014
W świecie chemii, gdzie pozornie proste wzory sumaryczne skrywają złożone zależności, jednym z najbardziej fascynujących zjawisk jest izomeria. To koncepcja, która wyjaśnia, dlaczego związki chemiczne mogą mieć dokładnie tę samą liczbę atomów poszczególnych pierwiastków, a mimo to różnić się od siebie niemal wszystkim – od temperatury wrzenia po aktywność biologiczną. Izomery to związki chemiczne, które wykazują to niezwykłe zjawisko, będące kluczem do zrozumienia złożoności materii. Różnice te wynikają z odmiennego sposobu połączenia atomów w cząsteczce lub ich różnego rozmieszczenia w przestrzeni. Zrozumienie izomerii jest fundamentalne dla wielu dziedzin chemii, od projektowania leków po inżynierię materiałową.
Zjawisko izomerii, choć na pierwszy rzut oka może wydawać się skomplikowane, jest logiczne i opiera się na podstawowych zasadach wiązań chemicznych i geometrii molekuł. Pozwala nam dostrzec, jak subtelne zmiany w układzie atomów mogą prowadzić do zupełnie nowych substancji o unikalnych cechach, co jest niezwykle istotne zarówno w naturze, jak i w przemyśle chemicznym.
Główne Rodzaje Izomerii: Podział i Charakterystyka
Izomeria dzieli się na dwie główne kategorie, które definiują naturę różnic między izomerami:
Izomeria Konstytucyjna (Strukturalna)
Izomeria konstytucyjna, często nazywana również izomerią strukturalną, odnosi się do związków, które mają ten sam wzór sumaryczny, ale różnią się kolejnością połączenia atomów w cząsteczce. Oznacza to, że atomy są połączone w różny sposób, tworząc odmienne układy wiązań. W ramach izomerii konstytucyjnej wyróżniamy kilka podtypów:
Izomeria Łańcuchowa (Szkieletowa)
Ten typ izomerii dotyczy różnic w budowie szkieletu węglowego cząsteczki. Atomy węgla mogą być połączone w łańcuch prosty, rozgałęziony lub cykliczny, co prowadzi do odmiennych związków. Klasycznym przykładem jest n-heksan i 2-metylopentan. Oba związki mają ten sam wzór sumaryczny C6H14. N-heksan to prosty, nierozgałęziony łańcuch sześciu atomów węgla, natomiast 2-metylopentan posiada rozgałęzienie – grupę metylową przy drugim atomie węgla w łańcuchu pięciu atomów węgla. Mimo identycznego składu atomowego, ich struktura jest na tyle różna, że wykazują odmienne temperatury wrzenia i gęstości, co ma znaczenie w procesach rafineryjnych i zastosowaniach przemysłowych.
Izomeria Położenia (Położeniowa)
Izomeria położenia występuje, gdy izomery różnią się miejscem, w którym znajduje się grupa funkcyjna lub wiązanie wielokrotne (podwójne lub potrójne) w łańcuchu węglowym. Przykładem są but-1-en i but-2-en. Oba alkeny mają wzór sumaryczny C4H8. W but-1-enie wiązanie podwójne znajduje się między pierwszym a drugim atomem węgla, natomiast w but-2-enie – między drugim a trzecim atomem węgla. Ta pozornie niewielka zmiana położenia wiązania podwójnego wpływa na ich stabilność chemiczną i reaktywność, co jest kluczowe w syntezach organicznych.
Izomeria Funkcyjna
Ten typ izomerii jest szczególnie interesujący, ponieważ izomery funkcyjne posiadają ten sam wzór sumaryczny, ale różnią się obecnością zupełnie odmiennych grup funkcyjnych. Oznacza to, że należą do różnych klas związków chemicznych i mają drastycznie różne właściwości chemiczne i fizyczne. Doskonałym przykładem są propanal (aldehyd) i propanon (keton), oba o wzorze sumarycznym C3H6O. Propanal zawiera grupę aldehydową (-CHO) na końcu łańcucha, podczas gdy propanon ma grupę ketonową (-CO-) w środku łańcucha. Aldehydy i ketony reagują w zupełnie inny sposób, co ma ogromne znaczenie w przemyśle chemicznym, np. w produkcji polimerów czy syntezie złożonych cząsteczek. Innym często spotykanym przykładem są alkohole i etery, np. etanol (alkohol) i eter dimetylowy (eter), oba o wzorze C2H6O.
Izomeria Przestrzenna (Stereoizomeria)
Izomeria przestrzenna, czyli stereoizomeria, dotyczy związków, które mają ten sam wzór sumaryczny i tę samą kolejność połączenia atomów, ale różnią się przestrzennym rozmieszczeniem tych atomów. Czyli atomy są połączone w ten sam sposób, ale ich orientacja w trójwymiarowej przestrzeni jest inna. Stereoizomeria ma ogromne znaczenie w biochemii i farmacji, ponieważ enzymy i receptory w organizmach żywych często rozpoznają tylko jedną określoną orientację przestrzenną cząsteczki.

Enancjomeria
Enancjomery to stereoizomery, które są swoimi nienakładalnymi odbiciami lustrzanymi. Można je porównać do lewej i prawej ręki – są do siebie podobne, ale nie da się ich nałożyć idealnie na siebie. Związki te posiadają centrum chiralności (najczęściej asymetryczny atom węgla, czyli taki, do którego przyłączone są cztery różne podstawniki). Enancjomery mają identyczne właściwości fizyczne (np. temperatury topnienia i wrzenia), z wyjątkiem ich oddziaływania ze światłem spolaryzowanym – obracają płaszczyznę światła spolaryzowanego w przeciwnych kierunkach. Przykładem są kwas (R)-mlekowy i kwas (S)-mlekowy, które różnią się konfiguracją wokół chiralnego atomu węgla. W biologii jeden enancjomer może być lekiem, a drugi toksyną, co podkreśla ich znaczenie.
Diastereoizomeria
Diastereoizomery to stereoizomery, które nie są swoimi odbiciami lustrzanymi i nie są nienakładalne. W przeciwieństwie do enancjomerów, diastereoizomery mają różne właściwości fizyczne i chemiczne (np. różne temperatury topnienia, wrzenia, rozpuszczalności), co ułatwia ich rozdzielanie. Występują, gdy cząsteczka ma dwa lub więcej centrów chiralności, ale nie wszystkie z nich są odwrócone w konfiguracji. Przykładem diastereoizomerów są (2R,3S)-2-amino-3-bromopentan i (2R,3R)-2-amino-3-bromopentan. Różnią się one konfiguracją tylko przy jednym z centrów chiralności, a nie przy wszystkich, co sprawia, że nie są wzajemnymi odbiciami lustrzanymi.
Jak Tworzyć Izomery? Praktyczne Wskazówki
Tworzenie izomerów, zwłaszcza konstytucyjnych, wymaga systematycznego podejścia i zrozumienia podstawowych zasad budowy cząsteczek. Oto kroki, które pomogą w ich identyfikacji i rysowaniu:
- Zacznij od prostego łańcucha węglowego: Narysuj najdłuższy możliwy prosty łańcuch atomów węgla odpowiadający danemu wzorowi sumarycznemu.
- Zmień położenie atomów węgla lub grup funkcyjnych: Następnie, zacznij skracać łańcuch główny o jeden atom węgla i „odcięty” atom (lub grupę metylową) dołączaj jako rozgałęzienie w różnych możliwych miejscach łańcucha głównego. Pamiętaj, aby nie tworzyć identycznych struktur (np. przez odwrócenie cząsteczki) i zawsze przestrzegaj zasad wartościowości atomów (węgiel jest czterowartościowy, wodór jednowartościowy itd.).
- Sprawdź wzór sumaryczny: Po każdej zmianie upewnij się, że nowa struktura ma ten sam wzór sumaryczny, co związek wyjściowy. To podstawowa zasada izomerii.
- Rozważ różne grupy funkcyjne lub ich położenie: Jeśli szukasz izomerów funkcyjnych lub izomerów położenia, zmieniaj typ grupy funkcyjnej lub jej umiejscowienie w łańcuchu.
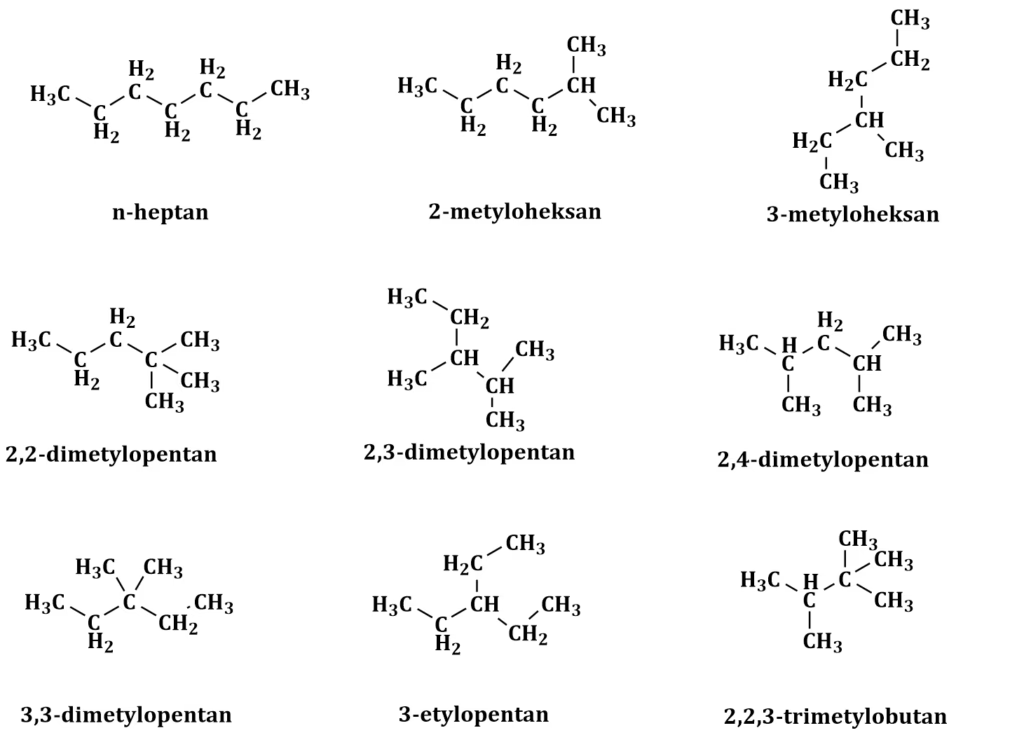
Dla węglowodoru o wzorze sumarycznym C7H16, którego przykład był podany w zadaniu maturalnym, istnieje aż 9 izomerów konstytucyjnych. Obejmują one n-heptan (prosty łańcuch) oraz liczne izomery rozgałęzione, takie jak 2-metyleheksan, 3-metyloheksan, 2,2-dimetylopentan, 2,3-dimetylopentan, 2,4-dimetylopentan, 3,3-dimetylopentan, 3-etyloheksan, a także 2,2,3-trimetylobutan. Ta liczba doskonale ilustruje, jak szybko rośnie złożoność izomerii wraz ze wzrostem liczby atomów węgla w cząsteczce.
Butan i Jego Izomery: Klasyczny Przykład
Butan (C4H10) to organiczny związek chemiczny, czwarty przedstawiciel szeregu homologicznego alkanów, czyli węglowodorów nasyconych. Jest powszechnie pozyskiwany podczas procesów przeróbki ropy naftowej i gazu ziemnego. Ze względu na swoje właściwości znajduje szerokie zastosowanie w przemyśle.
Butan jest doskonałym przykładem związku, który wykazuje izomerię konstytucyjną. Posiada on dokładnie dwa izomery:
- n-butan: Jest to izomer o prostym, nierozgałęzionym łańcuchu węglowym. Jego atomy węgla ułożone są liniowo.
- 2-metylopropan (izobutan): Ten izomer ma rozgałęziony łańcuch. Został on utworzony przez oderwanie końcowego członu -CH2 z cząsteczki liniowej butanu i przyłączenie go do drugiego atomu węgla cząsteczki propanu. Nazwa zwyczajowa „izobutan” doskonale oddaje jego rozgałęzioną strukturę.
Mimo identycznego wzoru sumarycznego C4H10, n-butan i izobutan różnią się strukturą przestrzenną, co prowadzi do subtelnych, ale istotnych różnic w ich właściwościach fizykochemicznych. Na przykład, n-butan ma wyższą temperaturę wrzenia (-0.5 °C) niż izobutan (-11.7 °C). Ta różnica jest wynikiem odmiennego upakowania cząsteczek – liniowy n-butan może ściślej przylegać do siebie, co zwiększa siły międzycząsteczkowe, podczas gdy kulisty kształt izobutanu ogranicza te oddziaływania. Obie formy są bezbarwnymi, łatwopalnymi gazami o słabym zapachu, które z powietrzem tworzą mieszaninę wybuchową. Są słabo rozpuszczalne w wodzie, ale dobrze w rozpuszczalnikach organicznych.
Butan i jego izomery są szeroko stosowane jako paliwo (np. w przenośnych piecach, zapalniczkach, gazie LPG w mieszaninie z propanem), czynniki chłodnicze (w małych lodówkach kempingowych) oraz gazy nośne w aerozolach (lakiery do włosów, dezodoranty). Są także ważnymi surowcami w przemyśle chemicznym, np. do produkcji benzyny syntetycznej czy innych związków organicznych, takich jak butanol czy kwas butanowy. Butanol, będący alkoholową pochodną butanu, również występuje w formach izomerycznych (1-butanol i 2-butanol), co dodatkowo komplikuje jego chemię, ale jednocześnie otwiera nowe możliwości zastosowań jako rozpuszczalnik czy surowiec do syntezy estrów.

Metan: Czy Posiada Izomery?
Pytanie o izomeryczność metanu (CH4) jest fundamentalne dla zrozumienia istoty izomerii. Metan to najprostszy węglowodór z szeregu alkanów, składający się z jednego atomu węgla połączonego z czterema atomami wodoru. Jego struktura jest tetrahedralna, co oznacza, że atom węgla znajduje się w centrum, a atomy wodoru na wierzchołkach czworościanu foremnego.
Odpowiedź na pytanie, czy metan ma izomery, jest jednoznaczna: nie, metan nie posiada izomerów. Dlaczego? Definicja izomerii wymaga, aby istniała możliwość przearanżowania atomów w cząsteczce w taki sposób, aby powstała inna struktura przy zachowaniu tego samego wzoru sumarycznego. W przypadku metanu, z tylko jednym atomem węgla i czterema atomami wodoru, nie ma żadnej innej możliwości ułożenia tych atomów. Niezależnie od tego, jak spojrzymy na cząsteczkę metanu, zawsze będzie ona identyczna. Nie ma tu miejsca na różnice w łańcuchu, położeniu grup funkcyjnych ani na chiralność. Jest to najprostsza możliwa struktura alkanu, która nie pozwala na żadne modyfikacje prowadzące do izomerów.
Metan jest głównym składnikiem gazu ziemnego i ważnym paliwem. Jest bezbarwnym, bezwonnym gazem, który podobnie jak butan, tworzy z powietrzem mieszaninę wybuchową. Jest stabilny chemicznie i ulega głównie reakcjom spalania (całkowitego lub niecałkowitego) oraz halogenowania rodnikowego, które prowadzą do powstania pochodnych, takich jak chlorometan. Mimo braku izomerów, jego właściwości i reakcje są intensywnie badane ze względu na jego znaczenie jako źródła energii i gazu cieplarnianego.
Ile Izomerów Mają Alkany? Zależność od Liczby Atomów Węgla
Liczba możliwych izomerów konstytucyjnych (strukturalnych) dla alkanów rośnie wykładniczo wraz ze wzrostem liczby atomów węgla w cząsteczce. Jest to fascynujące zjawisko, które pokazuje rosnącą złożoność chemii organicznej. O ile metan nie ma żadnych izomerów, a butan ma dwa, to dla większych alkanów liczba ta staje się znacząca:
- Metan (C1H4): 1 struktura (0 izomerów)
- Etan (C2H6): 1 struktura (0 izomerów)
- Propan (C3H8): 1 struktura (0 izomerów)
- Butan (C4H10): 2 izomery (n-butan i izobutan)
- Pentan (C5H12): 3 izomery
- Heksan (C6H14): 5 izomerów
- Heptan (C7H16): 9 izomerów
- Oktan (C8H18): 18 izomerów
- Nonan (C9H20): 35 izomerów
- Dekan (C10H22): 75 izomerów konstytucyjnych
Jak widać, dla alkanu zawierającego zaledwie 10 atomów węgla w cząsteczce, teoretycznie istnieje już 75 różnych struktur o tym samym wzorze sumarycznym. Ta ogromna różnorodność jest jednym z powodów, dla których chemia organiczna jest tak obszerną i złożoną dziedziną. Każdy z tych izomerów, mimo identycznego składu atomowego, będzie miał swoje unikalne właściwości fizyczne (np. temperatury wrzenia i topnienia) oraz chemiczne, co ma kluczowe znaczenie w ich identyfikacji, syntezie i zastosowaniach.
Podsumowanie i Najczęściej Zadawane Pytania (FAQ)
Zjawisko izomerii jest fundamentalnym filarem chemii organicznej, ukazującym, jak różnorodne mogą być struktury molekularne przy zachowaniu tego samego składu atomowego. Zrozumienie izomerów pozwala na głębszą analizę i syntezę związków chemicznych o pożądanych właściwościach, co ma nieocenione znaczenie w wielu gałęziach przemysłu i nauki.

Co to jest izomeria?
Izomeria to zjawisko, w którym związki chemiczne mają ten sam wzór sumaryczny (zawierają tę samą liczbę atomów poszczególnych pierwiastków chemicznych), ale różnią się strukturą lub przestrzennym rozmieszczeniem atomów, co prowadzi do różnych właściwości chemicznych i fizycznych.
Jakie są główne typy izomerów?
Główne typy izomerów to izomery konstytucyjne (strukturalne), które różnią się kolejnością połączenia atomów, oraz izomery przestrzenne (stereoizomery), które mają tę samą kolejność połączenia, ale różnią się rozmieszczeniem atomów w przestrzeni. Izomeria konstytucyjna dzieli się dalej na łańcuchową, położenia i funkcyjną, natomiast izomeria przestrzenna na enancjomery i diastereoizomery.
Ile izomerów ma butan?
Butan (C4H10) ma dwa izomery konstytucyjne: n-butan (o prostym łańcuchu węglowym) oraz 2-metylopropan, znany również jako izobutan (o rozgałęzionym łańcuchu węglowym).
Czy metan ma izomery?
Nie, metan (CH4) nie posiada izomerów. Ze względu na swoją prostą strukturę składającą się z jednego atomu węgla i czterech atomów wodoru, nie ma możliwości innego ułożenia atomów, które prowadziłoby do odmiennej struktury przy zachowaniu tego samego wzoru sumarycznego.
Dlaczego izomery są ważne w chemii?
Izomery są kluczowe, ponieważ nawet niewielkie zmiany w strukturze molekularnej mogą prowadzić do drastycznie różnych właściwości fizycznych, chemicznych i biologicznych. Ma to ogromne znaczenie w medycynie (np. działanie leków, gdzie tylko jeden enancjomer jest aktywny), w przemyśle (różne izomery mogą być wykorzystywane jako paliwa, rozpuszczalniki czy surowce do syntez), a także w zrozumieniu procesów biologicznych w żywych organizmach.
Zainteresował Cię artykuł Izomery: Tajemnice Różnych Struktur", "kategoria": "Chemia? Zajrzyj też do kategorii Edukacja, znajdziesz tam więcej podobnych treści!
