29/11/2010
W świecie fizyki i chemii, gdzie dążymy do zrozumienia najmniejszych cząsteczek i ich zachowań, często posługujemy się modelami upraszczającymi rzeczywistość. Jednym z najbardziej fundamentalnych i użytecznych pojęć jest koncepcja gazu doskonałego. Choć jest to model teoretyczny, nieistniejący w czystej postaci w naturze, stanowi on kamień węgielny termodynamiki i pozwala nam przewidywać zachowanie gazów w szerokim zakresie warunków. Zrozumienie, czym jest gaz doskonały, jakie ma właściwości i jak działa jego równanie stanu, otwiera drzwi do głębszego poznania otaczającego nas świata.

W tym artykule zagłębimy się w świat gazów, począwszy od definicji gazu doskonałego, poprzez jego kluczowe założenia, aż po słynne równanie stanu gazu doskonałego. Przyjrzymy się również, jak ten hipotetyczny model odnosi się do gazów rzeczywistych i dlaczego jest tak niezastąpiony w nauce i inżynierii.
Czym Jest Gaz Doskonały?
Gaz doskonały to hipotetyczny gaz, którego cząsteczki spełniają ściśle określone, idealne warunki. Jest to model teoretyczny, stworzony w celu uproszczenia analizy zachowania gazów i wyprowadzenia fundamentalnych praw fizyki. W rzeczywistości żaden gaz nie jest idealnie doskonały, ale wiele gazów rzeczywistych, takich jak powietrze, azot czy tlen, w określonych warunkach (wysoka temperatura, niskie ciśnienie) zachowuje się bardzo podobnie do gazu doskonałego.
Kluczowe założenia dotyczące cząsteczek gazu doskonałego to:
- Brak Oddziaływań Międzycząsteczkowych: Cząsteczki gazu doskonałego nie przyciągają się ani nie odpychają się wzajemnie. Oznacza to, że siły między nimi są zaniedbywalne. Jedynymi interakcjami są zderzenia.
- Nieskończenie Mała Objętość Cząsteczek: Cząsteczki gazu doskonałego są traktowane jako punkty materialne, co oznacza, że ich własna objętość jest pomijalnie mała w porównaniu z objętością zajmowaną przez cały gaz (objętością pojemnika).
- Sztywne Cząsteczki: Cząsteczki gazu doskonałego są traktowane jako sztywne kule, co oznacza, że nie występują drgania ani obroty wewnątrz samych cząsteczek. Ich energia kinetyczna jest związana wyłącznie z ruchem postępowym.
Warto również wspomnieć o gazie półdoskonałym. Różni się on od gazu doskonałego tym, że w jego cząsteczkach występują drgania i obroty, co oznacza, że ich energia wewnętrzna zależy nie tylko od ruchu postępowego, ale także od tych wewnętrznych stopni swobody. Nadal jednak zakłada się brak sił międzycząsteczkowych i pomijalną objętość własną cząsteczek.
Właściwości i Założenia Modelu Gazu Doskonałego
Aby móc skutecznie modelować i przewidywać zachowanie gazów, stworzono koncepcję gazu doskonałego, opierającą się na kilku kluczowych właściwościach i założeniach. Te założenia, choć idealizujące, pozwalają na wyprowadzenie prostych, ale potężnych równań:
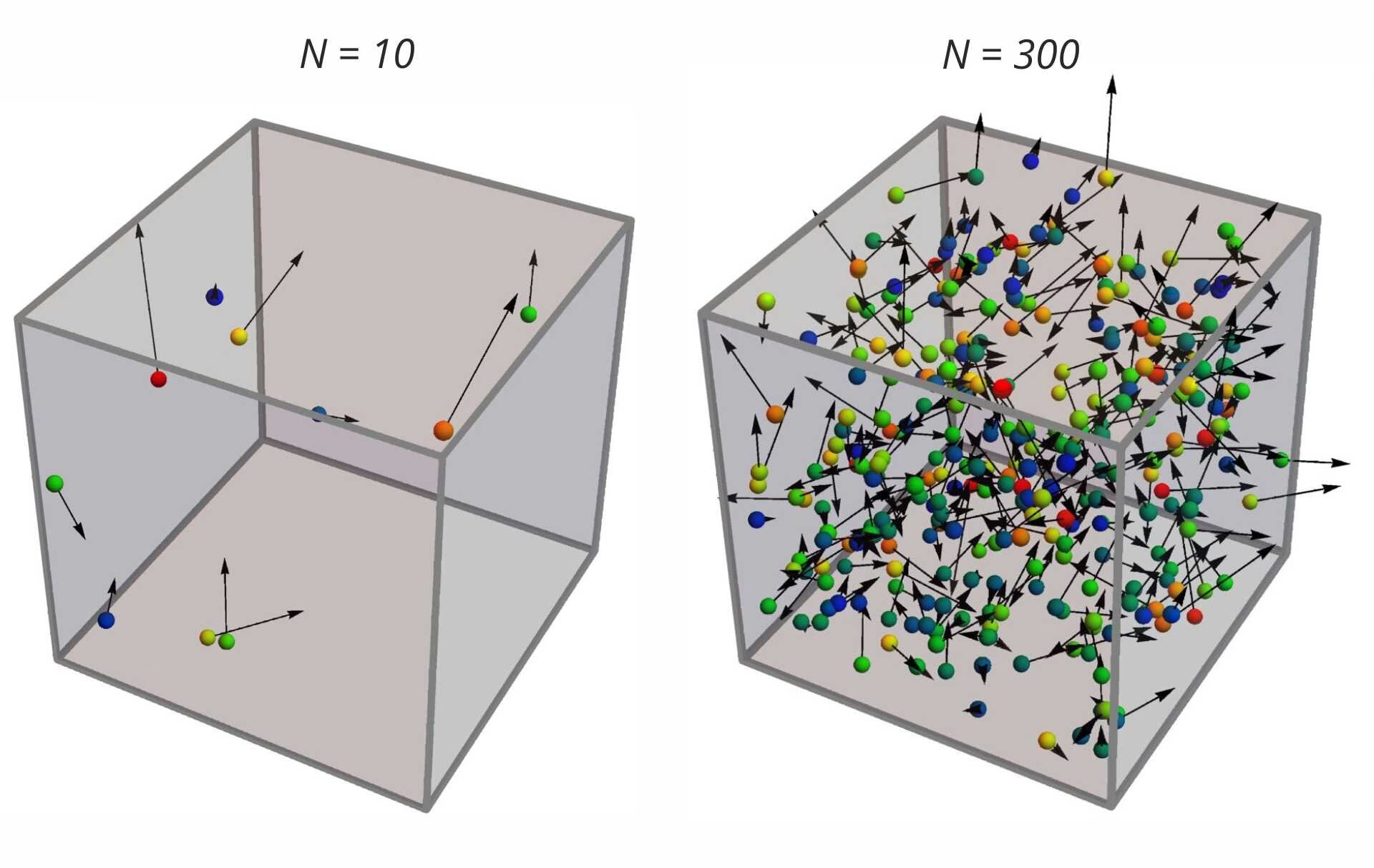
- Duża Liczba Cząsteczek w Ciągłym, Chaotycznym Ruchu: Gaz składa się z ogromnej liczby identycznych cząsteczek, które poruszają się w sposób ciągły, losowy i chaotyczny, zgodnie z prawami dynamiki Newtona.
- Pomijalna Objętość Cząsteczek: Objętość pojedynczych cząsteczek gazu jest zaniedbywalnie mała w porównaniu z całkowitą objętością zajmowaną przez gaz. Oznacza to, że większość objętości pojemnika jest pustą przestrzenią.
- Brak Sił Międzycząsteczkowych: Pomiędzy cząsteczkami gazu doskonałego nie występują żadne siły przyciągania ani odpychania. Oddziałują one ze sobą i ze ściankami pojemnika jedynie poprzez zderzenia.
- Doskonale Sprężyste Zderzenia: Wszystkie zderzenia między cząsteczkami gazu, a także między cząsteczkami a ściankami pojemnika, są doskonale sprężyste. Oznacza to, że podczas zderzeń nie ma strat energii kinetycznej. Energia kinetyczna jest jedynie przekazywana między cząsteczkami, a całkowita energia kinetyczna układu pozostaje stała. Zderzenia te wywierają stałe ciśnienie na ścianki.
Chociaż żaden gaz nie spełnia tych założeń w 100%, wiele gazów rzeczywistych, szczególnie w warunkach wysokiej temperatury i niskiego ciśnienia (gdzie cząsteczki są daleko od siebie i poruszają się szybko), zachowuje się bardzo zbliżenie do modelu gazu doskonałego. W takich warunkach siły międzycząsteczkowe stają się zaniedbywalne, a własna objętość cząsteczek jest niewielka w porównaniu z dostępną przestrzenią.
Równanie Stanu Gazu Doskonałego – Serce Termodynamiki
Koncepcja gazu doskonałego prowadzi nas do jednego z najważniejszych równań w fizyce i chemii – równania stanu gazu doskonałego. Jest to fundamentalna zależność, która opisuje, jak ciśnienie, objętość, temperatura i ilość materii gazu są ze sobą powiązane. Równanie to, często nazywane równaniem Clapeyrona lub równaniem Mendelejewa-Clapeyrona, jest niezwykle wszechstronne i pozwala przewidywać zachowanie gazów w wielu różnych scenariuszach.
Równanie stanu gazu doskonałego ma postać:
pV = nRT
Gdzie poszczególne symbole oznaczają:
p– Ciśnienie gazu. Mierzone jest zazwyczaj w paskalach (Pa), choć często używa się również atmosfer (atm) lub milimetrów słupa rtęci (mmHg). Ciśnienie jest miarą siły wywieranej przez cząsteczki gazu na ścianki pojemnika.V– Objętość gazu. Odnosi się do objętości zajmowanej przez gaz, która jest równa objętości pojemnika, w którym się znajduje. W układzie SI objętość mierzy się w metrach sześciennych (m³), ale często spotyka się również litry (L) lub decymetry sześcienne (dm³).n– Molowa ilość gazu. Wyraża liczbę moli cząsteczek gazu. Jeden mol to liczba Avogadra cząsteczek (ok. 6.022 x 1023).R– Uniwersalna stała gazowa (lub stała gazowa). Jest to fundamentalna stała fizyczna, która łączy ze sobą ciśnienie, objętość, temperaturę i ilość moli gazu. Jej wartość zależy od użytych jednostek. W układzie SI wynosi w przybliżeniu 8.314 J/(mol·K) (dżuli na mol kelwin).T– Temperatura gazu. Musi być wyrażona w skali bezwzględnej, czyli w kelwinach (K). Pamiętaj, że 0 K to absolutne zero, a temperatura w kelwinach jest równa temperaturze w stopniach Celsjusza plus 273.15 (TK = T°C + 273.15). Temperatura jest miarą średniej energii kinetycznej cząsteczek gazu.
To równanie jest potężnym narzędziem, ponieważ pozwala obliczyć jedną z tych zmiennych, jeśli znamy pozostałe. Jest szeroko stosowane w chemii, fizyce, inżynierii chemicznej i mechanicznej, a także w meteorologii.

Pochodzenie Prawa Gazu Doskonałego – Historyczny Kontekst
Równanie stanu gazu doskonałego nie powstało w jednej chwili, lecz jest wynikiem połączenia i syntezy wielu wcześniejszych odkryć i praw dotyczących gazów. Jego ostateczna forma, jaką znamy dzisiaj, została po raz pierwszy sformułowana przez francuskiego inżyniera i jednego z założycieli termodynamiki, Benoîta Paula Émile’a Clapeyrona, w 1834 roku.
Clapeyron połączył w swoim równaniu kluczowe zależności odkryte przez innych naukowców:
- Prawo Boyle’a (lub Boyle’a-Mariotte’a): Sformułowane niezależnie przez Roberta Boyle’a w XVII wieku, a później przez Edme Mariotte’a. Mówi, że przy stałej temperaturze i stałej ilości gazu, ciśnienie gazu jest odwrotnie proporcjonalne do jego objętości (p ~ 1/V). Oznacza to, że pV = const.
- Prawo Charles’a: Odkryte przez Jacques’a Charles’a pod koniec XVIII wieku. Stwierdza, że przy stałym ciśnieniu i stałej ilości gazu, objętość gazu jest wprost proporcjonalna do jego temperatury bezwzględnej (V ~ T). Oznacza to, że V/T = const.
- Prawo Gay-Lussaca: Sformułowane przez Josepha Louisa Gay-Lussaca na początku XIX wieku. Mówi, że przy stałej objętości i stałej ilości gazu, ciśnienie gazu jest wprost proporcjonalne do jego temperatury bezwzględnej (p ~ T). Oznacza to, że p/T = const.
- Prawo Avogadra: Sformułowane przez Amedeo Avogadra na początku XIX wieku. Stwierdza, że przy stałej temperaturze i ciśnieniu, objętość gazu jest wprost proporcjonalna do liczby moli gazu (V ~ n). Oznacza to, że V/n = const.
Poprzez połączenie tych empirycznych praw, Clapeyron stworzył jedno uniwersalne równanie, które kompleksowo opisuje zachowanie gazów w warunkach idealnych. To historyczne połączenie różnych perspektyw na zachowanie gazów jest przykładem synergii w nauce i budowania wiedzy na fundamentach wcześniejszych odkryć.
Jednostki w Prawie Gazu Doskonałego – Klucz do Poprawnych Obliczeń
Poprawne stosowanie równania stanu gazu doskonałego (pV = nRT) wymaga konsekwencji w używaniu jednostek. Wartość uniwersalnej stałej gazowej R zależy od jednostek, w jakich wyrażamy ciśnienie i objętość. Niezależnie od wyboru systemu jednostek, temperatura T zawsze musi być podana w kelwinach (K).
Jednostki w Układzie SI (Międzynarodowy System Jednostek)
Kiedy używamy jednostek SI, stała gazowa R ma konkretną wartość, która jest powszechnie stosowana w nauce:
p(ciśnienie): Paskale (Pa). 1 Pa = 1 N/m².V(objętość): Metry sześcienne (m³).n(liczba moli): Mole (mol).R(uniwersalna stała gazowa): Wartość 8.314 J/(mol·K) (dżuli na mol kelwin) lub równoważnie 8.314 Pa·m³/(mol·K).T(temperatura): Kelwiny (K).
Przykład: Jeśli ciśnienie jest w Pa, objętość w m³, a liczba moli w molach, to temperatura musi być w K, a stała R wyniesie 8.314.
Alternatywne Jednostki (Litr i Atmosfera)
W niektórych kontekstach, szczególnie w chemii laboratoryjnej, często wygodniej jest używać litrów dla objętości i atmosfer dla ciśnienia. W takim przypadku wartość stałej gazowej R ulegnie zmianie:
p(ciśnienie): Atmosfery (atm). 1 atm ≈ 101325 Pa.V(objętość): Litr (L). 1 L = 0.001 m³ = 1 dm³.n(liczba moli): Mole (mol).R(uniwersalna stała gazowa): Wartość 0.0821 L·atm/(mol·K).T(temperatura): Kelwiny (K).
Przykład: Jeśli ciśnienie jest w atm, objętość w L, a liczba moli w molach, to temperatura musi być w K, a stała R wyniesie 0.0821.
Niezależnie od wyboru jednostek, kluczowe jest zachowanie spójności w całym równaniu. Jeśli zaczniesz obliczenia z ciśnieniem w Pa i objętością w L, musisz najpierw przeliczyć jedną z tych wartości, aby były zgodne z wybraną wartością stałej R. Brak konsekwencji w jednostkach jest jednym z najczęstszych źródeł błędów w obliczeniach z prawem gazu doskonałego.

Gaz Doskonały vs. Gazy Rzeczywiste – Kiedy Model Działa, a Kiedy Nie?
Chociaż koncepcja gazu doskonałego jest niezwykle użyteczna i stanowi podstawę wielu obliczeń, ważne jest, aby pamiętać, że jest to idealizacja. W rzeczywistości wszystkie gazy są gazami rzeczywistymi i nie spełniają w pełni założeń modelu gazu doskonałego. Jednak w pewnych warunkach gazy rzeczywiste zachowują się bardzo zbliżenie do gazów doskonałych.
Oto porównanie kluczowych cech gazu doskonałego i gazów rzeczywistych:
| Cecha | Gaz Doskonały (Model Idealny) | Gaz Rzeczywisty |
|---|---|---|
| Objętość cząsteczek | Pomijalna w stosunku do objętości pojemnika. | Posiada własną, skończoną objętość. |
| Siły międzycząsteczkowe | Brak (zaniedbywalne). Cząsteczki nie oddziałują ze sobą. | Występują siły przyciągania i odpychania (np. siły Van der Waalsa). |
| Zderzenia | Doskonale sprężyste (brak strat energii). | Mogą być nieznacznie niesprężyste (niewielkie straty energii). |
| Zastosowanie prawa pV=nRT | Zawsze dokładnie spełnia to równanie. | Spełnia to równanie z dobrym przybliżeniem w określonych warunkach. |
Kiedy gazy rzeczywiste zachowują się jak gazy doskonałe?
Gazy rzeczywiste najbardziej zbliżają się do zachowania idealnego w warunkach:
- Wysokiej temperatury: Cząsteczki poruszają się bardzo szybko, a ich energia kinetyczna jest na tyle duża, że siły międzycząsteczkowe stają się zaniedbywalne w porównaniu z energią ruchu.
- Niskiego ciśnienia (lub dużej objętości): Cząsteczki są daleko od siebie, co minimalizuje siły międzycząsteczkowe i sprawia, że własna objętość cząsteczek jest znikoma w porównaniu z objętością zajmowaną przez gaz.
W warunkach niskiej temperatury i wysokiego ciśnienia (gdy cząsteczki są blisko siebie), siły międzycząsteczkowe stają się znaczące, a własna objętość cząsteczek zaczyna mieć wpływ na zachowanie gazu. W takich przypadkach model gazu doskonałego staje się niedokładny i konieczne jest stosowanie bardziej złożonych równań stanu, takich jak równanie Van der Waalsa, które uwzględniają zarówno objętość cząsteczek, jak i siły międzycząsteczkowe.
Zastosowania Prawa Gazu Doskonałego w Praktyce
Mimo że gaz doskonały jest modelem teoretycznym, jego równanie i koncepcje są szeroko stosowane w wielu dziedzinach nauki i inżynierii. Upraszczają one złożone problemy i pozwalają na szybkie i efektywne szacunki.
- Chemia: Do obliczania ilości reagujących gazów, wyznaczania mas molowych nieznanych gazów, czy określania warunków reakcji.
- Fizyka: Stanowi podstawę do zrozumienia termodynamiki, kinetycznej teorii gazów oraz zjawisk związanych z ciepłem i energią.
- Inżynieria Mechaniczna i Chemiczna: Projektowanie silników spalinowych, turbin, sprężarek, systemów klimatyzacyjnych, a także w procesach przemysłowych obejmujących gazy.
- Meteorologia: Modelowanie atmosfery, przewidywanie pogody, zrozumienie zmian ciśnienia i temperatury w masach powietrza.
- Nurkowanie: Obliczanie objętości i ciśnienia gazów w butlach nurkowych na różnych głębokościach i temperaturach.
Zdolność do przewidywania zachowania gazów w różnych warunkach sprawia, że prawo gazu doskonałego jest niezastąpionym narzędziem w rękach naukowców i inżynierów, nawet jeśli wymaga ono pewnych uproszczeń rzeczywistości.
Często Zadawane Pytania (FAQ)
Czy gaz doskonały istnieje w rzeczywistości?
Nie, gaz doskonały jest modelem teoretycznym, a nie rzeczywistą substancją. Jest to idealizacja stworzona w celu uproszczenia obliczeń i zrozumienia podstawowych praw fizyki dotyczących gazów. Jednak wiele gazów rzeczywistych, takich jak powietrze, tlen czy azot, zachowuje się bardzo zbliżenie do gazu doskonałego w warunkach wysokiej temperatury i niskiego ciśnienia.
Dlaczego koncepcja gazu doskonałego jest tak ważna?
Koncepcja gazu doskonałego jest ważna, ponieważ stanowi podstawę dla wielu teorii i obliczeń w termodynamice, chemii i inżynierii. Pozwala na wyprowadzenie prostych, ale potężnych równań, które opisują zachowanie gazów. Bez tego modelu analiza wielu zjawisk byłaby znacznie bardziej skomplikowana.

Jakie są ograniczenia prawa gazu doskonałego?
Główne ograniczenia wynikają z założeń modelu: pomijalna objętość cząsteczek i brak sił międzycząsteczkowych. Prawo gazu doskonałego staje się niedokładne w warunkach niskiej temperatury i wysokiego ciśnienia, gdzie cząsteczki są blisko siebie, siły międzycząsteczkowe stają się istotne, a własna objętość cząsteczek nie może być już zaniedbana. W takich warunkach gazy mogą skraplać się lub wykazywać inne odchylenia od idealnego zachowania.
Czy temperatura w równaniu gazu doskonałego musi być w kelwinach?
Tak, temperatura w równaniu stanu gazu doskonałego (pV = nRT) zawsze musi być wyrażona w kelwinach (K). Skala Kelvina jest skalą bezwzględną, gdzie 0 K oznacza absolutne zero, czyli stan, w którym cząsteczki mają minimalną energię kinetyczną. Użycie stopni Celsjusza lub Fahrenheita w tym równaniu prowadziłoby do błędnych wyników, ponieważ te skale mają arbitralne punkty zerowe.
Czym różni się stała gazowa R od stałej Boltzmana k?
Uniwersalna stała gazowa R (8.314 J/(mol·K)) odnosi się do jednego mola gazu (czyli liczby Avogadra cząsteczek). Stała Boltzmana k (około 1.38 x 10-23 J/K) odnosi się do pojedynczej cząsteczki gazu. W rzeczywistości R = NA * k, gdzie NA to liczba Avogadra. Obie stałe są ze sobą powiązane i opisują energię kinetyczną cząsteczek w zależności od temperatury.
Podsumowanie
Koncepcja gazu doskonałego jest jednym z najważniejszych filarów współczesnej fizyki i chemii. Choć jest to model idealizujący, jego prostota i zdolność do dokładnego opisu zachowania gazów w szerokim zakresie warunków sprawiają, że jest niezastąpionym narzędziem w nauce i inżynierii. Od zrozumienia fundamentalnych praw termodynamiki po projektowanie zaawansowanych systemów technologicznych, równanie stanu gazu doskonałego (pV = nRT) pozostaje kluczowym elementem naszej wiedzy o materii.
Pamiętając o założeniach, na których opiera się ten model, oraz o warunkach, w których gazy rzeczywiste najbardziej zbliżają się do ideału, możemy skutecznie wykorzystywać to potężne narzędzie do rozwiązywania problemów i pogłębiania naszego zrozumienia otaczającego nas świata.
Zainteresował Cię artykuł Gaz Doskonały: Fundament Termodynamiki? Zajrzyj też do kategorii Fizyka, znajdziesz tam więcej podobnych treści!