05/12/2006
W każdej sekundzie w Twoim ciele zachodzą biliony reakcji chemicznych. Od oddychania, przez trawienie, aż po myślenie – każdy proces życiowy jest możliwy dzięki niezwykłym cząsteczkom zwanym enzymami. Te białkowe katalizatory są prawdziwymi narzędziami natury, przyspieszającymi reakcje do prędkości niemożliwych do osiągnięcia w inny sposób i sprawiającymi, że życie, jakie znamy, jest w ogóle możliwe. Bez nich większość procesów metabolicznych trwałaby zbyt długo, by utrzymać funkcjonowanie organizmu. Ale czym dokładnie są enzymy i jak działają te niewidzialne siły napędowe życia?
Enzymy w Przyrodzie: Fundament Życia
Enzymy to białka – złożone makrocząsteczki, które są niezbędnymi składnikami każdego żywego organizmu, od najmniejszych mikroorganizmów, przez rośliny, aż po zwierzęta i ludzi. Można je porównać do wykwalifikowanych rzemieślników natury. Ich głównym zadaniem jest „rozbijanie” i „budowanie” cząsteczek, takich jak składniki odżywcze, oraz przyspieszanie wszystkich kluczowych procesów biologicznych. Co ciekawe, enzymy wykorzystywane w procesach przemysłowych często pochodzą z natury i mogą być stosowane w taki sam sposób, w jaki natura je wykorzystuje, co świadczy o ich wszechstronności i efektywności.

Rola enzymów w procesach naturalnych
Bez enzymów wiele fundamentalnych procesów w przyrodzie po prostu by się nie odbyło. Weźmy na przykład fotosyntezę roślin – proces, w którym rośliny przekształcają światło słoneczne w energię. Cały ten skomplikowany mechanizm, od wychwytywania energii świetlnej po syntezę glukozy, jest napędzany przez setki różnych enzymów działających w idealnej harmonii. Bez nich życie roślinne, a co za tym idzie, całe życie na Ziemi, byłoby niemożliwe.
Przykłady z natury: Fotosynteza i trawienie
Innym doskonałym przykładem są przeżuwacze, takie jak krowy czy owce, których dieta opiera się głównie na roślinach. Same nie są w stanie strawić celulozy – głównego składnika ścian komórkowych roślin. Z pomocą przychodzą im enzymy. W ich żołądkach bytują mikroby, które produkują enzym o nazwie celulaza. To właśnie celulaza rozkłada złożoną celulozę na proste cukry, które przeżuwacze mogą następnie wchłonąć i wykorzystać jako źródło energii. To pokazuje, jak precyzyjnie natura wykorzystuje enzymy do rozwiązywania problemów biologicznych i utrzymania równowagi ekosystemów.
Podstawy Biochemii Enzymów
Aby zrozumieć, jak enzymy działają, musimy zagłębić się w ich strukturę i mechanizmy. Enzymy to białka, a ich niezwykła efektywność wynika z ich unikalnej, trójwymiarowej budowy.
Czym są enzymy na poziomie molekularnym?
Enzymy są białkami składającymi się z aminokwasów połączonych w jeden lub więcej łańcuchów polipeptydowych. Sekwencja aminokwasów w łańcuchu polipeptydowym nazywana jest strukturą pierwszorzędową. To ona determinuje dalsze, bardziej złożone struktury. Struktura drugorzędowa opisuje lokalne struktury łańcucha polipeptydowego, takie jak alfa-helisy lub beta-harmonijki. Kompletne trójwymiarowe zwinięcie łańcucha polipeptydowego w podjednostkę białkową nazywane jest strukturą trzeciorzędową. Białko może składać się z jednej podjednostki (monomer) lub wielu podjednostek (np. dimer). Trójwymiarowe ułożenie podjednostek nazywane jest strukturą czwartorzędową.
Sześć głównych klas enzymów
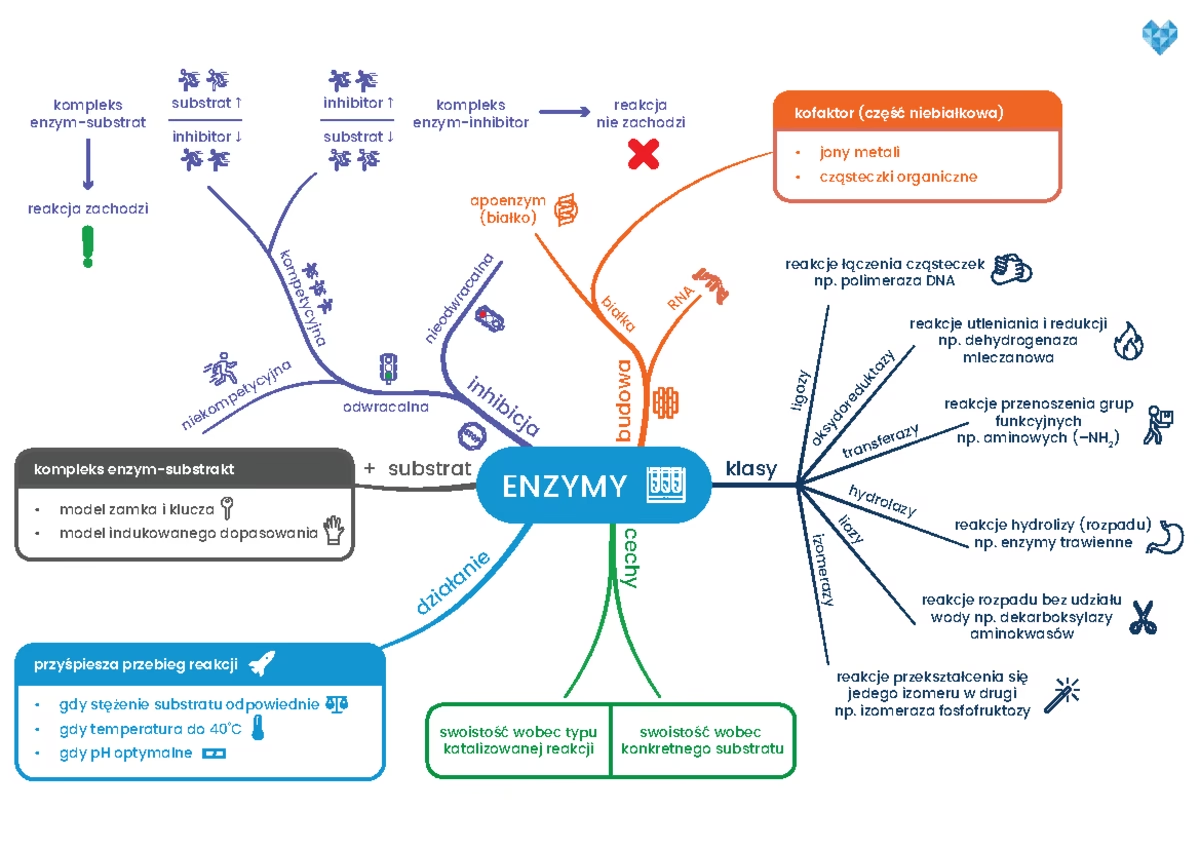
Mimo ogromnej różnorodności, enzymy można sklasyfikować w sześciu głównych kategoriach, w zależności od typu katalizowanej przez nie reakcji:
- Oksydoreduktazy: Katalizują reakcje utleniania i redukcji (transfer elektronów).
- Transferazy: Przenoszą grupy funkcyjne z jednej cząsteczki na drugą.
- Hydrolazy: Katalizują reakcje hydrolizy (rozpad cząsteczek z udziałem wody).
- Liazy: Katalizują rozpad wiązań bez udziału wody, często tworząc podwójne wiązania lub pierścienie.
- Izomerazy: Katalizują izomeryzację, czyli przekształcanie cząsteczek w ich izomery (cząsteczki o tym samym wzorze chemicznym, ale innej strukturze).
- Ligazy: Katalizują tworzenie nowych wiązań chemicznych, często z wykorzystaniem energii z ATP.
Każda kategoria przeprowadza ogólny typ reakcji, ale w jej obrębie katalizuje wiele różnych, specyficznych reakcji.
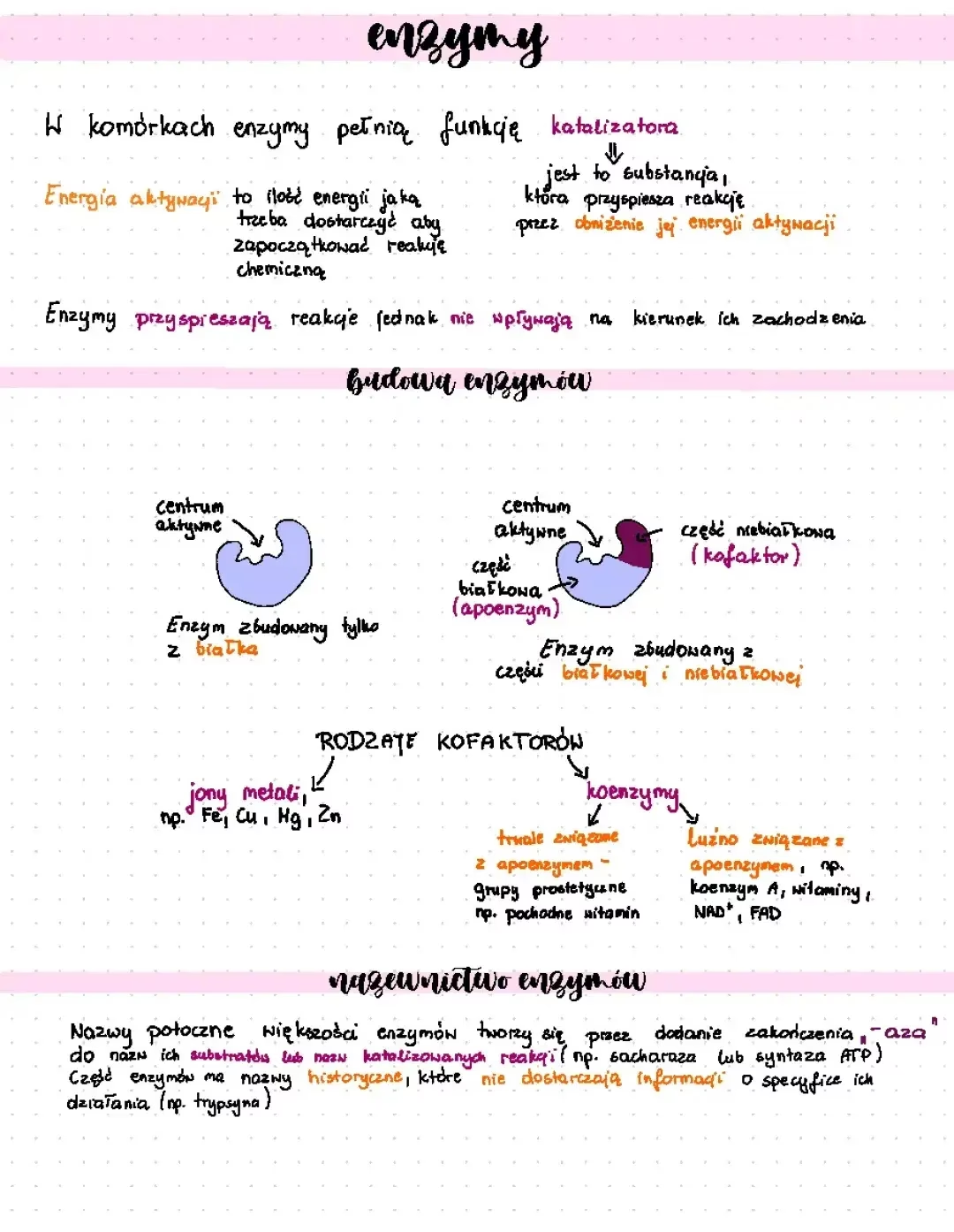
Miejsce aktywne i kofaktory
Kluczowym elementem każdego enzymu jest miejsce aktywne – specjalna kieszeń lub szczelina na powierzchni enzymu, do której wiąże się cząsteczka substratu (cząsteczka, na którą enzym działa). Kształt i skład chemiczny miejsca aktywnego są ściśle dopasowane do substratu, co zapewnia wysoką specyficzność enzymu. Miejsce aktywne zazwyczaj zajmuje stosunkowo niewielką część całego enzymu i jest wypełnione wolną wodą, gdy nie wiąże substratu.
Niektóre enzymy, zwane apoenzymami, są nieaktywne, dopóki nie zwiążą się z kofaktorem, który je aktywuje. Kofaktorem mogą być jony metali (np. cynk) lub związki organiczne (zwane koenzymami), które przyłączają się do enzymu kowalencyjnie lub niekowalencyjnie. Kompleks kofaktora i apoenzymu nazywany jest holoenzymem.

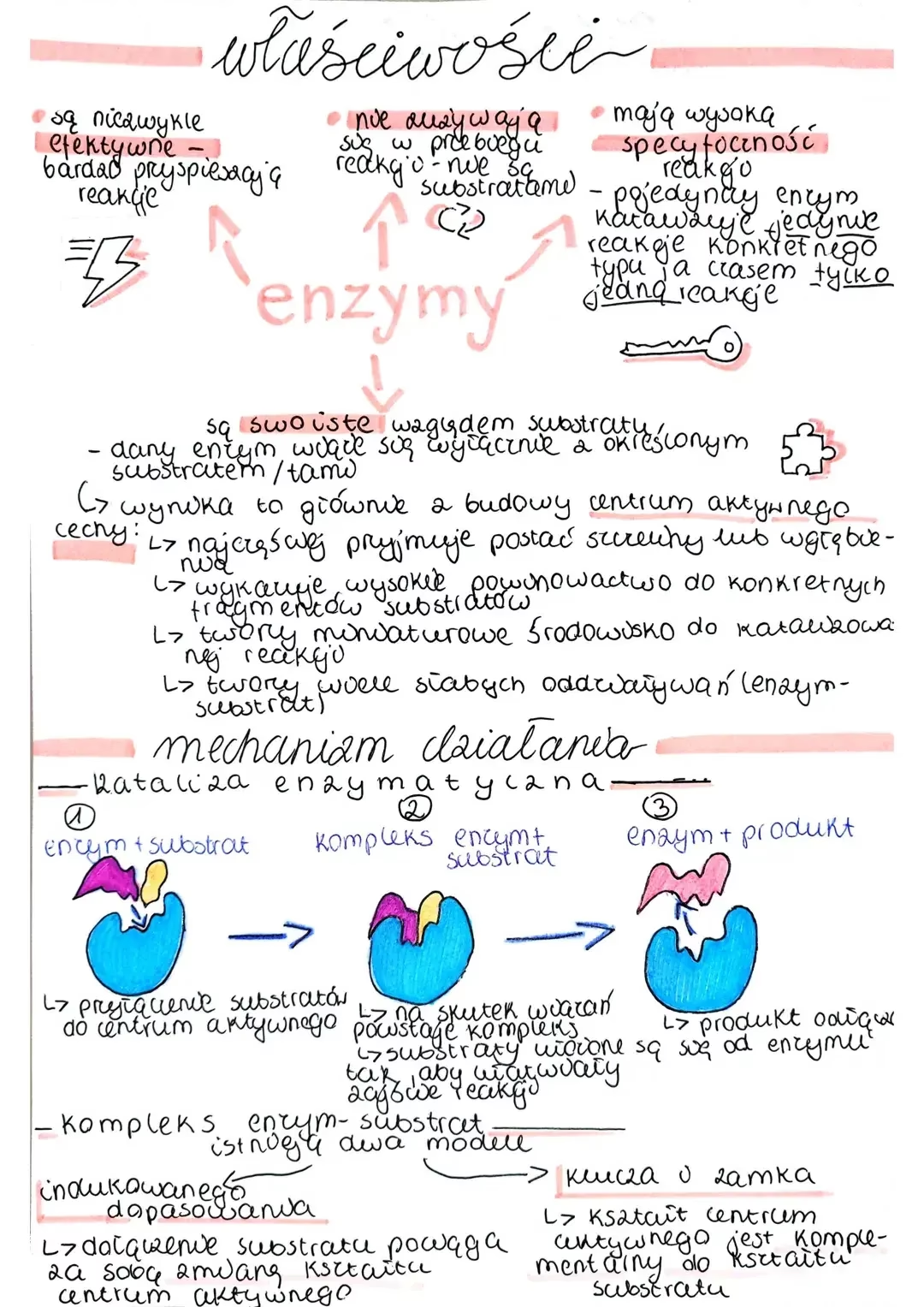
Jak Działają Enzymy? Modele i Mechanizmy
Działanie enzymów opiera się na obniżaniu energii aktywacji, czyli „progu energetycznego”, który musi zostać pokonany, aby reakcja chemiczna mogła zajść. Enzymy nie dodają energii do reakcji, ani nie zmieniają jej równowagi; jedynie przyspieszają jej przebieg, stabilizując stan przejściowy – najbardziej niestabilną konformację substratu w reakcji.
Model „klucza i zamka” vs. model „indukowanego dopasowania”
Istnieją dwa główne modele opisujące wiązanie substratu z miejscem aktywnym enzymu:
- Model „klucza i zamka”: Ten model zakłada, że kształt i skład chemiczny substratu są idealnie komplementarne do kształtu i składu chemicznego miejsca aktywnego enzymu, tak jak klucz pasuje do zamka. Gdy substrat wchodzi w miejsce aktywne, idealnie pasuje, tworząc kompleks enzym-substrat.
- Model „indukowanego dopasowania”: Ten model hipotezuje, że enzym i substrat początkowo nie mają idealnie komplementarnego kształtu lub ułożenia. Dopasowanie to jest „indukowane” w miejscu aktywnym poprzez wiązanie substratu. Enzym nieco zmienia swój kształt, aby lepiej dopasować się do substratu, a substrat również może ulec niewielkiej zmianie konformacyjnej. Ten model jest obecnie szerzej akceptowany, ponieważ lepiej wyjaśnia dynamiczny charakter interakcji enzym-substrat.
Wiązanie substratu z enzymem jest zazwyczaj stabilizowane przez lokalne interakcje molekularne z resztami aminokwasowymi w łańcuchu polipeptydowym.
Mechanizmy katalizy
Istnieją cztery powszechne mechanizmy, za pomocą których większość tych interakcji jest tworzona i zmienia miejsce aktywne w celu utworzenia kompleksu enzym-substrat:
- Kataliza kowalencyjna: Jedna lub wiele aminokwasów w miejscu aktywnym przejściowo tworzy kowalencyjne wiązanie z substratem. Reakcja ta zazwyczaj przyjmuje formę pośredniego związku, który pomaga stabilizować późniejsze stany przejściowe.
- Kataliza ogólna kwasowo-zasadowa: Cząsteczka inna niż woda działa jako donor lub akceptor protonów. Pomaga to uczynić reszty katalityczne lepszymi nukleofilami, dzięki czemu łatwiej atakują aminokwasy substratu.
- Kataliza przez aproksymację (zbliżenie): Dwa różne substraty współpracują w miejscu aktywnym, aby utworzyć kompleks enzym-substrat. Enzymy mogą zbliżać do siebie substraty w odpowiedniej orientacji, zwiększając prawdopodobieństwo reakcji.
- Kataliza jonami metali: Udział jonu metalu w miejscu aktywnym enzymu, który może pomóc uczynić atakującą resztę lepszym nukleofilem i stabilizować ładunek ujemny w miejscu aktywnym.
Kooperatywność i stany enzymów
Enzymy mogą być pojedynczymi podjednostkami lub składać się z wielu podjednostek. W enzymie wielopodjednostkowym podjednostki mogą czasami współpracować w mechanizmie zwanym „kooperatywnością”. Oznacza to, że jedna podjednostka wpływa na inną, wywołując pozytywne (zwiększające aktywność) lub negatywne (hamujące) efekty. Dzięki kooperatywności między podjednostkami enzym może przyjąć stan T (napięty) lub stan R (rozluźniony). Stan T skutkuje mniejszym powinowactwem do wiązania substratu, natomiast stan R skutkuje wyższym powinowactwem i zwiększonym wiązaniem substratu przez enzym jako całość.
Istnieją również dwa różne modele opisujące związek między tymi dwoma stanami enzymu wielopodjednostkowego:
- Model koncertowy (Concerted model): Gdy enzym jest w stanie T, jeśli jedna podjednostka zmieni się w stan R, to wszystkie pozostałe podjednostki zmienią się w stan R w tym samym czasie, co skutkuje zwiększonym wiązaniem i powinowactwem do innych efektorów. Ten model jest również odwracalny.
- Model sekwencyjny (Sequential model): Gdy jeden efektor zwiąże się z jedną z podjednostek, powinowactwo pozostałych podjednostek do efektora wzrasta, ale niekoniecznie wszystkie zmieniają się z jednego stanu w drugi. Są po prostu bardziej skłonne do zmiany.
Regulacja Aktywności Enzymów: Inhibicja
Aktywność enzymów może być precyzyjnie regulowana w organizmie, co jest kluczowe dla utrzymania homeostazy. Jednym z głównych mechanizmów regulacji jest inhibicja, czyli hamowanie działania enzymów przez specyficzne cząsteczki zwane inhibitorami. Inhibitory wiążą się z enzymem i zmniejszają lub całkowicie blokują jego funkcjonalność.
Rodzaje inhibitorów
Wyróżnia się trzy główne typy inhibicji, w zależności od sposobu, w jaki inhibitor wiąże się z enzymem i wpływa na jego aktywność:
| Typ inhibicji | Miejsce wiązania inhibitora | Wpływ na Vmax (maksymalną prędkość reakcji) | Wpływ na powinowactwo (Km) |
|---|---|---|---|
| Kompetycyjna | Miejsce aktywne enzymu | Bez zmian | Zmniejszone (wymaga więcej substratu do osiągnięcia połowy Vmax) |
| Niekompetycyjna | Inne miejsce niż aktywne (miejsce allosteryczne) | Zmniejszona | Bez zmian |
| Niekompleksowa (Uncompetitive) | Wyłącznie do kompleksu enzym-substrat (ES) | Zmniejszona | Zwiększone (pozorne zwiększenie powinowactwa, ponieważ kompleks ES jest stabilizowany) |
Szczegółowe wyjaśnienie:
- Inhibicja kompetycyjna: Zachodzi, gdy inhibitor wiąże się z miejscem aktywnym enzymu, tam gdzie normalnie wiązałby się substrat, uniemożliwiając w ten sposób wiązanie substratu. Enzymy podlegające kinetyce Michaelisa-Menten w tym przypadku osiągają tę samą maksymalną prędkość (Vmax), ale mają mniejsze powinowactwo do wiązania substratu (pozornie zwiększone Km). Można ją przezwyciężyć, zwiększając stężenie substratu.
- Inhibicja niekompetycyjna: Występuje, gdy inhibitor wiąże się z miejscem na enzymie innym niż miejsce aktywne (miejscem allosterycznym), ale skutkuje zmniejszoną zdolnością substratu do wiązania się z miejscem aktywnym lub zmniejszoną efektywnością miejsca aktywnego. Substrat nadal może się wiązać w tym modelu, ale miejsce aktywne działa mniej efektywnie. Maksymalna prędkość reakcji (Vmax) pod wpływem inhibicji niekompetycyjnej maleje, ale powinowactwo do substratu (Km) pozostaje takie samo.
- Inhibicja niekompleksowa (Uncompetitive inhibition): Zachodzi, gdy inhibitor wiąże się wyłącznie z kompleksem enzym-substrat (ES). Reakcja ta zazwyczaj występuje, gdy w reakcji są dwa lub więcej substratów lub produktów. W inhibicji niekompleksowej zarówno maksymalna prędkość (Vmax), jak i powinowactwo wiązania (Km) ulegają zmniejszeniu.
Innym rodzajem inhibicji jest ta występująca w przypadku enzymów allosterycznych. Mogą one wiązać cząsteczkę zwaną efektorem allosterycznym, która wpływa na Vmax reakcji katalitycznej lub na powinowactwo wiązania substratu, ale nie wiąże się bezpośrednio z miejscem aktywnym.
Znaczenie Kliniczne Enzymów
Wiedza o enzymach jest niezwykle istotna w medycynie, zwłaszcza w diagnostyce wielu chorób. W badaniach klinicznych enzymy mogą działać jako markery, które identyfikują stany chorobowe w organizmie. Lekarze często są w stanie określić rodzaj choroby dotykającej pacjenta oraz uszkodzony organ, charakteryzując enzymy uwalniane do krwiobiegu. Na przykład, podwyższony poziom specyficznych enzymów wątrobowych we krwi może wskazywać na uszkodzenie wątroby, a enzymów sercowych – na zawał serca. Enzymy mogą być również składnikiem biopsji tkankowej i dostarczać szczegółowych informacji diagnostycznych, pomagając w precyzyjnym określeniu charakteru zmian patologicznych.
Często Zadawane Pytania (FAQ)
- Czy enzymy zużywają się w reakcjach?
- Nie. Enzymy to katalizatory, co oznacza, że przyspieszają reakcje, ale same nie są zużywane w procesie. Po przekształceniu substratu w produkt, enzym jest gotowy do katalizowania kolejnej reakcji. To sprawia, że są niezwykle wydajne i mogą działać wielokrotnie.
- Dlaczego enzymy są tak ważne dla życia?
- Enzymy są kluczowe, ponieważ umożliwiają zajście reakcji chemicznych w organizmie w tempie wystarczającym do podtrzymania życia. Bez nich procesy metaboliczne, takie jak trawienie, oddychanie komórkowe, synteza DNA czy detoksykacja, trwałyby zbyt wolno, a organizmy nie mogłyby funkcjonować.
- Czy wszystkie enzymy są białkami?
- Zdecydowana większość enzymów to białka. Jednak istnieją nieliczne wyjątki, takie jak rybozymy (cząsteczki RNA o aktywności katalitycznej), które również pełnią funkcje enzymatyczne, choć są znacznie rzadsze.
- Jakie są główne kategorie enzymów?
- Enzymy są klasyfikowane na sześć głównych klas w zależności od typu katalizowanej reakcji: oksydoreduktazy, transferazy, hydrolazy, liazy, izomerazy i ligazy. Każda z tych klas obejmuje enzymy pełniące specyficzne funkcje metaboliczne.
- Czym różni się model „klucza i zamka” od modelu „indukowanego dopasowania”?
- Model „klucza i zamka” zakłada, że enzym i substrat mają idealnie komplementarne kształty od samego początku. Model „indukowanego dopasowania” jest bardziej dynamiczny i sugeruje, że enzym i substrat zmieniają nieco swoje kształty po związaniu, aby osiągnąć optymalne dopasowanie, co jest obecnie szerzej akceptowanym wyjaśnieniem.
Enzymy są prawdziwymi bohaterami biochemii, umożliwiającymi złożoność i dynamikę życia. Ich zrozumienie jest fundamentalne nie tylko dla biologii i medycyny, ale także dla wielu gałęzi przemysłu, gdzie ich potencjał jest wykorzystywany na coraz szerszą skalę.
Zainteresował Cię artykuł Enzymy: Niezbędne Narzędzia Życia? Zajrzyj też do kategorii Biologia, znajdziesz tam więcej podobnych treści!