14/06/2010
Zrozumienie aktywności chemicznej metali to fundament chemii nieorganicznej i klucz do przewidywania, jak metale zachowają się w różnych środowiskach. Odpowiedź na pytanie, dlaczego niektóre metale rdzewieją szybciej niż inne, lub dlaczego pewne reakcje zachodzą, a inne nie, leży właśnie w ich aktywności chemicznej. Ta właściwość decyduje o zdolności metalu do oddawania elektronów i tworzenia jonów dodatnich, co jest podstawą wielu procesów, od korozji po produkcję energii w ogniwach galwanicznych.
W tym artykule zagłębimy się w tajniki aktywności metali, wyjaśnimy, jak ją porównywać, i przedstawimy praktyczne narzędzia, które pomogą Ci zrozumieć i przewidzieć ich zachowanie w reakcjach chemicznych.
Co to jest aktywność chemiczna metali i jak ją porównywać?
Aktywność chemiczna metalu to miara jego skłonności do wchodzenia w reakcje chemiczne, zwłaszcza do oddawania elektronów. Im łatwiej metal oddaje elektrony, tym jest bardziej aktywny. Ta właściwość jest ściśle związana z budową atomu metalu, a konkretnie z liczbą elektronów walencyjnych i odległością tych elektronów od jądra.
Trendy w układzie okresowym
Aktywność metali wykazuje wyraźne trendy w układzie okresowym pierwiastków, co pozwala na szybką ocenę ich względnej aktywności bez konieczności przeprowadzania skomplikowanych eksperymentów:
- W grupach (pionowo): Aktywność metali rośnie wraz ze wzrostem liczby atomowej (czyli w dół grupy). Dzieje się tak, ponieważ wraz ze wzrostem liczby powłok elektronowych, elektrony walencyjne znajdują się coraz dalej od jądra, są słabiej przyciągane i łatwiej je oderwać. Najbardziej aktywne metale, takie jak lit (Li), sód (Na), potas (K), rubid (Rb), cez (Cs) i frans (Fr) z grupy 1 (metale alkaliczne) oraz beryl (Be), magnez (Mg), wapń (Ca), stront (Sr), bar (Ba) i rad (Ra) z grupy 2 (metale ziem alkalicznych), znajdują się na dole tych grup.
- W okresach (poziomo): Aktywność metali maleje wraz ze wzrostem liczby atomowej (czyli od lewej do prawej w okresie). W miarę przesuwania się w prawo, rośnie ładunek jądra, a elektrony walencyjne są silniej przyciągane, co utrudnia ich oddawanie.
Dlatego też metale z I i II grupy układu okresowego są uznawane za najbardziej aktywne. Wiele z nich, jak sód czy potas, reaguje gwałtownie z wodą, wypierając wodór i tworząc wodorotlenki, co jest klasycznym przykładem ich wysokiej aktywności.
Szereg Aktywności Metali: Kluczowe Narzędzie
Jednym z najpraktyczniejszych narzędzi do porównywania aktywności metali jest szereg aktywności metali (nazywany również szeregiem napięciowym metali). Jest to uporządkowana lista metali (i wodoru) według ich malejącej aktywności chemicznej.

Jak działa szereg aktywności?
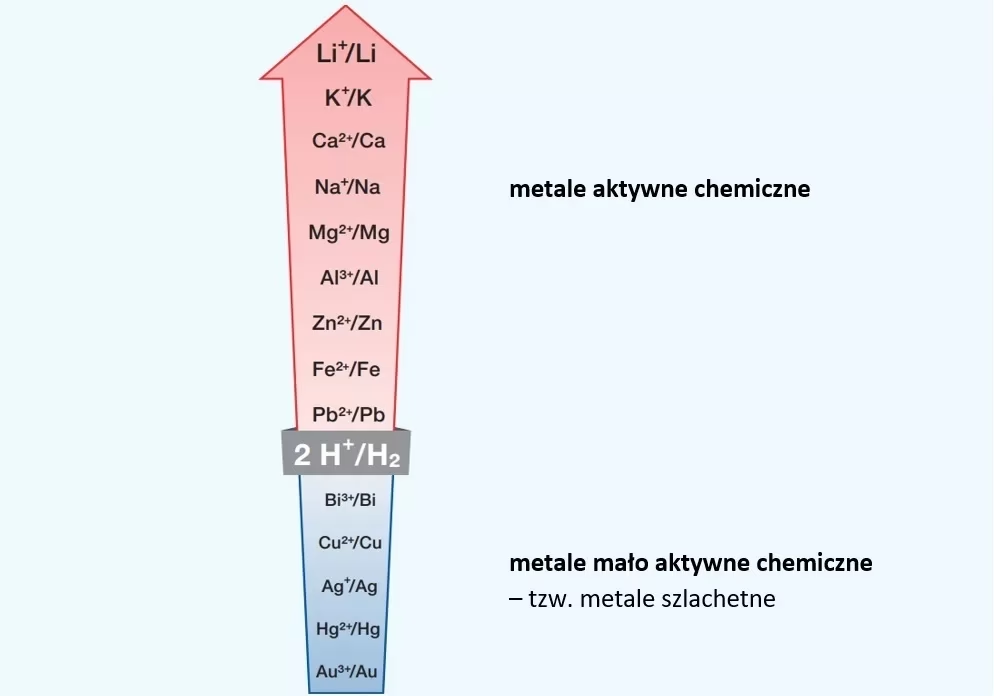
W szeregu aktywności metale są ułożone w kolejności malejącej zdolności do oddawania elektronów. Oznacza to, że metale znajdujące się na początku szeregu są najbardziej aktywne chemicznie, a te na końcu – najmniej aktywne.
Przykładowy szereg aktywności metali (od najbardziej do najmniej aktywnego):
K > Ba > Ca > Na > Mg > Al > Mn > Zn > Fe > Co > Ni > Pb > H > Cu > Hg > Ag > Pt > Au
Co możemy wywnioskować z tego szeregu?
- Metale po lewej stronie wodoru (H) są bardziej aktywne niż wodór. Oznacza to, że są w stanie wyprzeć wodór z kwasów (np. cynk reaguje z kwasem solnym, tworząc wodór i chlorek cynku).
- Metale po prawej stronie wodoru są mniej aktywne niż wodór i nie są w stanie wyprzeć go z kwasów (np. miedź nie reaguje z rozcieńczonym kwasem solnym).
- Każdy metal w szeregu jest w stanie wyprzeć metal znajdujący się po nim z roztworu jego soli.
Doświadczenie z cynkiem i miedzią: Praktyczny przykład
Klasycznym doświadczeniem ilustrującym zasadę szeregu aktywności jest reakcja cynku z solą miedzi oraz miedzi z solą cynku:
Probówka 1: Blaszka cynkowa w roztworze siarczanu(VI) miedzi(II) (CuSO₄)
Po zanurzeniu blaszki cynkowej w niebieskim roztworze siarczanu(VI) miedzi(II) zaobserwujemy, że na powierzchni cynku zaczyna osadzać się czerwona warstwa miedzi, a niebieski kolor roztworu stopniowo zanika. Oznacza to, że cynk, będąc metalem aktywniejszym chemicznie niż miedź (Zn znajduje się wcześniej w szeregu aktywności niż Cu), wypiera miedź z jej soli. Cynk przechodzi do roztworu w postaci jonów Zn²⁺, a jony Cu²⁺ z roztworu redukują się do atomów miedzi, osadzając się na blaszce.
Jest to przykład reakcji redoks (redukcji-utleniania), gdzie dochodzi do zmiany stopnia utlenienia cynku (z 0 na +2) i miedzi (z +2 na 0).
Probówka 2: Blaszka miedziana w roztworze siarczanu(VI) cynku (ZnSO₄)
W probówce drugiej, gdzie blaszka miedziana została zanurzona w roztworze siarczanu(VI) cynku, nie zaobserwujemy żadnych zmian. Miedź jest mniej aktywna chemicznie od cynku i nie jest w stanie wyprzeć cynku z jego soli. Oznacza to, że reakcja nie zachodzi.
To doświadczenie doskonale ilustruje zasadę: metal bardziej aktywny chemicznie wypiera mniej aktywny metal z wodnego roztworu jego soli.

Aktywność a właściwości redukujące i utleniające
Szereg aktywności metali jest również ściśle związany z ich właściwościami redukującymi i utleniającymi:
- Im wyżej metal znajduje się w szeregu aktywności (im jest bardziej aktywny), tym ma większą zdolność do oddawania elektronów, co oznacza, że jest silniejszym reduktorem. Jego jony (np. K⁺, Na⁺) są słabymi utleniaczami.
- Im niżej metal znajduje się w szeregu aktywności (im jest mniej aktywny), tym mniejszą ma zdolność do oddawania elektronów. Za to jego jony (np. Ag⁺, Au³⁺) są silniejszymi utleniaczami.
Jak sprawdzić, który metal jest bardziej aktywny?
Oprócz obserwacji reakcji wypierania i korzystania z szeregu aktywności, aktywność metali można mierzyć i porównywać w sposób ilościowy, bazując na ich potencjałach elektrody.
Standardowa elektroda wodorowa (SHE)
Standardowa elektroda wodorowa (SHE) jest punktem odniesienia w elektrochemii, służącym do pomiaru standardowych potencjałów elektrody innych metali. Składa się z platynowej blaszki (pokrytej czernią platynową dla zwiększenia powierzchni), zanurzonej w roztworze kwasu (np. HCl) o stężeniu jonów H⁺ równym 1 mol/dm³, przez którą przepuszcza się gazowy wodór pod ciśnieniem 1 atmosfery i w temperaturze 25°C. Potencjał tej elektrody jest umownie przyjęty jako 0 V.
Poprzez połączenie półogniwa zbudowanego z danego metalu (np. miedzi zanurzonej w roztworze jej soli) ze standardową elektrodą wodorową, można zmierzyć różnicę potencjałów, czyli siłę elektromotoryczną ogniwa. Wartość ta, nazywana standardowym potencjałem elektrody (E°), jest ilościową miarą aktywności danego metalu:
- Metale o ujemnych standardowych potencjałach elektrody (np. Zn: -0.76 V, Fe: -0.44 V) są bardziej aktywne niż wodór. Im bardziej ujemny potencjał, tym metal jest aktywniejszy.
- Metale o dodatnich standardowych potencjałach elektrody (np. Cu: +0.34 V, Ag: +0.80 V) są mniej aktywne niż wodór. Im bardziej dodatni potencjał, tym metal jest mniej aktywny.
Ta metoda pozwala na precyzyjne uszeregowanie metali pod względem ich aktywności i jest podstawą do tworzenia szeregu aktywności metali.
Porównanie aktywności wybranych metali
Poniższa tabela podsumowuje względną aktywność kilku popularnych metali, bazując na ich pozycji w szeregu aktywności i ogólnych właściwościach:
| Metal | Pozycja w szeregu aktywności | Typowa reakcja z wodą/kwasami | Zdolność do wypierania innych metali |
|---|---|---|---|
| Potas (K) | Bardzo wysoka (początek szeregu) | Gwałtowna reakcja z zimną wodą, tworząc wodorotlenek i wodór. | Wypiera prawie wszystkie metale. |
| Sód (Na) | Bardzo wysoka (blisko początku) | Gwałtowna reakcja z zimną wodą. | Wypiera większość metali. |
| Magnez (Mg) | Wysoka | Reaguje z gorącą wodą lub parą wodną; reaguje z kwasami. | Wypiera metale mniej aktywne niż Mg. |
| Cynk (Zn) | Średnia/Wysoka | Reaguje z kwasami, wypierając wodór. Nie reaguje z zimną wodą. | Wypiera m.in. miedź, srebro, złoto. |
| Żelazo (Fe) | Średnia | Reaguje z kwasami, wypierając wodór. Powoli reaguje z parą wodną. | Wypiera m.in. miedź, srebro. |
| Ołów (Pb) | Średnia/Niska (przed wodorem) | Reaguje z kwasami, ale często reakcja hamowana przez osady. | Wypiera metale po nim w szeregu. |
| Wodór (H) | Punkt odniesienia | --- | --- |
| Miedź (Cu) | Niska (po wodzie) | Nie reaguje z rozcieńczonymi kwasami nieutleniającymi; reaguje z kwasami utleniającymi. | Nie wypiera metali przed nią w szeregu. |
| Srebro (Ag) | Bardzo niska | Nie reaguje z większością kwasów; reaguje z silnymi kwasami utleniającymi. | Nie wypiera metali przed nią. |
| Złoto (Au) | Najniższa (koniec szeregu) | Nie reaguje z większością kwasów; rozpuszcza się w wodzie królewskiej. | Nie wypiera żadnych metali. |
Często Zadawane Pytania (FAQ)
Który z metali jest najbardziej aktywny?
Najbardziej aktywnym chemicznie metalem jest frans (Fr), a zaraz za nim cez (Cs). Oba te metale znajdują się na samym dole I grupy układu okresowego, co oznacza, że ich elektrony walencyjne są najdalej od jądra i najłatwiej je oddać. W praktyce laboratoryjnej często mówi się o potasie (K) i sodzie (Na) jako o bardzo aktywnych metalach, ponieważ frans i cez są niezwykle rzadkie i radioaktywne.
Które metale znajdują się wysoko w szeregu aktywności?
Wysoko w szeregu aktywności metali znajdują się metale alkaliczne (grupa 1, np. K, Na) i metale ziem alkalicznych (grupa 2, np. Ba, Ca, Mg), a także niektóre metale przejściowe, takie jak glin (Al) czy mangan (Mn).

Czy aktywność metalu zależy od jego położenia w układzie okresowym?
Tak, aktywność metalu jest ściśle związana z jego położeniem w układzie okresowym. Generalnie rośnie w dół grup i maleje wzdłuż okresów (od lewej do prawej).
Dlaczego metale aktywne są dobrymi reduktorami?
Metale aktywne mają silną tendencję do oddawania elektronów. Zgodnie z definicją, substancja, która oddaje elektrony w reakcji chemicznej, jest reduktorem. Dlatego im bardziej aktywny metal, tym silniejszym jest reduktorem.
Czy wszystkie metale reagują z kwasami?
Nie, nie wszystkie metale reagują z kwasami. Tylko metale bardziej aktywne niż wodór (czyli te, które w szeregu aktywności znajdują się przed wodorem, np. Zn, Fe, Mg) są w stanie wyprzeć wodór z kwasów nieutleniających. Metale mniej aktywne niż wodór (np. Cu, Ag, Au) nie reagują z takimi kwasami; mogą reagować jedynie z kwasami o właściwościach utleniających, takimi jak stężony kwas azotowy(V) czy gorący stężony kwas siarkowy(VI).
Podsumowanie
Zrozumienie aktywności chemicznej metali jest niezbędne w chemii. Pozwala przewidywać przebieg reakcji, wyjaśniać zjawiska takie jak korozja i jest podstawą wielu procesów przemysłowych. Kluczem do opanowania tej wiedzy jest znajomość trendów w układzie okresowym oraz umiejętność posługiwania się szeregiem aktywności metali, który w prosty sposób wizualizuje zdolność metali do reakcji i wzajemnego wypierania się z roztworów soli. Pamiętaj, że im metal jest bardziej aktywny, tym łatwiej oddaje elektrony i tym silniejszym jest reduktorem. To fundamentalna zasada, która otworzy przed Tobą drzwi do głębszego zrozumienia świata chemii.
Zainteresował Cię artykuł Aktywność Chemiczna Metali: Poradnik Studenta? Zajrzyj też do kategorii Chemia, znajdziesz tam więcej podobnych treści!
