16/05/2019
Chemia, choć bywa postrzegana jako nauka skomplikowana, posługuje się uniwersalnym językiem, który pozwala na precyzyjne opisanie materii. Tym językiem są wzory chemiczne – symbole, cyfry i nawiasy, które w skondensowany sposób przekazują ogrom informacji o budowie i składzie substancji. Zrozumienie ich jest absolutnie fundamentalne dla każdego, kto chce zgłębiać tajniki tej fascynującej dziedziny. Niezależnie od tego, czy jesteś uczniem przygotowującym się do matury, czy po prostu ciekawym świata entuzjastą, ten przewodnik pomoże Ci rozszyfrować chemiczne kody i zbudować solidne podstawy wiedzy chemicznej, niezbędne do dalszego rozwoju i osiągnięcia sukcesu.
Rodzaje Wzorów Chemicznych: Podstawy
W świecie chemii spotykamy się z różnymi sposobami przedstawiania składu i struktury związków. Kluczowe są trzy główne typy wzorów chemicznych, z których każdy dostarcza innych, specyficznych informacji o danej substancji. Poznanie ich różnic jest pierwszym krokiem do pełnego zrozumienia języka chemii.
Wzór empiryczny, nazywany również wzorem najprostszym, informuje nas o najprostszym stosunku liczby atomów poszczególnych pierwiastków w związku. Pokazuje, jakie atomy wchodzą w skład substancji i w jakich proporcjach się łączą, ale niekoniecznie odzwierciedla rzeczywistą liczbę atomów w cząsteczce. Jest to często pierwszy wzór, jaki można ustalić dla nieznanej substancji na podstawie analizy elementarnej. Na przykład, wzór empiryczny glukozy (C6H12O6) to CH2O, ponieważ wszystkie indeksy można podzielić przez 6. Podobnie dla etynu (C2H2) wzór empiryczny to CH.
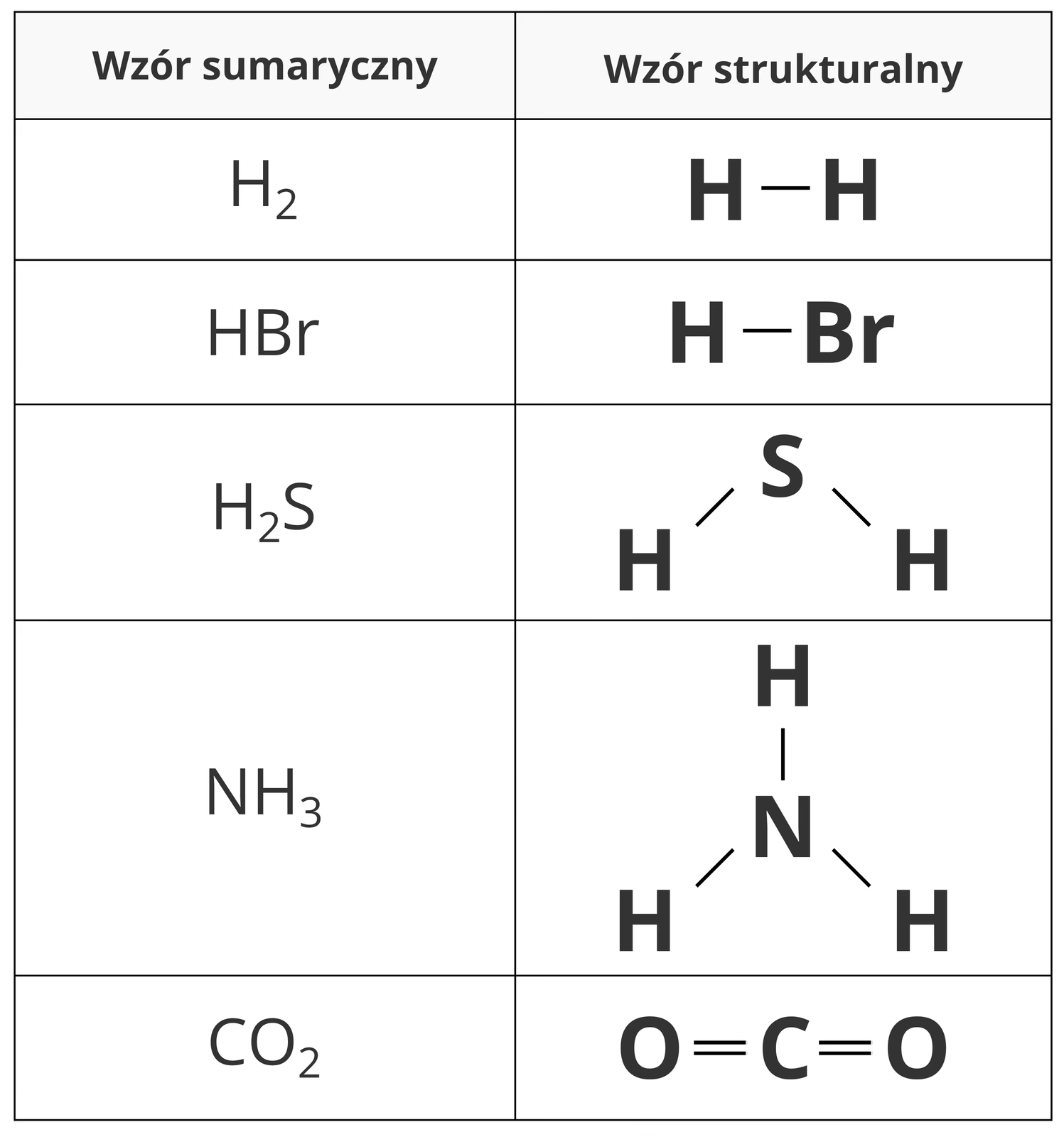
Wzór sumaryczny, inaczej wzór cząsteczkowy, to najbardziej powszechny typ wzoru, z którym będziesz miał do czynienia na co dzień. Pokazuje on dokładną liczbę atomów każdego pierwiastka w jednej cząsteczce związku chemicznego. Dla związków kowalencyjnych, które tworzą dyskretne cząsteczki, wzór sumaryczny precyzyjnie opisuje skład ich cząsteczki. Natomiast dla związków jonowych, które nie tworzą cząsteczek, a raczej uporządkowane sieci krystaliczne, wzór sumaryczny przedstawia najmniejszy zbiór tworzących ją jonów, zachowujący neutralność elektryczną. Przykłady to H2O dla wody, CO2 dla dwutlenku węgla czy NH3 dla amoniaku. Wzór sumaryczny pozwala nam określić masę cząsteczkową substancji, co jest kluczowe w obliczeniach stechiometrycznych.
Wzór strukturalny idzie o krok dalej, dostarczając najbardziej szczegółowych informacji. Oprócz informacji o rodzaju i liczbie atomów, przedstawia również sposób ich połączenia w przestrzeni, czyli ich wzajemne ułożenie oraz rodzaj wiązań chemicznych między nimi. Może to być wzór kreskowy, gdzie wiązania chemiczne symbolizują kreski (np. H-O-H dla wody), lub bardziej zaawansowane modele przestrzenne, pokazujące trójwymiarową orientację atomów. Wzory strukturalne są niezwykle ważne w chemii organicznej, gdzie wiele związków ma ten sam wzór sumaryczny, ale różną strukturę (tzw. izomeria), co wpływa na ich właściwości fizyczne i chemiczne.
Poniższa tabela przedstawia podstawowe różnice między tymi wzorami, ułatwiając ich zrozumienie:
| Typ Wzoru | Informacje | Przykład dla Glukozy (C6H12O6) |
|---|---|---|
| Empiryczny | Najprostszy stosunek liczbowy atomów pierwiastków. | CH2O |
| Sumaryczny | Dokładna liczba atomów każdego pierwiastka w cząsteczce. | C6H12O6 |
| Strukturalny | Rodzaj, liczba atomów oraz sposób ich połączenia (wiązania, układ przestrzenny). | Szczegółowe przedstawienie atomów węgla, wodoru i tlenu oraz wiązań między nimi, w tym grup -OH i -CHO/-C=O. |
Sekrety Języka Chemii: Jak Odczytywać Wzory?
Język chemiczny, choć nieużywany w codziennej komunikacji, jest językiem międzynarodowym. Niezależnie od miejsca na kuli ziemskiej, chemicy posługują się tymi samymi znakami i symbolami, aby wyrażać ilości i rodzaje substancji. Rozkodowanie tych zapisów nie jest trudne, o ile zapamięta się kilka ważnych reguł. Już wiesz, że związki chemiczne to substancje złożone z co najmniej dwóch pierwiastków chemicznych połączonych trwale ze sobą. Pamiętaj też, że istnieją związki kowalencyjne zbudowane z cząsteczek i związki jonowe zbudowane z jonów. Zrozumienie, jak interpretować te zapisy, jest kluczowe do nauki chemii.
Indeks Stechiometryczny: Skład Cząsteczki
Wzór chemiczny związku kowalencyjnego opisuje budowę jego cząsteczek. Użyte we wzorach symbole pierwiastków informują o rodzaju atomów tworzących cząsteczkę, a cyfry umieszczone z prawej strony u dołu symbolu informują o ich liczbie. Te cyfry, za pomocą których wyrażamy liczbę atomów w cząsteczce, nazywają się indeksami stechiometrycznymi. Są one także nazywane indeksami dolnymi. Umieszcza się je we wzorze zawsze za symbolem pierwiastka, do którego atomów się odnoszą. Jeśli indeks stechiometryczny jest równy jedności, cyfry „1” nie wstawiamy – jest ona domyślna. Na przykład, symbol Cl oznacza jeden atom chloru, a nie Cl1.
Przykład: Wzór chemiczny wody to H2O. Indeks stechiometryczny dla wodoru wynosi 2, a dla tlenu – 1 (pomijany, ponieważ jest jednością). Na tej podstawie możemy powiedzieć, że cząsteczka wody składa się z dwóch atomów wodoru i jednego atomu tlenu. Jest to fundamentalna informacja o składzie cząsteczki.
Inny przykład to wzór NH3 – wzór amoniaku. Cząsteczki amoniaku są zbudowane z jednego atomu azotu (indeks 1, pominięty) i trzech atomów wodoru (indeks 3). Ta prosta zasada pozwala nam natychmiastowo określić skład jakościowy (jakie pierwiastki) i ilościowy (ile atomów każdego pierwiastka) każdej cząsteczki opisanej wzorem sumarycznym.
Bez znajomości dokładnej budowy i nazwy substancji kowalencyjnej, a tylko na podstawie wzoru sumarycznego, można określić skład jej cząsteczki (rodzaj tworzących ją atomów i ich liczbę). Na przykład ze wzoru H2SO4 (kwas siarkowy(VI)) możemy wywnioskować, że cząsteczka związku opisanego tym wzorem składa się z dwóch atomów wodoru, jednego atomu siarki i czterech atomów tlenu. Podobnie wzór H3PO4 (kwas fosforowy(V)) mówi nam, że cząsteczka substancji o tym wzorze zbudowana jest z trzech atomów wodoru, jednego atomu fosforu i czterech atomów tlenu. Ta umiejętność jest niezwykle przydatna w wielu obliczeniach chemicznych.
Współczynnik Stechiometryczny: Liczba Cząsteczek
W sytuacji, gdy chcemy przedstawić zbiór składający się z więcej niż jednej cząsteczki, np. z trzech cząsteczek wody, to liczbę tych cząsteczek umieszczamy przed wzorem związku. Trzy cząsteczki wody (H2O, H2O, H2O) opiszemy jako 3H2O. Liczbę umieszczoną przed wzorem związku nazywa się współczynnikiem stechiometrycznym. Współczynnik ten odnosi się do całego wzoru, który następuje po nim, i wskazuje, ile takich jednostek (cząsteczek lub jednostek formalnych) występuje w danym zbiorze.
Spróbujmy określić liczbę poszczególnych atomów pierwiastków w zbiorze trzech cząsteczek wody: 3H2O. Jedna cząsteczka H2O zawiera dwa atomy wodoru i jeden atom tlenu. Zatem w trzech cząsteczkach znajduje się razem (3 · 2 = 6) sześć atomów wodoru i (3 · 1 = 3) trzy atomy tlenu. Jest to proste mnożenie, które pozwala na szybkie zsumowanie liczby atomów w większych zbiorach.
Inny przykład to pięć cząsteczek amoniaku, 5NH3. Oznacza to łącznie (5 · 1 = 5) pięć atomów azotu i (5 · 3 = 15) piętnaście atomów wodoru. Ta zasada jest fundamentalna przy bilansowaniu równań chemicznych, gdzie współczynniki stechiometryczne są używane do zachowania zasady zachowania masy.
Poniższa tabela ilustruje interpretację zapisu zbiorów przykładowych cząsteczek, pokazując, jak współczynniki wpływają na całkowitą liczbę atomów:
| Zapis Symboliczny | Opis Słowny Zbioru | Liczba Atomów N | Liczba Atomów H | Liczba Atomów O | Liczba Atomów Cl | Liczba Atomów C | Liczba Wszystkich Atomów |
|---|---|---|---|---|---|---|---|
| 4NH3 | cztery cząsteczki amoniaku | 4 | 12 | - | - | - | 16 |
| 2HCl | dwie cząsteczki chlorowodoru | - | 2 | - | 2 | - | 4 |
| 100CO2 | sto cząsteczek dwutlenku węgla | - | - | 200 | - | 100 | 300 |
| 106O2 | milion cząsteczek tlenu | - | - | 2 · 106 | - | - | 2 · 106 |
| 1024N2 | kwadrylion cząsteczek azotu | 2 · 1024 | - | - | - | - | 2 · 1024 |
Warto pamiętać o istotnej różnicy: indeks stechiometryczny opisuje, ile atomów poszczególnych pierwiastków tworzy cząstkę (jest częścią wzoru cząsteczki), natomiast współczynnik stechiometryczny mówi o liczbie całych cząstek (jest przed wzorem). Ta fundamentalna różnica jest kluczowa dla poprawnej interpretacji zapisów chemicznych.
Należy również wspomnieć, że niektóre niemetale (np. azot, tlen, fluor, chlor, brom, jod, siarka i fosfor) występują w przyrodzie w stanie wolnym w postaci cząsteczek, a nie pojedynczych atomów. Na przykład atomy tlenu tworzą przede wszystkim cząsteczki dwuatomowe O2 (tlen atmosferyczny, składnik powietrza) oraz cząsteczki trójatomowe O3 (ozon, obecny w powietrzu w trakcie wyładowań atmosferycznych i w warstwie ozonowej). Indeks stechiometryczny przy symbolu pierwiastka równy liczbie 3 wskazuje, że cząsteczki ozonu są zbudowane z trzech atomów tlenu. Współczynnik stechiometryczny zapisany przed symbolem (np. 6Cl – 6 atomów chloru) lub wzorem (np. 6Cl2 – 6 cząsteczek chloru) informuje o liczbie atomów lub cząsteczek. Zapis 6Cl wskazuje na 6 wolnych, niezwiązanych atomów chloru, natomiast 6Cl2 – na obecność 6 dwuatomowych cząsteczek chloru, czyli łącznie 12 atomów.
Wzory Związków Jonowych: Inna Perspektywa
Związki jonowe powstają z połączenia metali z niemetalami, lub też zawierają jony wieloatomowe. Związki te nie tworzą dyskretnych cząsteczek w tradycyjnym rozumieniu. Zamiast tego, są zbudowane z jonów (kationów i anionów), które ułożone są naprzemiennie w ściśle uporządkowane struktury zwane sieciami krystalicznymi. W krysztale nie występują izolowane grupy atomów, które można byłoby nazwać cząsteczkami, lecz raczej niekończąca się powtarzalna struktura jonów. Wzór sumaryczny związku jonowego przedstawia zatem najmniejszy zbiór powtarzających się jonów w krysztale (tzw. jednostkę formalną), który jest elektrycznie obojętny. Indeksy stechiometryczne w tym przypadku określają stosunek liczbowy jonów danego pierwiastka w tej jednostce.
W związkach jonowych składających się z dwóch pierwiastków, metal jest zawsze kationem (jonem dodatnim, np. Na+, Mg2+, Al3+), a niemetal – anionem (jonem ujemnym, np. Cl-, S2-). Przykładem takiego związku jest chlorek sodu, czyli popularna sól kuchenna. Jego wzór, NaCl, informuje, że kryształ chlorku sodu jest zbudowany z kationów sodu (Na+) i anionów chlorkowych (Cl-), a ich stosunek ilościowy wynosi 1:1. Indeksy "1" są pominięte, ale rozumie się, że na każdy jon sodu przypada jeden jon chlorkowy.
Inna substancja jonowa, chlorek glinu, o wzorze AlCl3, jest zbudowana z kationów glinu (Al3+) i anionów chlorkowych (Cl-). W tym związku najmniejszy zbiór powtarzających się jonów tworzą jeden jon glinu (kation) i trzy jony chlorkowe (aniony), co jest konieczne do zachowania neutralności elektrycznej (ładunek +3 od glinu jest równoważony przez trzy ładunki -1 od chloru).
W krysztale kolejnej substancji jonowej, siarczku potasu, o wzorze K2S, na jeden anion siarczkowy (S2-) przypadają dwa kationy potasu (K+). Ponownie, bilans ładunków (+1 od każdego K+, czyli +2 łącznie, równoważy -2 od S2-) decyduje o stosunku stechiometrycznym.
Podobnie jak w przypadku cząsteczek, liczby umieszczone przed wzorem związku jonowego (współczynniki stechiometryczne) określają liczbę najmniejszych zbiorów tworzących kryształ. Na przykład zapis 10NaCl oznacza dziesięć zbiorów składających się z jednego kationu sodu (Na+) i jednego anionu chlorkowego (Cl-). Oznacza to, że mamy do czynienia z 10 jonami Na+ i 10 jonami Cl-. Jest to używane do określania ilości substancji w reakcjach chemicznych, nawet jeśli substancja nie występuje w formie cząsteczek.
Interpretacja zapisów chemicznych dotyczących związków jonowych wymaga zrozumienia roli jonów i ich ładunków:
| Zapis Symboliczny | Liczba Kationów Al3+ | Liczba Anionów Cl- | Liczba Kationów K+ | Liczba Kationów Mg2+ | Liczba Anionów S2- |
|---|---|---|---|---|---|
| 5AlCl3 | 5 | 15 | - | - | - |
| 7MgCl2 | - | 14 | - | 7 | - |
| 1024K2S | - | - | 2 · 1024 | - | 1 · 1024 |
Złożone Wzory i Nawiasy: Klucz do Rozszyfrowania
W niektórych wzorach chemicznych, zwłaszcza tych dotyczących związków z jonami wieloatomowymi (np. grupy hydroksylowej OH-, siarczanowej SO42- czy fosforanowej PO43-), grupy atomów zapisuje się w nawiasie, po którym występuje liczba. Ta liczba, będąca indeksem stechiometrycznym dla całej grupy, odnosi się do wszystkich atomów znajdujących się w nawiasie. Przykładem jest wzór Ca3(PO4)2, który opisuje fosforan(V) wapnia – składnik kości i zębów.
W zaprezentowanym zbiorze liczba 2 poza nawiasem odnosi się do całej grupy fosforanowej (PO4). Aby dokładnie pokazać, jak należałoby ilościowo rozumieć zastosowany zapis, rozpiszmy ten wzór krok po kroku:
- Symbol Ca3 informuje nas o obecności trzech atomów wapnia.
- Grupa (PO4)2 oznacza, że cała grupa fosforanowa (składająca się z jednego atomu fosforu i czterech atomów tlenu) występuje dwukrotnie.
Zatem wzór Ca3(PO4)2 możemy zinterpretować następująco: w zbiorze znajdują się trzy atomy wapnia (Ca), dwa atomy fosforu (ponieważ 1 atom P w grupie PO4 pomnożony przez indeks 2 daje 2 · 1 = 2 atomy P) i osiem atomów tlenu (ponieważ 4 atomy O w grupie PO4 pomnożone przez indeks 2 dają 2 · 4 = 8 atomów O). To podejście jest kluczowe dla poprawnego obliczania mas cząsteczkowych i składu procentowego złożonych związków.
Jeśli przed takim wzorem pojawi się współczynnik stechiometryczny, mnożymy przez niego wszystkie atomy w formule, włączając w to atomy w nawiasach. Na przykład w zbiorze opisanym wzorem 2Ca3(PO4)2 mamy:
- (2 · 3 = 6) sześć atomów wapnia,
- (2 · 2 = 4) cztery atomy fosforu,
- (2 · 2 · 4 = 16) szesnaście atomów tlenu.
Jest to kompleksowe podejście do interpretacji, które pozwala na precyzyjne określenie liczby każdego typu atomu w dowolnym zbiorze cząsteczek lub jednostek formalnych.
Interpretacja przykładowych zapisów chemicznych z nawiasami i bez nich:
| Zapis Chemiczny | Al | Ca | H | Mg | N | O | P | S | Wszystkich Atomów |
|---|---|---|---|---|---|---|---|---|---|
| Al2S3 | 2 | - | - | - | - | - | - | 3 | 5 |
| 3Al2S3 | 6 | - | - | - | - | - | - | 9 | 15 |
| Ca(OH)2 | - | 1 | 2 | - | - | 2 | - | - | 5 |
| 4HNO3 | - | - | 4 | - | 4 | 12 | - | - | 20 |
| 2H3PO4 | - | - | 6 | - | - | 8 | 2 | - | 16 |
| 2Mg(OH)2 | - | - | 4 | 2 | - | 4 | - | - | 10 |
Matura z Chemii: Wzory w Praktyce
Podczas egzaminu maturalnego z chemii, umiejętność odczytywania i interpretowania wzorów chemicznych jest absolutnie kluczowa i często decyduje o sukcesie. Będziesz korzystać zarówno z tablic maturalnych, jak i wzorów i stałych chemicznych udostępnianych przez Centralną Komisję Egzaminacyjną (CKE). Już teraz pobierz i zapoznaj się z nimi – są to narzędzia, które musisz opanować do perfekcji. Z pewnością przydadzą Ci się zarówno podczas rozwiązywania zadań maturalnych z chemii, które często wymagają precyzyjnego odczytu i interpretacji wzorów, jak i w trakcie kursu przygotowującego do matury, gdzie będziesz doskonalić te umiejętności.

Zrozumienie, czym jest indeks stechiometryczny, a czym współczynnik stechiometryczny, pozwoli Ci poprawnie bilansować równania reakcji chemicznych (np. reakcje spalania, reakcje redoks), obliczać masy molowe poszczególnych związków, a także przewidywać produkty reakcji i określać ich proporcje. Pamiętaj, że matura często wymaga nie tylko znajomości teorii, ale także praktycznego zastosowania wiedzy do konkretnych problemów chemicznych, takich jak obliczenia stechiometryczne, ustalanie wzorów związków na podstawie danych eksperymentalnych czy interpretacja równań reakcji. Regularne ćwiczenie odczytywania i interpretowania wzorów z różnorodnych związków chemicznych, zarówno prostych, jak i złożonych, jest najlepszą drogą do sukcesu i osiągnięcia wysokiego wyniku na egzaminie.
Najczęściej Zadawane Pytania (FAQ)
Czym jest wzór empiryczny, a czym sumaryczny?
Wzór empiryczny (nazywany również wzorem najprostszym) przedstawia najprostszy stosunek liczbowy atomów pierwiastków w związku, np. CH2O dla glukozy. Wzór sumaryczny (cząsteczkowy) podaje dokładną liczbę atomów każdego pierwiastka w cząsteczce, np. C6H12O6 dla glukozy. Wzór sumaryczny zawsze jest wielokrotnością wzoru empirycznego.
Jaka jest różnica między indeksem a współczynnikiem stechiometrycznym?
Indeks stechiometryczny to mała cyfra zapisana u dołu po prawej stronie symbolu pierwiastka we wzorze (np. H2O) i oznacza liczbę atomów danego pierwiastka w jednej cząsteczce lub jednostce formalnej. Współczynnik stechiometryczny to duża cyfra zapisana przed całym wzorem (np. 3H2O) i oznacza liczbę całych cząsteczek lub jednostek formalnych, które bierzemy pod uwagę.
Dlaczego związki jonowe nie mają cząsteczek?
Związki jonowe tworzą uporządkowane struktury krystaliczne, w których kationy i aniony są ułożone naprzemiennie w sieci przestrzennej, tworząc niekończącą się, powtarzalną strukturę. Nie ma w nich pojedynczych, izolowanych grup atomów, które można by nazwać cząsteczkami. Wzór sumaryczny związku jonowego, np. NaCl, opisuje jedynie najmniejszy, elektrycznie obojętny zbiór powtarzających się jonów w tej sieci krystalicznej, czyli jednostkę formalną.
Jak odróżnić związek kowalencyjny od jonowego na podstawie wzoru?
Związki kowalencyjne zazwyczaj składają się z dwóch lub więcej niemetali (np. CO2, H2O, NH3, CCl4). Związki jonowe powstają z połączenia metalu z niemetalem (np. NaCl, MgCl2, K2S) lub zawierają jony wieloatomowe, które są zazwyczaj zbudowane z niemetali, ale posiadają ładunek (np. Ca(OH)2, Na2SO4, NH4Cl).
Podsumowanie
Język chemii, oparty na wzorach chemicznych, jest uniwersalnym narzędziem do opisu materii. Za pomocą wzorów chemicznych można przedstawiać określoną liczbę cząsteczek, atomów i jonów, a także ich wzajemne proporcje i sposób połączenia. Zrozumienie poszczególnych elementów wzoru jest kluczowe dla każdego, kto chce zgłębiać tę fascynującą naukę.
Liczbę atomów w cząsteczce bądź jonów w jednostce formalnej przedstawia się przy użyciu indeksu stechiometrycznego. We wzorze substancji liczbę tę zapisuje się z prawej strony u dołu symbolu pierwiastka. Jest to informacja o składzie wewnętrznym pojedynczej jednostki.
Liczbę atomów, cząsteczek bądź jednostek formalnych związku jonowego określa się, wykorzystując współczynnik stechiometryczny – liczbę zapisywaną przed wzorem sumarycznym związku. Jest to informacja o ilości (liczbie) tych jednostek w danym zbiorze.
Zrozumienie tych podstawowych zasad, a także różnic między wzorami empirycznymi, sumarycznymi i strukturalnymi, jest fundamentem do dalszej nauki chemii i kluczem do sukcesu na egzaminie maturalnym. Dzięki tej wiedzy będziesz w stanie z łatwością interpretować zapisy chemiczne i rozwiązywać nawet najbardziej złożone zadania.
Słowniczek
indeks stechiometryczny – liczba umieszczana u dołu z prawej strony symbolu pierwiastka we wzorze chemicznym substancji; jest ona równa liczbie atomów tego pierwiastka w cząsteczce lub w najmniejszym zbiorze powtarzających się jonów w krysztale (tzw. jednostce formalnej).
współczynnik stechiometryczny – liczba zapisywana przed symbolem lub wzorem chemicznym, która określa liczbę atomów, cząsteczek lub najmniejszych zbiorów powtarzających się jonów w krysztale.
Zainteresował Cię artykuł Wzory Chemiczne: Klucz do Zrozumienia Świata", "kategoria": "Chemia? Zajrzyj też do kategorii Edukacja, znajdziesz tam więcej podobnych treści!
