05/09/2014
Sole to niezwykle ważna i wszechobecna grupa związków chemicznych. Odgrywają kluczową rolę w naszym codziennym życiu, przemyśle, a nawet w funkcjonowaniu organizmów biologicznych. Chociaż najczęściej kojarzą nam się z popularną solą kuchenną (chlorkiem sodu), świat soli jest znacznie bardziej złożony i różnorodny. Są to substancje jonowe, których kryształy zawierają naprzemiennie ułożone kationy metalu (lub kationu amonu) i aniony reszty kwasowej. Ich obecność w roztworach wodnych sprawia, że roztwory te doskonale przewodzą prąd elektryczny, co czyni sole ważnymi elektrolitami. W tym artykule przyjrzymy się bliżej ich budowie, nazewnictwu, sposobom otrzymywania, różnym typom oraz szerokim zastosowaniom.
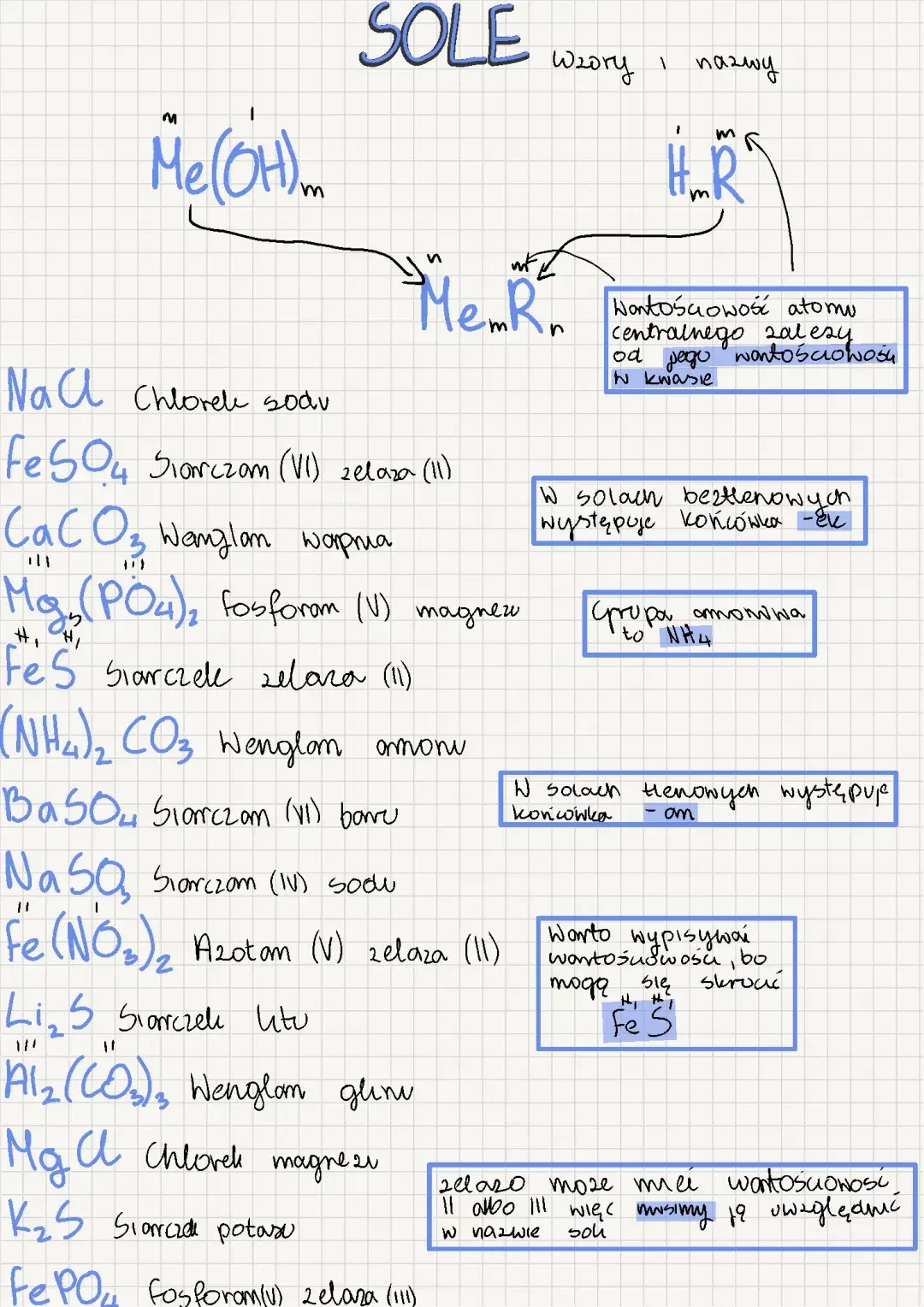
Budowa Soli: Fundament Związków Jonowych
Sole są związkami jonowymi, co oznacza, że składają się z jonów połączonych wiązaniami elektrostatycznymi. Ich podstawową strukturę tworzą kationy metali (lub wyjątkowo kation amonu, NH4+) oraz aniony reszt kwasowych. Ogólny wzór soli można przedstawić jako:
MemRn
gdzie:
Me– symbol metalu, którego kation wchodzi w skład soli,R– symbol reszty kwasowej, której anion współuczestniczy w tworzeniu soli,n,m– indeksy stechiometryczne, które są ustalane na podstawie wartościowości metalu i reszty kwasowej. Odzwierciedlają one proporcje, w jakich kationy i aniony łączą się, aby związek był elektrycznie obojętny.
Poniższa tabela przedstawia przykładowe wzory sumaryczne soli, zbudowanych z różnych kationów i anionów:
| Rodzaj kationu | Rodzaj anionu | Wzór sumaryczny soli |
|---|---|---|
| Na+ | Cl- | NaCl |
| Ca2+ | Cl- | CaCl2 |
| Al3+ | Cl- | AlCl3 |
| Na+ | SO42- | Na2SO4 |
| Ca2+ | SO42- | CaSO4 |
| Al3+ | SO42- | Al2(SO4)3 |
| Na+ | PO43- | Na3PO4 |
| Ca2+ | PO43- | Ca3(PO4)2 |
| Al3+ | PO43- | AlPO4 |
Nazewnictwo Soli: Klucz do Zrozumienia
Nazwy soli składają się z dwóch członów. Pierwszy człon odnosi się do rodzaju reszty kwasowej, a drugi do metalu. Ważne jest rozróżnienie kwasów tlenowych i beztlenowych, ponieważ od tego zależy końcówka pierwszego członu nazwy soli:
- W przypadku soli kwasów tlenowych, pierwszy człon nazwy przyjmuje końcówkę -an (np. siarczan, azotan, fosforan).
- Dla soli kwasów beztlenowych, pierwszy człon nazwy otrzymuje końcówkę -ek (np. chlorek, siarczek).
Jeśli metal tworzy jony o różnych wartościowościach, jego wartościowość jest podawana w nawiasie rzymską cyfrą (np. chlorek żelaza(II), siarczan(VI) miedzi(II)).
| Rodzaj kwasu | Wzór sumaryczny kwasu | Nazwa kwasu | Jon reszty kwasowej | Pierwszy człon nazwy soli |
|---|---|---|---|---|
| Kwas tlenowy | H2SO4 | Kwas siarkowy(VI) | SO42- | Siarczan(VI) |
| Kwas tlenowy | H2SO3 | Kwas siarkowy(IV) | SO32- | Siarczan(IV) |
| Kwas tlenowy | H2CO3 | Kwas węglowy | CO32- | Węglan |
| Kwas tlenowy | HNO3 | Kwas azotowy(V) | NO3- | Azotan(V) |
| Kwas tlenowy | H3PO4 | Kwas fosforowy(V) | PO43- | Fosforan(V) |
| Kwas beztlenowy | HCl | Kwas chlorowodorowy | Cl- | Chlorek |
| Kwas beztlenowy | H2S | Kwas siarkowodorowy | S2- | Siarczek |
Dysocjacja Elektrolityczna Soli: Dlaczego Przewodzą Prąd?
Sole rozpuszczalne w wodzie są elektrolitami. Oznacza to, że w roztworach wodnych ulegają dysocjacji, czyli rozpadowi na jony, z których są zbudowane. Te swobodnie poruszające się jony – kationy metali i aniony reszt kwasowych – są odpowiedzialne za przewodzenie prądu elektrycznego przez wodne roztwory soli. Proces dysocjacji jest kluczowy dla wielu reakcji chemicznych zachodzących w roztworach.
Poniżej przedstawiono równania reakcji opisujących proces dysocjacji przykładowych soli:
| Nazwa soli | Wzór sumaryczny soli | Równanie dysocjacji soli |
|---|---|---|
| Chlorek sodu | NaCl | NaCl →H2O Na+ + Cl- |
| Azotan(V) potasu | KNO3 | KNO3 →H2O K+ + NO3- |
| Siarczan(VI) miedzi(II) | CuSO4 | CuSO4 →H2O Cu2+ + SO42- |
| Fosforan(V) potasu | K3PO4 | K3PO4 →H2O 3K+ + PO43- |
| Azotan(V) ołowiu(II) | Pb(NO3)2 | Pb(NO3)2 →H2O Pb2+ + 2NO3- |
| Siarczan(VI) żelaza(III) | Fe2(SO4)3 | Fe2(SO4)3 →H2O 2Fe3+ + 3SO42- |
Metody Otrzymywania Soli: Od Laboratorium do Przemysłu
Sole można otrzymać na wiele sposobów, nie zawsze wymagają one bezpośredniej reakcji kwasu z zasadą. Poniżej przedstawiono najczęściej spotykane metody:
1. Reakcja Zobojętniania: Kwas + Zasada
Jedną z najbardziej podstawowych metod otrzymywania soli jest reakcja zobojętniania, czyli reakcja kwasu z zasadą. Istotą tej przemiany jest połączenie anionów wodorotlenkowych (OH-) z kationami wodoru (H+), w wyniku czego powstają obojętne cząsteczki wody. Skrócony zapis jonowy tej przemiany to:
OH- + H+ → H2O
W wyniku reakcji zobojętniania zawsze powstaje sól i woda. Przykłady:
- NaOH + HCl → NaCl + H2O
(Wodorotlenek sodu + Kwas solny → Chlorek sodu + Woda) - KOH + HCl → KCl + H2O
(Wodorotlenek potasu + Kwas solny → Chlorek potasu + Woda) - Ca(OH)2 + 2HCl → CaCl2 + 2H2O
(Wodorotlenek wapnia + Kwas solny → Chlorek wapnia + Woda) - 2NaOH + H2SO3 → Na2SO3 + 2H2O
(Wodorotlenek sodu + Kwas siarkowy(IV) → Siarczan(IV) sodu + Woda) - Mg(OH)2 + 2HNO3 → Mg(NO3)2 + 2H2O
(Wodorotlenek magnezu + Kwas azotowy(V) → Azotan(V) magnezu + Woda)
2. Reakcje Tlenków z Kwasami i Zasadami
Sole mogą powstawać również w reakcjach tlenków metali z kwasami lub tlenków niemetali z zasadami. Podobnie jak w reakcji zobojętniania, produktami są sól i woda.
Przykłady reakcji tlenków metali z kwasami:
- CaO + 2HCl → CaCl2 + H2O
(Tlenek wapnia + Kwas solny → Chlorek wapnia + Woda) - CaO + 2HNO3 → Ca(NO3)2 + H2O
(Tlenek wapnia + Kwas azotowy(V) → Azotan(V) wapnia + Woda) - MgO + 2HNO3 → Mg(NO3)2 + H2O
(Tlenek magnezu + Kwas azotowy(V) → Azotan(V) magnezu + Woda) - CuO + H2SO4 → CuSO4 + H2O
(Tlenek miedzi(II) + Kwas siarkowy(VI) → Siarczan(VI) miedzi(II) + Woda) - Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O
(Tlenek żelaza(III) + Kwas siarkowy(VI) → Siarczan(VI) żelaza(III) + Woda) - Li2O + 2HCl → 2LiCl + H2O
(Tlenek litu + Kwas solny → Chlorek litu + Woda)
Przykłady reakcji tlenków niemetali z zasadami:
- CO2 + Ca(OH)2 → CaCO3↓ + H2O
(Tlenek węgla(IV) + Wodorotlenek wapnia → Węglan wapnia + Woda) - SO2 + 2KOH → K2SO3 + H2O
(Tlenek siarki(IV) + Wodorotlenek potasu → Siarczan(IV) potasu + Woda) - SO3 + Ba(OH)2 → BaSO4↓ + H2O
(Tlenek siarki(VI) + Wodorotlenek baru → Siarczan(VI) baru + Woda) - P4O10 + 12KOH → 4K3PO4 + 6H2O
(Tlenek fosforu(V) + Wodorotlenek potasu → Fosforan(V) potasu + Woda)
3. Reakcja Kwasów z Metalami
Niektóre metale reagują z kwasami, wypierając z nich wodór i tworząc sól. Możliwość zajścia takiej reakcji zależy od aktywności metalu w szeregu aktywności metali. Metale położone w szeregu aktywności przed wodorem są w stanie wyprzeć wodór z kwasów (np. magnez, cynk, żelazo). Metale znajdujące się po wodorze (np. miedź, srebro, złoto) nie reagują w ten sposób z kwasami nieutleniającymi.
Przykłady reakcji metali z kwasem solnym:
- Mg + 2HCl → MgCl2 + H2↑
(Magnez + Kwas solny → Chlorek magnezu + Wodór) - Zn + 2HCl → ZnCl2 + H2↑
(Cynk + Kwas solny → Chlorek cynku + Wodór) - Fe + 2HCl → FeCl2 + H2↑
(Żelazo + Kwas solny → Chlorek żelaza(II) + Wodór) - 2Na + 2HCl → 2NaCl + H2↑
(Sód + Kwas solny → Chlorek sodu + Wodór) - 2Al + 6HCl → 2AlCl3 + 3H2↑
(Glin + Kwas solny → Chlorek glinu + Wodór)
Przykłady reakcji metali z kwasem siarkowym(VI):
- Mg + H2SO4 → MgSO4 + H2↑
(Magnez + Kwas siarkowy(VI) → Siarczan(VI) magnezu + Wodór) - Zn + H2SO4 → ZnSO4 + H2↑
(Cynk + Kwas siarkowy(VI) → Siarczan(VI) cynku + Wodór) - Fe + H2SO4 → FeSO4 + H2↑
(Żelazo + Kwas siarkowy(VI) → Siarczan(VI) żelaza(II) + Wodór)
4. Otrzymywanie Trudno Rozpuszczalnych Soli – Reakcja Strącania
Reakcja strącania (reakcja strąceniowa) to proces chemiczny zachodzący w roztworze wodnym, w którym jony pochodzące od zmieszanych ze sobą substancji tworzą trudno rozpuszczalny związek, wytrącający się z roztworu w postaci osadu. Tablice rozpuszczalności są nieocenionym narzędziem do przewidywania, czy po zmieszaniu dwóch roztworów substancji jonowych powstanie osad.
Przykłady reakcji strącania, w których powstają sole:
- Zapis cząsteczkowy: AgNO3 + NaCl → AgCl↓ + NaNO3
Zapis jonowy pełny: Ag+ + NO3- + Na+ + Cl- → AgCl↓ + Na+ + NO3-
Zapis jonowy skrócony: Ag+ + Cl- → AgCl↓ - Zapis cząsteczkowy: Na2SO4 + CaCl2 → CaSO4↓ + 2NaCl
Zapis jonowy pełny: 2Na+ + SO42- + Ca2+ + 2Cl- → CaSO4↓ + 2Na+ + 2Cl-
Zapis jonowy skrócony: Ca2+ + SO42- → CaSO4↓ - Zapis cząsteczkowy: BaCl2 + Na2SO4 → BaSO4↓ + 2NaCl
Zapis jonowy pełny: Ba2+ + 2Cl- + 2Na+ + SO42- → BaSO4↓ + 2Cl- + 2Na+
Zapis jonowy skrócony: Ba2+ + SO42- → BaSO4↓
Rodzaje Soli w Chemii: Klasyfikacje i Przykłady
Sole można klasyfikować na wiele sposobów, w zależności od ich pochodzenia, składu czy poziomu pH w roztworze wodnym. Oto główne kategorie:
1. Sole Proste (Normalne)
Powstają w wyniku całkowitej reakcji zobojętniania kwasu przez zasadę, nie zawierają wymiennych jonów wodorowych ani hydroksylowych. Mogą być:
- Sole kwaśne: Powstają w reakcji mocnego kwasu ze słabą zasadą lub gdy kwas wieloprotonowy nie został całkowicie zobojętniony. Ich pH jest poniżej 7. Przykłady: wodorowęglan sodu (NaHCO3), chlorek amonu (NH4Cl).
- Sole zasadowe: Powstają w reakcji słabego kwasu z mocną zasadą lub gdy zasada wielowodorotlenowa nie została całkowicie zobojętniona. Ich pH jest powyżej 7. Przykłady: octan sodu (CH3COONa), wodorotlenek chlorku cynku (Zn(OH)Cl).
- Sole obojętne: Powstają, gdy zarówno kwas, jak i zasada są mocne. Ich pH jest bliskie 7. Przykłady: chlorek sodu (NaCl), chloran(V) potasu (KClO3), azotan(V) sodu (NaNO3).
2. Sole Podwójne
Powstają w wyniku krystalizacji dwóch prostych soli w tej samej sieci jonowej. Zawierają więcej niż jeden rodzaj kationu lub anionu. Przykłady: fluorek potasowo-cerowy (KCeF4), sól Mohra ((NH4)2Fe(SO4)2·6H2O).

3. Sole Kompleksowe (Złożone)
To połączenie związków molekularnych i jonów, co oznacza, że posiadają zarówno naładowane jony, jak i neutralne cząsteczki. Centralny metal jest otoczony jonami i neutralnymi cząsteczkami, tworząc kompleks. Przykłady: siarczan tetraaminomiedzi(II) ([Cu(NH3)4]SO4), chlorek heksaaminochromu(III) ([Cr(NH3)6]Cl3).
4. Sole Mieszane
Składają się z dwóch anionów, które dzielą kation, lub odwrotnie. Powstają w wyniku reakcji więcej niż jednego kwasu lub zasady. Przykład: proszek wybielający (Ca(ClO)2), siarczan sodowo-potasowy (NaKSO4).
Właściwości Soli: Różnorodność w Smaku, Kolorze i Nie Tylko
Sole wykazują szeroki zakres właściwości, które są determinowane przez ich skład chemiczny i strukturę krystaliczną. Należą do nich:
- Smak: Chociaż wiele soli ma charakterystyczny „słony” smak (jak NaCl), inne mogą smakować zupełnie inaczej. Octan ołowiu(II) jest słodki (lecz trujący), siarczan magnezu ma smak gorzki, a wodorowinian potasu jest kwaśny. Glutaminian sodu ma smak umami, wzmacniający smaki innych składników żywności.
- Kolor: Wiele soli jest przezroczystych lub półprzezroczystych, ale niektóre są nieprzezroczyste. Kolor soli zależy w dużej mierze od składu jonowego. Na przykład azotan kobaltu(II) jest czerwony ze względu na obecność uwodnionego kobaltu(II), a siarczan miedzi(II) jest niebieski.
- Zapach: Sole powstałe w reakcjach mocnych kwasów z mocnymi zasadami zazwyczaj nie mają zapachu. Jednak te, które powstają ze słabego kwasu i mocnej zasady lub odwrotnie, mogą mieć zapach. Najbardziej znanym przykładem są sole cyjankowe, które mają charakterystyczny zapach migdałowy.
- Rozpuszczalność: Ponieważ sole są związkami jonowymi, większość z nich jest dobrze rozpuszczalna w wodzie i innych rozpuszczalnikach polarnych. Istnieją jednak wyjątki, takie jak większość węglanów metali czy niektóre sole metali ciężkich.
- Przewodnictwo: Stopione sole i roztwory soli przewodzą prąd elektryczny ze względu na ich właściwości jonowe i polarne.
- Temperatura topnienia: Sole mają tendencję do wysokich temperatur topnienia ze względu na silne wiązania jonowe. Na przykład chlorek sodu topi się w temperaturze 801°C.
Praktyczne Zastosowania Soli: Niezbędne w Przemyśle i Codzienności
Zastosowania soli są niezwykle szerokie i zróżnicowane. Odgrywają one kluczową rolę w wielu dziedzinach:
- Chlorki (np. NaCl, KCl):
Najbardziej znany chlorek, chlorek sodu (sól kuchenna), jest używany do przyprawiania i konserwowania żywności, a także do posypywania dróg zimą, aby zapobiec zamarzaniu wody (obniża temperaturę krzepnięcia). Chlorek potasu (KCl) jest składnikiem nawozów sztucznych, przyspieszających wzrost roślin. Chlorki magnezu i potasu są często składnikami soli do kąpieli. Sól fizjologiczna (wodny roztwór NaCl) jest używana w medycynie do przemywania ran i wlewów dożylnych. - Węglany (np. Na2CO3, CaCO3, NaHCO3):
Węglan sodu (Na2CO3) jest składnikiem proszków do prania jako substancja zmiękczająca wodę. Węglan wapnia (CaCO3) ma zastosowanie w budownictwie (cement, wapno), przemyśle spożywczym i medycynie. Wodorowęglan sodu (NaHCO3), czyli soda oczyszczona, jest głównym składnikiem proszków do pieczenia i środkiem regulującym pH w produktach spożywczych. - Azotany (np. KNO3, NaNO3, NH4NO3, AgNO3):
Azotany potasu, sodu i amonu są szeroko wykorzystywane do produkcji nawozów sztucznych, dostarczając roślinom niezbędnego azotu. Azotan(V) potasu i azotan(V) sodu są stosowane w produkcji materiałów wybuchowych. Azotan(V) potasu jest również używany do peklowania mięsa, zapobiegając jego psuciu i utrzymując naturalną barwę. Azotan(V) srebra (AgNO3) jest substancją czynną w lekach wspomagających gojenie skóry i leczenie zmian wirusowych, a także wykorzystuje się go do produkcji luster. - Siarczany(VI) (np. CaSO4, MgSO4, CuSO4):
Uwodniony siarczan(VI) wapnia (gips palony, 2CaSO4·H2O) jest stosowany do tworzenia zaprawy gipsowej w budownictwie i medycynie (opatrunki usztywniające). Siarczan(VI) magnezu (MgSO4) to główny składnik soli gorzkiej, stosowanej w medycynie jako środek przeczyszczający. Siarczan(VI) miedzi(II) (CuSO4) jest używany jako środek grzybobójczy do impregnacji drewna. - Fosforany(V) (np. Na3PO4, Cu3(PO4)2):
Fosforan sodu (Na3PO4) jest wykorzystywany do produkcji środków zmiękczających wodę i jest składnikiem nawozów sztucznych. Inne fosforany(V) są surowcami do produkcji nawozów sztucznych, stanowiąc źródło fosforu niezbędnego do wzrostu korzeni i pędów roślin.
Sole w Układach Biologicznych: Niezbędne dla Życia
Sole odgrywają kluczową rolę w systemach biologicznych. W organizmach, takich jak ludzki, sole pełnią funkcję elektrolitów, które umożliwiają przekazywanie sygnałów nerwowych z mózgu do mięśni i narządów oraz w drugą stronę. Sygnały nerwowe kontrolują zarówno ruchy dobrowolne, jak i mimowolne mięśni. Przekazują również informacje z narządów zmysłów (jak oczy i język) i regulują uwalnianie hormonów z układu hormonalnego. Sole pomagają również w utrzymaniu integralności komórkowej, kontrolując równowagę wody i składników odżywczych poprzez ciśnienie turgorowe.
Bezpieczeństwo i Aspekty Środowiskowe
Chociaż wiele soli jest niezbędnych dla życia i ma pozytywne zastosowania, ich nadmierne stężenie może stanowić zagrożenie dla środowiska. Na przykład, zbyt duża ilość chlorku sodu w słodkiej wodzie może uszkodzić zasoby wody pitnej. Wysokie stężenie soli w glebie może być szkodliwe dla roślin, ograniczając ich produktywność i wzrost.
Sole zawarte w nawozach sztucznych (np. chlorek potasu i siarczan potasu) również stwarzają zagrożenie dla środowiska. Spływ nawozów może zanieczyścić oceany i zwiększyć ryzyko eutrofizacji. Jest to błędne koło zakwitu glonów i nadprodukcji bakterii odżywiających się rozkładającymi się glonami. Proces ten wyczerpuje ilość rozpuszczonego tlenu w wodzie, co ostatecznie prowadzi do śmierci wielu organizmów morskich.
Często Zadawane Pytania (FAQ)
Co to są sole?
Sole to związki jonowe, składające się z kationów metalu (lub kationu amonu) i anionów reszt kwasowych. W roztworach wodnych dysocjują na jony, co sprawia, że przewodzą prąd elektryczny.

Jakie są główne rodzaje soli?
Główne rodzaje soli to sole proste (kwaśne, zasadowe, obojętne), sole podwójne, sole kompleksowe i sole mieszane. Klasyfikacja zależy od ich składu i sposobu powstawania.
Dlaczego sole przewodzą prąd elektryczny?
Sole przewodzą prąd elektryczny, gdy są w stanie stopionym lub rozpuszczone w wodzie, ponieważ w tych stanach ich jony są swobodne i mogą przemieszczać się, przenosząc ładunek elektryczny. Sole są więc elektrolitami.
Gdzie w życiu codziennym spotykamy sole?
Sole spotykamy w wielu miejscach: w soli kuchennej (NaCl), nawozach sztucznych, proszkach do prania, lekach, środkach do czyszczenia, a nawet w naszym organizmie jako elektrolity niezbędne do funkcjonowania układu nerwowego i mięśniowego.
Jakie są zagrożenia związane z solami?
Nadmierne stężenie soli w środowisku może prowadzić do zanieczyszczenia wody pitnej, uszkodzenia roślin w glebie oraz eutrofizacji zbiorników wodnych, co negatywnie wpływa na ekosystemy wodne.
Podsumowanie
Sole to fascynująca i niezwykle ważna grupa związków chemicznych o szerokim spektrum właściwości i zastosowań. Od prostego chlorku sodu po skomplikowane sole kompleksowe, ich rola w chemii, przemyśle, biologii i naszym codziennym życiu jest nie do przecenienia. Zrozumienie ich budowy, nazewnictwa, metod otrzymywania oraz różnorodnych właściwości pozwala lepiej docenić ich znaczenie i świadomie wykorzystywać ich potencjał, jednocześnie pamiętając o aspektach środowiskowych związanych z ich stosowaniem.
Zainteresował Cię artykuł Sole: Wzór, Budowa, Rodzaje i Zastosowania", "kategoria": "Chemia? Zajrzyj też do kategorii Edukacja, znajdziesz tam więcej podobnych treści!

