22/06/2019
Świat chemii jest pełen fascynujących procesów, które nieustannie zachodzą wokół nas, od złożonych reakcji w naszych ciałach po przemysłowe syntezy tworzące codzienne produkty. Wiele z tych reakcji ma charakter odwracalny, co oznacza, że mogą zachodzić w obu kierunkach – od substratów do produktów i z powrotem. W pewnym momencie, w odpowiednich warunkach, reakcje te osiągają stan, w którym wydaje się, że nic się nie zmienia. Ten pozornie statyczny stan nazywamy równowagą chemiczną. Ale co się dzieje, gdy warunki te zostają zmienione? Jak układ reaguje na takie zakłócenia? Odpowiedzi dostarcza nam jedna z fundamentalnych zasad chemii fizycznej: Reguła Le Chateliera, znana również jako reguła przekory. Zrozumienie tej zasady jest kluczowe nie tylko dla teoretyków, ale i dla praktyków, pozwalając na przewidywanie i manipulowanie przebiegiem reakcji chemicznych w przemyśle i laboratorium.

Równowaga Chemiczna: Dynamiczny Stan Stabilności
Zanim zagłębimy się w Regułę Le Chateliera, musimy dokładnie zrozumieć, czym jest równowaga chemiczna. Wbrew intuicyjnemu skojarzeniu ze „spoczynkiem”, równowaga chemiczna to stan, w którym reakcja chemiczna zachodzi z jednakową szybkością w obu kierunkach – reakcji prostej (od substratów do produktów) i reakcji odwrotnej (od produktów do substratów). Oznacza to, że stężenia wszystkich reagentów – zarówno substratów, jak i produktów – pozostają stałe w czasie. Nie zmieniają się, ponieważ w każdej chwili tyle samo cząsteczek substratów przekształca się w produkty, ile cząsteczek produktów wraca do formy substratów. Jest to zatem równowaga dynamiczna, a nie statyczna.
Wyobraźmy sobie dwie grupy ludzi przechodzących przez drzwi w obu kierunkach. Jeśli w każdej sekundzie tyle samo osób przechodzi z pokoju A do pokoju B, co z pokoju B do pokoju A, liczba osób w obu pokojach pozostanie stała, mimo ciągłego ruchu. Podobnie jest z cząsteczkami w stanie równowagi chemicznej.
Potencjały termodynamiczne układu w stanie równowagi osiągają wartości minimalne, charakterystyczne dla danych warunków (temperatura, ciśnienie). Ta minimalizacja funkcji termodynamicznych, takich jak energia swobodna Gibbsa, jest siłą napędową dążenia układu do równowagi.
Przykład Reakcji Równowagowej: Hydroliza Estru
Klasycznym przykładem reakcji równowagowej jest hydroliza estru (np. octanu metylu) i odwrotna do niej estryfikacja:
CH₃COOCH₃ (octan metylu) + H₂O (woda) ⇌ CH₃COOH (kwas octowy) + CH₃OH (metanol)
W zamkniętym naczyniu, po pewnym czasie, osiągnięty zostanie stan, w którym szybkość powstawania kwasu octowego i metanolu z octanu metylu i wody będzie równa szybkości ich powrotnego łączenia się w octan metylu i wodę. Stężenia wszystkich czterech substancji przestaną się zmieniać.
Kiedy Równowaga Może Nie Zostać Osiągnięta?
Teoretycznie, każda reakcja odwracalna dąży do stanu równowagi. Jednak w praktyce nie zawsze jest on osiągany lub może trwać to bardzo długo. Oto kilka powodów:
- Usuwanie produktów: Jeśli jeden z produktów jest stale usuwany z układu (np. wytrąca się jako osad, ulatnia się jako gaz), reakcja będzie przebiegać w jednym kierunku, dążąc do wyczerpania substratów.
- Separacja faz: Reagenty mogą występować w różnych fazach (np. ciało stałe i ciecz) i nie mieszać się ze sobą efektywnie. Reakcja zachodzi wtedy tylko na granicy faz, bardzo powoli, lub wcale.
- Niska szybkość reakcji: W danych warunkach reakcja może być ze swej natury bardzo powolna. Układ może wydawać się w spoczynku, ale w rzeczywistości reakcja netto wciąż postępuje, choć niezauważalnie w skali czasowej obserwacji. Katalizatory mogą przyspieszyć osiągnięcie równowagi, ale nie zmieniają jej położenia.
- Ciągłe dodawanie substratów: Jeśli jeden z substratów jest stale dodawany do systemu z zewnątrz, układ może osiągnąć stan ustalony, ale niekoniecznie równowagowy.
Stała Równowagi (K)
Stężenia reagentów w stanie równowagi są ze sobą powiązane poprzez stałą równowagi (oznaczaną zazwyczaj jako K). Stała równowagi jest stosunkiem iloczynów stężeń (lub aktywności) produktów do iloczynów stężeń (lub aktywności) substratów, podniesionych do potęg równych współczynnikom stechiometrycznym w zbilansowanym równaniu reakcji. Wartość stała równowagi zależy wyłącznie od temperatury i ciśnienia, a nie od mechanizmu reakcji czy obecności katalizatora (choć katalizator wpływa na szybkość jej osiągnięcia). Im większa wartość K, tym bardziej równowaga jest przesunięta w stronę produktów.

Reguła Le Chateliera: Prawo Przekory
Reguła Le Chateliera (pełna nazwa: Reguła Le Chateliera-Brauna) stanowi fundament w zrozumieniu, jak układy chemiczne reagują na zmiany zewnętrzne. Mówi ona, że kiedy układowi w stanie równowagi narzuci się zmianę warunków zewnętrznych (np. stężenia, temperatury, ciśnienia), równowaga przesunie się w taki sposób, aby przeciwdziałać tej zmianie i przywrócić nowy stan równowagi. Innymi słowy, układ „przeciwdziała” narzuconemu mu stresowi.
To prawo jest niezwykle potężne, ponieważ pozwala przewidzieć kierunek, w którym przesunie się równowaga, bez konieczności wykonywania skomplikowanych obliczeń termodynamicznych. Jest to jakościowe narzędzie do analizy systemów chemicznych.
Wpływ Zmian Stężenia
Zmiana stężenia jednego z reagentów jest jednym z najczęstszych sposobów wpływania na położenie równowagi. Zgodnie z regułą przekory:
- Dodanie substratu: Układ zareaguje, próbując zmniejszyć stężenie dodanego substratu, co oznacza, że równowaga przesunie się w stronę produktów (w prawo), zwiększając ich ilość.
- Usunięcie substratu: Układ zareaguje, próbując zwiększyć stężenie usuniętego substratu, co spowoduje przesunięcie równowagi w stronę substratów (w lewo), zmniejszając ilość produktów.
- Dodanie produktu: Układ zareaguje, próbując zmniejszyć stężenie dodanego produktu, co spowoduje przesunięcie równowagi w stronę substratów (w lewo), zwiększając ich ilość.
- Usunięcie produktu: Układ zareaguje, próbując zwiększyć stężenie usuniętego produktu, co spowoduje przesunięcie równowagi w stronę produktów (w prawo), zwiększając ich ilość.
Praktyczne zastosowanie tej zasady jest kluczowe w przemyśle chemicznym. Na przykład, aby zwiększyć wydajność pożądanego produktu, można go na bieżąco usuwać z mieszaniny reakcyjnej, co stale przesuwa równowagę w prawo.
Wpływ Zmian Temperatury
Temperatura jest jedynym czynnikiem, który zmienia wartość stałej równowagi (K). Wpływ temperatury zależy od tego, czy reakcja jest egzotermiczna (wydziela ciepło) czy endotermiczna (pochłania ciepło).
- Reakcje egzotermiczne (ΔH < 0): Ciepło jest traktowane jako produkt reakcji.
- Wzrost temperatury: Układ zareaguje, próbując pochłonąć dodane ciepło, co przesunie równowagę w stronę substratów (w lewo).
- Spadek temperatury: Układ zareaguje, próbując wytworzyć więcej ciepła, co przesunie równowagę w stronę produktów (w prawo).
- Reakcje endotermiczne (ΔH > 0): Ciepło jest traktowane jako substrat reakcji.
- Wzrost temperatury: Układ zareaguje, próbując pochłonąć dodane ciepło, co przesunie równowagę w stronę produktów (w prawo).
- Spadek temperatury: Układ zareaguje, próbując wytworzyć mniej ciepła, co przesunie równowagę w stronę substratów (w lewo).
Dla reakcji egzotermicznych, obniżenie temperatury sprzyja tworzeniu produktów, podczas gdy dla reakcji endotermicznych, podwyższenie temperatury jest korzystne. Ta zasada jest fundamentalna przy optymalizacji warunków reakcji w przemysł chemiczny.
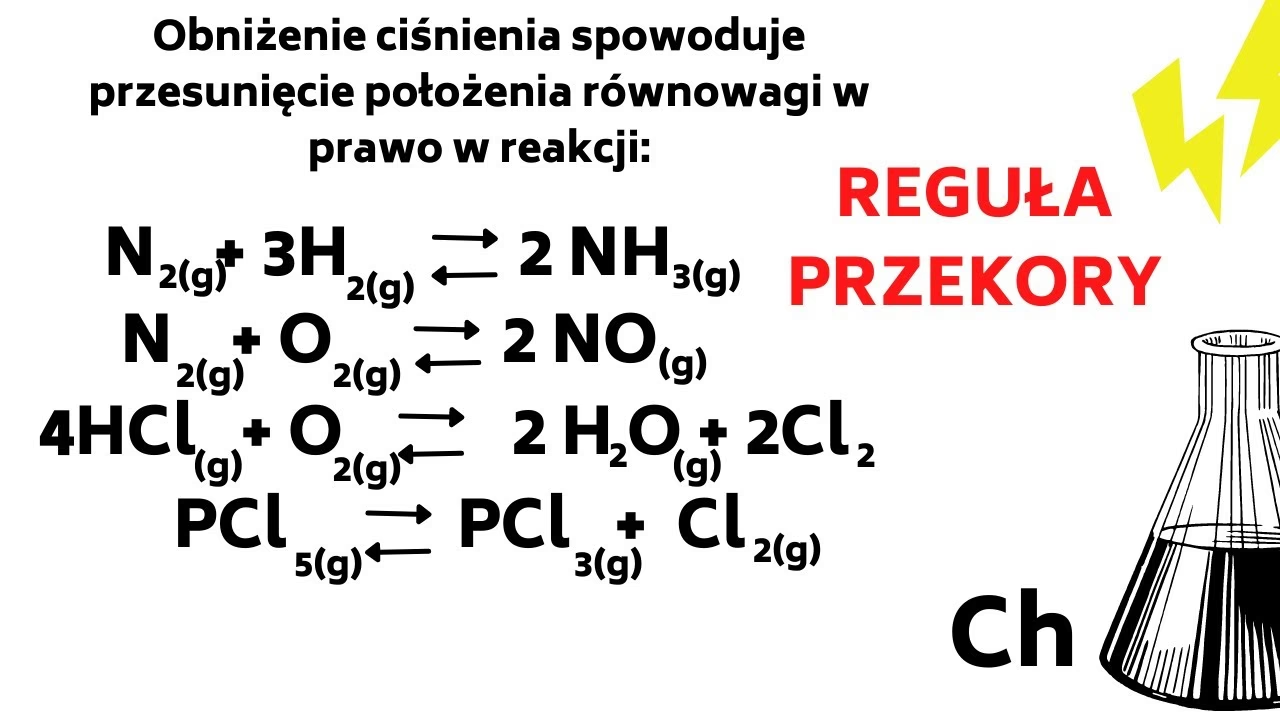
Wpływ Zmian Ciśnienia
Zmiana ciśnienia ma znaczący wpływ na równowagę tylko wtedy, gdy w reakcji biorą udział gazy i następuje zmiana całkowitej liczby moli gazów.
- Wzrost ciśnienia: Układ zareaguje, próbując zmniejszyć ciśnienie, co osiągnie poprzez przesunięcie równowagi w stronę, gdzie jest mniejsza liczba moli gazów.
- Spadek ciśnienia: Układ zareaguje, próbując zwiększyć ciśnienie, co osiągnie poprzez przesunięcie równowagi w stronę, gdzie jest większa liczba moli gazów.
Jeśli liczba moli gazów po obu stronach równania jest taka sama (np. H₂ (g) + I₂ (g) ⇌ 2HI (g)), zmiana ciśnienia nie wpłynie na położenie równowagi. Podobnie, dodanie gazu obojętnego (który nie bierze udziału w reakcji) do układu o stałej objętości nie zmieni ciśnień parcjalnych reagentów, a zatem nie wpłynie na równowagę.
Rola Katalizatorów
Warto podkreślić, że katalizatory nie wpływają na położenie równowagi chemicznej ani na wartość stałej równowagi. Katalizatory działają poprzez obniżenie energii aktywacji zarówno dla reakcji prostej, jak i odwrotnej, przyspieszając tym samym osiągnięcie stanu równowagi. Umożliwiają szybsze dojście do równowagi, ale nie zmieniają tego, gdzie ta równowaga się ustali. W praktyce przemysłowej są jednak niezwykle ważne, bo pozwalają na prowadzenie reakcji w krótszym czasie i/lub w łagodniejszych warunkach.
Podsumowanie Wpływu Czynników na Równowagę
Poniższa tabela porównawcza przedstawia, jak różne czynniki wpływają na położenie równowagi dla reakcji egzotermicznych i endotermicznych:
| Zmiana Warunku | Reakcja Egzotermiczna (A ⇌ B + ciepło) | Reakcja Endotermiczna (A + ciepło ⇌ B) | Komentarz |
|---|---|---|---|
| Wzrost Stężenia Substratu | Przesunięcie w prawo (w stronę produktów) | Przesunięcie w prawo (w stronę produktów) | Układ próbuje zużyć dodany substrat. |
| Usunięcie Stężenia Substratu | Przesunięcie w lewo (w stronę substratów) | Przesunięcie w lewo (w stronę substratów) | Układ próbuje odtworzyć usunięty substrat. |
| Wzrost Stężenia Produktu | Przesunięcie w lewo (w stronę substratów) | Przesunięcie w lewo (w stronę substratów) | Układ próbuje zużyć dodany produkt. |
| Usunięcie Stężenia Produktu | Przesunięcie w prawo (w stronę produktów) | Przesunięcie w prawo (w stronę produktów) | Układ próbuje odtworzyć usunięty produkt. |
| Wzrost Temperatury | Przesunięcie w lewo (w stronę substratów) | Przesunięcie w prawo (w stronę produktów) | Układ próbuje pochłonąć dodane ciepło. |
| Spadek Temperatury | Przesunięcie w prawo (w stronę produktów) | Przesunięcie w lewo (w stronę substratów) | Układ próbuje wytworzyć więcej ciepła. |
| Wzrost Ciśnienia (dla gazów, mniej moli po prawej) | Przesunięcie w prawo (w stronę produktów) | Przesunięcie w prawo (w stronę produktów) | Układ próbuje zmniejszyć objętość/liczbę moli gazów. |
| Spadek Ciśnienia (dla gazów, więcej moli po prawej) | Przesunięcie w lewo (w stronę substratów) | Przesunięcie w lewo (w stronę substratów) | Układ próbuje zwiększyć objętość/liczbę moli gazów. |
| Dodanie Katalizatora | Brak wpływu na położenie równowagi | Brak wpływu na położenie równowagi | Przyspiesza osiągnięcie równowagi, nie zmienia jej położenia. |
Praktyczne Zastosowania Reguły Le Chateliera
Reguła Le Chateliera ma ogromne znaczenie w przemyśle chemicznym, gdzie jest wykorzystywana do optymalizacji warunków reakcji w celu maksymalizacji wydajności pożądanych produktów. Jednym z najbardziej znanych przykładów jest:
- Proces Habera-Boscha: Synteza amoniaku (NH₃) z azotu (N₂) i wodoru (H₂):
N₂ (g) + 3H₂ (g) ⇌ 2NH₃ (g) + ciepło (reakcja egzotermiczna)
Aby zwiększyć wydajność amoniaku, stosuje się:- Wysokie ciśnienie: Po prawej stronie (produkty) są 2 mole gazu, po lewej (substraty) są 4 mole gazu. Zwiększenie ciśnienia przesuwa równowagę w stronę mniejszej liczby moli gazu, czyli w stronę amoniaku.
- Umiarkowaną temperaturę: Reakcja jest egzotermiczna, więc niska temperatura sprzyja tworzeniu amoniaku. Jednak zbyt niska temperatura spowalnia reakcję. Dlatego stosuje się temperaturę kompromisową (ok. 400-500°C) i katalizator, aby przyspieszyć osiągnięcie równowagi.
- Ciągłe usuwanie amoniaku: Amoniak jest skraplany i usuwany z układu, co zgodnie z regułą Le Chateliera stale przesuwa równowagę w prawo, w stronę jego produkcji.
- Produkcja kwasu siarkowego (proces kontaktowy): Synteza SO₃ z SO₂ i O₂ jest również reakcją egzotermiczną, a jej optymalizacja również opiera się na zasadach Le Chateliera.
Często Zadawane Pytania (FAQ)
Czy równowaga chemiczna oznacza, że reakcja ustała?
Nie, równowaga chemiczna to stan równowagi dynamicznej. Reakcje nadal zachodzą w obu kierunkach (od substratów do produktów i z powrotem), ale z jednakową szybkością, co powoduje, że stężenia reagentów pozostają stałe w czasie. Układ na poziomie makroskopowym wydaje się być w spoczynku, ale na poziomie molekularnym cząsteczki nieustannie reagują.
Czy katalizator wpływa na położenie równowagi chemicznej?
Nie, katalizator nie wpływa na położenie równowagi chemicznej ani na wartość stałej równowagi. Jego jedyną funkcją jest przyspieszenie osiągnięcia stanu równowagi poprzez obniżenie energii aktywacji zarówno dla reakcji prostej, jak i odwrotnej. Pozwala to na prowadzenie reakcji w krótszym czasie lub w niższych temperaturach, co jest korzystne ekonomicznie.

Jak odróżnić reakcję egzotermiczną od endotermicznej?
Reakcje egzotermiczne to te, które wydzielają ciepło do otoczenia (ΔH < 0). Można je traktować tak, jakby ciepło było produktem reakcji. Reakcje endotermiczne to te, które pochłaniają ciepło z otoczenia (ΔH > 0). Można je traktować tak, jakby ciepło było substratem reakcji. Zmiana entalpii (ΔH) dla reakcji jest kluczowym wskaźnikiem.
Co to jest stała równowagi (K) i do czego służy?
Stała równowagi (K) to wartość numeryczna, która opisuje stosunek stężeń produktów do stężeń substratów w stanie równowagi, podniesionych do potęg równych ich współczynnikom stechiometrycznym. Jest ona miarą położenia równowagi – duża wartość K oznacza, że równowaga jest przesunięta w stronę produktów (reakcja przebiega niemal do końca), natomiast mała wartość K oznacza, że w równowadze dominują substraty. K zależy wyłącznie od temperatury i ciśnienia.
Czy Reguła Le Chateliera ma zastosowanie tylko do gazów?
Nie, Reguła Le Chateliera ma zastosowanie do wszystkich typów reakcji chemicznych w stanie równowagi, niezależnie od stanu skupienia reagentów. Wpływ ciśnienia jest najbardziej widoczny i znaczący dla reakcji, w których biorą udział gazy i zmienia się ich całkowita liczba moli. Zmiany stężenia i temperatury mają wpływ na równowagi obejmujące również ciecze i ciała stałe.
Podsumowanie
Reguła Le Chateliera jest niezastąpionym narzędziem w chemii, pozwalającym przewidywać, jak systemy w stanie równowagi chemicznej reagują na zmiany warunków zewnętrznych. Zrozumienie, w jaki sposób zmiana stężenia reagentów, temperatury czy ciśnienia wpływa na położenie równowagi, jest fundamentalne dla każdego, kto zajmuje się chemią – od studentów po inżynierów w przemyśle. Dzięki tej regule możliwe jest nie tylko głębsze poznanie natury procesów chemicznych, ale także ich efektywne kontrolowanie i optymalizowanie, co przekłada się na rozwój nowych technologii i produktów. Pamiętajmy, że chemia to dynamiczny świat, a reguła przekory jest kluczem do jego zrozumienia i opanowania.
Zainteresował Cię artykuł Reguła Le Chateliera: Klucz do Równowagi Chemicznej", "kategoria": "Chemia? Zajrzyj też do kategorii Edukacja, znajdziesz tam więcej podobnych treści!
