13/11/2011
W świecie chemii, zrozumienie struktury materii zaczyna się od najbardziej fundamentalnych elementów – elektronów i ich zachowania. Nie poruszają się one jednak po prostych orbitach, jak planety wokół słońca, lecz zajmują specyficzne obszary przestrzeni, zwane orbitalami. To właśnie kształty tych orbitali, a zwłaszcza orbitali molekularnych, decydują o tym, jak atomy łączą się ze sobą, tworząc cząsteczki i nadając im unikalne właściwości. Poznajmy tę fascynującą koncepcję, która leży u podstaw całej chemii.
Podstawy Orbitali: Czym Są i Dlaczego Są Ważne?
W ujęciu mechaniki kwantowej, orbital to nic innego jak matematyczna funkcja falowa, będąca rozwiązaniem równania Schrödingera dla pojedynczego elektronu. Nie jest to fizyczna „ścieżka” elektronu, lecz abstrakcyjny opis stanu kwantowego. Kwadrat modułu tej funkcji falowej określa gęstość prawdopodobieństwa znalezienia elektronu w danym punkcie przestrzeni. Oznacza to, że orbital reprezentuje obszar, w którym prawdopodobieństwo napotkania elektronu jest największe, zazwyczaj przyjmuje się wartość bliską 0,9 (90%).
Pojęcie orbitalu jest kluczowe dla zrozumienia budowy atomów i cząsteczek. Pozwala przewidywać, jak elektrony rozmieszczą się wokół jąder, a co za tym idzie – jak atomy będą reagować chemicznie. Warto również pamiętać, że orbitale często są zdegenerowane, co oznacza, że jednemu poziomowi energetycznemu może odpowiadać wiele stanów kwantowych, a tym samym wiele orbitali o tej samej energii, ale różnej orientacji przestrzennej.
Rodzaje Orbitali: Atomowe vs. Molekularne
Aby w pełni zrozumieć kształty orbitali molekularnych, musimy najpierw rozróżnić ich podstawowe kategorie.
Orbitale Atomowe
Orbitale atomowe opisują elektrony, które są przypisane do pojedynczych jąder atomowych i nie uczestniczą w tworzeniu wiązań chemicznych. Ich kształty zależą od liczb kwantowych przypisanych do danego elektronu i są kluczowe dla zrozumienia konfiguracji elektronowej atomu. Wyróżniamy kilka podstawowych typów:
- Orbitale s: Charakteryzują się kształtem sferycznym. Oznacza to, że gęstość prawdopodobieństwa znalezienia elektronu jest równomiernie rozłożona wokół jądra.
- Orbitale p: Posiadają kształt przypominający „hantle” lub dwie połączone kule. Występują trzy orbitale p (px, py, pz), zorientowane wzdłuż osi układu współrzędnych, prostopadle do siebie.
- Orbitale d i f: Mają znacznie bardziej złożone kształty, będące kombinacją „hantli” i torusów (kształtów przypominających pączka). Występuje pięć orbitali d i siedem orbitali f, każdy o specyficznej orientacji przestrzennej.
- Orbitale zhybrydyzowane: Powstają w wyniku „mieszania się” orbitali atomowych (np. s i p) w celu utworzenia nowych orbitali o kształtach i orientacjach przestrzennych najlepiej odpowiadających geometrii cząsteczek. Przykłady to orbitale sp, sp2, sp3.
Orbitale Molekularne
Orbitale molekularne to z kolei te, które opisują elektrony w całej cząsteczce, a nie tylko w pojedynczych atomach. Są one kluczowe dla zrozumienia wiązań chemicznych, ponieważ elektrony na tych orbitalach mogą (ale nie muszą) tworzyć wiązania między atomami. Dzielimy je na trzy główne typy w zależności od ich energii w porównaniu do energii orbitali atomowych, z których powstały:
- Orbitale wiążące: Elektrony w tych orbitalach posiadają niższą energię niż na swoich pierwotnych orbitalach atomowych. Ich obsadzenie prowadzi do stabilizacji cząsteczki i tworzenia wiązania.
- Orbitale antywiążące: Elektrony na tych orbitalach mają wyższą energię niż na orbitalach atomowych. Obsadzenie ich prowadzi do destabilizacji cząsteczki i osłabienia lub zerwania wiązania. Często oznaczane są gwiazdką, np. σ*, π*.
- Orbitale niewiążące: Elektrony na tych orbitalach posiadają taką samą energię, jak gdyby znajdowały się na swoich orbitalach atomowych. Nie uczestniczą aktywnie w tworzeniu wiązania, ale mogą wpływać na właściwości cząsteczki.
Kształty Orbitali Molekularnych: Tajemnice Wiązań Chemicznych
Kształty orbitali molekularnych są bardziej złożone niż atomowych, ponieważ opisują elektrony poruszające się w polu wielu jąder atomowych. Ich formowanie wynika z nakładania się orbitali atomowych w przestrzeni.
Klasyfikacja Orbitali Molekularnych
Orbitale molekularne wiążące klasyfikuje się najczęściej na podstawie symetrii względem osi międzyjądrowej, która łączy centra atomów tworzących wiązanie. Ta klasyfikacja jest analogiczna do orbitali atomowych (s, p, d, f), ale używa się greckich liter:
- Orbitale σ (sigma): Powstają w wyniku czołowego nałożenia się orbitali atomowych, np. dwóch orbitali s, orbitalu s z orbitalem p, lub dwóch orbitali p (wzdłuż osi). Charakteryzują się brakiem płaszczyzn węzłowych zawierających oś międzyjądrową. Są to najsilniejsze wiązania, ponieważ nakładanie jest maksymalne wzdłuż osi wiązania. Orbital atomowy „s” (0 płaszczyzn węzłowych) odpowiada orbitalowi molekularnemu σ.
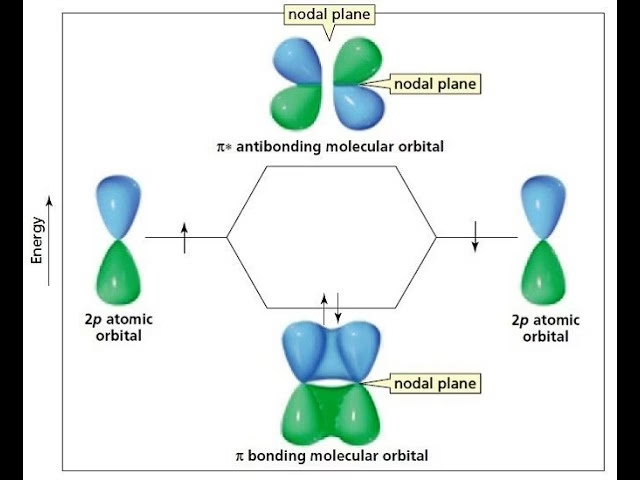
- Orbitale π (pi): Tworzą się w wyniku bocznego nałożenia się orbitali atomowych, najczęściej orbitali p, ale także d lub f. Posiadają dokładnie jedną płaszczyznę węzłową zawierającą oś międzyjądrową. Wiązania π są zazwyczaj słabsze niż σ. Orbital atomowy „p” (1 płaszczyzna węzłowa) odpowiada orbitalowi molekularnemu π.
- Orbitale δ (delta): Są rzadsze i powstają w wyniku nałożenia się czterech płatów orbitali d. Mają dwie płaszczyzny węzłowe zawierające oś międzyjądrową. Orbital atomowy „d” (2 płaszczyzny węzłowe) odpowiada orbitalowi molekularnemu δ.
Warto zaznaczyć, że orbitale molekularne antywiążące (σ*, π*, δ*) przyjmują szereg, nieraz bardzo złożonych kształtów. Często są to twory „wirtualne”, trudne do wizualizacji i nie zawsze mające bezpośrednią interpretację fizyczną, lecz ich istnienie jest kluczowe dla pełnego opisu układu.
Zapełnianie orbitali przez elektrony zawsze przebiega zgodnie z zakazem Pauliego, który mówi, że dany orbital może pomieścić co najwyżej dwa elektrony o przeciwnych spinach. Jest to fundamentalna zasada leżąca u podstaw budowy układu okresowego pierwiastków.
Jak Powstają Orbitale Molekularne? Teoria i Przykłady
Zrozumienie, jak atomy łączą się w cząsteczki, wymaga sięgnięcia po Teorię Orbitali Molekularnych (MOT), która oferuje bardziej kompleksowy opis wiązań niż klasyczna Teoria Wiązań Walencyjnych, szczególnie w przypadkach rezonansu.
Teoria Orbitali Molekularnych (MOT)
MOT jest wykorzystywana do wyjaśniania wiązań w cząsteczkach, których nie da się w pełni opisać za pomocą prostych wiązań pojedynczych, podwójnych czy potrójnych, a które wykazują rezonans. W MOT elektrony nie są przypisane do poszczególnych atomów, ale są delokalizowane na całej cząsteczce. Oto cztery kluczowe zasady MOT:
- Zasada I: Zachowanie liczby orbitali. Liczba powstałych orbitali molekularnych jest zawsze równa liczbie orbitali atomowych, które połączyły się w celu ich utworzenia. Na przykład, jeśli dwa atomy wodoru (każdy z jednym orbitalem 1s) łączą się, powstaną dwa orbitale molekularne.
- Zasada II: Energetyka orbitali. Orbitale molekularne wiążące mają niższą energię niż wyjściowe orbitale atomowe, co prowadzi do stabilizacji. Orbitale antywiążące mają natomiast wyższą energię, co oznacza destabilizację.
- Zasada III: Zapełnianie orbitali. Elektrony w cząsteczce obsadzają orbitale molekularne od najniższej energii do sukcesywnie wyższych, zgodnie z regułą Hunda i zakazem Pauliego. To naturalne dążenie do osiągnięcia najniższego stanu energetycznego, czyli największej stabilności.
- Zasada IV: Efektywność kombinacji. Orbitale atomowe łączą się, tworząc orbitale molekularne najefektywniej, gdy mają podobną energię. Oznacza to, że orbitale 1s najlepiej łączą się z 1s, 2p z 2p itd., tworząc najbardziej stabilne orbitale molekularne.
Przykład: Cząsteczka wodoru (H2)
Każdy atom wodoru ma jeden orbital walencyjny 1s. Zgodnie z zasadą I, z połączenia dwóch orbitali 1s powstaną dwa orbitale molekularne: wiążący σ (sigma) i antywiążący σ* (sigma gwiazdka). Dwa elektrony walencyjne (po jednym z każdego atomu H) zajmują niżej energetyczny orbital σ, co prowadzi do utworzenia stabilnego wiązania pojedynczego.
Rząd Wiązania:
Rząd wiązania jest miarą siły wiązania i może być obliczony z liczby elektronów wiążących i antywiążących:
Rząd wiązania = ½ (liczba elektronów wiążących − liczba elektronów antywiążących).

Dla H2: Rząd wiązania = ½ (2 − 0) = 1 (wiązanie pojedyncze).
Dla He2: Każdy atom He ma 2 elektrony w orbitalu 1s. Powstaną σ i σ*. Cztery elektrony zajmą σ (2) i σ* (2). Rząd wiązania = ½ (2 − 2) = 0. Oznacza to, że cząsteczka He2 nie jest stabilna i nie istnieje.
Przykład: Cząsteczka azotu (N2)
Każdy atom azotu ma konfigurację elektronową 1s2 2s2 2p3, co daje łącznie 14 elektronów walencyjnych. Z połączenia orbitali atomowych 2s i 2p powstaną odpowiednie orbitale molekularne σ i π (oraz ich antywiążące odpowiedniki). Elektrony zapełniają je zgodnie z zasadami MOT. W przypadku N2, elektrony zajmują orbitale σ2s, σ*2s, π2p, σ2p. W rezultacie powstaje wiązanie potrójne: jedno wiązanie σ i dwa wiązania π. Rząd wiązania = ½ (10 − 4) = 3.
Mechanizm Tworzenia Wiązań: Hybrydyzacja i Nakładanie Orbitali
Tworzenie wiązania pi jest doskonałym przykładem, gdy tylko część orbitali atomowych ulega hybrydyzacji, a pozostałe niezhybrydyzowane orbitale tworzą wiązania boczne.
Przykład 1: Wiązanie π w cząsteczce etenu (C2H4)
W cząsteczce etenu każdy atom węgla ulega hybrydyzacji sp2. Oznacza to, że jeden orbital s i dwa orbitale p mieszają się, tworząc trzy równocenne orbitale sp2, które leżą w jednej płaszczyźnie i są skierowane pod kątem 120° względem siebie. Te orbitale sp2 tworzą wiązania sigma (σ) z atomami wodoru oraz jedno wiązanie σ między atomami węgla (przez czołowe nałożenie).
Jednak na każdym atomie węgla pozostaje jeden niezhybrydyzowany orbital p, prostopadły do płaszczyzny orbitali sp2. Te dwa niezhybrydyzowane orbitale p (po jednym z każdego atomu węgla) nakładają się bocznie – powyżej i poniżej osi międzyjądrowej – tworząc wiązanie pi (π). Co istotne, choć wiązanie π jest pojedynczym wiązaniem (jedna para elektronów), to jego kombinacja z jednym wiązaniem σ odpowiada za występowanie wiązania podwójnego między atomami węgla w etenie.
Przykład 2: Powstawanie wiązań w cząsteczce CO2 (dwutlenek węgla)
W cząsteczce CO2 atom węgla przyjmuje hybrydyzację typu sp. Oznacza to, że dwa jego orbitale p (py i pz) pozostają niezhybrydyzowane. Atomy tlenu ulegają hybrydyzacji sp2, posiadając po jednym niezhybrydyzowanym orbitalu p.
W wyniku czołowego nakładania się zhybrydyzowanych orbitali sp atomu węgla z orbitalami sp2 atomów tlenu powstają dwa wiązania sigma (σ), po jednym z każdej strony atomu węgla. Równocześnie, niezhybrydyzowane orbitale 2py i 2pz atomu węgla tworzą dwa wiązania pi (π) z niezhybrydyzowanymi orbitalami p atomów tlenu – po jednym wiązaniu π z każdym atomem tlenu. W rezultacie, w cząsteczce CO2 mamy dwa wiązania podwójne, a każde z nich składa się z jednego wiązania σ i jednego wiązania π.
Kluczowa różnica: Wiązanie sigma powstaje przez czołowe nakładanie się orbitali i jest silniejsze. Wiązanie pi powstaje przez boczne nakładanie się orbitali p (lub d, f) i jest słabsze. Należy zapamiętać, że wiązanie π nigdy nie występuje samodzielnie, lecz zawsze towarzyszy wiązaniu σ. Krotność wiązania jest ustalana w zależności od rodzaju orbitali molekularnych:
- Wiązanie pojedyncze = 1 wiązanie σ
- Wiązanie podwójne = 1 wiązanie σ + 1 wiązanie π
- Wiązanie potrójne = 1 wiązanie σ + 2 wiązania π
Głębsze Spojrzenie na Orbitale jako Funkcje Falowe
Pojęcie orbitalu jest fundamentalne, ale ma sens wyłącznie w ramach tzw. przybliżenia jednoelektronowego, stosowanego w metodach takich jak Hartree-Fock czy DFT (teoria funkcjonałów gęstości). W tych teoriach wieloelektronowa funkcja falowa jest konstruowana z jednoelektronowych orbitali (spinorbitali).
Należy podkreślić, że dla danego układu istnieje nieskończenie wiele „zestawów” orbitali molekularnych, które mogą opisywać tę samą wieloelektronową funkcję falową. Najczęściej korzysta się z tzw. kanonicznych (lub spektroskopowych) orbitali Hartree’go-Focka lub z orbitali lokalizowanych, które są bardziej intuicyjne.

Orbitale atomowe są w tym kontekście albo orbitalami elektronów w izolowanych atomach, albo funkcjami bazowymi, na które rozwijane są orbitale molekularne. Te ostatnie to funkcje falowe elektronów poruszających się w uśrednionym polu pozostałych elektronów cząsteczki i w polu jąder. Zwykle przedstawia się je w postaci kombinacji liniowej funkcji bazowych (metoda LCAO MO, czyli Linearnych Kombinacji Atomowych Orbitali Molekularnych).
Ciekawym aspektem są również orbitale niezajęte, nazywane wirtualnymi lub antywiążącymi. Opisują one stany, które nie są obsadzone przez elektrony w stanie podstawowym cząsteczki. W dużych bazach funkcyjnych mogą przyjmować bardzo dziwne, rozmyte kształty i nie zawsze mają sensowną interpretację wizualną.
Z każdym orbitalem związana jest tzw. energia orbitalna. Zgodnie z twierdzeniem Koopmansa, energia orbitalu HOMO (Highest Occupied Molecular Orbital, czyli najwyższego zajętego orbitalu molekularnego) jest zbliżona do potencjału jonizacji cząsteczki. Z kolei energia orbitalu LUMO (Lowest Unoccupied Molecular Orbital, czyli najniższego niezajętego orbitalu molekularnego) jest przybliżeniem energii powinowactwa elektronowego. Te pojęcia są niezwykle ważne w chemii kwantowej i spektroskopii, pozwalając przewidywać reaktywność i właściwości optyczne cząsteczek.
Orbitale Atomowe Wodoru: Podstawa Zrozumienia
Zrozumienie kształtów orbitali molekularnych często zaczyna się od analizy najprostszego atomu – wodoru. W atomie wodoru, na podstawie trzech liczb kwantowych (głównej n, pobocznej l i magnetycznej m), można jednoznacznie określić funkcję falową elektronu, będącą rozwiązaniem równania Schrödingera. Funkcje te są „porządne”, co oznacza, że przyjmują skończone, ciągłe i jednoznaczne wartości.
Opis orbitali w sferycznym układzie współrzędnych (r, φ, ϑ) jest najbardziej intuicyjny. Funkcję falową orbitalu można przedstawić jako iloczyn dwóch funkcji: radialnej R (zależnej od odległości r od jądra) oraz kątowej Y (zależnej od kątów φ i ϑ, określających orientację w przestrzeni). Funkcja radialna R zależy od liczb kwantowych n i l, natomiast funkcja kątowa Y – od l i m.
Kształty orbitali s (l=0) są sferyczne, co oznacza, że funkcja kątowa Y jest stała, niezależna od kątów. Dla orbitali p (l=1), funkcja kątowa Y zależy od kątów, co nadaje im charakterystyczny kształt hantli, zorientowanych wzdłuż osi. Wraz ze wzrostem wartości n (głównej liczby kwantowej), orbitale stają się większe i mają więcej płaszczyzn węzłowych (obszarów, gdzie prawdopodobieństwo znalezienia elektronu jest zerowe).
Ważna uwaga końcowa: Pojęcie orbitalu, choć fundamentalne, często nastręcza trudności w wyobrażeniu sobie ruchu elektronów. Nie należy myśleć o elektronach jako o miniaturowych kulkach krążących po ściśle określonych torach. Orbital można porównać do trójwymiarowej, długo naświetlanej fotografii ruchu elektronu wokro jądra. Taka fotografia obrazowałaby obszar, w którym elektron najprawdopodobniej przebywa. Jednak ta analogia nie wyjaśnia zasady nieoznaczoności Heisenberga, która mówi, że niemożliwe jest jednoczesne dokładne wyznaczenie położenia i pędu elektronu. Elektrony, podobnie jak inne cząstki elementarne, mają złożony charakter falowo-korpuskularny, a ich naturę da się opisywać jedynie złożonymi równaniami matematycznymi. Nie można ich sobie „uzmysłowić” w konwencjonalny, mechaniczny sposób. Możemy jedynie mówić o prawdopodobieństwie uzyskania określonego wyniku pomiaru, a nie o niezbywalnych cechach układu.
Często Zadawane Pytania (FAQ)
- Czym jest orbital w chemii kwantowej?
- Orbital to matematyczna funkcja falowa opisująca stan jednego elektronu w atomie lub cząsteczce. Kwadrat jej modułu określa gęstość prawdopodobieństwa znalezienia elektronu w danym punkcie przestrzeni.
- Jaka jest podstawowa różnica między orbitalem atomowym a molekularnym?
- Orbital atomowy opisuje elektron przypisany do pojedynczego jądra atomowego, natomiast orbital molekularny opisuje elektron delokalizowany na całą cząsteczkę, poruszający się w polu wielu jąder atomowych.
- Dlaczego orbitale molekularne mają różne kształty, np. sigma (σ) i pi (π)?
- Kształty te wynikają ze sposobu nakładania się orbitali atomowych. Orbitale σ powstają przez czołowe nakładanie się wzdłuż osi wiązania, natomiast orbitale π powstają przez boczne nakładanie się, tworząc obszary gęstości elektronowej powyżej i poniżej osi wiązania.
- Czy wiązanie pi może istnieć bez wiązania sigma?
- Nie, wiązanie π nigdy nie występuje samodzielnie. Zawsze towarzyszy wiązaniu σ. W wiązaniach wielokrotnych (podwójnych, potrójnych) zawsze jest jedno wiązanie σ i jedno lub dwa wiązania π.
- Jak teoria orbitali molekularnych (MOT) wyjaśnia rezonans?
- MOT wyjaśnia rezonans poprzez koncepcję delokalizacji elektronów na orbitalach molekularnych obejmujących całą cząsteczkę, a nie tylko pojedyncze wiązania. W przeciwieństwie do teorii wiązań walencyjnych, która wymaga wielu struktur rezonansowych, MOT opisuje rzeczywistą strukturę jako pojedynczy stan, w którym elektrony są rozłożone na odpowiednich orbitalach molekularnych.
- Co oznaczają terminy HOMO i LUMO?
- HOMO (Highest Occupied Molecular Orbital) to najwyżej położony energetycznie orbital molekularny zajęty przez elektrony. LUMO (Lowest Unoccupied Molecular Orbital) to najniżej położony energetycznie orbital molekularny niezajęty przez elektrony. Są one kluczowe dla przewidywania reaktywności chemicznej i właściwości optycznych cząsteczek.
Podsumowanie
Świat orbitali molekularnych jest złożony, ale fascynujący. Od sferycznych orbitali s, przez hantlowate p, aż po skomplikowane kształty orbitali d i f, każdy z nich odgrywa kluczową rolę w determinowaniu struktury i reaktywności materii. Zrozumienie, jak orbitale atomowe łączą się, tworząc orbitale molekularne typu sigma (σ) i pi (π), jest fundamentalne dla każdego, kto chce zgłębić tajniki chemii. Choć pojęcie orbitalu jest abstrakcyjne i matematyczne, jego konsekwencje są bardzo realne i widoczne w otaczającym nas świecie. Pamiętajmy, że chemia to nie tylko wzory, ale przede wszystkim niezwykła taniec elektronów w przestrzeni, rządzony przez prawa mechaniki kwantowej, które pozwalają nam przewidywać i kontrolować transformacje materii.
Zainteresował Cię artykuł Kształty Orbitali Molekularnych: Kompletny Przewodnik", "kategoria": "Chemia? Zajrzyj też do kategorii Edukacja, znajdziesz tam więcej podobnych treści!
