24/06/2007
Wzory strukturalne są niczym mapy molekularnego świata – pozwalają nam wizualizować, jak atomy łączą się ze sobą, tworząc złożone cząsteczki. W przeciwieństwie do prostych wzorów sumarycznych, które informują nas jedynie o liczbie i typie atomów, wzory strukturalne ukazują pełną architekturę chemiczną, włącznie z układem wiązań i przestrzenną orientacją. Zrozumienie sposobu ich tworzenia i interpretacji jest kluczowe dla każdego, kto zagłębia się w tajniki chemii, zwłaszcza organicznej. W tym artykule przeprowadzimy Cię przez proces tworzenia wzorów strukturalnych, omówimy ich różnorodne typy i wyjaśnimy, co dokładnie możemy z nich wyczytać.
Co to jest wzór strukturalny?
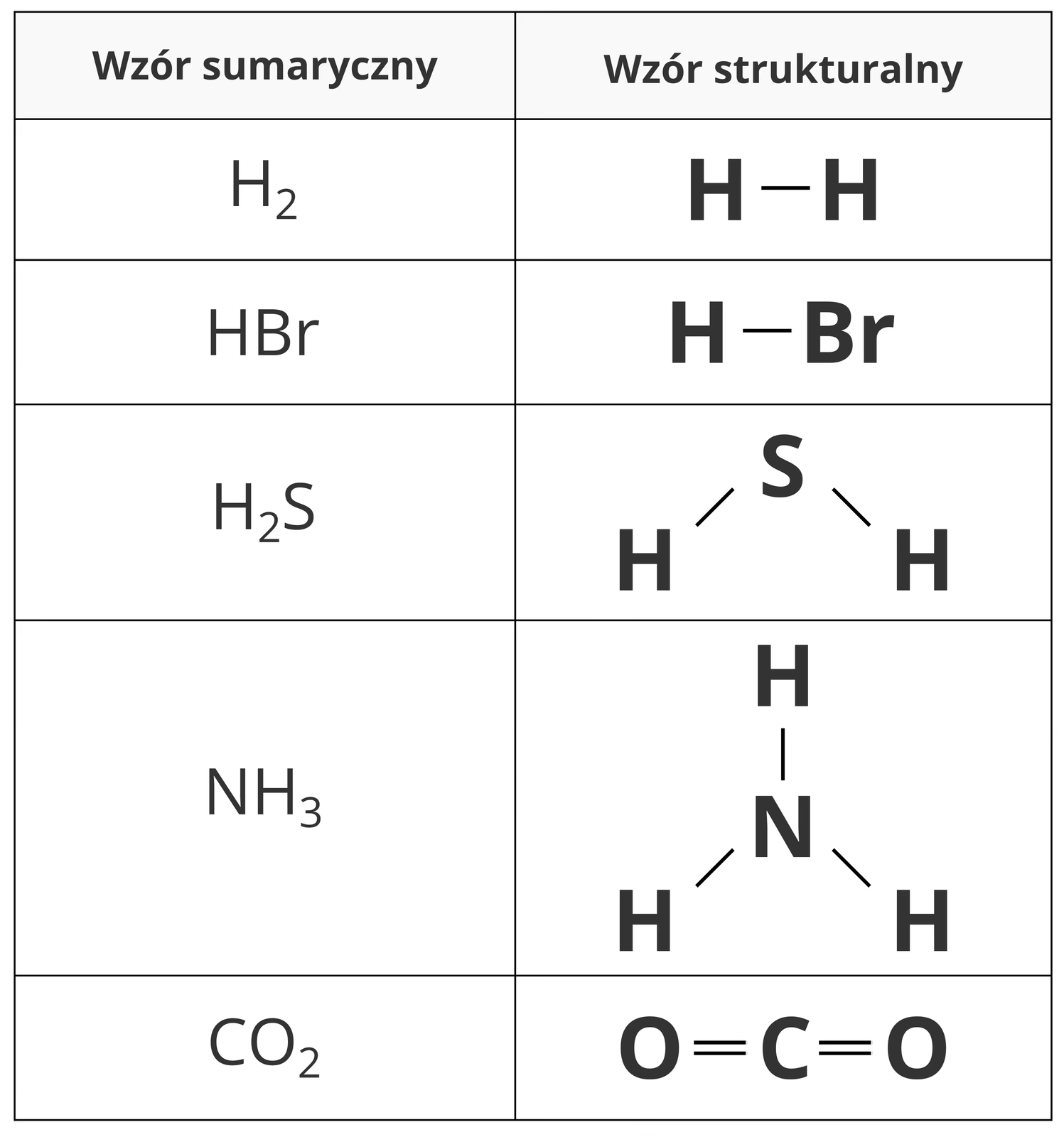
Wzór strukturalny to graficzna reprezentacja cząsteczki chemicznej, która pokazuje rozmieszczenie atomów oraz rodzaj i liczbę wiązań chemicznych między nimi. Aby go utworzyć, musimy znać nie tylko symbole pierwiastków wchodzących w skład cząsteczki, ale także liczbę atomów każdego pierwiastka. Połączone atomy przedstawiamy za pomocą linii, a każdy symbol pierwiastka umieszczamy w odpowiednim miejscu. Jedna kreska symbolizuje wiązanie pojedyncze, dwie kreski – wiązanie podwójne, a trzy – wiązanie potrójne. Dzięki temu możemy dokładnie zobaczyć, jak atomy są ze sobą połączone i jakie mają sąsiedztwo w cząsteczce.
Jak rysować wzory strukturalne? Ogólne zasady i szczegółowe instrukcje
Proces rysowania wzorów strukturalnych opiera się na kilku fundamentalnych zasadach, które pozwalają nam poprawnie oddać budowę cząsteczki. Zawsze zaczynamy od zidentyfikowania atomów centralnych i ich połączeń, a następnie dodajemy pozostałe atomy, pamiętając o ich wartościowościach i liczbie wiązań, które mogą utworzyć. W przypadku złożonych cząsteczek, takich jak kwasy, istnieją specyficzne kroki, które ułatwiają precyzyjne przedstawienie ich struktury.
Tworzenie wzorów strukturalnych kwasów
Rysowanie wzorów strukturalnych kwasów wymaga zastosowania nieco bardziej złożonych reguł, które różnią się w zależności od tego, czy mamy do czynienia z kwasami beztlenowymi, czy tlenowymi.
Kwasy beztlenowe
Dla kwasów beztlenowych proces jest stosunkowo prosty i składa się z kilku kroków:
- Zapisz symbol niemetalu, który jest centralnym atomem kwasu.
- Od symbolu niemetalu narysuj tyle kresek (wiązań), ile atomów wodoru znajduje się w cząsteczce kwasu. Każda kreska symbolizuje wiązanie z wodorem.
- Na końcu każdej kreski zapisz symbol wodoru (H).
Przykład: Kwas chlorowodorowy (HCl) – Cl—H. Kwas siarkowodorowy (H2S) – H—S—H.
Kwasy tlenowe
Kwasy tlenowe mają bardziej złożoną strukturę, ponieważ zawierają atomy tlenu, które pełnią rolę łączników między niemetalem a wodorem. Proces ich rysowania wymaga większej uwagi:
- Zapisz symbol niemetalu, który jest atomem centralnym kwasu.
- Obok symbolu niemetalu, jeden pod drugim, zapisz tyle symboli tlenu (O), ile atomów wodoru znajduje się w kwasie. Te atomy tlenu będą tworzyć grupy hydroksylowe (-OH).
- Połącz te symbole tlenu kreskami z symbolem niemetalu.
- Od każdego z tych atomów tlenu narysuj jeszcze jedną kreskę (pamiętaj, że tlen jest dwuwartościowy i w grupie -OH tworzy jedno wiązanie z niemetalem, a drugie z wodorem). Na końcu tej kreski zapisz symbol wodoru (H). W ten sposób tworzysz grupy -OH.
- Jeśli w cząsteczce kwasu pozostały jeszcze jakieś atomy tlenu (które nie tworzą grup -OH), zapisz je po drugiej stronie niemetalu. Połącz je podwójnymi kreskami (tlen jest dwuwartościowy) z symbolem niemetalu. Te atomy tlenu tworzą wiązania podwójne z atomem centralnym.
Ważna zasada: Całkowita liczba kresek (wiązań) odchodzących od symbolu niemetalu musi być zgodna z jego wartościowością podaną w nazwie kwasu (np. kwas siarkowy(VI) – siarka tworzy 6 wiązań). Wszystkie te czynności wykonuje się na jednym wzorze, stopniowo go rozbudowując.

Jeśli w kwasie tlenowym występują dwa atomy niemetalu (np. w niektórych kwasach wieloprotonowych lub w przypadku połączeń dwóch centralnych atomów), przy każdym z nich zapisujemy jednakową ilość połączeń -O-H i atomów tlenu z podwójnymi wiązaniami. Pozostały atom tlenu (jeśli jest) przyłączamy jedną kreską do jednego, a drugą kreską do drugiego atomu niemetalu, tworząc mostek tlenowy.
Rodzaje wzorów strukturalnych i ich zastosowania
Chemia, zwłaszcza organiczna, wykorzystuje różnorodne sposoby przedstawiania wzorów strukturalnych, aby jak najdokładniej oddać właściwości i budowę cząsteczek. Każdy z nich ma swoje specyficzne zastosowania i poziom szczegółowości.
Wiązania, elektrony i ładunki
Podstawą każdego wzoru strukturalnego są wiązania, symbolizowane liniami: pojedyncza linia to wiązanie pojedyncze, dwie linie to wiązanie podwójne, a trzy linie to wiązanie potrójne. W niektórych wzorach, zwłaszcza w strukturach Lewisa, widoczne są również elektrony, przedstawiane jako kropki lub pary kropek. Jedna kropka oznacza jeden elektron, dwie kropki – parę elektronów, często symbolizującą wolną parę elektronową lub ujemny ładunek.
Ładunki na atomach są również ważnym elementem wzorów strukturalnych. Atom, któremu brakuje pary elektronów lub który posiada dodatkowy proton, może mieć ładunek dodatni, oznaczany symbolem ⊕. Natomiast atom posiadający wolne elektrony, które nie są związane z innym atomem, będzie miał ładunek ujemny, oznaczany symbolem ⊖. Te oznaczenia dostarczają informacji o reaktywności atomu w cząsteczce.
Wzory skondensowane
Wzory skondensowane to uproszczony sposób zapisu struktury cząsteczki w jednej linii tekstu, szczególnie użyteczny, gdy grafika jest ograniczona. Są one wygodne do przedstawiania prostych struktur, takich jak CH3CH2OH (etanol). W tego typu wzorach wszystkie atomy, włącznie z atomami wodoru, są jawnie pokazane. Nawiasy są używane do wskazania wielu identycznych grup, które są przyłączone do najbliższego atomu niebędącego wodorem po lewej stronie (np. (CH3)2CHOH – 2-propanol) lub do atomu po prawej stronie, jeśli pojawiają się na początku wzoru.
Wzory skondensowane mogą również implikować wiązania podwójne, np. grupa karbonylowa (C=O) może być zapisana jako C(O), np. CH3C(O)CH3 (aceton). Ważne jest, aby zwracać uwagę na atom w nawiasach, aby określić, do którego atomu jest on przyłączony. Różne grupy funkcyjne mają swoje specyficzne skróty: aldehydy jako CHO, kwasy karboksylowe jako CO2H lub COOH, estry jako CO2R lub COOR. Należy jednak pamiętać, że wzory skondensowane nie dają natychmiastowego wyobrażenia o geometrii molekularnej ani liczbie wiązań między atomami węgla; te informacje muszą być wywnioskowane na podstawie liczby atomów przyłączonych do węgla i ewentualnych ładunków.

Wzory szkieletowe (liniowo-kreskowe)
Wzory szkieletowe stanowią standardową notację dla bardziej złożonych cząsteczek organicznych. W tym typie diagramu, który po raz pierwszy zastosował Friedrich August Kekulé von Stradonitz, atomy węgla są implikowane – znajdują się w wierzchołkach (rogach) i na końcach segmentów linii, zamiast być oznaczonymi symbolem C. Atomy wodoru przyłączone do atomów węgla również nie są zaznaczone; rozumie się, że każdy atom węgla jest związany z wystarczającą liczbą atomów wodoru, aby węgiel miał cztery wiązania. Obecność ładunku dodatniego lub ujemnego na atomie węgla zastępuje jeden z implikowanych atomów wodoru. Atomy wodoru przyłączone do atomów innych niż węgiel (np. do tlenu, azotu) muszą być jawnie zapisane.
Dodatkową cechą wzorów szkieletowych jest możliwość przedstawiania stereochemii, czyli trójwymiarowej struktury związku. Używa się do tego klinów zamiast prostych linii: klin pełny (solid wedge) wskazuje, że atom znajduje się przed płaszczyzną rysunku (w stronę obserwatora), natomiast klin przerywany (dashed wedge) oznacza, że atom znajduje się za płaszczyzną rysunku (od obserwatora). Prosta, nieprzerywana linia oznacza, że atom leży w płaszczyźnie rysunku. Wzory szkieletowe mogą również przedstawiać izomery cis i trans alkenów. Faliste pojedyncze wiązania są standardowym sposobem reprezentowania nieznanej lub nieokreślonej stereochemii, bądź mieszaniny izomerów.
Projekcje i rysunki perspektywiczne
Dla szczegółowego przedstawienia trójwymiarowego układu atomów w przestrzeni, chemicy wykorzystują różne rodzaje projekcji i rysunków perspektywicznych.
Projekcja Newmana i rzut piły (Sawhorse projection)
Projekcja Newmana i rzut piły służą do przedstawiania konkretnych konformerów lub do rozróżniania stereochemii wicynalnej (atomów sąsiadujących). W obu przypadkach uwaga skupia się na dwóch konkretnych atomach węgla i wiązaniu, które je łączy. Różnica polega na nieco innej perspektywie: projekcja Newmana patrzy prosto wzdłuż interesującego wiązania, natomiast rzut piły patrzy na to samo wiązanie, ale z nieco ukośnego punktu widzenia. W projekcji Newmana, okrąg reprezentuje płaszczyznę prostopadłą do wiązania, rozróżniając podstawniki na przednim atomie węgla od podstawników na tylnym atomie węgla. W rzucie piły, przedni atom węgla jest zazwyczaj po lewej stronie i jest zawsze nieco niżej. Rzut piły jest bardzo podobny do wzoru szkieletowego i może nawet używać klinów zamiast linii do wskazania stereochemii cząsteczki. Obie projekcje mogą być użyte do stworzenia projekcji Fischera.
Konformacje cykloheksanu
Niektóre konformacje cykloheksanu i innych związków pierścieniowych mogą być przedstawione za pomocą standardowej konwencji. Na przykład, standardowa konformacja krzesłowa cykloheksanu obejmuje widok perspektywiczny nieco powyżej średniej płaszczyzny atomów węgla i wyraźnie wskazuje, które grupy są aksjalne (skierowane pionowo w górę lub w dół), a które ekwatorialne (prawie poziome, lekko nachylone w górę lub w dół). Wiązania z przodu mogą być wyróżnione mocniejszymi liniami lub klinami. Konformacje te przechodzą od krzesłowej do półkrzesłowej, łódkowej skręconej, łódkowej, ponownie łódkowej skręconej, półkrzesłowej i z powrotem do krzesłowej. Konformacje cykloheksanu mogą również służyć do pokazania energii potencjalnej obecnej na każdym etapie – konformacje krzesłowe mają najniższą energię, podczas gdy półkrzesłowe mają najwyższą. Występuje lokalne maksimum w konformacji łódkowej i lokalne minima w konformacjach łódkowych skręconych. Dodatkowo, konformacje cykloheksanu mogą być używane do wskazania, czy cząsteczka ma jakiekolwiek interakcje 1,3-diaksjalne, które są interakcjami sterycznymi między aksjalnymi podstawnikami na węglach 1, 3 i 5.

Projekcja Hawortha
Projekcja Hawortha jest używana głównie dla cukrów cyklicznych. Pozycje aksjalne i ekwatorialne nie są rozróżniane; zamiast tego, podstawniki są umieszczane bezpośrednio nad lub pod atomem pierścienia, do którego są przyłączone. Podstawniki wodorowe są zazwyczaj pomijane. Ważne jest jednak, aby pamiętać, że struktury pierścieniowe w projekcji Hawortha nie są płaskie. Dlatego Haworth nie oddaje pełnego kształtu 3D. Cieńsze wiązania na górze pierścienia oznaczają, że wiązania są dalej, a grubsze wiązania na dole pierścienia oznaczają koniec pierścienia, który jest bliżej obserwatora. Piranoza jest przedstawiana jako sześciokąt, a furanoza jako pięciokąt, zazwyczaj z atomem tlenu w prawym górnym rogu piranozy i w górnym centrum furanozy.
Projekcja Fischera
Projekcja Fischera jest najczęściej stosowana dla liniowych monosacharydów. Na każdym centrum chiralnym, pionowe linie wiązań są równoważne oznaczeniom stereochemicznym klinów przerywanych (skierowanych od obserwatora), podczas gdy poziome linie są równoważne klinom pełnym (skierowanym w stronę obserwatora). Projekcja ta jest nierealistyczna, ponieważ sacharyd nigdy nie przyjąłby tej wielokrotnie zaćmionej konformacji. Niemniej jednak, projekcja Fischera jest prostym sposobem przedstawiania wielu kolejnych centrów stereogenicznych, który nie wymaga ani nie implikuje żadnej wiedzy o rzeczywistej konformacji. Projekcja Fischera ogranicza cząsteczkę 3D do 2D, dlatego istnieją ograniczenia w zmianie konfiguracji centrów chiralnych. Projekcje Fischera są używane do określania konfiguracji R i S na chiralnym atomie węgla, zgodnie z regułami Cahna-Ingolda-Preloga. Jest to wygodny sposób reprezentowania i rozróżniania enancjomerów i diastereoizomerów.
Co wzór strukturalny nam mówi?
Wzór strukturalny dostarcza znacznie więcej informacji niż tylko lista atomów. Pozwala on zrozumieć:
- Rodzaj i liczbę wiązań: Czy atomy są połączone wiązaniami pojedynczymi, podwójnymi czy potrójnymi.
- Sekwencję atomów: Kolejność, w jakiej atomy są ze sobą połączone.
- Obecność wolnych par elektronowych: Niewiążące pary elektronów na atomach, które wpływają na kształt cząsteczki i jej reaktywność. Na przykład, atom azotu w amoniaku ma jedną wolną parę elektronów.
- Ładunki formalne: Obecność ładunków dodatnich lub ujemnych na poszczególnych atomach.
- Geometrię cząsteczki (w niektórych przypadkach): Choć nie wszystkie wzory to precyzyjnie oddają, niektóre, jak projekcje perspektywiczne czy wzory szkieletowe z klinami, pozwalają na zrozumienie trójwymiarowego kształtu.
- Grupy funkcyjne: Łatwo identyfikowalne są charakterystyczne grupy atomów, które nadają cząsteczce specyficzne właściwości chemiczne (np. grupa -OH w alkoholach, -COOH w kwasach karboksylowych).
Przykładowo, wzór grupy metylenowej (-CH2-) połączonej z grupą metylową (-CH3) i atomem azotu (-NH2) z wolną parą elektronów na azocie od razu mówi nam o obecności aminy. Inny przykład, atom węgla połączony z grupą metylową, podwójnym wiązaniem z atomem tlenu (grupa karbonylowa), a po drugiej stronie z kolejnym atomem tlenu, który następnie łączy się z grupą metylenową i metylową, wskazuje na obecność estru lub eteru z grupą karbonylową, w zależności od szczegółów wiązań.
Ograniczenia wzorów strukturalnych
Mimo swojej użyteczności, wzory strukturalne są uproszczonymi modelami i nie zawsze są w stanie w pełni oddać wszystkie aspekty struktur chemicznych. Oto niektóre z ich ograniczeń:
- Systemy dynamiczne i zdelokalizowane wiązania: Formalne wiązania mogą nie mieć zastosowania do systemów dynamicznych, takich jak wiązania zdelokalizowane, np. w związkach aromatycznych (jak benzen). Aromatyczność opiera się na konwencji, aby przedstawić wiązania, a różne style wzorów strukturalnych mogą przedstawiać aromatyczność na różne sposoby, co prowadzi do różnych przedstawień tego samego związku chemicznego.
- Charakter wiązań podwójnych: Formalne wiązania podwójne, gdzie gęstość elektronowa jest rozłożona poza formalnym wiązaniem, prowadzą do częściowego charakteru wiązania podwójnego i wolnej interkonwersji w temperaturze pokojowej. Wzory strukturalne często nie oddają tego subtelnego aspektu.
- Temperatura: Dla wszystkich efektów dynamicznych, temperatura wpływa na szybkość interkonwersji i może zmieniać sposób, w jaki struktura powinna być reprezentowana. Nie ma jawnej temperatury związanej ze wzorem strukturalnym, chociaż wielu zakłada, że byłaby to temperatura standardowa.
- Brak pełnego obrazu 3D: Chociaż niektóre projekcje (np. kliny) próbują oddać trójwymiarowość, żaden wzór 2D nie jest w stanie w pełni odtworzyć złożonej geometrii molekularnej w przestrzeni.
Tabela porównawcza typów wzorów strukturalnych
Poniższa tabela podsumowuje kluczowe cechy i zastosowania omówionych typów wzorów strukturalnych, ułatwiając ich zrozumienie i wybór odpowiedniego dla danej sytuacji.
| Typ wzoru | Główne cechy | Co pokazuje? | Zastosowanie | Ograniczenia |
|---|---|---|---|---|
| Ogólny wzór strukturalny | Wszystkie atomy i wiązania jawnie pokazane. | Kolejność połączeń atomów. | Podstawowe przedstawienie małych cząsteczek. | Niepraktyczny dla dużych, złożonych cząsteczek. |
| Wzór skondensowany | Tekstowy zapis, atomy H jawnie. Nawiasy dla grup. | Sekwencja atomów w linii. | Proste cząsteczki organiczne, pisemna komunikacja. | Brak jasnej geometrii 3D, wiązań C-C. |
| Wzór szkieletowy | C i H (na C) implikowane. Kliny dla stereochemii. | Podstawowa struktura węgla, stereochemia. | Złożone cząsteczki organiczne, cykliczne. | H na heteroatomach muszą być jawne. |
| Projekcja Newmana | Widok wzdłuż wiązania C-C. | Konformacje, wzajemne położenie podstawników. | Analiza konformacyjna, izomeria rotacyjna. | Tylko dla dwóch atomów węgla. |
| Projekcja Hawortha | Pierścień płaski, podstawniki nad/pod. | Struktura cyklicznych cukrów. | Sacharydy, nie oddaje pełnego 3D. | Nie oddaje rzeczywistego kształtu pierścienia. |
| Projekcja Fischera | Pionowe (od obserwatora), poziome (do obserwatora). | Stereochemia wielu centrów chiralnych. | Liniowe monosacharydy, aminokwasy. | Nierealistyczna konformacja, ograniczenia obrotu. |
Często zadawane pytania (FAQ)
- Czym różni się wzór sumaryczny od strukturalnego?
- Wzór sumaryczny (np. C2H6O) informuje jedynie o typie i liczbie atomów w cząsteczce. Wzór strukturalny (np. CH3CH2OH dla etanolu lub CH3OCH3 dla eteru dimetylowego) pokazuje, jak te atomy są ze sobą połączone i jakie tworzą wiązania, umożliwiając rozróżnienie izomerów.
- Czy wzory strukturalne zawsze pokazują elektrony?
- Nie zawsze. Wzory strukturalne, zwłaszcza szkieletowe, zazwyczaj pomijają wolne pary elektronowe i wszystkie elektrony. Jedynie w strukturach Lewisa lub w bardziej szczegółowych rysunkach elektronowych elektrony są jawnie przedstawione.
- Dlaczego atomy wodoru są często pomijane we wzorach szkieletowych?
- Atomy wodoru przyłączone do atomów węgla są pomijane dla uproszczenia i czytelności, zwłaszcza w złożonych cząsteczkach organicznych. Zakłada się, że każdy atom węgla tworzy cztery wiązania, więc liczbę brakujących wodorów można łatwo wywnioskować na podstawie liczby jawnie pokazanych wiązań z innymi atomami.
- Czy wzory strukturalne mogą pokazywać reakcje chemiczne?
- Same wzory strukturalne pokazują budowę cząsteczki, a nie przebieg reakcji. Jednak są one kluczowym narzędziem w mechanizmach reakcji, gdzie strzałki i inne oznaczenia są dodawane do wzorów, aby przedstawić ruch elektronów i tworzenie/rozrywanie wiązań.
- Jaka jest najważniejsza informacja, którą można uzyskać z wzoru strukturalnego?
- Najważniejszą informacją jest połączenie atomów i rodzaj wiązań między nimi. To decyduje o tożsamości chemicznej cząsteczki i jej podstawowych właściwościach. W przypadku izomerów, wzór sumaryczny jest taki sam, ale wzór strukturalny ujawnia różnice w połączeniach, które prowadzą do odmiennych właściwości.
Podsumowując, wzory strukturalne są niezastąpionym narzędziem w chemii, pozwalającym nam zajrzeć w głąb cząsteczek i zrozumieć ich skomplikowaną budowę. Od prostych wzorów liniowych po zaawansowane projekcje przestrzenne, każda forma ma swoje miejsce i cel, pomagając chemikom na całym świecie wizualizować, analizować i projektować nowe substancje. Opanowanie sztuki rysowania i interpretowania wzorów strukturalnych otwiera drzwi do głębszego poznania fascynującego świata chemii.
Zainteresował Cię artykuł Jak Tworzyć Wzory Strukturalne w Chemii?? Zajrzyj też do kategorii Chemia, znajdziesz tam więcej podobnych treści!
