28/04/2021
Zrozumienie budowy cząsteczki w przestrzeni jest absolutnie kluczowe w chemii. To nie tylko abstrakcyjne zagadnienie, ale fundament, który wpływa na niezliczone właściwości substancji – od jej stanu skupienia, przez reaktywność, aż po działanie biologiczne. Wyobraź sobie, że lek, który ma zbawienny wpływ na organizm, może stać się trucizną tylko dlatego, że jego atomy są inaczej ułożone w przestrzeni. Klasycznym i niestety tragicznym przykładem jest talidomid, lek, który występował w dwóch „wersjach przestrzennych”: jedna była skutecznym lekiem, druga zaś powodowała poważne wady płodu. Ten przykład dobitnie pokazuje, dlaczego chemicy tak wiele uwagi poświęcają stereochemii, czyli dziedzinie zajmującej się przestrzennym ułożeniem cząsteczek. Ale jak właściwie określić tę skomplikowaną geometrię? Na szczęście istnieją proste, a jednocześnie potężne narzędzia, takie jak teoria VSEPR i koncepcja hybrydyzacji, które pozwalają nam przewidzieć i zrozumieć kształt cząsteczek.

Teoria VSEPR: Odpychanie Par Elektronowych w Służbie Chemii
Jedną z najbardziej intuicyjnych i szeroko stosowanych metod przewidywania geometrii cząsteczek jest teoria VSEPR, czyli teoria odpychania par elektronowych powłoki walencyjnej (ang. Valence Shell Electron Pair Repulsion). Jej podstawowe założenie jest niezwykle proste i opiera się na naturze elektronów: ponieważ wszystkie elektrony (niezależnie od tego, czy tworzą wiązania, czy są wolnymi parami) mają taki sam, ujemny ładunek, będą się wzajemnie odpychać. Logiczne jest zatem, że w cząsteczce elektrony te będą dążyć do zajęcia pozycji, w której będą od siebie jak najdalej, minimalizując odpychanie. To właśnie to wzajemne odpychanie pomiędzy grupami elektronów na zewnętrznej powłoce atomu centralnego determinuje kształt całej cząsteczki.
Pamiętajmy, że VSEPR, choć skuteczna, nie jest teorią idealną i ma swoje ograniczenia. Elektrony są przecież przyciągane również przez dodatnio naładowane jądra atomowe, co jest kluczowe dla stabilności cząsteczki. Jednakże, w kontekście przewidywania kształtu, skupienie się na odpychaniu okazuje się zadziwiająco efektywne i wystarczające dla większości przypadków, zwłaszcza na poziomie edukacji średniej i akademickiej.
Czym są grupy elektronowe?
W teorii VSEPR nie liczymy każdego pojedynczego elektronu, lecz tzw. „grupy elektronowe”. Dlaczego? Ponieważ elektrony w wiązaniach (pojedynczych, podwójnych czy potrójnych) oraz wolne pary elektronowe zachowują się jak spójne jednostki, które zajmują określoną przestrzeń i wzajemnie się odpychają. Co ważne, zarówno wiązanie pojedyncze, podwójne, jak i potrójne, traktujemy jako jedną grupę elektronową, ponieważ elektrony w nich są zlokalizowane blisko siebie. Podobnie wolna para elektronowa stanowi jedną grupę. Liczba tych grup elektronowych wokół atomu centralnego jest kluczowa i często określa się ją mianem liczby przestrzennej (Lp).
Im więcej grup elektronowych wokół atomu centralnego, tym bardziej skomplikowana staje się geometria, ponieważ atomy muszą znaleźć kompromis, aby zmaksymalizować odległość między wszystkimi grupami. To właśnie liczba przestrzenna decyduje o podstawowym układzie przestrzennym cząsteczki.
Przykłady Geometrii Cząsteczek: Od Prostej Linii do Złożonego Tetraedru
Przyjrzyjmy się kilku podstawowym przykładom geometrii cząsteczek, zaczynając od tych, w których atom centralny nie posiada wolnych par elektronowych.
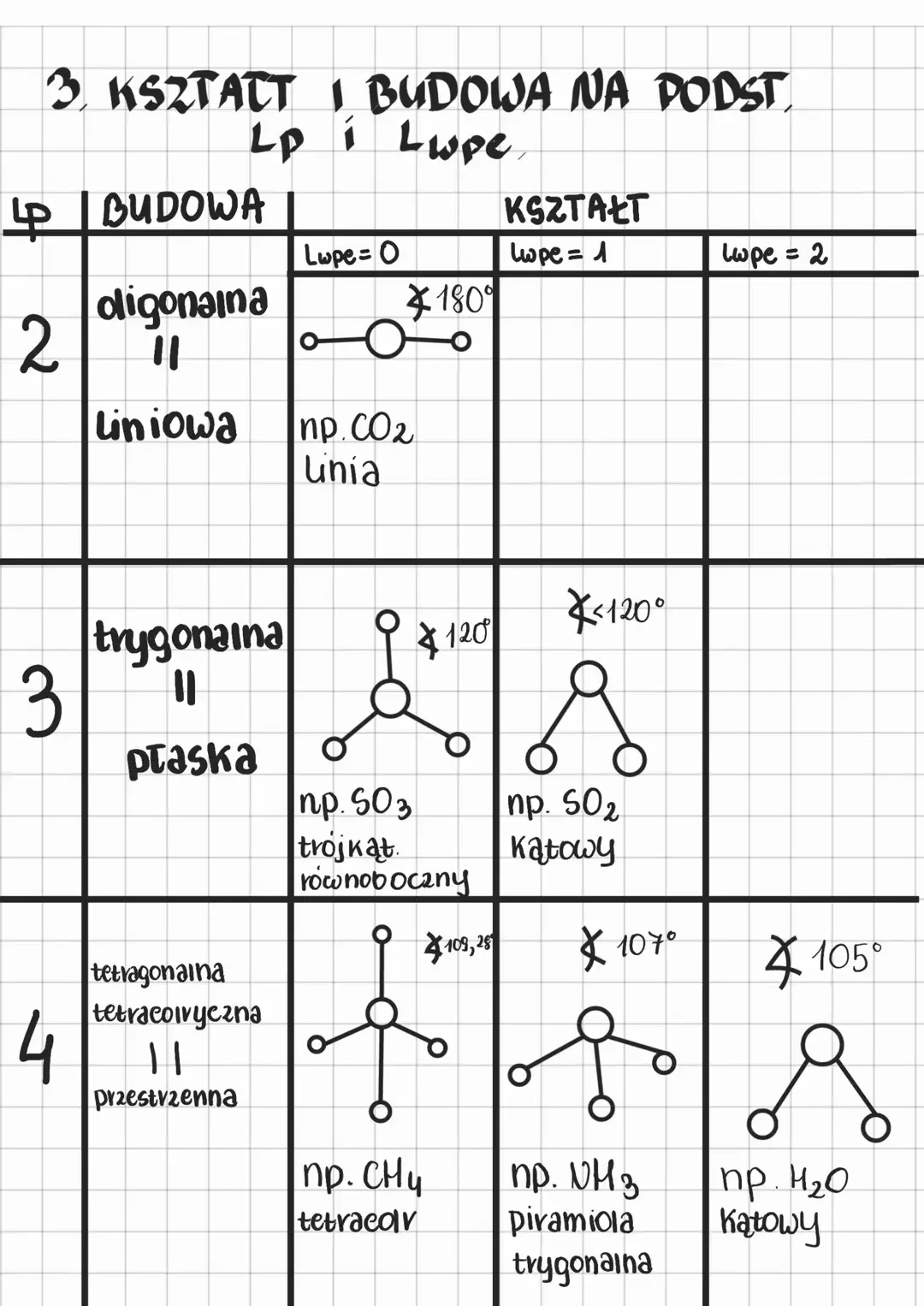
Dwie grupy elektronowe: Geometria liniowa
Jeśli wokół atomu centralnego znajdują się tylko dwie grupy elektronowe (np. w postaci dwóch wiązań), to najdalej od siebie znajdą się one, układając się w linii prostej. Kąt między wiązaniami wynosi wówczas 180 stopni. Przykładem takiej cząsteczki jest chlorek berylu (BeCl2) lub dwutlenek węgla (CO2). W przypadku CO2, mimo obecności dwóch wiązań podwójnych, każde z nich jest traktowane jako jedna grupa elektronowa, co prowadzi do liniowej struktury. Cząsteczki liniowe są płaskie, dwuwymiarowe.

Trzy grupy elektronowe: Geometria płaska trygonalna
Gdy wokół atomu centralnego znajdują się trzy grupy elektronowe, atomy układają się w płaskim trójkącie (trygonalnie płaskim), z atomem centralnym w środku. Kąty między wiązaniami wynoszą idealnie 120 stopni. Przykładem jest fluorek boru (BF3). Jest to również cząsteczka płaska, którą można łatwo narysować na kartce papieru. Warto jednak pamiętać, że w cząsteczkach, gdzie podstawniki nie są identyczne (np. formaldehyd, CH2O), kąty mogą ulec niewielkim zniekształceniom. W formaldehydzie, atom tlenu jest większy i posiada wolne pary elektronowe, co sprawia, że zajmuje więcej miejsca niż atomy wodoru, skutkując nieznacznie różnymi kątami.
Cztery grupy elektronowe: Geometria tetraedryczna
Cztery grupy elektronowe wokół atomu centralnego prowadzą do geometrii tetraedrycznej (czworościennej). W tym przypadku, atomy nie układają się już w płaszczyźnie, ale w trójwymiarowej bryle – tetraedrze. Kąty między wiązaniami wynoszą około 109.5 stopnia. Jest to optymalne ułożenie, które maksymalizuje odległość między czterema grupami w przestrzeni. Klasycznym przykładem jest cząsteczka metanu (CH4). Wyobrażenie sobie i narysowanie tetraedrycznej cząsteczki jest trudniejsze niż w przypadku struktur płaskich, dlatego często zaleca się budowanie modeli, aby lepiej zrozumieć ich trójwymiarową naturę.
Ważne jest, aby zrozumieć, że geometria cząsteczki zależy nie tylko od liczby wiązań, ale także od obecności wolnych par elektronowych na atomie centralnym. Wolne pary elektronowe zajmują więcej miejsca niż wiązania, co powoduje większe odpychanie i zniekształcenie idealnych kątów. Na przykład, cząsteczki z czterema grupami elektronowymi, ale z jedną lub dwiema wolnymi parami elektronowymi (jak amoniak czy woda), będą miały inną geometrię niż metan, pomimo tej samej liczby przestrzennej.
Szczegółowe Zasady i Przykłady Metody VSEPR
Metoda VSEPR (Valence Shell Electron Pair Repulsion) opiera się na ocenie wzajemnego oddziaływania par elektronowych tworzących wiązanie pomiędzy atomem centralnym (A) a ligandami (L) oraz wolnych par elektronowych (E) rozmieszczonych wokół atomu centralnego. Dla cząsteczki o ogólnym wzorze ALnEm, należy określić ilość par elektronowych tworzących wiązania (n) oraz ilość wolnych par elektronowych atomu centralnego (m). O geometrii cząsteczki decyduje konieczność zapewnienia możliwie największej odległości pomiędzy sąsiadującymi parami elektronowymi.
Reguły Określania Struktury Cząsteczek wg VSEPR:
- Pary elektronów tworzące wiązania (σ, π) oddziałują z wolnymi parami elektronów, zajmując położenia jak najbardziej oddalone od siebie.
- Najsilniej odpychają się dwie wolne pary elektronowe.
- Słabiej odpychają się wolna para elektronowa i para tworząca wiązanie.
- Najsłabiej odpychają się pary elektronowe tworzące wiązania.
- Siły odpychania par elektronowych wiązań zmniejszają się w miarę wzrostu elektroujemności ligandów.
- Siły odpychania wolnych par elektronowych zmniejszają się w miarę wzrostu promienia atomu centralnego.
Ustalanie Struktury Przestrzennej Krok po Kroku:
- Określenie atomu centralnego i ligandów (wzór cząsteczki).
- Określenie liczby elektronów walencyjnych atomu centralnego.
- Określenie liczby elektronów wykorzystywanych do utworzenia wiązań σ.
- Określenie liczby wolnych par elektronowych na atomie centralnym.
- Określenie liczby elektronów wykorzystywanych do utworzenia wiązań typu π (jeśli występują).
- Określenie łącznej liczby grup elektronowych (n + m).
- Określenie typu struktury i geometrii cząsteczki na podstawie liczby grup elektronowych i wolnych par.
Przykłady Zastosowania VSEPR:
Poniżej przedstawiono kilka przykładów, które ilustrują zastosowanie reguł VSEPR do określania geometrii cząsteczek:
Przykład 1: BCl3
- Atom centralny: Bor (B).
- Liczba elektronów walencyjnych boru: 3.
- Liczba wiązań z ligandami (Cl): 3.
- Liczba wolnych par elektronowych na borze: 0.
- Łączna liczba grup elektronowych (n + m): 3 + 0 = 3.
- Typ struktury: AL3.
- Geometria cząsteczki: Płaska trygonalna (trójkąt równoboczny, kąty między wiązaniami B-Cl wynoszą 120°).
Przykład 2: PCl3
- Atom centralny: Fosfor (P).
- Liczba elektronów walencyjnych fosforu: 5.
- Liczba wiązań z ligandami (Cl): 3.
- Liczba wolnych par elektronowych na fosforze: (5 - 3) / 2 = 1.
- Łączna liczba grup elektronowych (n + m): 3 + 1 = 4.
- Typ struktury: AL3E.
- Geometria cząsteczki: Piramida trygonalna (ze względu na obecność wolnej pary elektronowej, kąty między wiązaniami P-Cl są mniejsze niż idealne 109.5°).
Przykład 3: SF4
- Atom centralny: Siarka (S).
- Liczba elektronów walencyjnych siarki: 6.
- Liczba wiązań z ligandami (F): 4.
- Liczba wolnych par elektronowych na siarce: (6 - 4) / 2 = 1.
- Łączna liczba grup elektronowych (n + m): 4 + 1 = 5.
- Typ struktury: AL4E.
- Geometria cząsteczki: Kształt huśtawki (pochodna bipiramidy trygonalnej, gdzie wolna para zajmuje jedno z miejsc).
Przykład 4: PF6-
- Atom centralny: Fosfor (P).
- Liczba elektronów walencyjnych fosforu: 5.
- Liczba wiązań z ligandami (F): 6.
- Liczba wolnych par elektronowych na fosforze: 0.
- Ładunek anionu: -1 (dodatkowy elektron).
- Liczba elektronów fosforu tworzących wiązanie: 5 (z własnych) + 1 (z ładunku) = 6.
- Łączna liczba grup elektronowych (n + m): 6 + 0 = 6.
- Typ struktury: AL6.
- Geometria cząsteczki: Oktaedryczna (kąty między wiązaniami P-F wynoszą 90°).
Hybrydyzacja: Mieszanie Orbitali Atomowych
Obok teorii VSEPR, koncepcja hybrydyzacji jest kolejnym potężnym narzędziem, które pomaga nam zrozumieć i przewidzieć przestrzenną strukturę cząsteczek. Hybrydyzacja polega na tworzeniu superpozycji (mieszaniu) orbitali atomowych należących do tej samej powłoki energetycznej. Głównym celem hybrydyzacji jest wyjaśnienie powstawania równocennych energetycznie wiązań kowalencyjnych, które często obserwujemy w rzeczywistości, a których nie można by wytłumaczyć, biorąc pod uwagę tylko „czyste” orbitale atomowe (s, p, d).
Typy Hybrydyzacji i Ich Związek z Geometrią:
Atom zawierający tylko orbitale s i p w swojej powłoce walencyjnej może utworzyć trzy podstawowe typy orbitali zhybrydyzowanych:
- Hybrydyzacja sp: Odpowiada cząsteczkom o geometrii liniowej. Powstają dwa równocenne orbitale hybrydowe, skierowane w przeciwnych kierunkach (np. w etynie).
- Hybrydyzacja sp2: Odpowiada cząsteczkom o geometrii płaskiej trygonalnej. Powstają trzy równocenne orbitale hybrydowe, skierowane ku narożom trójkąta równobocznego (np. w etenie).
- Hybrydyzacja sp3: Odpowiada cząsteczkom o geometrii tetraedrycznej. Powstają cztery równocenne orbitale hybrydowe, skierowane ku narożom czworościanu (np. w metanie).
Z udziałem orbitali d mogą powstać bardziej złożone typy orbitali zhybrydyzowanych, które tłumaczą geometrie takie jak bipiramida trygonalna, oktaedr czy kwadrat płaski:
- Hybrydyzacja sp3d2 (lub d2sp3): Geometria oktaedryczna, gdzie powstaje sześć równoważnych orbitali skierowanych ku narożom ośmiościanu.
- Hybrydyzacja sp3d (lub dsp3): Geometria bipiramidalna trygonalna, gdzie powstaje pięć orbitali skierowanych ku narożom podwójnej piramidy trygonalnej.
- Hybrydyzacja sp2d: Geometria kwadratowa płaska, gdzie powstają cztery równoważne orbitale skierowane ku wierzchołkom kwadratu w płaszczyźnie.
Przykłady Hybrydyzacji:
Przykład 1: BCl3 i hybrydyzacja sp2
Atom boru w stanie podstawowym ma konfigurację elektronową 1s22s22p1. Aby utworzyć trzy równocenne wiązania z atomami chloru, jeden elektron z orbitalu 2s zostaje wzbudzony na orbital 2p. Następnie jeden orbital 2s i dwa orbitale 2p ulegają hybrydyzacji, tworząc trzy orbitale zhybrydyzowane sp2. Każdy z tych orbitali jest obsadzony jednym elektronem i nakłada się z orbitalem 3p atomu chloru, tworząc trzy wiązania σ. W rezultacie cząsteczka BCl3 ma strukturę płaską trygonalną.
Przykład 2: NH3 i hybrydyzacja sp3
Atom azotu w stanie podstawowym ma konfigurację elektronową 1s22s22p3. W cząsteczce amoniaku (NH3), orbital 2s i trzy orbitale 2p azotu ulegają hybrydyzacji, tworząc cztery orbitale zhybrydyzowane sp3. Dwa elektrony zajmują jeden z tych orbitali jako wolna para elektronowa, natomiast pozostałe trzy elektrony na trzech orbitalach sp3 tworzą wiązania σ z atomami wodoru. Mimo że liczba przestrzenna wynosi 4 (trzy wiązania i jedna wolna para), obecność wolnej pary elektronowej, która zajmuje więcej miejsca i silniej odpycha, powoduje, że geometria cząsteczki amoniaku jest piramidalna (pochodna tetraedru), a kąty wiązań są mniejsze niż idealne 109.5°.

Przykład 3: PCl5 i hybrydyzacja dsp3 (lub sp3d)
Atom fosforu w PCl5 ma konfigurację elektronową 1s22s22p63s23p3. W tym przypadku, oprócz orbitali s i p, do hybrydyzacji włączają się również orbitale d. Jeden orbital 3s, trzy orbitale 3p i jeden orbital 3d ulegają hybrydyzacji, tworząc pięć orbitali zhybrydyzowanych dsp3. Te pięć orbitali jest obsadzonych pięcioma elektronami i tworzy pięć wiązań σ z atomami chloru, skierowanych ku narożom podwójnej piramidy trygonalnej.
Eten i Jego Wyjątkowa Geometria: Przykład Zastosowania Hybrydyzacji sp2
Eten (C2H4) jest najprostszym alkenem i stanowi doskonały przykład zastosowania koncepcji hybrydyzacji do zrozumienia geometrii cząsteczki z wiązaniem podwójnym. W alkenach, w przeciwieństwie do alkanów, występuje co najmniej jedno wiązanie podwójne pomiędzy atomami węgla (C=C). Ta cecha fundamentalnie zmienia ich budowę przestrzenną i właściwości.
W etenie, oba atomy węgla ulegają hybrydyzacji sp2. Oznacza to, że każdy atom węgla tworzy trzy równocenne orbitale hybrydowe sp2 oraz pozostaje mu jeden niezhybrydyzowany orbital p. Trzy orbitale sp2 leżą w jednej płaszczyźnie, skierowane w stronę naroży trójkąta równobocznego, a kąty między nimi wynoszą idealnie 120°. Cząsteczka etenu jest zatem płaska. Wiązania C-H w etenie są wiązaniami typu sigma (σ) powstałymi z nakładania się orbitali sp2 węgla i orbitali s wodoru.
Wiązanie podwójne C=C w etenie składa się z dwóch części: jednego wiązania sigma (σ), powstałego z nakładania się orbitali sp2 obu atomów węgla, oraz jednego wiązania pi (π). Wiązanie pi powstaje w wyniku bocznego nakładania się niezhybrydyzowanych orbitali p, które leżą prostopadle do płaszczyzny utworzonej przez orbitale sp2. To wiązanie pi jest słabsze i bardziej reaktywne niż wiązanie sigma, co jest charakterystyczną cechą alkenów i odpowiada za ich zdolność do reakcji addycji.
Tabela poniżej przedstawia fragment szeregu homologicznego alkenów, ilustrując zmianę liczby atomów węgla i odpowiadających im wzorów oraz nazw, podkreślając powtarzalność strukturalną:
| Liczba atomów węgla w łańcuchu | Wzór alkanu | Nazwa alkanu | Wzór alkenu | Nazwa alkenu |
|---|---|---|---|---|
| 2 | C2H6 | Etan | C2H4 | Eten |
| 3 | C3H8 | Propan | C3H6 | Propen |
| 4 | C4H10 | Butan | C4H8 | Buten |
| 5 | C5H12 | Pentan | C5H10 | Penten |
| 6 | C6H14 | Heksan | C6H12 | Heksen |
Podsumowując, każdy alken posiada wiązanie podwójne pi (π), przy którym tworzone są płaskie struktury. Atomy węgla posiadają hybrydyzację sp2, charakteryzującą się budową trygonalną. Rotacja występuje wyłącznie dookoła wiązań pojedynczych, ale jest zablokowana w przypadku wiązania C=C, co prowadzi do zjawiska izomerii geometrycznej (cis-trans).
Geometria Cząsteczek: Podsumowanie i Wnioski
Zrozumienie i przewidywanie geometrii cząsteczek jest fundamentalnym elementem chemii, mającym wpływ na niezliczone właściwości substancji. Teoria VSEPR i koncepcja hybrydyzacji to dwa komplementarne narzędzia, które pozwalają nam odszyfrować przestrzenny układ atomów i elektronów. Dzięki nim możemy nie tylko przewidzieć kształt cząsteczki, ale także wyjaśnić jej reaktywność, polarność, a nawet działanie biologiczne.
Pamiętajmy, że teoria VSEPR opiera się na prostym założeniu odpychania się grup elektronowych, dążących do jak największej odległości od siebie. Hybrydyzacja natomiast tłumaczy, w jaki sposób orbitale atomowe mieszają się, tworząc nowe, równocenne orbitale, które umożliwiają powstawanie stabilnych wiązań i określają podstawowy kształt wokół atomu centralnego. Obie te koncepcje, stosowane razem, dają nam potężne narzędzie do analizy i projektowania molekuł.
Często Zadawane Pytania (FAQ)
Czym jest VSEPR?
VSEPR (Valence Shell Electron Pair Repulsion) to teoria przewidywania geometrii cząsteczek, która zakłada, że pary elektronowe (zarówno wiążące, jak i wolne) w powłoce walencyjnej atomu centralnego odpychają się wzajemnie, dążąc do jak największej odległości od siebie, co determinuje trójwymiarowy kształt cząsteczki.
Jakie są ograniczenia teorii VSEPR?
Choć VSEPR jest bardzo skuteczna, ma swoje ograniczenia. Nie zawsze precyzyjnie przewiduje kąty wiązań w przypadku skomplikowanych cząsteczek, zwłaszcza tych z atomami o dużej liczbie elektronów walencyjnych lub w związkach metali przejściowych. Jest to model uproszczony, który działa zaskakująco dobrze z „niewłaściwych” powodów, ale dla większości typowych zastosowań jest w zupełności wystarczający.
Czym jest hybrydyzacja i dlaczego jest ważna?
Hybrydyzacja to proces mieszania się orbitali atomowych o różnej energii i kształcie w celu utworzenia nowych, równocennych orbitali zhybrydyzowanych. Jest ważna, ponieważ pozwala wyjaśnić tworzenie równocennych wiązań kowalencyjnych oraz przewidzieć przestrzenną strukturę cząsteczek, której nie można by wytłumaczyć na podstawie samych „czystych” orbitali atomowych.
Czy eten ulega hybrydyzacji?
Tak, atomy węgla w cząsteczce etenu (C2H4) ulegają hybrydyzacji typu sp2. Dzięki temu cząsteczka etenu jest płaska, a kąty między wiązaniami wokół każdego atomu węgla wynoszą około 120 stopni.
Dlaczego geometria cząsteczki jest tak ważna?
Geometria cząsteczki jest fundamentalna, ponieważ wpływa na jej właściwości fizyczne (np. temperaturę wrzenia, rozpuszczalność), chemiczne (np. reaktywność, zdolność do tworzenia wiązań) oraz biologiczne (np. sposób oddziaływania leków z białkami w organizmie, jak w przypadku modelu klucza i zamka).
Jak rysować cząsteczki trójwymiarowe na płaskiej kartce?
Do przedstawiania cząsteczek trójwymiarowych na dwuwymiarowej płaszczyźnie używa się specjalnych konwencji. Wiązania wychodzące „do przodu” (w stronę obserwatora) są często przedstawiane jako kliny pogrubione, natomiast wiązania idące „do tyłu” (od obserwatora) jako linie przerywane lub kliny kreskowane. Wiązania leżące w płaszczyźnie kartki są rysowane jako zwykłe linie. Aby lepiej zrozumieć te struktury, zawsze zaleca się budowanie fizycznych modeli cząsteczek.
Zainteresował Cię artykuł Geometria Cząsteczek: Klucz do Świata Chemii", "kategoria": "Chemia? Zajrzyj też do kategorii Edukacja, znajdziesz tam więcej podobnych treści!
