23/12/2025
Wszystko wokół nas – od skał, przez metale, po lód w szklance – składa się z atomów i cząsteczek. Ale to, w jaki sposób te maleńkie elementy są ze sobą połączone i ułożone w przestrzeni, decyduje o unikalnych właściwościach każdego materiału. Wiele substancji, zwłaszcza w stanie stałym, przyjmuje formę uporządkowanych struktur, znanych jako ciała krystaliczne. Zrozumienie ich budowy to klucz do poznania tajemnic materii i projektowania nowych, innowacyjnych materiałów. Ale czym dokładnie jest ta tajemnicza budowa krystaliczna i dlaczego jest tak fundamentalna dla nauki i technologii?
Czym jest Ciało Krystaliczne?
Ciało krystaliczne to nic innego jak ciało stałe, w którym atomy, cząsteczki lub jony są ułożone w ściśle uporządkowany, powtarzalny wzór, rozciągający się we wszystkich trzech wymiarach przestrzennych. Wyobraź sobie idealnie ułożone cegły w ścianie – każda na swoim miejscu, tworząc regularny, przewidywalny schemat. Podobnie jest w kryształach, gdzie cząsteczki zajmują ściśle określone miejsca, zwane węzłami sieci krystalicznej. W tych węzłach cząsteczki nie są statyczne; mogą jedynie drgać wokół swoich położeń równowagi, co jest charakterystyczne dla stanu stałego.
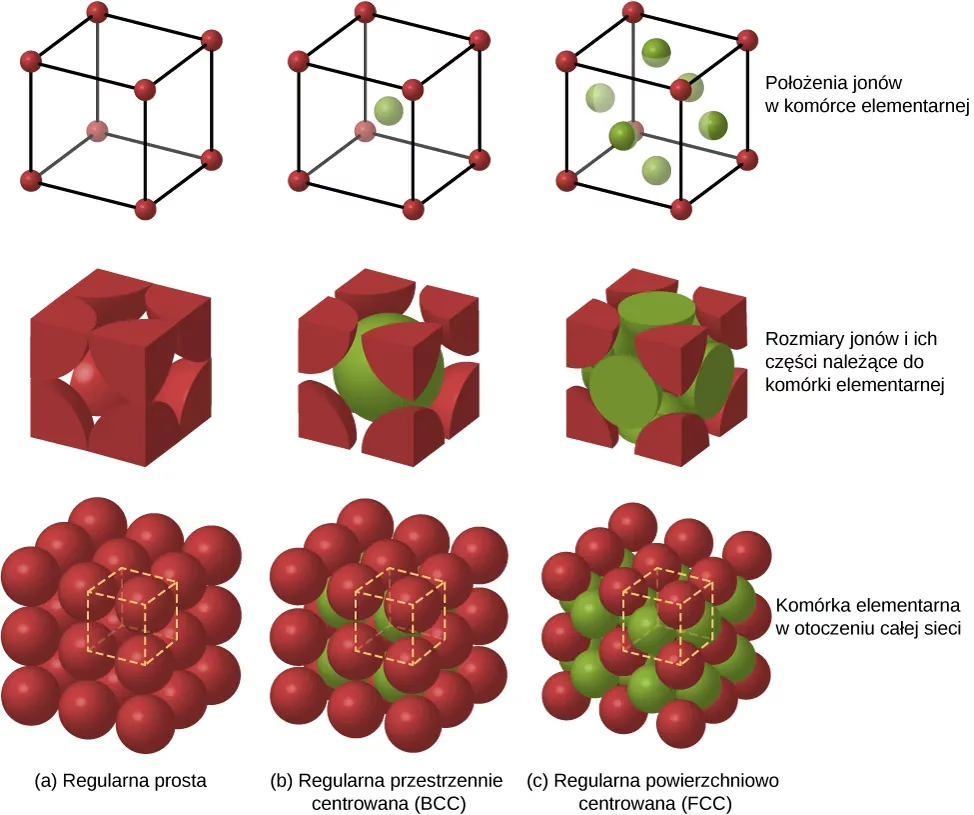
Każdy kryształ zbudowany jest z nieskończenie wielu powtarzających się jednostek, nazywanych komórkami elementarnymi. To właśnie kształt i symetria tych komórek decydują o tym, do którego z siedmiu układów krystalograficznych zaliczymy dany kryształ. Ta regularność i uporządkowanie na poziomie atomowym przekładają się na makroskopowe właściwości kryształów, takie jak ich kształt, twardość, temperatura topnienia czy zdolność do przewodzenia prądu elektrycznego.
Typy Wiązań – Klucz do Zrozumienia Kryształów
Właściwości fizyczne i chemiczne kryształów są bezpośrednio związane z rodzajem wiązań chemicznych, które utrzymują atomy, cząsteczki lub jony razem w ich uporządkowanej strukturze. Wyróżniamy cztery główne typy kryształów, klasyfikowane właśnie na podstawie dominujących sił wiążących:
- Kryształy kowalencyjne
- Kryształy molekularne
- Kryształy jonowe
- Kryształy metaliczne
Każdy z tych typów charakteryzuje się unikalnym zestawem cech, które czynią go przydatnym w różnych zastosowaniach – od biżuterii, przez elektronikę, aż po materiały budowlane.
Kryształy Kowalencyjne: Siła i Twardość
Kryształy kowalencyjne to prawdziwi giganci wytrzymałości w świecie materiałów. Składają się z atomów połączonych niezwykle mocnymi wiązaniami kowalencyjnymi, tworzącymi rozległe, trójwymiarowe sieci. Każdy atom jest związany z sąsiednimi atomami w sposób, który tworzy jedną, olbrzymią „cząsteczkę”. Ta struktura nadaje im wyjątkową stabilność.
Przykłady: Najbardziej znanym przykładem jest diament – najtwardszy znany naturalny minerał. Inne to krzem (podstawa przemysłu elektronicznego) oraz kwarc (dwutlenek krzemu, SiO2), powszechny składnik piasku i wielu skał.
Właściwości:
- Wysoka twardość: Wynika z siły i kierunkowości wiązań kowalencyjnych. Diament jest tego najlepszym przykładem.
- Wysokie temperatury topnienia i wrzenia: Aby stopić lub odparować taki kryształ, trzeba dostarczyć ogromną ilość energii do zerwania licznych, mocnych wiązań.
- Brak przewodnictwa elektrycznego: Elektrony są ściśle zlokalizowane w wiązaniach, nie ma swobodnych nośników ładunku. Krzem jest półprzewodnikiem, ale jego przewodnictwo wymaga domieszkowania lub odpowiedniej temperatury.
- Kruche: Pomimo swojej twardości, kryształy kowalencyjne mogą pękać pod wpływem silnych uderzeń, ponieważ nie wykazują plastyczności – wiązania są zbyt sztywne, by atomy mogły się przesuwać względem siebie bez zerwania.
Kryształy Molekularne: Delikatne Piękno
W przeciwieństwie do kryształów kowalencyjnych, kryształy molekularne składają się z odrębnych cząsteczek, które są ze sobą połączone znacznie słabszymi siłami międzycząsteczkowymi, takimi jak siły van der Waalsa czy wiązania wodorowe. Same cząsteczki mogą być bardzo stabilne (posiadać mocne wiązania wewnątrzcząsteczkowe), ale to słabe oddziaływania między nimi decydują o właściwościach całego kryształu.
Przykłady: Typowe przykłady to jod (I2), lód (H2O), dwutlenek węgla w stanie stałym (znany jako suchy lód, CO2) oraz wiele organicznych związków, takich jak naftalen czy cukier.
Właściwości:
- Niska twardość: Ponieważ siły oddziaływań międzycząsteczkowych są znacznie słabsze niż wiązania kowalencyjne czy jonowe, kryształy molekularne są miękkie i łatwe do zarysowania.
- Niskie temperatury topnienia i wrzenia: Wymagana jest niewielka energia do pokonania słabych sił międzycząsteczkowych, co sprawia, że łatwo przechodzą w stan ciekły lub gazowy. Wiele z nich topi się już w temperaturze pokojowej lub niewiele wyższej.
- Brak przewodnictwa elektrycznego: Podobnie jak w kryształach kowalencyjnych, nie zawierają swobodnych nośników ładunku (elektronów ani jonów).
- Często lotne: Wiele kryształów molekularnych łatwo sublimuje, czyli przechodzi bezpośrednio ze stanu stałego w gazowy, np. jod czy suchy lód.
Kryształy Jonowe: Porządek i Przewodnictwo
Kryształy jonowe to fascynujące struktury, w których budulcem są kationy (jony dodatnie) i aniony (jony ujemne), połączone silnymi oddziaływaniami elektrostatycznymi, czyli wiązaniami jonowymi. Te siły są silne i bezkierunkowe, co prowadzi do tworzenia regularnych sieci, w których każdy jon jest otoczony jonami o przeciwnym ładunku.
Przykłady: Najbardziej znany to chlorek sodu (NaCl), czyli sól kuchenna. Inne przykłady to fluorek wapnia (CaF2) czy azotan(V) potasu (KNO3).
Właściwości:
- Twarde i kruche: Silne oddziaływania jonowe utrzymują strukturę w ryzach, co czyni je twardymi. Jednakże, ze względu na sztywność sieci i odpychanie ładunków jednoimiennych przy przesunięciu warstw, kryształy jonowe mogą pękać pod wpływem sił mechanicznych.
- Wysokie temperatury topnienia: Wynika to z dużej energii potrzebnej do pokonania silnych sił elektrostatycznych między jonami.
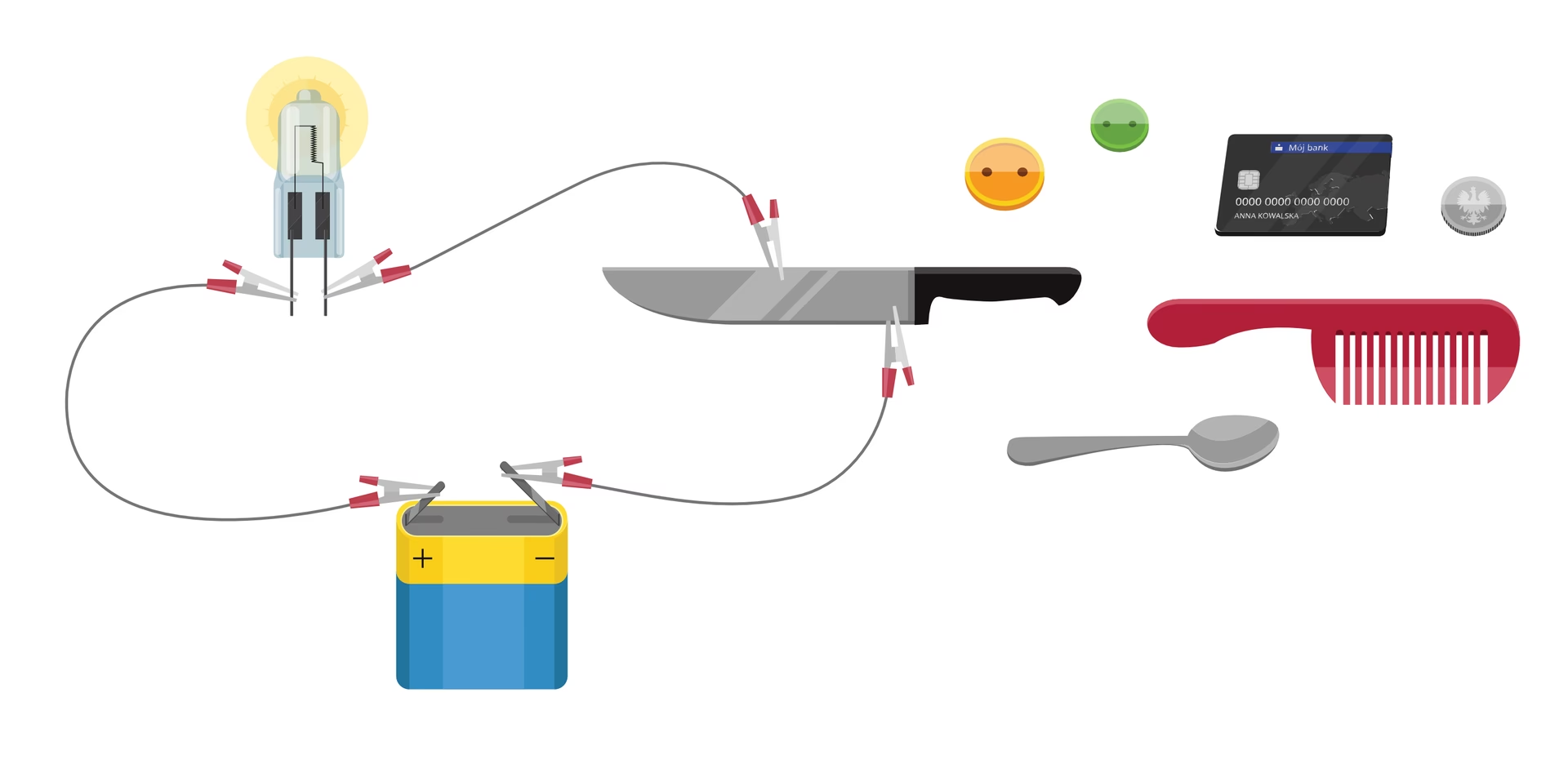
- Przewodnictwo elektryczne: Tu pojawia się interesująca cecha. Kryształy jonowe nie przewodzą prądu elektrycznego w stanie stałym, ponieważ jony są unieruchomione w sieci i nie mogą się swobodnie przemieszczać. Jednakże, gdy zostaną stopione lub rozpuszczone w odpowiednim rozpuszczalniku (np. wodzie), jony stają się swobodne i mogą przenosić ładunek, co umożliwia przewodzenie prądu.
- Często dobrze rozpuszczalne w wodzie: Wiele kryształów jonowych, jak NaCl, łatwo rozpuszcza się w wodzie. Dzieje się tak, ponieważ polarne cząsteczki wody są w stanie oddziaływać z jonami i skutecznie je otaczać, rozrywając sieć krystaliczną.
Kryształy Metaliczne: Swoboda Elektronów
Kryształy metaliczne to wyjątkowa kategoria, która charakteryzuje się obecnością kationów metali zanurzonych w „chmurze” swobodnie poruszających się elektronów walencyjnych. Te zdelokalizowane elektrony nie są związane z konkretnym atomem, lecz swobodnie przemieszczają się po całej objętości kryształu. To właśnie ta „chmura elektronowa” odpowiada za unikalne właściwości metali.
Przykłady: Wszystkie metale, takie jak żelazo (Fe), miedź (Cu), aluminium (Al), a także ich stopy (np. stal, brąz).

Właściwości:
- Dobre przewodnictwo elektryczne i cieplne: Jest to bezpośrednia konsekwencja swobodnego ruchu elektronów. Mogą one łatwo przenosić ładunek elektryczny i energię cieplną przez cały materiał.
- Plastyczność i kowalność: Metale można zginać, kuć, walcować i ciągnąć bez ich łamania. Kiedy warstwy atomów są przesuwane względem siebie, „chmura elektronowa” dostosowuje się, utrzymując wiązania i zapobiegając rozpadowi struktury.
- Połysk metaliczny: Swobodne elektrony łatwo absorbują i emitują fotony światła, co nadaje metalom ich charakterystyczny, błyszczący wygląd.
- Zróżnicowane temperatury topnienia: Od bardzo wysokich (np. wolfram, W) po niskie (np. rtęć, Hg, która jest cieczą w temperaturze pokojowej). Siła wiązań metalicznych jest zmienna i zależy od liczby elektronów walencyjnych i rozmiaru atomów.
Porównanie Właściwości Różnych Typów Kryształów
Aby lepiej zrozumieć różnice między poszczególnymi typami kryształów, warto je zestawić w tabeli, która uwypukli ich kluczowe cechy:
| Cecha | Kryształy Kowalencyjne | Kryształy Molekularne | Kryształy Jonowe | Kryształy Metaliczne |
|---|---|---|---|---|
| Elementy budulcowe | Atomy | Cząsteczki | Kationy i aniony | Kationy metali i zdelokalizowane elektrony |
| Rodzaj wiązania | Mocne wiązania kowalencyjne | Słabe siły międzycząsteczkowe (van der Waalsa, wiązania wodorowe) | Silne oddziaływania elektrostatyczne (jonowe) | Wiązania metaliczne (chmura elektronowa) |
| Twardość | Bardzo wysoka | Niska | Twarde | Zróżnicowana (od miękkich po twarde) |
| Temperatura topnienia | Bardzo wysoka | Niska | Wysoka | Zróżnicowana |
| Przewodnictwo elektryczne | Brak (izolatory) | Brak (izolatory) | Brak w stałym stanie; dobre w roztworach/stopach | Dobre (przewodniki) |
| Kruchość/Plastyczność | Kruche | Kruche | Kruche | Plastyczne, kowalne |
| Rozpuszczalność w wodzie | Niska/Brak | Niska/Brak (chyba że polarne) | Często dobra | Brak |
| Przykłady | Diament, Krzem, Kwarc | Jod, Lód, Suchy lód | NaCl, CaF2, KNO3 | Żelazo, Miedź, Aluminium |
Najczęściej Zadawane Pytania (FAQ)
Jakie substancje tworzą kryształy jonowe, a jakie molekularne?
Rozpoznanie typu kryształu na podstawie wzoru chemicznego wymaga znajomości podstawowych zasad tworzenia wiązań. Kryształy jonowe powstają z połączenia metalu z niemetalem (lub grupą atomów o ładunku, np. jony wieloatomowe), tworząc jony. Kryształy molekularne składają się z cząsteczek, czyli grup atomów połączonych wiązaniami kowalencyjnymi, które z kolei oddziałują ze sobą słabymi siłami międzycząsteczkowymi. Poniżej przedstawiamy przykłady z podziałem:
- Kryształy jonowe: NaCl (chlorek sodu), K2O (tlenek potasu). Są to związki, gdzie występują wyraźne jony.
- Kryształy molekularne: S8 (siarka rombowa), H2O (lód), I2 (jod). Są to substancje zbudowane z pojedynczych, dyskretnych cząsteczek.
- Warto zaznaczyć, że Zn (cynk) i Cu (miedź) to metale, więc tworzą kryształy metaliczne, natomiast SiO2 (dwutlenek krzemu, kwarc) to kryształ kowalencyjny.
Dlaczego kryształy jonowe nie przewodzą prądu w stanie stałym, ale przewodzą po stopieniu?
To bardzo ważne pytanie, które często pojawia się w kontekście właściwości materiałów. Kryształy jonowe, takie jak chlorek sodu, w stanie stałym mają jony (kationy i aniony) ściśle związane w sztywnej sieci krystalicznej. Jony te są unieruchomione w swoich węzłach i choć posiadają ładunek, nie mogą się swobodnie przemieszczać. Aby prąd elektryczny mógł płynąć, potrzebne są swobodne nośniki ładunku, które mogą się poruszać.
Sytuacja zmienia się diametralnie, gdy kryształ jonowy zostanie stopiony. Wysoka temperatura dostarcza wystarczającej energii do rozerwania wiązań jonowych i uwolnienia jonów z sieci. W stopionym stanie, jony stają się ruchliwe i mogą swobodnie przemieszczać się w polu elektrycznym, pełniąc rolę nośników ładunku. Dzięki temu stopione związki jonowe doskonale przewodzą prąd elektryczny. Podobnie dzieje się, gdy związek jonowy rozpuści się w rozpuszczalniku polarnym, takim jak woda – jony dysocjują i stają się ruchliwe.
Jak rozpoznać typ kryształu na podstawie jego właściwości przewodnictwa?
Przewodnictwo elektryczne jest kluczową cechą, która pozwala odróżnić typy kryształów. Poniżej przedstawiono schemat rozpoznawania na podstawie dwóch substancji, A i B, o wysokich temperaturach topnienia:
- Substancja A: Przewodzi prąd elektryczny w ciele stałym. To jednoznacznie wskazuje na obecność swobodnie poruszających się elektronów. Zatem substancja A tworzy kryształ metaliczny. Typowe przykłady to miedź, żelazo, aluminium.
- Substancja B: Nie przewodzi prądu w ciele stałym, ale przewodzi go po stopieniu. To klasyczny przypadek substancji, w której nośniki ładunku (jony) są unieruchomione w sieci w stanie stałym, ale stają się ruchliwe po przejściu w stan ciekły. Zatem substancja B tworzy kryształ jonowy. Przykładem jest chlorek sodu czy tlenek magnezu.
Kryształy kowalencyjne i molekularne zazwyczaj nie przewodzą prądu elektrycznego ani w stanie stałym, ani po stopieniu (o ile nie ulegają rozkładowi), ponieważ nie posiadają swobodnych elektronów ani ruchomych jonów.
Podsumowanie
Budowa krystaliczna to niezwykłe zjawisko, które leży u podstaw właściwości niezliczonych materiałów. Od twardości diamentu, przez plastyczność miedzi, aż po zdolność soli do rozpuszczania się w wodzie – wszystko to jest determinowane przez precyzyjne ułożenie atomów, cząsteczek czy jonów oraz rodzaj wiązań, które je łączą. Zrozumienie tych podstawowych zasad pozwala nie tylko docenić złożoność otaczającego nas świata, ale także projektować nowe materiały o pożądanych cechach, co ma ogromne znaczenie dla postępu technologicznego i naukowego. Niezależnie od tego, czy patrzymy na kryształ soli, czy na zaawansowany półprzewodnik, wszędzie dostrzeżemy ten sam, fundamentalny porządek – porządek krystaliczny.
Zainteresował Cię artykuł Budowa Krystaliczna: Świat Uporządkowanych Struktur", "kategoria": "Nauka? Zajrzyj też do kategorii Edukacja, znajdziesz tam więcej podobnych treści!

