03/09/2022
W 1911 roku Ernest Rutherford opublikował wyniki swoich przełomowych badań, które dowiodły, że atom zbudowany jest z niezwykle małego, lecz niezwykle gęstego jądra, w którym skupiona jest niemal cała masa atomu. To jądro, otoczone przez powłokę elektronową, sprawia, że atom jako całość pozostaje elektrycznie obojętny. To odkrycie zapoczątkowało nową, pasjonującą gałąź fizyki – fizykę jądrową, stawiającą sobie za cel dogłębne poznanie tego nowo odkrytego, fundamentalnego elementu materii. Ale co tak naprawdę znajduje się w tym maleńkim, potężnym jądrze?
Od Protonów do Nukleonów: Ewolucja Zrozumienia
W początkowym okresie badań nad atomem, w ramach planetarnego modelu Rutherforda, niemal cała masa atomu była skoncentrowana w niewielkim jądrze (o rozmiarach rzędu 10-15 m) o ładunku dodatnim, wokół którego krążyły elektrony. Pojawiła się jednak poważna wątpliwość: jeśli jądro atomowe składałoby się wyłącznie z dodatnio naładowanych protonów, to ogromne siły elektrostatycznego odpychania między nimi powinny rozerwać jądro. Dwa protony oddalone od siebie o zaledwie 10-15 m odpychają się siłą o wartości 230 N – to olbrzymia siła w skali mikroskopowej, biorąc pod uwagę, że masa protonu wynosi około 1,67 × 10-27 g. Przez pewien czas sądzono nawet, że w jądrze znajdują się również elektrony, które miałyby równoważyć ładunek. Problem ten został rozwiązany dopiero w 1932 roku, wraz z odkryciem neutronu przez Jamesa Chadwicka (choć jego istnienie przewidział Ernest Rutherford już dwanaście lat wcześniej).
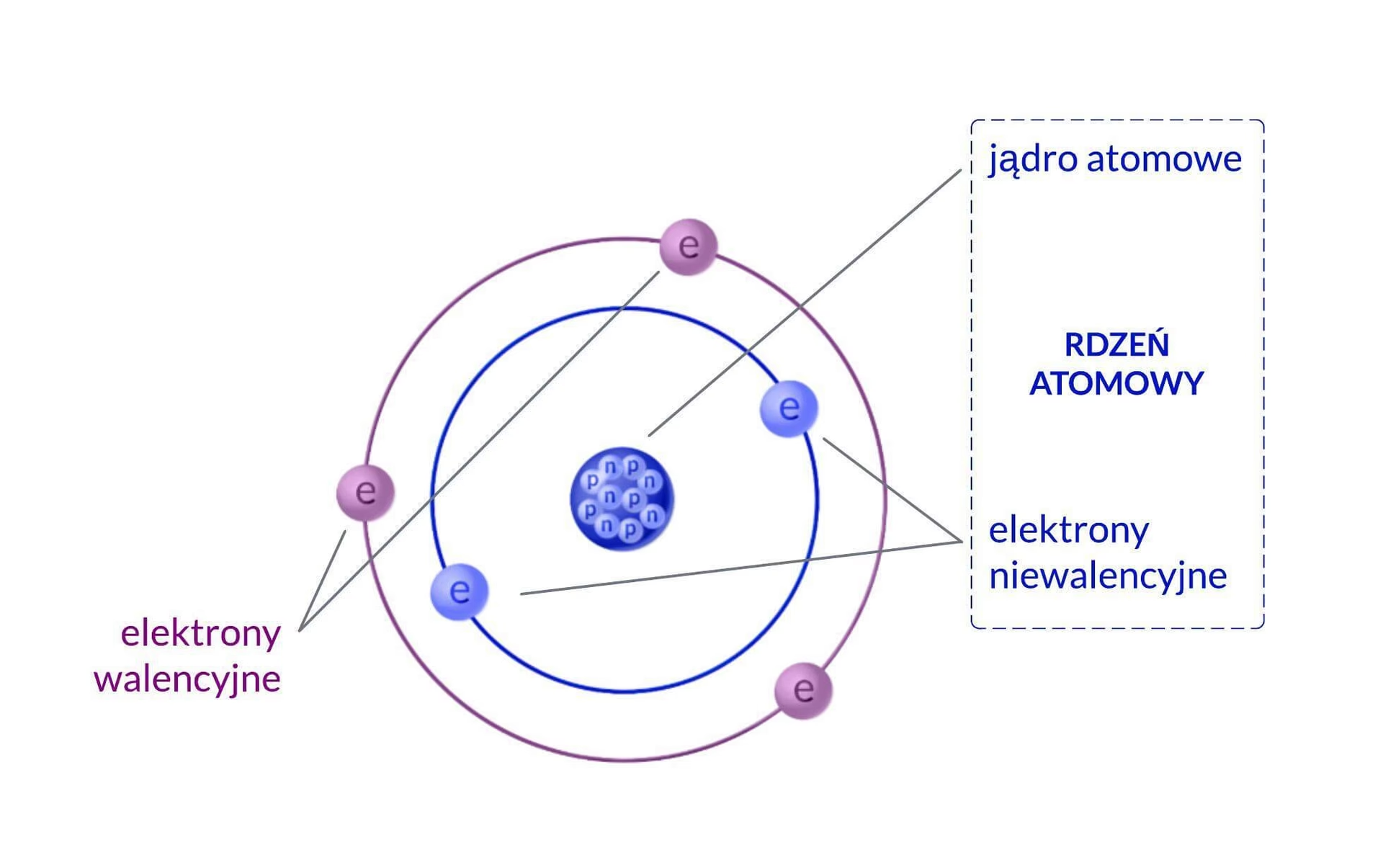
Obecnie wiemy, że jądro – centralna część atomu – zbudowane jest z cząstek zwanych nukleonami, czyli protonów i neutronów. Protony i neutrony są do siebie podobne pod względem rozmiarów i mają zbliżone masy (masa neutronu jest nieznacznie większa). Proton ma ładunek +1e (gdzie e = 1,602 × 10-19 C), natomiast neutron jest elektrycznie obojętny. Co utrzymuje te składniki razem? Między nukleonami w jądrze działają olbrzymie siły przyciągania, znane jako siły jądrowe. Są to siły krótkozasięgowe, ale niezwykle silne, zdolne do pokonania elektrycznych sił odpychania między protonami, utrzymując jądro atomowe w całości. Warto podkreślić, że jądro stanowi zaledwie niewielką część całego atomu. Jeśli atom miałby średnicę rzędu 10-10 m, to jądro byłoby od niego aż 100 000 razy mniejsze! Mimo to, w jądrze skupione jest ponad 99,9% masy całego atomu, a ponad 99,99999% objętości atomu stanowi pusta przestrzeń.
Cząstki Elementarne: W Poszukiwaniu Najmniejszych Składników
W latach 30. XX wieku pojęcie cząstek elementarnych obejmowało elektrony, protony, neutrony i fotony. Jednak badania promieniowania kosmicznego oraz analiza produktów reakcji jądrowych (zderzenia dwóch jąder) doprowadziły do odkrycia ponad dwustu nowych rodzajów cząstek, często o masach znacznie większych niż masa elektronu. Większość z nich okazywała się nietrwała. Eksperymentalnie udowodniono również istnienie antycząstek, takich jak pozyton (cząstka o masie elektronu, ale ładunku dodatnim) odkryty w produktach zderzeń promieniowania kosmicznego z atmosferą. W 1955 roku odkryto antyproton, co doprowadziło do wniosku, że praktycznie każda cząstka elementarna ma swoją antycząstkę. Model cząstek elementarnych stawał się coraz bardziej skomplikowany. Ciekawostką jest polski wkład w te badania: w 1952 roku Marian Danysz i Jerzy Pniewski odkryli hiperjądro, zawierające cząstkę zwaną „hiperonem lambda”.
Kwarki i Gluony: Fundament Materii
Fizycy szybko doszli do wniosku, że świat cząstek elementarnych jest zbyt złożony. W 1964 roku Murray Gell-Mann i George Zweig wysunęli hipotezę, że protony i neutrony, uważane wcześniej za niepodzielne, składają się z jeszcze mniejszych cząstek, nazwanych kwarkami. Choć kwarki nie występują jako cząstki swobodne, ich istnienie zostało potwierdzone eksperymentalnie. Od 1968 roku cykl doświadczeń badających zderzenia elektronów z protonami wykazał, że protony mają wewnętrzną strukturę, a ich elementy są obdarzone ładunkiem elektrycznym. Za te pionierskie badania w 1990 roku Friedman, Kendall i Taylor otrzymali Nagrodę Nobla. Poniższa tabela przedstawia nazwy i ładunki poszczególnych typów kwarków:
| Nazwa | Symbol | Ładunek [e] |
|---|---|---|
| górny | u | +⅔ |
| dolny | d | −⅓ |
| dziwny | s | −⅓ |
| powabny | c | +⅔ |
| niski, piękny | b | −⅓ |
| wysoki, prawdziwy | t | +⅔ |
Kwarki utrzymują się razem dzięki cząstkom nazywanym gluonami, których nazwa pochodzi od angielskiego słowa „glue” (klej). Gluony są nośnikami silnych oddziaływań jądrowych i powodują, że kwarki w protonie czy neutronie tworzą stabilny układ. Obecnie uważa się, że kwarki są fundamentalnym budulcem materii i są niepodzielne.
Zgodnie z modelem kwarkowym, proton składa się z dwóch kwarków 'u' i jednego kwarku 'd' (co daje ładunek: +⅔ + ⅔ - ⅓ = +1e). Neutron natomiast składa się z jednego kwarku 'u' i dwóch kwarków 'd' (co daje ładunek: +⅔ - ⅓ - ⅓ = 0e). To potwierdza obserwowane ładunki protonów i neutronów.
Izotopy: Różnorodność Tego Samego Pierwiastka
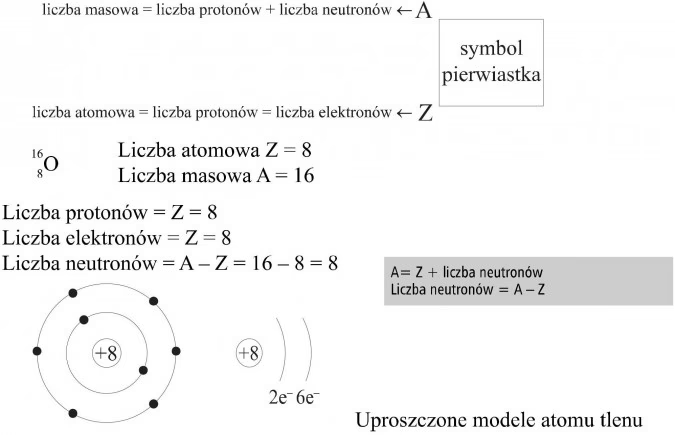
Wiesz już, że jądro każdego atomu składa się z pewnej liczby dodatnio naładowanych protonów oraz elektrycznie obojętnych neutronów. Liczbę protonów w jądrze oznaczamy literą „Z” i nazywamy ją liczbą atomową (lub porządkową). Iloczyn Z · e to ładunek jądra atomu. W atomie elektrycznie obojętnym liczba protonów w jądrze jest równa liczbie elektronów krążących wokół jądra. Natomiast liczba wszystkich nukleonów (protonów i neutronów) w jądrze jest oznaczana literą „A” i nazywana jest liczbą masową.
Budowę atomu symbolicznie zapisujemy jako: XAZ, gdzie X to symbol pierwiastka, A to liczba masowa, a Z to liczba atomowa. Odmiany tego samego pierwiastka, które różnią się liczbą masową (czyli liczbą neutronów), nazywamy izotopami. Jądra wszystkich izotopów danego pierwiastka mają tę samą liczbę atomową Z, ale różnią się wartościami liczby masowej A.
Przykładem są izotopy wodoru: zwykły wodór (prot) ma w jądrze tylko jeden proton (11H), deuter ma jeden proton i jeden neutron (21H), a tryt ma jeden proton i dwa neutrony (31H). Węgiel również ma kilka izotopów, np. 126C, 136C i promieniotwórczy 146C.
Modele Jądra Atomowego: Jak Rozumiemy Jego Strukturę?
Badania jąder atomowych polegają na analizowaniu samorzutnych i wymuszonych rozpadów, a także na badaniu rozpraszania cząstek (promieniowanie gamma, elektrony, neutrony, protony) na jądrach. Stwierdzono, że większość jąder ma kształt zbliżony do kuli, choć niektóre są owalne. Gęstość wewnątrz jąder jest jednolita i szybko spada do zera na pewnej odległości od środka, określanej jako promień jądra (rzędu 10-14 – 10-15 m).
Model Kroplowy
Jednym z pierwszych modeli jądra był model kroplowy, opracowany przez Nielsa Bohra i Johna Wheelera na podstawie koncepcji George'a Gamowa. Zakłada on, że nukleony w jądrze zachowują się jak cząsteczki w kropli cieczy, a własności jądra jako całości są podobne do własności kropli. Mikroskopowe oddziaływania jądrowe i elektrostatyczne są w tym modelu przedstawiane przez analogię do sił lepkości i napięcia powierzchniowego. Najważniejszym założeniem jest kulisty kształt jąder. Model ten, choć przybliżony i nie wyjaśniający wszystkich własności jąder, pozwala dość dobrze rozpatrywać właściwości materii i przewiduje stałą energię wiązania na jeden nukleon dla jąder lekkich oraz mniejszą dla ciężkich, co wyjaśnia zjawiska rozszczepienia.
Model Powłokowy
Model powłokowy jądra atomowego powstał na zasadzie analogii do powłokowego modelu atomu. Zakłada on, że nukleony wewnątrz jądra nie mogą przyjmować dowolnych stanów energetycznych, lecz tylko te zgodne z energiami kolejnych powłok. Wyjaśnia on istnienie „liczb magicznych” (2, 8, 20, 28, 50, 82, 126), dla których jądra atomowe są najstabilniejsze. Jeżeli jądro ma jeden nukleon mniej lub więcej, energia wiązania jest wyraźnie mniejsza. Model zakłada, że nukleony poruszają się w jądrze prawie niezależnie, a oddziaływanie nukleonu z pozostałymi można zastąpić oddziaływaniem ze średnim polem. Wyjaśnia on odstępstwa energii wiązania od modelu kroplowego oraz istnienie oddzielnych powłok dla neutronów i protonów. Jądra, w których zarówno liczba neutronów, jak i liczba protonów jest równa liczbie magicznej (tzw. „podwójnie magiczne”, np. hel), cechują się wyjątkową trwałością. Model ten przewiduje również istnienie „wyspy stabilności” dla superciężkich pierwiastków.
Modele Kolektywne
Modele te zakładają, że nie wszystkie zjawiska jądrowe da się wytłumaczyć jako oddziaływanie pojedynczych nukleonów. Według nich nukleony, łącząc się w grupy, tworzą nowe cząstki wewnątrz jądra. Przykładem jest koncepcja bozonów (Interacting Boson Model, IBM), oparta na analogii do zjawisk kwantowych w nadprzewodnikach, gdzie cząstki łączą się w pary, uzyskując nowe własności.
Jądra Trwałe i Nietrwałe: Dlaczego Się Rozpadają?
Tylko niektóre jądra atomowe są trwałe. Decydują o tym oddziaływania między tworzącymi je nukleonami. Dla pierwiastków o liczbie atomowej od 1 (wodór) do 83 (bizmut), 80 z nich ma trwałe lub bardzo długożyciowe izotopy (wyjątki to technet i promet). Cięższe pierwiastki nie mają trwałych izotopów, ale niektóre z nich (np. pluton o Z=94) mają tak długi czas połowicznego rozpadu, że można je znaleźć w naturze. Pierwiastki cięższe od plutonu nie występują na Ziemi naturalnie, ale mogą być sztucznie wytwarzane w akceleratorach cząstek (np. oganeson o Z=118).
Trwałość jądra można przewidzieć na podstawie energii wiązania, którą wyznacza się doświadczalnie, porównując masę jądra z sumą mas jego składników (tzw. niedobór masy). Jeśli energia potrzebna do oderwania cząsteczki od jądra jest większa od zera, reakcja rozpadu zazwyczaj zachodzi. Jeśli energia jest mniejsza od zera, reakcja nie zachodzi, a jądro jest trwałe. Dla średnich i ciężkich jąder energia wiązania jest wprost proporcjonalna do liczby nukleonów, rosnąc zwykle o 7–8 MeV na każdy dodatkowy nukleon w zakresie A od 30 do 70. Jednak dla cięższych jąder zależność ta ulega zmianie.
Jądra z parzystą liczbą neutronów i protonów (tzw. parzysto-parzyste) cechują się największą trwałością. Jądra z nieparzystą liczbą protonów lub neutronów (parzysto-nieparzyste) są znacznie mniej trwałe. Zjawisko to wyjaśnia model powłokowy jądra atomowego.
Przemiany Jądrowe: Narodziny Nowych Elementów
Zarówno występujące w naturze, jak i sztucznie wytworzone jądra atomowe podlegają przemianom zwanym reakcjami lub przemianami jądrowymi. Przemiany te mogą być samorzutne (rozpad jąder nietrwałych) lub inicjowane przez dostarczenie energii do jądra. Jądro posiadające wyższą energię niż jądro podstawowe nazywane jest jądrem wzbudzonym. Zmiana jądra może być zainicjowana przez pochłonięcie cząstki elementarnej lub pobudzenie do wyższego stanu kwantowego przez cząstki niosące energię (np. neutrony, neutrina, inne jądra).
W przemianach jądrowych nie jest zachowana masa w sensie klasycznym, ale zachowana jest suma energii i materii, zgodnie z równaniem Einsteina E=mc2. Energia wydziela się w postaci promieniowania elektromagnetycznego (gamma) oraz emisji cząstek (jąder helu, elektronów, protonów, neutronów i neutrin), często o dużych energiach. Proces rozpadu wielu jąder atomowych prowadzi do powstania promieniowania jonizującego. Przemiany jądrowe zapisuje się analogicznie do reakcji chemicznych, np.: 2411Na → 2412Mg + e- + ν̅e, co oznacza, że jądro sodu-24 przechodzi w jądro magnezu-24, emitując elektron i antyneutrino elektronowe.
Efekty Kwantowe: Spin i Rezonans Jądrowy
Jądra atomowe można w uproszczeniu traktować jako wirujące ciała naładowane elektrycznie. W kategoriach mechaniki kwantowej to „wirowanie” określa się terminem spinu. Jądra o parzystej liczbie atomowej mają w stanie podstawowym spin całkowity (zwykle zero), a o nieparzystej – połówkowy. Spin jąder nie jest prostym wirowaniem mechanicznym, lecz złożonym zjawiskiem kwantowym. Opis pola magnetycznego jądra jest pełny tylko z uwzględnieniem jego własności kwantowych.
Gdy do jąder atomowych o spinie połówkowym przyłożymy zewnętrzne pole magnetyczne, jądra nie ustawią się idealnie zgodnie z wektorem pola, lecz ulegną zjawisku precesji. Jądra ustawione niezgodnie z wektorem pola będą zajmować określone kwantowe stany energetyczne. Jeśli przyłożone pole magnetyczne oscyluje zgodnie z częstotliwością precesji, jądra wzmacniają to pole, prowadząc do zjawiska magnetycznego rezonansu jądrowego (MRJ), niezwykle przydatnego w chemii i medycynie. W kategoriach kwantowych, gdy energia fotonów zewnętrznego pola magnetycznego jest zgodna z różnicą kwantowych stanów energetycznych jąder, ich pola magnetyczne przechodzą do stanu wzbudzonego, co następnie prowadzi do emisji fotonów o tej samej energii. Choć opisy MRJ w mechanice klasycznej i kwantowej różnią się, w większości przypadków obliczone na ich podstawie zachowanie jąder jest podobne, a w praktyce oba modele są wykorzystywane dla zwiększenia dokładności pomiarów.
Podsumowanie: Składniki Jądra Atomowego
Jądro atomowe, choć mikroskopijne, jest niezwykle złożoną strukturą i stanowi serce atomu, skupiając w sobie niemal całą jego masę. Jego budowa, odkrywana i opisywana przez dziesięciolecia badań, jest kluczem do zrozumienia materii i energii.
- Jądro atomowe zbudowane jest z ciężkiego jądra o niewielkich rozmiarach i otaczającej je powłoki elektronowej.
- Centralna część atomu składa się z nukleonów: protonów (o ładunku +1e) i neutronów (elektrycznie obojętnych). Ich masy są zbliżone.
- Protony i neutrony nie są cząstkami elementarnymi, lecz składają się z mniejszych jednostek zwanych kwarkami. Istnieje sześć typów kwarków o różnych ładunkach elektrycznych.
- Kwarki w nukleonach są spajane przez gluony, które są nośnikami silnych oddziaływań jądrowych. Uważa się, że kwarki są fundamentalnym budulcem materii.
- Zwarta struktura jądra jest wynikiem równowagi między odpychającymi siłami elektrycznymi między protonami a silnymi, krótkozasięgowymi siłami jądrowymi, które je przyciągają. Neutrony są kluczowe dla stabilności jąder (z wyjątkiem jądra wodoru).
- Liczba protonów w jądrze nazywana jest liczbą atomową (Z) i określa rodzaj pierwiastka. Ładunek jądra to Z·e.
- Liczba wszystkich nukleonów (protonów i neutronów) to liczba masowa (A).
- Odmiany tego samego pierwiastka, różniące się liczbą neutronów (a tym samym liczbą masową), nazywane są izotopami.
- Rozmiar jądra atomowego to około 10-15 m, podczas gdy atomu to około 10-10 m. Jądro jest około 100 000 razy mniejsze od atomu, ale skupia w sobie ponad 99,9% jego masy.
- Zjawiska takie jak magnetyczny rezonans jądrowy (MRJ) wykorzystują kwantowe właściwości spinu jądra, znajdując praktyczne zastosowania w nauce i medycynie.
Często Zadawane Pytania (FAQ)
1. Czy proton i neutron są cząstkami elementarnymi?
Nie, protony i neutrony nie są cząstkami elementarnymi w najnowszym rozumieniu. Składają się one z jeszcze mniejszych cząstek, zwanych kwarkami. Proton składa się z dwóch kwarków 'u' (górnych) i jednego kwarku 'd' (dolnego), natomiast neutron z jednego kwarku 'u' i dwóch kwarków 'd'.
2. Jakie siły utrzymują jądro atomowe w całości?
Jądro atomowe jest utrzymywane w całości przez silne oddziaływania jądrowe (siły jądrowe). Są one znacznie silniejsze niż elektrostatyczne siły odpychania między dodatnio naładowanymi protonami i działają na bardzo małych odległościach wewnątrz jądra.
3. Czym różnią się izotopy tego samego pierwiastka?
Izotopy tego samego pierwiastka różnią się liczbą neutronów w jądrze. Mają tę samą liczbę protonów (czyli tę samą liczbę atomową Z), co oznacza, że należą do tego samego pierwiastka chemicznego, ale ich masa (liczba masowa A) jest różna.
4. Co to są kwarki i gluony?
Kwarki to fundamentalne cząstki, z których zbudowane są protony i neutrony. Gluony to cząstki, które „sklejają” kwarki ze sobą, odpowiadając za silne oddziaływania jądrowe i tworząc stabilne układy, takie jak protony i neutrony.
5. Dlaczego jądro atomowe jest tak małe w porównaniu do całego atomu?
Jądro atomowe jest niezwykle małe (ok. 10-15 m) w porównaniu do rozmiaru całego atomu (ok. 10-10 m). Oznacza to, że atom jest w większości pustą przestrzenią, a masa jest skoncentrowana w jego niewielkim, gęstym jądrze. Jądro jest około 100 000 razy mniejsze od atomu.
Zainteresował Cię artykuł Tajemnice Jądra Atomowego: Co Je Tworzy?", "kategoria": "Fizyka? Zajrzyj też do kategorii Edukacja, znajdziesz tam więcej podobnych treści!

