06/03/2010
W świecie chemii, zrozumienie struktury atomu jest absolutnie fundamentalne. Atom, często postrzegany jako najmniejsza, niepodzielna cegiełka materii, w rzeczywistości jest skomplikowanym układem, który rządzi się własnymi prawami i decyduje o właściwościach wszystkich znanych nam substancji. Od najprostszych gazów po złożone białka, każdy element składa się z atomów, a ich unikalna budowa determinuje, jak łączą się w molekuły i wchodzą w reakcje chemiczne. W tym artykule zagłębimy się w podstawowe składniki atomu, ich wzajemne oddziaływania oraz kluczowe pojęcia, które są niezbędne dla każdego studenta chemii, a także dla każdego, kto pragnie zrozumieć otaczający nas świat na poziomie molekularnym.
Zrozumienie atomu nie jest jedynie akademicką ciekawostką. To wiedza, która ma praktyczne zastosowania w niezliczonych dziedzinach, od medycyny po inżynierię materiałową. Począwszy od jego podstawowych cząstek, przez pojęcia takie jak liczba atomowa i masowa, aż po intrygujący świat izotopów i ich zastosowanie w datowaniu, każdy aspekt budowy atomu otwiera nowe drzwi do głębszego poznania materii. Przygotuj się na podróż do mikroświata, gdzie zasady fizyki kwantowej spotykają się z chemią, tworząc podstawy dla całego wszechśświata, jaki znamy.
Podstawowe Cząstki Subatomowe
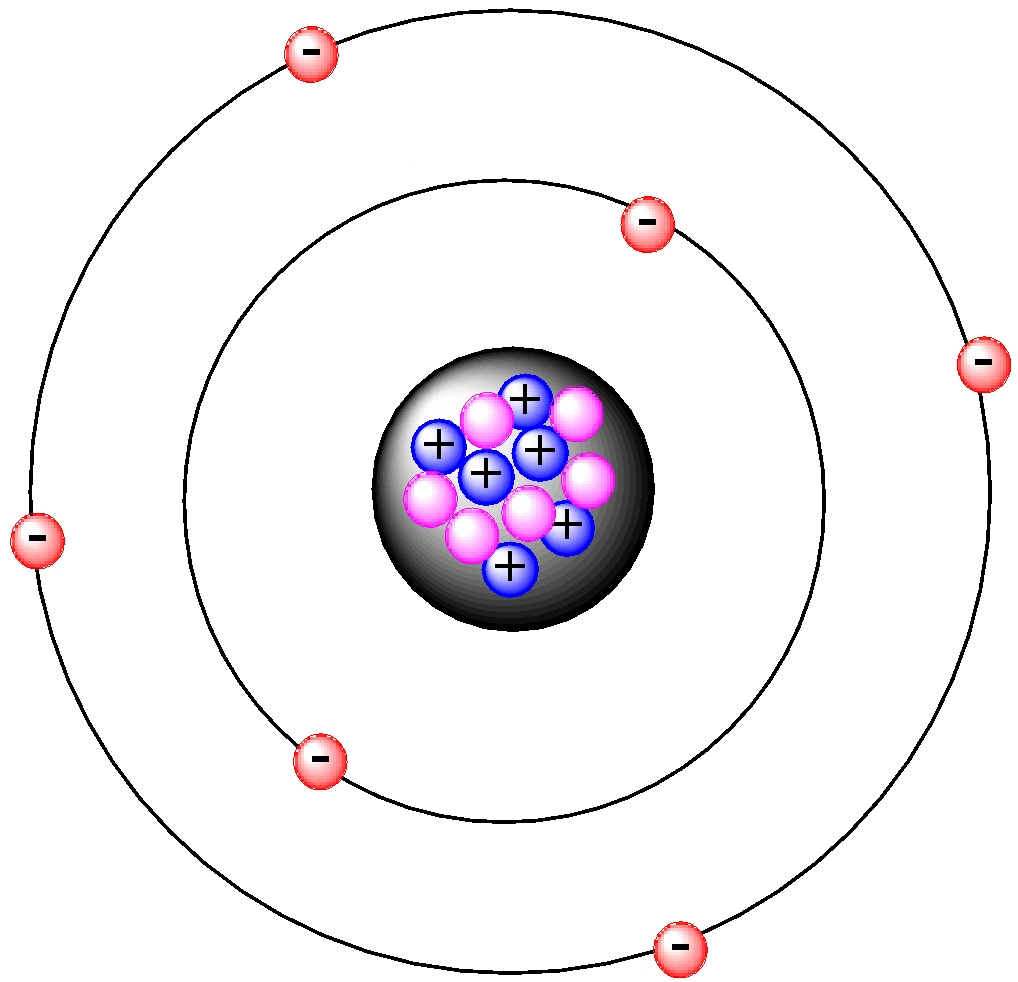
Atom, mimo swojej pozornej prostoty, składa się z trzech podstawowych rodzajów cząstek subatomowych: protonów, neutronów i elektronów. Każda z tych cząstek odgrywa kluczową rolę w określaniu właściwości atomu i jego zachowania chemicznego. Centralnym punktem atomu jest jądro, niezwykle gęsta i niewielka przestrzeń, w której znajdują się protony i neutrony. Dookoła jądra, w obszarach zwanych powłokami elektronowymi, krążą elektrony.
Protony: Strażnicy Tożsamości Elementu
Protony to cząstki posiadające dodatni ładunek elektryczny (+1). Ich masa jest znaczna, wynosząca około 1,67 × 10-24 grama, co jest zdefiniowane jako jedna atomowa jednostka masy (amu) lub jeden Dalton. Co najważniejsze, liczba protonów w jądrze atomu decyduje o jego tożsamości chemicznej, czyli o tym, jakim pierwiastkiem jest dany atom. Na przykład, każdy atom węgla zawsze będzie miał dokładnie 6 protonów. Zmiana liczby protonów automatycznie oznacza zmianę pierwiastka.
Neutrony: Stabilizatory Jądra
Neutrony, jak sama nazwa wskazuje, są cząstkami elektrycznie obojętnymi, co oznacza, że nie posiadają ładunku. Podobnie jak protony, znajdują się w jądrze atomu i mają zbliżoną masę, również około 1 amu. Główną funkcją neutronów jest stabilizacja jądra atomowego, zapobiegając wzajemnemu odpychaniu się dodatnio naładowanych protonów. Liczba neutronów w atomie danego pierwiastka może się różnić, prowadząc do zjawiska izotopów, o czym powiemy więcej w dalszej części.
Elektrony: Architekci Wiązań Chemicznych
Elektrony to cząstki o ujemnym ładunku elektrycznym (-1), równym co do wartości ładunkowi protonu. W przeciwieństwie do protonów i neutronów, elektrony są znacznie lżejsze – ich masa wynosi zaledwie około 9,11 × 10-28 grama, czyli około 1/1800 masy atomowej jednostki masy. Oznacza to, że ich wkład w całkowitą masę atomu jest praktycznie pomijalny. Elektrony krążą wokół jądra w określonych obszarach, tworząc tak zwane powłoki elektronowe. To właśnie elektrony na najbardziej zewnętrznych powłokach decydują o tym, jak atom będzie reagował z innymi atomami, tworząc wiązania chemiczne i molekuły. W neutralnym (nie naładowanym) atomie liczba elektronów zawsze odpowiada liczbie protonów, co sprawia, że ładunki dodatnie i ujemne wzajemnie się równoważą, dając atomowi zerowy ładunek netto.
Poniższa tabela podsumowuje kluczowe właściwości tych fundamentalnych cząstek:
| Cząstka | Lokalizacja | Ładunek | Masa (w amu) |
|---|---|---|---|
| Proton | Jądro | +1 | ~1 |
| Neutron | Jądro | 0 | ~1 |
| Elektron | Powłoki elektronowe | -1 | ~1/1800 |
Masa Atomowa i Objętość Atomu: Więcej Niż Myślisz
Choć mogłoby się wydawać, że atom jest ciałem zwartym, to w rzeczywistości jego budowa jest zaskakująco „pusta”. Ponad 99% objętości atomu stanowi pusta przestrzeń. Jądro, choć zawiera prawie całą masę atomu, jest niezwykle małe w porównaniu do całkowitej objętości zajmowanej przez elektrony krążące wokół niego. Wyobraź sobie stadion sportowy, gdzie jądro to piłka na środku boiska, a elektrony krążące na trybunach to zaledwie pyłki – reszta to pusta przestrzeń. Mimo tak dużej pustej przestrzeni, obiekty stałe nie przenikają przez siebie. Dzieje się tak, ponieważ ujemnie naładowane elektrony, otaczające wszystkie atomy, odpychają się wzajemnie, zapobiegając zajmowaniu tej samej przestrzeni przez dwa atomy. To te siły międzycząsteczkowe sprawiają, że nie przenikamy przez krzesło, na którym siedzimy.
Jeśli chodzi o masę atomu, to, jak już wspomniano, główny wkład pochodzi od protonów i neutronów. Masa każdego z nich wynosi około 1 atomowej jednostki masy (amu). Masa elektronów jest tak znikoma, że dla celów obliczeń masy atomowej zazwyczaj jest pomijana. W chemii, gdy mówimy o masie atomowej pierwiastka, często mamy na myśli średnią masę wszystkich jego naturalnie występujących izotopów, wyrażoną w amu. Ta wartość jest kluczowa w obliczeniach stechiometrycznych i zrozumieniu proporcji, w jakich pierwiastki łączą się ze sobą.
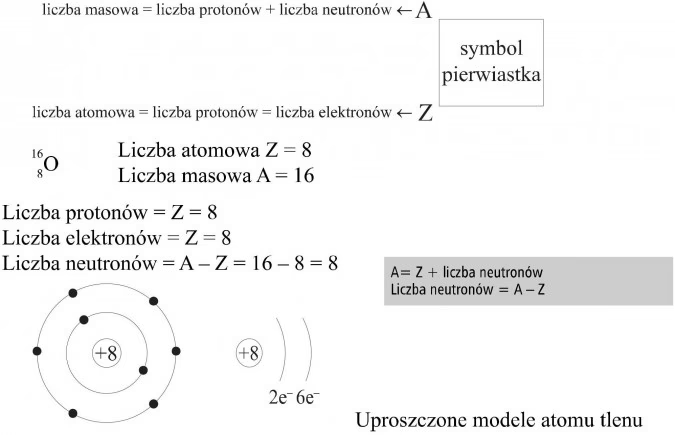
Liczba Atomowa (Z) i Liczba Masowa (A): Identyfikacja Pierwiastka
Dwa fundamentalne pojęcia, które pozwalają nam precyzyjnie identyfikować i charakteryzować atomy, to liczba atomowa i liczba masowa.
Liczba Atomowa (Z)
Liczba atomowa, oznaczana symbolem Z, to nic innego jak liczba protonów znajdujących się w jądrze atomu. Jest to najbardziej podstawowa cecha identyfikująca pierwiastek chemiczny. Każdy pierwiastek ma unikalną liczbę atomową. Na przykład, wodór (H) zawsze ma Z=1 (1 proton), hel (He) ma Z=2 (2 protony), a węgiel (C) ma Z=6 (6 protonów). W neutralnym atomie, liczba elektronów jest zawsze równa liczbie protonów. Dzięki temu ładunki dodatnie i ujemne się równoważą, a atom jako całość jest elektrycznie obojętny. Zmiana liczby elektronów prowadzi do powstania jonów (atomów naładowanych), ale nie zmienia tożsamości pierwiastka.
Liczba Masowa (A)
Liczba masowa, oznaczana symbolem A, to suma liczby protonów i liczby neutronów w jądrze atomu. Ponieważ masa elektronów jest pomijalna, liczba masowa stanowi przybliżoną miarę całkowitej masy atomu wyrażonej w amu. Znając liczbę atomową i liczbę masową, możemy łatwo obliczyć liczbę neutronów w jądrze, odejmując liczbę protonów od liczby masowej (Neutrony = A - Z). Na przykład, atom litu o liczbie atomowej 3 (3 protony) i liczbie masowej 7 (7 amu) będzie miał 3 elektrony (w atomie neutralnym) i 4 neutrony (7 - 3 = 4).
Warto zwrócić uwagę, że „liczba masowa” to nie to samo co „masa atomowa”. Masa atomowa, którą znajdujemy w układzie okresowym, jest średnią ważoną mas wszystkich naturalnie występujących izotopów danego pierwiastka, uwzględniającą ich względne obfitości. Dlatego często jest to liczba dziesiętna. Na przykład, masa atomowa chloru (Cl) wynosi 35,45 amu, ponieważ chlor naturalnie występuje jako mieszanina izotopów, głównie chloru-35 (17 protonów, 18 neutronów) i chloru-37 (17 protonów, 20 neutronów).
Świat Izotopów: Te Same, Ale Różne
Jednym z najbardziej fascynujących aspektów struktury atomu jest istnienie izotopów. Są to atomy tego samego pierwiastka, co oznacza, że mają tę samą liczbę protonów (a więc i tę samą liczbę atomową Z), ale różnią się liczbą neutronów w jądrze. Ta różnica w liczbie neutronów prowadzi do odmiennej liczby masowej (A) i nieco innej masy atomowej, ale zazwyczaj nie wpływa znacząco na ich właściwości chemiczne, ponieważ to elektrony, a nie neutrony, decydują o reaktywności chemicznej.
Przykłady Izotopów
Najlepszym przykładem są izotopy węgla:
- Węgiel-12 (12C): Posiada 6 protonów, 6 neutronów i 6 elektronów. Jego liczba masowa wynosi 12 amu. Jest to najczęściej występujący izotop węgla.
- Węgiel-14 (14C): Posiada 6 protonów, 8 neutronów i 6 elektronów. Jego liczba masowa wynosi 14 amu. Jest to izotop promieniotwórczy, który odgrywa kluczową rolę w datowaniu.
Mimo różnicy w masie, zarówno Węgiel-12, jak i Węgiel-14 zachowują się chemicznie niemal identycznie, tworząc te same związki i wchodząc w te same reakcje.
Izotopy Promieniotwórcze i Półokres Rozpadu
Niektóre izotopy są niestabilne. Oznacza to, że ich jądra atomowe mają nadmiar energii i z czasem ulegają rozpadowi promieniotwórczemu, przekształcając się w inne, bardziej stabilne pierwiastki. Proces ten jest przewidywalny i charakteryzuje się tzw. półokresem rozpadu (lub czasem połowicznego rozpadu), czyli czasem, po którym połowa początkowej ilości izotopu ulegnie rozpadowi. Półokres rozpadu jest unikalny dla każdego radioizotopu i może wynosić od ułamków sekundy do miliardów lat. To właśnie ta przewidywalność sprawia, że izotopy promieniotwórcze są niezwykle użyteczne w wielu dziedzinach, w tym w medycynie, energetyce i, co najważniejsze, w datowaniu.
Datowanie Radiowęglowe i Inne Metody: Odczytywanie Historii Z Atomów
Jednym z najbardziej spektakularnych zastosowań wiedzy o izotopach jest datowanie radiowęglowe, znane również jako datowanie węglem-14. Ta metoda pozwala naukowcom określać wiek artefaktów archeologicznych, szczątków organicznych i innych materiałów pochodzenia biologicznego, które niegdyś były częścią żywych organizmów.
Jak Działa Datowanie Radiowęglowe (Węgiel-14)?
Węgiel-14 (14C) jest naturalnie występującym radioizotopem, który powstaje w atmosferze ziemskiej w wyniku oddziaływania promieni kosmicznych z azotem-14 (14N). Jest to proces ciągły, więc w atmosferze zawsze obecny jest Węgiel-14. Po jego powstaniu, 14C łączy się z tlenem, tworząc dwutlenek węgla (14CO2). Ten radioaktywny dwutlenek węgla jest następnie wchłaniany przez rośliny w procesie fotosyntezy, a następnie przez zwierzęta, które zjadają rośliny. W rezultacie, w żywych organizmach stosunek 14C do stabilnego izotopu 12C jest zbliżony do stosunku występującego w atmosferze.
Kiedy organizm umiera, przestaje wymieniać węgiel z otoczeniem. Oznacza to, że nie pobiera już nowego 14C. Od tego momentu, ilość 14C w organizmie zaczyna stopniowo maleć, ponieważ ulega on rozpadowi promieniotwórczemu (tzw. rozpadowi beta) z powrotem do azotu-14 (14N). Półokres rozpadu 14C wynosi około 5730 lat. Oznacza to, że po 5730 latach połowa początkowej ilości 14C w próbce ulegnie rozpadowi. Mierząc stosunek 14C do 12C w badanym obiekcie i porównując go ze znanym stosunkiem w atmosferze, naukowcy mogą dokładnie obliczyć, ile półokresów rozpadu minęło, a tym samym określić wiek próbki. Metoda ta jest skuteczna dla obiektów liczących do około 50 000 lat.
Inne Metody Datowania Radiometrycznego
Dla obiektów starszych niż 50 000 lat, stosuje się inne izotopy promieniotwórcze o znacznie dłuższych półokresach rozpadu. Przykłady to:
- Potas-40 (40K): Posiada półokres rozpadu wynoszący około 1,25 miliarda lat. Jest używany do datowania skał i minerałów.
- Uran-235 (235U): Posiada półokres rozpadu wynoszący około 700 milionów lat. Jest powszechnie używany do datowania najstarszych formacji geologicznych na Ziemi.
Dzięki tym metodom radiometrycznym naukowcy mogą badać wiek skamieniałości, starożytnych artefaktów i formacji geologicznych, odkrywając historię naszej planety i życia na niej.
Często Zadawane Pytania (FAQ)
Czy atomy są naprawdę „puste”?
Tak, z punktu widzenia objętości, atomy są w większości pustą przestrzenią. Jądro atomowe, które zawiera prawie całą masę, jest niezwykle małe w porównaniu do przestrzeni zajmowanej przez elektrony krążące wokół niego. Jednak ta „pustość” nie oznacza, że materia może przez siebie przenikać. Ujemnie naładowane elektrony skutecznie odpychają się, tworząc barierę, która zapobiega przenikaniu obiektów.
Dlaczego elektrony nie wpadają do jądra, skoro są przyciągane przez protony?
To złożone pytanie, którego pełne wyjaśnienie wymaga zagłębienia się w mechanikę kwantową. W uproszczeniu, elektrony nie „krążą” wokół jądra w sensie planetarnym. Zamiast tego, ich zachowanie jest opisywane przez funkcje falowe, a ich położenie jest probabilistyczne. Elektrony zajmują określone poziomy energetyczne i obszary przestrzeni (powłoki i orbitale), a ich energia i pęd zapobiegają wpadnięciu do jądra. Jest to wynik równowagi między przyciąganiem elektrostatycznym ze strony jądra a ich własną energią kinetyczną i zasadami kwantowymi, takimi jak zasada nieoznaczoności Heisenberga i zasada Pauliego.
Jaka jest różnica między liczbą masową a masą atomową?
Liczba masowa (A) to liczba całkowita, która stanowi sumę protonów i neutronów w jądrze konkretnego izotopu. Jest to liczba bezwymiarowa. Masa atomowa natomiast to średnia ważona mas wszystkich naturalnie występujących izotopów danego pierwiastka, wyrażona w atomowych jednostkach masy (amu). Masa atomowa jest często liczbą dziesiętną, ponieważ uwzględnia względne obfitości różnych izotopów danego pierwiastka w naturze.
Czy izotopy mają różne właściwości chemiczne?
Zasadniczo nie. Właściwości chemiczne pierwiastka są determinowane przede wszystkim przez liczbę elektronów walencyjnych, czyli elektronów na najbardziej zewnętrznej powłoce atomu. Ponieważ izotopy tego samego pierwiastka mają tę samą liczbę protonów, a w atomach neutralnych także tę samą liczbę elektronów, ich właściwości chemiczne są praktycznie identyczne. Różnice w masie mogą prowadzić do bardzo subtelnych zmian w szybkości reakcji (tzw. efekty izotopowe), ale fundamentalne właściwości chemiczne pozostają takie same.
Podsumowanie
Struktura atomu jest kamieniem węgielnym współczesnej chemii i fizyki. Zrozumienie roli protonów, neutronów i elektronów w określaniu tożsamości, masy i reaktywności chemicznej pierwiastków jest niezbędne. Pojęcia takie jak liczba atomowa i masowa pozwalają nam precyzyjnie kategoryzować atomy, a zjawisko izotopów otwiera drzwi do zaawansowanych zastosowań, takich jak datowanie radiowęglowe. Wiedza ta nie tylko zaspokaja naszą ciekawość o świecie na poziomie fundamentalnym, ale także dostarcza potężnych narzędzi do badania historii Ziemi i wszechświata, a także do rozwijania nowych technologii w medycynie, energetyce i materiałoznawstwie. Atom, choć niewidzialny gołym okiem, jest sercem wszelkiej materii i kluczem do zrozumienia chemicznego wszechświata.
Zainteresował Cię artykuł Tajemnice Atomu: Fundament Chemii", "kategoria": "Chemia? Zajrzyj też do kategorii Edukacja, znajdziesz tam więcej podobnych treści!