04/01/2008
W sercu każdego organizmu żywego leży niezwykła instrukcja, zapisana w postaci cząsteczki DNA. To właśnie ta cząsteczka, niczym precyzyjny kod, decyduje o naszych cechach, funkcjach biologicznych i predyspozycjach. Ale jak odczytujemy ten złożony język życia? Odpowiedzią jest sekwencjonowanie DNA – proces, który zrewolucjonizował biologię, medycję i biotechnologię, otwierając przed nami drzwi do zrozumienia mechanizmów życia na poziomie molekularnym. Pozwala nam nie tylko identyfikować mutacje odpowiedzialne za choroby, ale także śledzić ewolucję gatunków, rozwijać nowe terapie i projektować organizmy o pożądanych cechach. W niniejszym artykule zagłębimy się w świat sekwencjonowania DNA, poznając jego podstawy, kluczowe metody i niezliczone zastosowania, które kształtują naszą przyszłość.
Czym Jest Sekwencjonowanie DNA?
Sekwencjonowanie DNA to nic innego jak ustalanie dokładnej kolejności zasad azotowych – adeniny (A), guaniny (G), cytozyny (C) i tyminy (T) – w cząsteczce DNA. Te cztery "litery" tworzą genetyczny alfabet, z którego zapisane są wszystkie informacje niezbędne do budowy i funkcjonowania organizmu. Wyobraź sobie, że DNA to ogromna, skomplikowana książka, a sekwencjonowanie to proces odczytywania każdej litery po kolei, aby zrozumieć jej treść. Jest to fundament całej genetyki i biologii molekularnej, umożliwiający badaczom rozszyfrowanie genów, identyfikację wariantów genetycznych i analizę całych genomów.
Proces sekwencjonowania, niezależnie od wybranej metody, zazwyczaj obejmuje kilka kluczowych etapów:
- Izolacja DNA: Pierwszym krokiem jest zawsze pozyskanie czystego DNA z materiału biologicznego, takiego jak krew, tkanki, ślina czy mikroorganizmy. Jakość i czystość izolowanego DNA są kluczowe dla powodzenia dalszych etapów.
- Przygotowanie Matrycy: Izolowane DNA jest często zbyt długie, aby mogło być sekwencjonowane w całości. Dlatego dzieli się je na mniejsze, zarządzalne fragmenty, a następnie poddaje modyfikacjom, które ułatwiają proces odczytu, np. przez dołączanie specjalnych adapterów.
- Selekcja Metody: Istnieje wiele technik sekwencjonowania, z których każda ma swoje specyficzne zalety i ograniczenia. Najbardziej znane to klasyczna metoda Sangera oraz nowoczesne metody sekwencjonowania nowej generacji (NGS), a także emerging technologies takie jak sekwencjonowanie oparte na nanoporach. Wybór metody zależy od celu badania, wymaganej dokładności i dostępnego budżetu.
- Reakcja Sekwencjonowania: W zależności od wybranej metody, następuje właściwa reakcja, podczas której polimeraza DNA syntetyzuje nowe nici DNA, wykorzystując przygotowaną matrycę. Kluczowe są tu specjalnie zmodyfikowane nukleotydy, często znakowane znacznikami fluorescencyjnymi, które umożliwiają identyfikację kolejności zasad.
- Odczyt i Analiza: Sekwenatory – zaawansowane urządzenia – odczytują sygnały z znaczników fluorescencyjnych, konwertując je na cyfrową sekwencję DNA. Następnie te surowe dane są przetwarzane przez specjalistyczne oprogramowanie.
- Interpretacja Danych: Otrzymane sekwencje są analizowane, porównywane z bazami danych i interpretowane w kontekście konkretnych pytań badawczych. Jest to często najbardziej złożony i czasochłonny etap, wymagający wiedzy z zakresu bioinformatyki.
Jak Wygląda Sekwencja DNA?
Sekwencja DNA jest zapisywana w formie prostego ciągu liter: A, T, G, C. Przykładowo, fragment sekwencji może wyglądać tak: ATTTGCAAGGCCCTC. Ten z pozoru prosty zapis zawiera w sobie ogromne ilości informacji. Aby uzmysłowić sobie skalę, wystarczy pomyśleć, że genom bakterii Escherichia coli, choć niewielki, zapisany w ten sposób zajmuje niemal 300 stron. Genom człowieka to już prawdziwa encyklopedia – liczy aż 200 000 stron! Każda „strona” tej książki kryje w sobie instrukcje, które determinują nasze życie. Zrozumienie tego zapisu jest kluczem do odkrycia tajemnic genetyki i biologii.
Metody Sekwencjonowania DNA: Od Klasyki do Rewolucji
Na przestrzeni lat techniki sekwencjonowania DNA ewoluowały od pracochłonnych i niskoprzepustowych metod do szybkich i masowych technologii, które są w stanie sekwencjonować całe genomy w rekordowo krótkim czasie. Dwie główne kategorie to metoda Sangera i Sekwencjonowanie Nowej Generacji (NGS).

Metoda Sangera: Klasyka w Genetyce
Metoda Sangera, znana również jako metoda dideoksy, jest kamieniem węgielnym sekwencjonowania DNA. Opracowana przez Fredericka Sangera, za którą otrzymał Nagrodę Nobla w 1980 roku, przez dziesięciolecia stanowiła złoty standard w odczytywaniu sekwencji DNA. Jej podstawą jest kontrolowane przerywanie syntezy nowej nici DNA w specyficznych miejscach.
Proces sekwencjonowania metodą Sangera można podzielić na pięć głównych etapów:
- Preparatywny PCR: Na początku, z badanej próbki DNA, przy użyciu reakcji łańcuchowej polimerazy (PCR), wytwarza się dużą liczbę identycznych kopii interesującego fragmentu DNA, co zapewnia jednorodny materiał do dalszych etapów.
- Denaturacja: Podwójna helisa DNA jest rozdzielana na dwie pojedyncze nici, zazwyczaj poprzez podgrzewanie. Tylko pojedyncza nić może służyć jako matryca do syntezy nowej nici.
- Synteza Nowych Nici: Ten kluczowy etap odbywa się w czterech oddzielnych probówkach. Każda probówka zawiera:
- Badany, jednoniciowy DNA (matryca).
- Starter – krótki odcinek DNA, który inicjuje syntezę.
- Polimeraza DNA – enzym odpowiedzialny za budowanie nowej nici.
- Wszystkie cztery standardowe nukleotydy (dATP, dCTP, dGTP, dTTP) w dużym nadmiarze.
- Niewielką ilość jednego rodzaju zmodyfikowanych nukleotydów, zwanych dideoksynukleotydami (ddNTP: ddATP, ddCTP, ddGTP lub ddTTP).
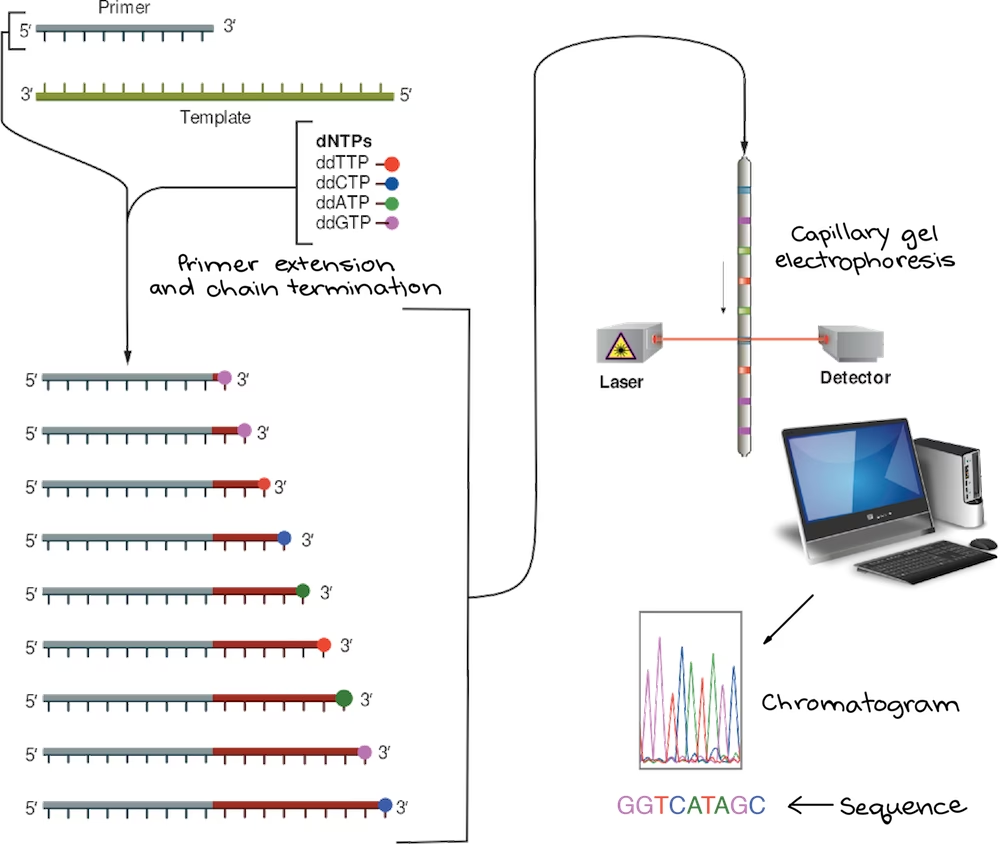
Specyfika ddNTP polega na tym, że brakuje im grupy hydroksylowej w pozycji 3' rybozy, co uniemożliwia przyłączenie kolejnego nukleotydu po ich wbudowaniu do rosnącej nici. Powoduje to natychmiastowe zakończenie syntezy (terminację). W każdej z czterech probówek reakcja zatrzymuje się w innym miejscu, zależnie od tego, który ddNTP został dodany. W rezultacie powstaje mieszanina fragmentów DNA o różnej długości, z których każdy kończy się konkretnym dideoksynukleotydem.
- Elektroforeza na Żelu Poliakrylamidowym: Fragmenty DNA z każdej probówki są rozdzielane według długości za pomocą elektroforezy żelowej. Krótsze fragmenty wędrują szybciej przez żel niż dłuższe. Tradycyjnie, próbki z czterech probówek były nanoszone na cztery sąsiadujące ze sobą ścieżki żelu.
- Analiza Prążków: Po rozdzieleniu, fragmenty DNA są wizualizowane. W starszych wersjach metody Sangera używano radioizotopów (np. P-32) do znakowania nici, a następnie autoradiografii (klisza rentgenowska) do uwidocznienia prążków. Odczytując kolejność prążków od najkrótszych (na dole żelu) do najdłuższych (na górze), można było określić sekwencję DNA. Współczesne sekwenatory Sangera wykorzystują znaczniki fluorescencyjne (każdy ddNTP ma inny kolor) i lasery do automatycznego odczytu sekwencji, co znacznie przyspieszyło i zautomatyzowało proces.
Metoda Sangera jest nadal używana do sekwencjonowania krótkich fragmentów DNA, potwierdzania wyników uzyskanych innymi metodami oraz w mniejszych laboratoriach ze względu na jej stosunkową prostotę i niezawodność.
Sekwencjonowanie Nowej Generacji (NGS): Przełom w Badaniach
Sekwencjonowanie Nowej Generacji (Next-Generation Sequencing, NGS), znane również jako sekwencjonowanie o wysokiej przepustowości, to rewolucyjna technologia, która umożliwia masowe, równoległe sekwencjonowanie milionów, a nawet miliardów fragmentów DNA jednocześnie. Dzięki temu stało się możliwe szybkie i ekonomiczne sekwencjonowanie całych genomów, transkryptomów (wszystkich cząsteczek RNA) oraz analiza złożonych próbek. NGS to obecnie jedna z najpotężniejszych technik w biologii molekularnej, genomicznej i medycynie.

Przebieg sekwencjonowania nowej generacji, niezależnie od konkretnej platformy (takich jak Illumina, IonTorrent czy Pacific Biosciences), zazwyczaj obejmuje trzy główne etapy:
- Izolacja DNA i Tworzenie Biblioteki: Podobnie jak w metodzie Sangera, DNA jest izolowane z próbki. Następnie jest ono fragmentowane na mniejsze odcinki, a do ich końców przyłączane są specjalne sekwencje adapterowe. Te adaptery są kluczowe, ponieważ umożliwiają przyczepienie fragmentów DNA do stałego podłoża (np. szklanej płytki) oraz służą jako miejsca wiązania dla starterów w kolejnych etapach. W ten sposób tworzona jest "biblioteka" fragmentów DNA gotowych do sekwencjonowania.
- Amplifikacja Matrycy: Każdy fragment DNA w bibliotece jest amplifikowany (powielany) miliony razy. Odbywa się to na stałym podłożu, co prowadzi do powstania "klastrow" – skupisk identycznych kopii jednego fragmentu DNA. Dzięki temu sygnał odczytywany w kolejnym etapie jest wystarczająco silny.
- Masowe Równoległe Sekwencjonowanie: W tym etapie, na każdej z milionów klastrów, jednocześnie odbywa się synteza nowej nici DNA. Nukleotydy, każdy z innym znacznikiem fluorescencyjnym, są dodawane kolejno. Po wbudowaniu każdego nukleotydu, kamera rejestruje emitowane światło, a następnie znacznik jest usuwany, aby umożliwić wbudowanie kolejnego nukleotydu. Proces ten jest powtarzany wielokrotnie, co pozwala na odczytanie sekwencji dla każdego klastra. Wszystkie te odczyty są następnie składane w całość przez zaawansowane algorytmy bioinformatyczne, odtwarzając pierwotną sekwencję DNA.
NGS w Diagnostyce Medycznej: Przykład Zespołu Alporta
Zastosowanie NGS ma ogromne znaczenie w diagnostyce chorób genetycznych, radykalnie zmieniając podejście do wykrywania mutacji. Klasycznym przykładem jest diagnostyka zespołu Alporta. Jest to dziedziczna choroba kolagenu typu IV, charakteryzująca się postępującymi zaburzeniami funkcjonowania nerek, upośledzeniem słuchu oraz uszkodzeniami oczu. Dziedziczenie może być sprzężone z chromosomem X lub autosomalne recesywne.
Tradycyjne metody diagnostyczne, takie jak DHPLC czy sekwencjonowanie Sangera, były w przypadku zespołu Alporta długotrwałe i kosztowne. Proces mógł trwać nawet kilka miesięcy, a jego utrudnieniem był brak tzw. „gorących miejsc” (hot spots), czyli fragmentów genów, w których mutacje występują najczęściej. Dodatkowo, duża liczba egzonów (kodujących fragmentów genów) w genach związanych z zespołem Alporta sprawiała, że sekwencjonowanie Sangera każdego z nich było niezwykle czasochłonne i wymagało wielu oddzielnych reakcji. Ograniczenia te zostały skutecznie wyeliminowane dzięki zastosowaniu technik NGS. NGS umożliwia jednoczesne sekwencjonowanie wszystkich istotnych genów i wykrywanie wszystkich możliwych wariantów w wybranym panelu genów, co znacząco skraca czas diagnostyki i zwiększa jej efektywność.
Porównanie Metody Sangera i NGS
Aby lepiej zrozumieć różnice i zalety obu metod, przedstawiamy ich porównanie w tabeli:
| Cecha | Metoda Sangera | Sekwencjonowanie Nowej Generacji (NGS) |
|---|---|---|
| Przepustowość | Niska (pojedyncze fragmenty DNA) | Wysoka (miliony/miliardy fragmentów równolegle) |
| Długość odczytu | Dłuższe odczyty (do 1000 pz) | Krótsze odczyty (50-600 pz, zależnie od platformy), ale wiele z nich |
| Koszt na parę zasad | Wyższy | Znacznie niższy |
| Szybkość | Wolniejsza (szczególnie dla dużych projektów) | Znacznie szybsza (od dni do godzin dla całych genomów) |
| Zastosowania | Potwierdzanie wyników, sekwencjonowanie pojedynczych genów, krótkich fragmentów | Sekwencjonowanie całych genomów/egzomów/transkryptomów, badania metagenomiczne, diagnostyka kompleksowych chorób genetycznych |
| Wymagania bioinformatyczne | Niskie do umiarkowanych | Bardzo wysokie (złożona analiza danych) |
| Wykrywalność rzadkich wariantów | Ograniczona | Znacznie wyższa dzięki głębokiemu sekwencjonowaniu |
Zastosowania Sekwencjonowania DNA
Możliwości, jakie otwiera sekwencjonowanie DNA, są niemal nieograniczone. To potężne narzędzie, które znajduje zastosowanie w wielu dziedzinach, od podstawowych badań naukowych po praktyczne zastosowania medyczne i przemysłowe.
- Badania Genetyczne i Diagnostyka Chorób: Sekwencjonowanie DNA jest niezastąpione w identyfikacji mutacji genetycznych odpowiedzialnych za choroby dziedziczne, takie jak mukowiscydoza, zespół Downa czy właśnie zespół Alporta. Pozwala na określenie predyspozycji do chorób (np. nowotworowych), diagnostykę prenatalną oraz wykrywanie patogenów.
- Badania Naukowe i Ewolucyjne: Umożliwia odkrywanie nowych gatunków, analizę różnorodności genetycznej w populacjach, badanie wzajemnych zależności między organizmami oraz rekonstrukcję drzewa życia. Sekwencjonowanie DNA jest kluczowe w badaniach ewolucji, pozwalając śledzić zmiany genetyczne na przestrzeni milionów lat.
- Medycyna Personalizowana: To dziedzina, która dynamicznie się rozwija dzięki sekwencjonowaniu. Pozwala na dostosowanie leczenia do indywidualnego profilu genetycznego pacjenta. Na przykład, można przewidzieć, jak pacjent zareaguje na dany lek, optymalizując dawkowanie i minimalizując skutki uboczne. To przyszłość farmakologii i terapii, gdzie każdy pacjent otrzymuje „szyte na miarę” leczenie.
- Biotechnologia i Inżynieria Genetyczna: Sekwencjonowanie jest fundamentem inżynierii genetycznej, umożliwiając precyzyjne modyfikowanie genów, tworzenie organizmów genetycznie zmodyfikowanych (GMO) do celów rolniczych, medycznych (np. produkcja insuliny) czy przemysłowych (np. biopaliwa). Jest również wykorzystywane w produkcji leków, szczepionek i rozwoju nowych technologii.
- Kryminologia i Medycyna Sądowa: Analiza DNA z próbek śladów biologicznych (np. włosów, krwi) pozwala na identyfikację sprawców przestępstw, ustalanie ojcostwa czy identyfikację ofiar katastrof.
- Rolnictwo i Hodowla Zwierząt: Sekwencjonowanie wspomaga selekcję roślin i zwierząt o pożądanych cechach (np. odporność na choroby, wyższa wydajność), co przekłada się na efektywniejszą produkcję żywności.
Wyzwania i Przyszłość Sekwencjonowania
Rozwój technik sekwencjonowania, zwłaszcza NGS, otworzył niezliczone możliwości, ale jednocześnie stworzył nowe wyzwania. Jednym z największych jest ogromna ilość generowanych danych. Sekwencjonowanie nowej generacji jest niezwykle wydajne w dostarczaniu surowych danych genetycznych. Jednakże, przetworzenie, analiza i interpretacja tych danych to złożony proces, który wymaga specjalistycznych narzędzi, potężnych komputerów i przede wszystkim wysoko wykwalifikowanych specjalistów – bioinformatyków.

Bioinformatycy to osoby, które łączą wiedzę z biologii, informatyki i statystyki, aby zarządzać, analizować i interpretować dane genetyczne. Ich praca jest kluczowa dla przekształcenia milionów odczytów sekwencyjnych w zrozumiałe informacje, które mogą prowadzić do nowych odkryć naukowych, lepszych diagnoz czy bardziej efektywnych terapii. Bez odpowiedniej analizy, surowe dane sekwencyjne pozostają tylko ciągiem liter.
Przyszłość sekwencjonowania DNA wydaje się być niezwykle obiecująca. Spodziewamy się dalszej miniaturyzacji urządzeń, obniżenia kosztów i zwiększenia szybkości odczytu. Rozwój technologii pojedynczych komórek pozwoli na analizę DNA z pojedynczych komórek, otwierając nowe perspektywy w badaniach nad nowotworami czy rozwojem embrionalnym. Coraz większa dostępność sekwencjonowania na skalę kliniczną, jak i w codziennym życiu, stawia jednak także pytania etyczne i prawne dotyczące prywatności danych genetycznych i ich wykorzystania. Niewątpliwie, sekwencjonowanie DNA będzie nadal napędzać przełomy w nauce i medycynie, zmieniając nasze rozumienie życia i sposób, w jaki podchodzimy do zdrowia.
Najczęściej Zadawane Pytania (FAQ)
- Czym jest para zasad w DNA?
- Para zasad (ang. base pair, bp) to dwie komplementarne zasady azotowe połączone wiązaniami wodorowymi w cząsteczce DNA. Adenina (A) zawsze łączy się z tyminą (T), a guanina (G) z cytozyną (C). Genomy i długości fragmentów DNA często podaje się w parach zasad (np. kilobazy – tysiące par zasad, megabazy – miliony par zasad).
- Ile czasu zajmuje sekwencjonowanie DNA?
- Czas sekwencjonowania zależy od metody i wielkości sekwencjonowanego fragmentu/genomu. Sekwencjonowanie Sangera krótkich fragmentów może trwać kilka godzin. Sekwencjonowanie całego ludzkiego genomu za pomocą NGS, które kiedyś zajmowało lata, obecnie może być wykonane w ciągu kilku dni, a nawet kilkunastu godzin, w zależności od dostępnej infrastruktury i przepustowości platformy.
- Czy sekwencjonowanie DNA jest drogie?
- Koszty sekwencjonowania znacząco spadły na przestrzeni lat, zwłaszcza dzięki rozwojowi technologii NGS. Kiedyś sekwencjonowanie ludzkiego genomu kosztowało miliony dolarów, dziś jest to kwota rzędu kilkuset do kilku tysięcy dolarów, w zależności od zakresu sekwencjonowania (np. cały genom, egzom, panel genów) i dostawcy usług. Nadal jednak jest to inwestycja, zwłaszcza w przypadku dużych projektów badawczych.
- Jaka jest główna różnica między metodą Sangera a NGS?
- Główną różnicą jest przepustowość i sposób sekwencjonowania. Metoda Sangera sekwencjonuje pojedyncze, stosunkowo długie fragmenty DNA w sposób sekwencyjny. NGS natomiast umożliwia masowe, równoległe sekwencjonowanie milionów krótszych fragmentów DNA jednocześnie, co czyni ją znacznie szybszą i bardziej ekonomiczną do analizy dużych genomów i złożonych próbek.
- Kto korzysta z sekwencjonowania DNA?
- Z sekwencjonowania DNA korzystają naukowcy w laboratoriach badawczych (biologia, genetyka, mikrobiologia, ewolucja), lekarze i genetycy kliniczni (diagnostyka chorób, medycyna personalizowana), firmy biotechnologiczne (rozwój leków, inżynieria genetyczna), rolnicy i hodowcy (ulepszanie upraw i hodowli), a także organy ścigania i laboratoria kryminalistyczne.
Podsumowanie
Sekwencjonowanie DNA to jedna z najważniejszych technologii w historii biologii. Pozwoliło nam zajrzeć w najgłębsze warstwy kodu genetycznego, odczytać instrukcje, które kierują życiem, i wykorzystać tę wiedzę do niezliczonych celów. Od zrozumienia fundamentalnych procesów biologicznych, przez precyzyjną diagnostykę i leczenie chorób, po innowacje w rolnictwie i przemyśle – sekwencjonowanie DNA nieustannie poszerza granice naszej wiedzy i możliwości. W miarę dalszego rozwoju tej technologii, możemy spodziewać się jeszcze większych przełomów, które zmienią nasze życie i otworzą nowe, fascynujące perspektywy w nauce i medycynie.
Zainteresował Cię artykuł Sekwencjonowanie DNA: Klucz do Zrozumienia Życia? Zajrzyj też do kategorii Edukacja, znajdziesz tam więcej podobnych treści!

