24/10/2016
Białka stanowią fundament życia na Ziemi, będąc jednymi z najbardziej złożonych i wszechstronnych cząsteczek organicznych w naszych organizmach. Odpowiadają za niezliczone procesy biologiczne – od budowy komórek, przez transport substancji, po katalizowanie reakcji chemicznych. Ich niezwykła różnorodność wynika z unikalnej struktury, która przyjmuje ściśle określoną konformację przestrzenną. Wśród tej mnogości form i funkcji, jeden z podstawowych podziałów białek opiera się na ich kształcie, wyróżniając białka globularne i fibrylarne. Zrozumienie różnic między nimi jest kluczowe do pojęcia, jak te molekuły wykonują swoje specyficzne zadania. Zapraszamy w podróż po świecie białek, aby odkryć, dlaczego kształt ma tak fundamentalne znaczenie dla ich właściwości i funkcji.
Podstawy białek: Czym są i z czego się składają?
Zanim zagłębimy się w szczegóły dotyczące różnic między białkami globularnymi a fibrylarnymi, warto przypomnieć sobie ich podstawową budowę. Białka to polimery, czyli wielkocząsteczkowe związki chemiczne, które zbudowane są z mniejszych jednostek, zwanych aminokwasami. Te aminokwasy łączą się ze sobą w długie łańcuchy za pomocą specjalnych wiązań peptydowych. Wyobraź sobie koraliki nawleczone na nitkę – każdy koralik to aminokwas, a cała nitka to łańcuch białkowy. Liczba aminokwasów w jednym białku może być zdumiewająco duża, dochodząc nawet do tysiąca.
Każdy aminokwas ma unikalną budowę, zawierającą dwie kluczowe grupy funkcyjne: grupę aminową (NH2) na jednym końcu (tzw. N-koniec) oraz grupę karboksylową (COOH) na drugim (tzw. C-koniec). W przyrodzie występuje 20 rodzajów aminokwasów, które są podstawowymi "cegiełkami" do budowy wszystkich białek. Choć wszystkie zawierają atomy węgla, wodoru, tlenu i azotu, niektóre z nich, takie jak metionina, cystyna i cysteina, posiadają w swojej strukturze również atom siarki. To właśnie obecność siarki w cysteinie jest kluczowa dla powstawania tzw. mostków dwusiarczkowych, które odgrywają istotną rolę w stabilizacji trójwymiarowej struktury białek.
Architektura życia: Struktury białek
Kluczem do zrozumienia funkcji białek jest ich złożona struktura przestrzenna. Nie są to jedynie proste łańcuchy aminokwasów, ale skomplikowane, trójwymiarowe konstrukcje, które decydują o ich aktywności biologicznej. Wyróżniamy cztery poziomy organizacji struktury białek:
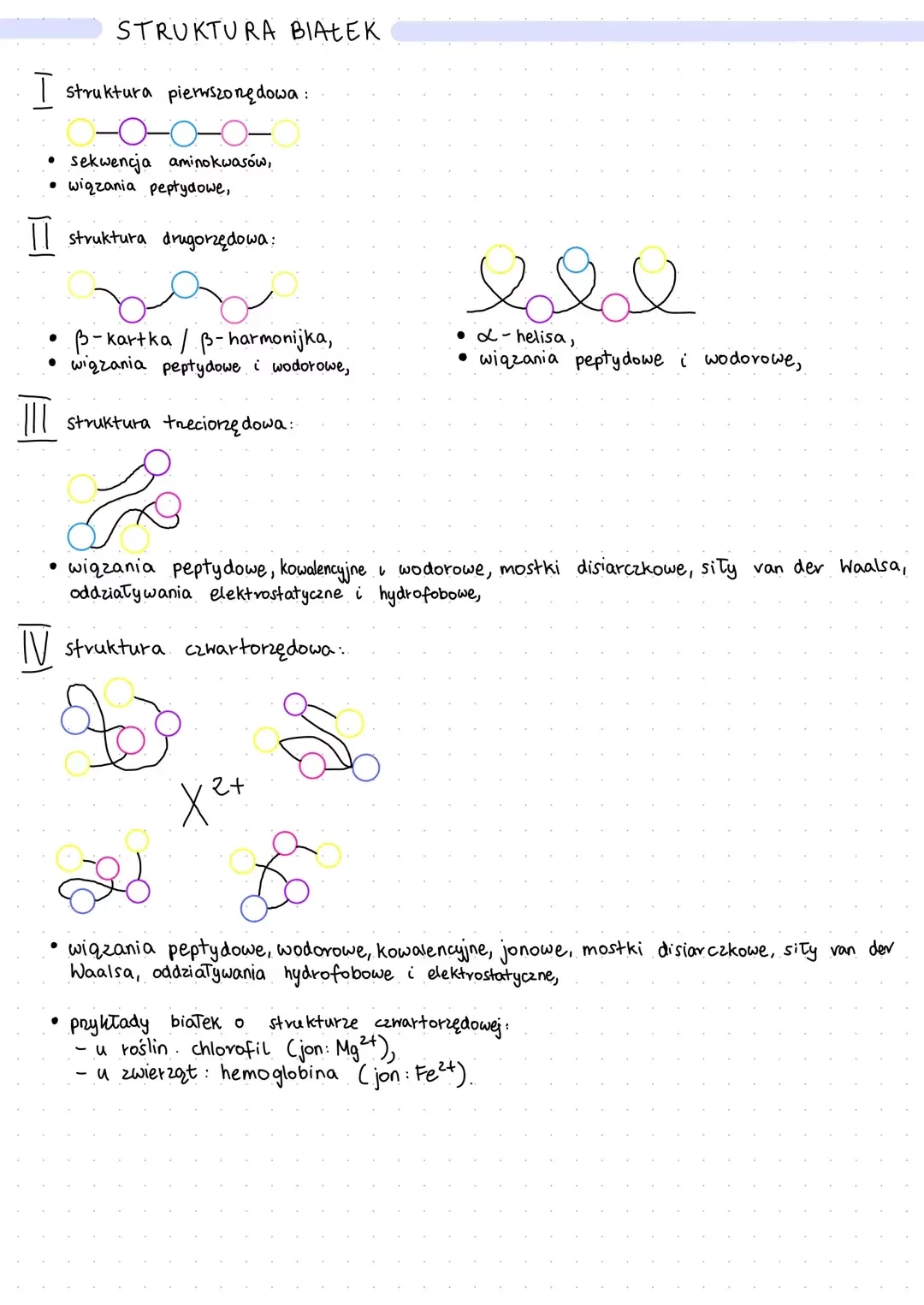
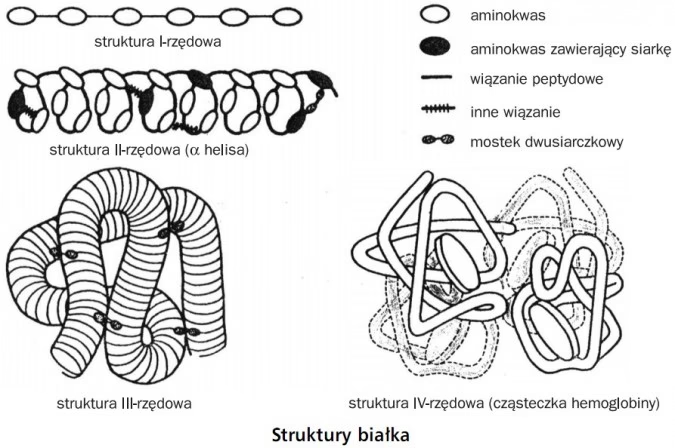
- Struktura pierwszorzędowa (pierwotna): To najprostszy poziom, który opisuje liniową sekwencję aminokwasów w łańcuchu polipeptydowym. Jest ona stabilizowana wyłącznie przez wiązania peptydowe. Ta sekwencja jest jak przepis na białko – decyduje o wszystkich kolejnych poziomach organizacji.
- Struktura drugorzędowa (wtórna): Powstaje w wyniku lokalnych oddziaływań między aminokwasami, najczęściej poprzez wiązania wodorowe. Przyjmuje ona dwie główne formy: alfa-helisy (prawoskrętne spirale) oraz beta-harmonijki (struktury przypominające "pogiętą kartkę"). To właśnie te wiązania wodorowe nadają białku pierwsze regularne kształty.
- Struktura trzeciorzędowa (wtórna): Jest to trójwymiarowa struktura przestrzenna całego łańcucha polipeptydowego. Powstaje w wyniku dalszego skręcania i wyginania struktur drugorzędowych, stabilizowanego przez różnorodne oddziaływania, takie jak wiązania wodorowe, oddziaływania jonowe, hydrofobowe, siły van der Waalsa, a co najważniejsze – wspomniane wcześniej mostki dwusiarczkowe, tworzące się pomiędzy resztami cysteiny. To właśnie struktura trzeciorzędowa nadaje białku jego unikalny kształt i funkcję.
- Struktura czwartorzędowa (wtórna): Ten poziom organizacji występuje tylko w białkach zbudowanych z kilku niezależnych łańcuchów polipeptydowych (podjednostek), które łączą się ze sobą w jedną funkcjonalną całość. Przykładem jest hemoglobina, składająca się z czterech podjednostek.
Warto pamiętać, że struktury drugorzędowa, trzeciorzędowa i czwartorzędowa są określane mianem struktur wtórnych białka, podczas gdy pierwszorzędowa to struktura pierwotna. Zachowanie tej precyzyjnej struktury przestrzennej jest absolutnie kluczowe dla prawidłowego funkcjonowania białka. Kiedy ta delikatna równowaga zostaje zaburzona przez czynniki takie jak wysoka temperatura (powyżej 50°C), drastyczne zmiany pH, detergenty, alkohole, stężone kwasy i zasady czy jony metali ciężkich, dochodzi do procesu zwanego denaturacją. Denaturacja to zniszczenie struktur wtórnych białka, co prowadzi do utraty jego właściwości biologicznych i jest zazwyczaj procesem nieodwracalnym. Klasycznym przykładem jest smażenie jajka – białko jaja ulega denaturacji, zmieniając konsystencję i tracąc swoje pierwotne właściwości.
Kształt ma znaczenie: Białka globularne vs. fibrylarne
Najbardziej intuicyjny podział białek, który bezpośrednio odnosi się do ich funkcji w organizmie, to klasyfikacja ze względu na ich kształt. Wyróżniamy dwie główne grupy: białka globularne i białka fibrylarne. Różnice między nimi są fundamentalne i wpływają na ich właściwości fizykochemiczne oraz role biologiczne.
Białka fibrylarne (włókienkowe)
Jak sama nazwa wskazuje, białka fibrylarne charakteryzują się wydłużonym, włókienkowym kształtem. Można je sobie wyobrazić jako długie nici lub pęki włókien. Ich struktura jest zazwyczaj bardzo uporządkowana i powtarzalna, co nadaje im wyjątkową wytrzymałość mechaniczną. Kluczową cechą białek fibrylarnych jest ich nierozpuszczalność w wodzie oraz w wodnych roztworach soli. Ta właściwość sprawia, że idealnie nadają się do pełnienia funkcji strukturalnych i ochronnych w organizmach.
Przykłady białek fibrylarnych:
- Keratyny: Są to jedne z najbardziej wytrzymałych białek w przyrodzie. Wchodzą w skład włosów, paznokci, kopyt, rogów i piór. Charakteryzują się dużą liczbą wiązań dwusiarczkowych, co dodatkowo zwiększa ich odporność i sztywność.
- Kolageny: To najobficiej występujące białka u ssaków, stanowiące około 25-35% wszystkich białek. Są głównym składnikiem tkanki łącznej – ścięgien, więzadeł, chrząstek, kości i skóry. Kolagen jest słabo rozpuszczalny w zimnej wodzie, ale po zagotowaniu tworzy żelatynę. Jego rola polega na zapewnieniu tkankom elastyczności i wytrzymałości na rozciąganie.
- Elastyna: Jak sama nazwa wskazuje, białko to odpowiada za elastyczność tkanek. Występuje w ścięgnach, więzadłach oraz ścianach naczyń krwionośnych, umożliwiając im rozciąganie i powrót do pierwotnego kształtu.
- Fibryna (powstająca z fibrynogenu): Fibrynogen występuje w osoczu krwi i jest białkiem rozpuszczalnym. Jednak w procesie krzepnięcia krwi, fibrynogen przekształca się w nierozpuszczalną fibrynę, tworząc sieć włókien, która stanowi podstawę skrzepu. Jest to doskonały przykład białka, które zmienia swoje właściwości (rozpuszczalność i kształt) w zależności od potrzeb organizmu.
- Fibroina: Główny składnik naturalnego jedwabiu, nadający mu jego charakterystyczną wytrzymałość i połysk.
Białka globularne (kuliste)
Białka globularne, w przeciwieństwie do fibrylarnych, przyjmują kształt znacznie zbliżony do kuli lub nieregularnej, zwartej bryły. Ich struktura jest bardziej złożona i często zawiera hydrofilowe grupy aminokwasów na zewnątrz, co sprawia, że są znacznie lepiej rozpuszczalne w wodzie i wodnych roztworach soli. Po rozpuszczeniu tworzą roztwory koloidalne, co jest kluczowe dla ich funkcji w płynach ustrojowych.
Przykłady białek globularnych:
- Albuminy: Są to jedne z najliczniejszych białek osocza krwi, a także występują w mleku, jajach i nasionach. Łatwo rozpuszczają się w wodzie i pełnią kluczowe funkcje transportowe (np. przenoszenie hormonów, kwasów tłuszczowych) oraz regulują ciśnienie osmotyczne krwi.
- Globuliny: Podobnie jak albuminy, są składnikami płynów ustrojowych. Dobrze rozpuszczają się w roztworach soli fizjologicznych. Wśród globulin wyróżniamy m.in. immunoglobuliny (przeciwciała), które pełnią funkcje obronne w układzie odpornościowym.
- Enzymy: Niemal wszystkie enzymy, które katalizują reakcje metaboliczne w komórkach, są białkami globularnymi. Ich kulisty kształt pozwala na precyzyjne tworzenie miejsca aktywnego, do którego pasują specyficzne substraty. Przykładem jest katalaza, enzym rozkładający nadtlenek wodoru.
- Mioglobina i Hemoglobina: Mioglobina magazynuje tlen w mięśniach, natomiast hemoglobina (białko złożone, chromoproteina) jest odpowiedzialna za transport tlenu w erytrocytach. Obie mają zwartą, kulistą strukturę.
- Miozyna i aktyna: Stanowią około 40% tkanki mięśniowej. Choć są zaangażowane w ruch i ich włókna oddziałują ze sobą, to pojedyncze cząsteczki aktyny i miozyny mają charakter globularny, a ich zdolność do „ślizgania się” po sobie umożliwia skurcz mięśni, działając jako „molekularny motor”.
- Hormony białkowe: Wiele hormonów, takich jak insulina czy adrenalina, ma budowę białkową i globularny kształt, co umożliwia im swobodne przemieszczanie się w płynach ustrojowych i oddziaływanie z receptorami.
Porównanie Białek Globularnych i Fibrylarnych
Aby jeszcze lepiej zobrazować różnice, przedstawiamy tabelę porównawczą:
| Cecha | Białka Fibrylarne (Włókienkowe) | Białka Globularne (Kuliste) |
|---|---|---|
| Kształt | Wydłużony, włókienkowaty, nitkowaty | Zbliżony do kuli, zwarty, nieregularny |
| Rozpuszczalność w wodzie | Nierozpuszczalne | Rozpuszczalne (tworzą roztwory koloidalne) |
| Wytrzymałość mechaniczna | Bardzo wysoka, duża odporność na rozciąganie | Zazwyczaj niższa, bardziej wrażliwe na zmiany środowiska |
| Funkcje główne | Strukturalne, ochronne, mechaniczne | Enzymatyczne, transportowe, regulacyjne, obronne, magazynujące |
| Przykłady | Keratyna, Kolagen, Elastyna, Fibryna, Fibroina | Albuminy, Globuliny, Enzymy (np. Katalaza), Hemoglobina, Mioglobina, Insulina, Aktyna, Miozyna |
| Stabilność | Bardzo stabilne, często dzięki licznym wiązaniom dwusiarczkowym | Mniej stabilne, łatwiej ulegają denaturacji |
Różnorodność w działaniu: Funkcje białek w organizmie
Niezależnie od kształtu, białka pełnią w organizmie niezliczone funkcje, które są absolutnie niezbędne do utrzymania życia. Ich wszechstronność wynika właśnie z unikalnej struktury przestrzennej, która pozwala im na specyficzne oddziaływania z innymi molekułami. Przyjrzyjmy się najważniejszym rolom białek:
- Funkcja strukturalna: Białka stanowią rusztowanie dla komórek i tkanek. Białka fibrylarne, takie jak kolagen i elastyna, budują tkankę łączną, zapewniając jej wytrzymałość i elastyczność. Keratyny tworzą struktury ochronne, takie jak włosy i paznokcie. Białka globularne, choć mniej kojarzone z funkcją strukturalną, są składnikami błon biologicznych, chromatyny jądrowej i cytoplazmy.
- Funkcja enzymatyczna (katalityczna): Białka globularne są niemal wyłącznie enzymami, które przyspieszają i kontrolują przebieg wszystkich reakcji metabolicznych w organizmie. Bez enzymów życie w znanej nam formie nie byłoby możliwe. Każdy enzym jest specyficzny dla swojej reakcji, a jego kulisty kształt jest kluczowy dla tworzenia miejsca aktywnego.
- Funkcja transportowa: Białka transportują różnorodne substancje w organizmie. Hemoglobina (białko globularne) jest odpowiedzialna za przenoszenie tlenu z płuc do tkanek i dwutlenku węgla w odwrotnym kierunku. Albuminy (również globularne) transportują kwasy tłuszczowe, hormony i leki. W błonach komórkowych białka tworzą specyficzne przenośniki i kanały jonowe, umożliwiające selektywny transport substancji przez błonę.
- Funkcja regulacyjna i hormonalna: Wiele hormonów, które regulują procesy fizjologiczne, ma budowę białkową (np. insulina regulująca poziom cukru we krwi, adrenalina). Białka receptorowe na powierzchni komórek odbierają sygnały z otoczenia, umożliwiając komunikację międzykomórkową.
- Funkcja obronna (immunologiczna): Immunoglobuliny, czyli przeciwciała (białka globularne), są kluczowymi elementami układu odpornościowego. Rozpoznają i neutralizują patogeny, chroniąc organizm przed infekcjami.
- Funkcja magazynująca: Niektóre białka magazynują ważne substancje. Przykładem jest ferrytyna (metaloproteina), która magazynuje żelazo w organizmie, czy mioglobina magazynująca tlen w mięśniach.
- Funkcja ruchowa (kurczliwa): Aktyna i miozyna (białka globularne, które tworzą fibrylarne struktury w mięśniach) są odpowiedzialne za skurcz mięśni, umożliwiając ruch.
- Inne funkcje: Białka biorą również udział w naprawie tkanek, regulacji równowagi wodnej, procesie widzenia (np. rodopsyna) i wielu innych, bardziej wyspecjalizowanych procesach.
Białka w diecie: Dlaczego są kluczowe?
Białka są nie tylko budulcem i maszynami w naszym ciele, ale także kluczowym składnikiem naszej diety. Organizm ludzki nie jest w stanie samodzielnie syntetyzować wszystkich aminokwasów (tzw. aminokwasy egzogenne), dlatego muszą być one dostarczane z pożywieniem. W kontekście żywienia, białka dzielimy na:
- Białka pełnowartościowe: Zawierają wszystkie niezbędne aminokwasy egzogenne w odpowiednich proporcjach. Ich głównym źródłem jest pokarm pochodzenia zwierzęcego, np. mięso, ryby, jaja, mleko i produkty mleczne.
- Białka niepełnowartościowe: Nie zawierają pełnego kompletu niezbędnych aminokwasów lub występują one w niewystarczających proporcjach. Źródłem białka niepełnowartościowego jest głównie pokarm roślinny. Dlatego w diecie wegetariańskiej i wegańskiej niezwykle ważne jest odpowiednie bilansowanie posiłków, aby zapewnić organizmowi wszystkie niezbędne aminokwasowe. Kombinowanie różnych źródeł białka roślinnego (np. rośliny strączkowe z zbożami) pozwala na uzupełnienie brakujących aminokwasów.
Wartość odżywcza białka zależy nie tylko od zawartości aminokwasów egzogennych i endogennych, ale także od ich wzajemnych proporcji, które powinny być zbliżone do proporcji występujących w białku ustrojowym, oraz od strawności produktów białkowych. Dlatego jakość i źródło białka w diecie mają ogromne znaczenie dla zdrowia i prawidłowego funkcjonowania organizmu.

Często Zadawane Pytania (FAQ)
Co to jest denaturacja białek?
Denaturacja białek to proces, w którym białko traci swoją naturalną, trójwymiarową strukturę przestrzenną (strukturę drugorzędową, trzeciorzędową, a czasem czwartorzędową), zachowując jedynie strukturę pierwszorzędową (sekwencję aminokwasów). Jest to zazwyczaj proces nieodwracalny, prowadzący do utraty właściwości biologicznych białka. Może być wywołana przez wysoką temperaturę, skrajne pH, sole metali ciężkich, alkohole, detergenty i inne czynniki.
Czy wszystkie białka są rozpuszczalne w wodzie?
Nie, nie wszystkie białka są rozpuszczalne w wodzie. Białka dzielimy pod tym względem na dwie główne kategorie: białka globularne, które są zazwyczaj dobrze rozpuszczalne w wodzie i wodnych roztworach soli (tworząc roztwory koloidalne), oraz białka fibrylarne, które są nierozpuszczalne w wodzie i pełnią funkcje strukturalne.
Jakie są główne funkcje białek?
Białka pełnią w organizmach wiele kluczowych funkcji. Do najważniejszych należą: funkcja strukturalna (budują komórki i tkanki), enzymatyczna (katalizują reakcje chemiczne), transportowa (przenoszą substancje, np. tlen), regulacyjna (np. hormony), obronna (przeciwciała), magazynująca (np. żelazo) oraz ruchowa (umożliwiają skurcz mięśni).

Czym różnią się białka proste od złożonych?
Białka proste (proteiny) zbudowane są wyłącznie z aminokwasów. Natomiast białka złożone (proteidy) oprócz aminokwasów posiadają dodatkowe, niebiałkowe składniki, takie jak lipidy (lipoproteiny), węglowodany (glikoproteiny), kwasy nukleinowe (nukleoproteiny), reszty kwasu fosforowego (fosfoproteiny) czy atomy metali (metaloproteiny). Te dodatkowe składniki często są kluczowe dla ich specyficznych funkcji.
Dlaczego kształt białka jest tak ważny?
Kształt białka, czyli jego trójwymiarowa struktura przestrzenna, jest absolutnie fundamentalny dla jego funkcji. To właśnie unikalny kształt białka decyduje o tym, jak białko oddziałuje z innymi cząsteczkami, czy może pełnić rolę enzymu, transportera, czy elementu strukturalnego. Nawet niewielka zmiana w kształcie, np. w wyniku denaturacji, może całkowicie uniemożliwić białku wykonywanie jego biologicznej roli.
Podsumowując, białka, choć wszystkie zbudowane z aminokwasów, wykazują zdumiewającą różnorodność kształtów i funkcji. Podział na białka globularne i fibrylarne jest jednym z kluczowych sposobów ich klasyfikacji, odzwierciedlającym ich odmienne właściwości fizyczne i biologiczne. Białka fibrylarne, o włókienkowym kształcie i nierozpuszczalne w wodzie, są mistrzami wytrzymałości i budulca, tworząc struktury takie jak włosy, paznokcie czy kolagen. Białka globularne, o kulistym kształcie i rozpuszczalne w wodzie, pełnią dynamiczne role enzymów, transporterów i hormonów, niezbędne dla funkcjonowania procesów życiowych. Zrozumienie tych różnic pozwala docenić niezwykłą precyzję i złożoność, z jaką natura konstruuje molekuły niezbędne do podtrzymania życia.
Zainteresował Cię artykuł Białka Globularne kontra Fibrylarne: Kluczowe Różnice? Zajrzyj też do kategorii Biologia, znajdziesz tam więcej podobnych treści!
