14/07/2014
Witaj w świecie molekularnych cudów! Jeśli kiedykolwiek zastanawiałeś się, jak Twoje ciało trawi jedzenie, jak rośliny przetwarzają światło słoneczne w energię, lub jak w ogóle możliwe jest utrzymanie życia na poziomie komórkowym, odpowiedź często sprowadza się do jednego słowa: enzymy. Te niezwykłe białka, a czasami cząsteczki RNA, są prawdziwymi bohaterami biochemii, kontrolując tempo i przebieg niezliczonych reakcji chemicznych, które są niezbędne dla funkcjonowania każdego organizmu żywego.

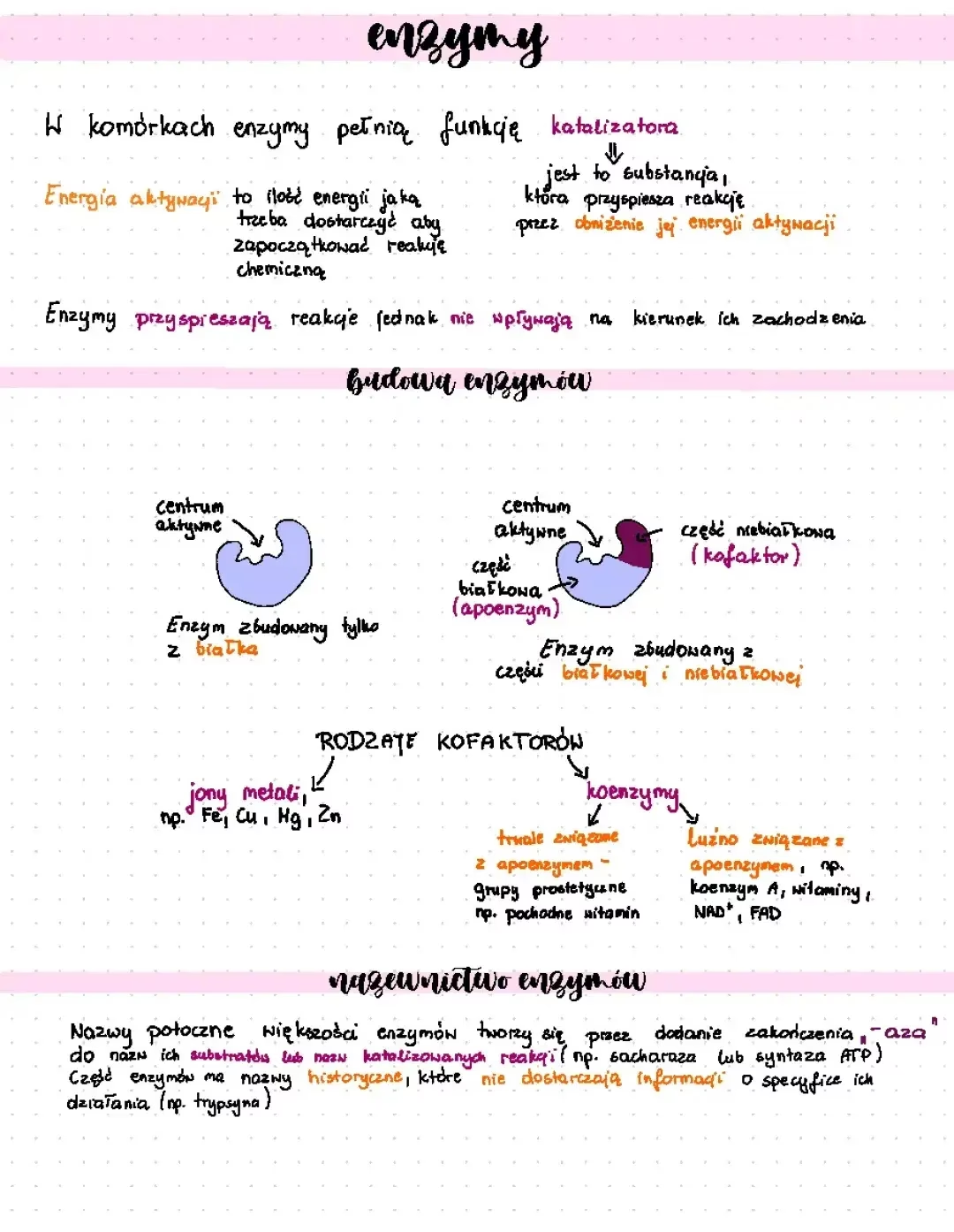
Na poziomie biologii rozszerzonej, zrozumienie enzymów to podstawa. Są to biologiczne katalizatory, co oznacza, że przyspieszają reakcje chemiczne bez bycia w nich zużywanymi. Wyobraź sobie, że każda komórka to miniaturowa fabryka, a enzymy to wyspecjalizowani pracownicy, którzy sprawiają, że wszystkie procesy produkcyjne zachodzą w odpowiednim tempie i we właściwym miejscu. Bez nich, większość reakcji zachodziłaby tak wolno, że życie, jakie znamy, byłoby niemożliwe.
Czym Dokładnie Są Enzymy?
Większość enzymów to złożone białka, zbudowane z długich łańcuchów aminokwasów, które zwijają się w unikalne, trójwymiarowe kształty. Ten specyficzny kształt jest kluczowy dla ich funkcji. Każdy enzym posiada tzw. miejsce aktywne – to unikalna kieszeń lub szczelina, do której idealnie pasuje tylko jedna, konkretna cząsteczka lub grupa cząsteczek, zwana substratem. Podobieństwo do klucza i zamka jest tu niezwykle trafne.
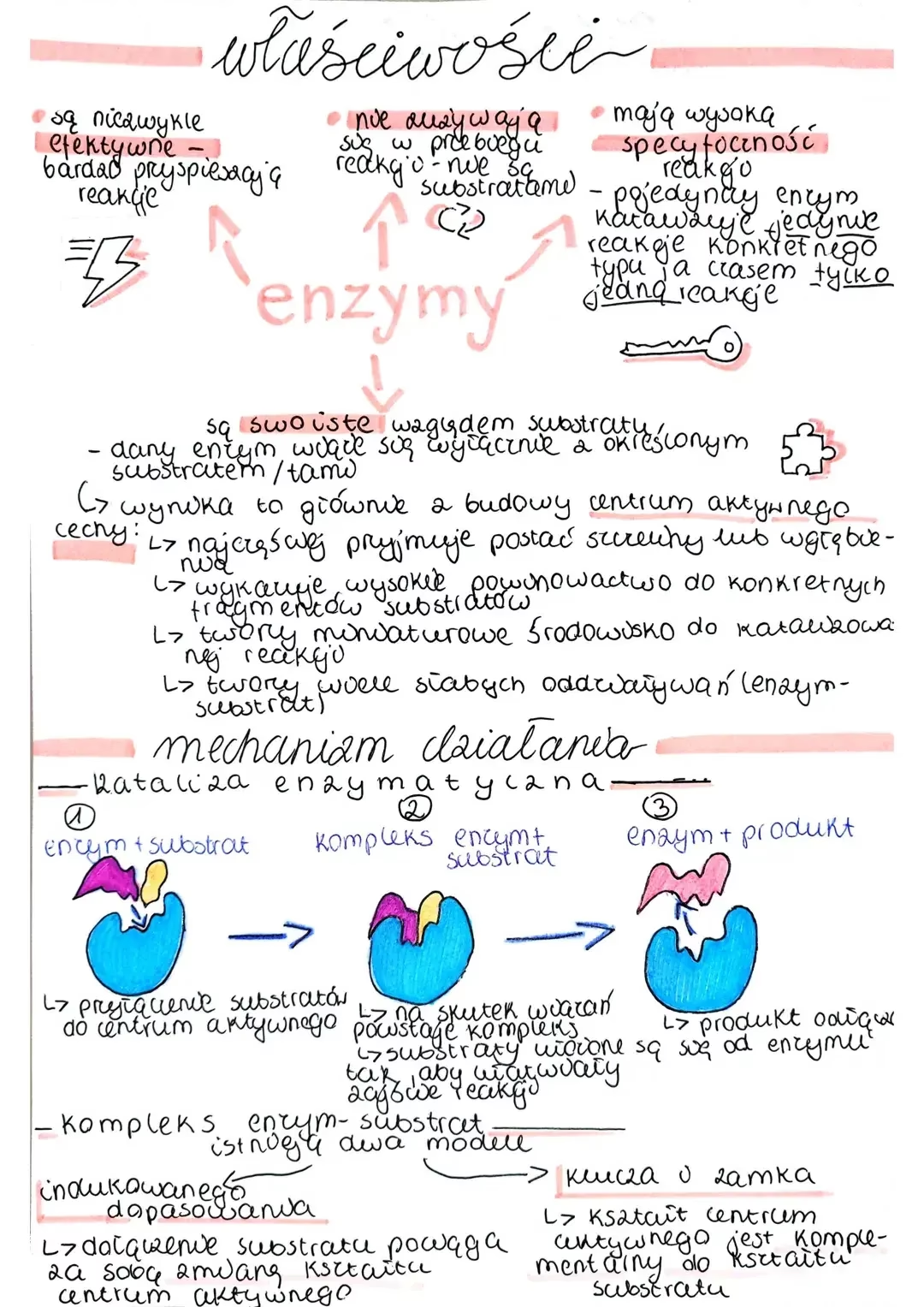
Model Klucza i Zamka kontra Dopasowanie Indukowane
Początkowo, w 1894 roku, niemiecki chemik Emil Fischer zaproponował model „klucza i zamka” dla działania enzymów. Zgodnie z nim, miejsce aktywne enzymu ma sztywny, niezmienny kształt, który jest komplementarny do kształtu substratu, tak jak klucz pasuje do konkretnego zamka. Substrat idealnie wpasowuje się w miejsce aktywne, tworząc kompleks enzym-substrat. Następnie, w miejscu aktywnym zachodzi reakcja chemiczna, a powstałe produkty są uwalniane, pozostawiając enzym gotowy do kolejnej reakcji.
Jednakże, z biegiem czasu i postępem wiedzy, naukowcy zauważyli, że model ten nie wyjaśnia wszystkich obserwacji. W 1958 roku Daniel Koshland zaproponował bardziej dynamiczny model, znany jako „dopasowanie indukowane” (ang. induced fit). Według tej koncepcji, miejsce aktywne enzymu nie jest sztywne, lecz elastyczne. Kiedy substrat zbliża się do enzymu i zaczyna się z nim wiązać, wywołuje to niewielkie zmiany konformacyjne w enzymie. Enzym niejako „dopasowuje się” do substratu, obejmując go i zapewniając optymalne ułożenie do zajścia reakcji. To dopasowanie jest dwustronne – zarówno enzym, jak i substrat, ulegają subtelnym zmianom, które maksymalizują efektywność katalizy. Ten model lepiej oddaje dynamiczną naturę interakcji molekularnych w komórce.
Jak Enzymy Przyspieszają Reakcje?
Kluczową rolą enzymów jest obniżanie energii aktywacji. Wyobraź sobie wzgórze, które musisz pokonać, aby dostać się na drugą stronę. Energia aktywacji to wysokość tego wzgórza – ilość energii, jaką musisz włożyć, aby reakcja w ogóle mogła zajść. Enzymy działają jak tunele przez to wzgórze, znacznie skracając drogę i zmniejszając potrzebną energię. Dzięki temu reakcje, które normalnie trwałyby miliony lat, w obecności enzymów zachodzą w ułamku sekundy.
Enzymy osiągają to na kilka sposobów:
- Orientacja substratów: Zbliżają substraty do siebie w odpowiedniej orientacji przestrzennej, ułatwiając im zderzenia.
- Wytwarzanie odpowiedniego środowiska: Tworzą w miejscu aktywnym mikrośrodowisko (np. specyficzne pH, obecność jonów), które sprzyja reakcji.
- Naprężanie wiązań: Mogą delikatnie „rozciągać” lub naprężać wiązania w substracie, co ułatwia ich rozerwanie.
- Uczestnictwo w reakcji: Niektóre enzymy tymczasowo tworzą kowalencyjne wiązania z substratem, tworząc niestabilne pośrednie, które szybko przekształcają się w produkty.
Czynniki Wpływające na Aktywność Enzymów
Aktywność enzymów jest niezwykle wrażliwa na warunki środowiska. Zrozumienie tych czynników jest kluczowe dla ich funkcjonowania w organizmach żywych i wykorzystania w przemyśle.
1. Temperatura
Każdy enzym ma swoją temperaturę optymalną, w której jego aktywność jest największa. Dla większości enzymów w organizmach ludzkich wynosi ona około 37°C. Podwyższenie temperatury powyżej optimum początkowo zwiększa aktywność enzymu (zwiększa energię kinetyczną cząsteczek, co prowadzi do częstszych zderzeń substratu z enzymem). Jednak zbyt wysoka temperatura powoduje denaturację enzymu – jego trójwymiarowa struktura ulega nieodwracalnym zmianom, szczególnie w miejscu aktywnym, co prowadzi do utraty funkcji. Z kolei obniżenie temperatury spowalnia ruch cząsteczek, zmniejszając aktywność enzymu, ale zazwyczaj nie powoduje denaturacji – po powrocie do optymalnej temperatury enzym odzyskuje aktywność.
2. pH
Podobnie jak temperatura, pH środowiska ma ogromny wpływ na aktywność enzymów. Każdy enzym ma swoje optymalne pH, w którym jego aktywność jest największa. Skrajne wartości pH (zarówno bardzo kwaśne, jak i bardzo zasadowe) mogą prowadzić do denaturacji enzymu poprzez zmianę ładunków elektrycznych aminokwasów, co zakłóca delikatne wiązania utrzymujące strukturę przestrzenną. Na przykład, pepsyna (enzym trawiący białka w żołądku) działa optymalnie w bardzo kwaśnym środowisku (pH 1.5-2.5), podczas gdy trypsyna (enzym trawiący białka w jelicie cienkim) preferuje środowisko zasadowe (pH 8).
3. Stężenie Substratu
W miarę zwiększania stężenia substratu, szybkość reakcji enzymatycznej rośnie, ponieważ więcej cząsteczek substratu jest dostępnych do wiązania się z miejscami aktywnymi enzymów. Jednak w pewnym momencie osiąga się maksymalną szybkość reakcji (Vmax). Dzieje się tak, gdy wszystkie miejsca aktywne enzymów są zajęte przez substrat – enzymy są „nasycone”. Dalsze zwiększanie stężenia substratu nie spowoduje już wzrostu szybkości reakcji, chyba że zwiększy się również ilość enzymu.
4. Stężenie Enzymu
Przy stałym, nasycającym stężeniu substratu, zwiększanie stężenia enzymu powoduje liniowy wzrost szybkości reakcji. Im więcej cząsteczek enzymu jest dostępnych, tym więcej miejsc aktywnych może jednocześnie przetwarzać substrat, co przekłada się na szybsze powstawanie produktów.
5. Inhibitory i Aktywatory
Niektóre cząsteczki mogą wpływać na aktywność enzymów poprzez wiązanie się z nimi. Inhibitory to substancje, które zmniejszają lub całkowicie blokują aktywność enzymu. Mogą działać konkurencyjnie (konkurując z substratem o miejsce aktywne) lub niekonkurencyjnie (wiążąc się z enzymem w innym miejscu i zmieniając kształt miejsca aktywnego). Aktywatory natomiast zwiększają aktywność enzymu. Kontrola aktywności enzymów za pomocą inhibitorów i aktywatorów jest kluczowym mechanizmem regulacji metabolicznej w komórkach.
Enzymy w Organizmach Żywych: Niezliczone Funkcje
Rola enzymów w biologii jest nie do przecenienia. Są one zaangażowane praktycznie we wszystkie procesy życiowe:
- Trawienie: Enzymy trawienne, takie jak amylaza (rozkładająca węglowodany), proteazy (trawiące białka, np. pepsyna, trypsyna) i lipazy (trawiące tłuszcze), rozkładają złożone cząsteczki pokarmowe na mniejsze, przyswajalne jednostki.
- Oddychanie komórkowe: Cały szlak oddychania komórkowego, od glikolizy po cykl Krebsa i łańcuch transportu elektronów, jest precyzyjnie regulowany przez setki enzymów, które kontrolują uwalnianie energii z glukozy.
- Fotosynteza: W roślinach, enzymy takie jak RuBisCO (rybulozo-1,5-bisfosforanokarboksylaza/oksygenaza) są kluczowe w cyklu Calvina, odpowiedzialnym za wiązanie dwutlenku węgla i produkcję cukrów.
- Replikacja i naprawa DNA: Enzymy takie jak polimerazy DNA i ligazy są niezbędne do kopiowania materiału genetycznego oraz naprawy wszelkich uszkodzeń, zapewniając stabilność genomu.
- Synteza białek: Enzymy są zaangażowane w każdy etap syntezy białek, od transkrypcji po translację, zapewniając prawidłowe tworzenie nowych cząsteczek.
- Detoksykacja: Enzymy w wątrobie (np. cytochrom P450) odgrywają kluczową rolę w neutralizowaniu toksyn i leków.
Tabela Porównawcza Enzymów Trawiennych Człowieka
| Enzym | Miejsce Produkcji | Miejsce Działania | Optymalne pH | Substrat | Produkt |
|---|---|---|---|---|---|
| Amylaza ślinowa | Ślinianki | Jama ustna | ~6.7 | Skrobia | Dekstryny, maltoza |
| Pepsyna | Żołądek | Żołądek | 1.5 - 2.5 | Białka | Krótkie peptydy |
| Trypsyna | Trzustka | Jelito cienkie | ~8.0 | Białka, peptydy | Krótkie peptydy |
| Lipaza trzustkowa | Trzustka | Jelito cienkie | ~8.0 | Tłuszcze (triglicerydy) | Kwasy tłuszczowe, monoglicerydy |
| Laktaza | Jelito cienkie | Jelito cienkie | ~6.0 | Laktoza | Glukoza, galaktoza |
Zastosowania Enzymów w Przemyśle i Medycynie
Zrozumienie działania enzymów otworzyło drogę do ich szerokiego zastosowania poza żywymi organizmami. Ich specyficzność i efektywność czynią je cennymi narzędziami w wielu dziedzinach.
W Przemyśle
Enzymy są wykorzystywane w przemyśle spożywczym, tekstylnym, detergentowym, papierniczym, a nawet w produkcji biopaliw. Oto kilka przykładów:
- Przemysł spożywczy:
- Fermentacja: Enzymy drożdży są kluczowe w produkcji piwa, wina (przekształcanie cukru w alkohol) i chleba (powstawanie dwutlenku węgla, który powoduje wzrost ciasta).
- Produkcja sera: Podpuszczka (zawierająca enzym chymozynę) jest używana do koagulacji mleka.
- Soki owocowe: Pektynazy rozkładają pektyny, zwiększając klarowność i wydajność soków.
- Syropy glukozowo-fruktozowe: Enzymy izomerazy przekształcają glukozę we fruktozę.
- Detergenty: Enzymy takie jak proteazy (rozkładające białka, np. plamy z krwi, trawy), lipazy (rozkładające tłuszcze, np. plamy z oleju) i amylazy (rozkładające skrobię, np. plamy z sosu) są dodawane do proszków do prania, aby skuteczniej usuwać zabrudzenia w niższych temperaturach.
- Przemysł tekstylny: Celulazy są używane do zmiękczania dżinsu i usuwania jego zmechaceń.
- Produkcja biopaliw: Enzymy są wykorzystywane do rozkładania biomasy roślinnej na cukry, które mogą być następnie fermentowane do produkcji etanolu.
W Medycynie
Enzymy odgrywają również znaczącą rolę w diagnostyce i leczeniu wielu chorób:
- Diagnostyka: Poziom pewnych enzymów we krwi może wskazywać na uszkodzenie organów. Na przykład, podwyższony poziom aminotransferazy alaninowej (ALT) lub asparaginianowej (AST) może świadczyć o uszkodzeniu wątroby, a kinazy kreatynowej (CK) o zawale serca. Testy enzymatyczne są również wykorzystywane do wykrywania chorób genetycznych.
- Terapia: Niektóre enzymy są stosowane jako leki. Na przykład, streptokinaza i urokinaza są używane do rozpuszczania zakrzepów krwi u pacjentów z zawałem serca lub udarem. Enzymy proteolityczne mogą być stosowane w leczeniu stanów zapalnych lub do wspomagania gojenia ran poprzez usuwanie martwych tkanek. W niektórych chorobach genetycznych, takich jak choroba Gauchera, pacjentom podaje się brakujący enzym (enzymatyczna terapia zastępcza).
Pytania i Odpowiedzi (FAQ)
1. Czy wszystkie enzymy to białka?
Większość enzymów to białka. Jednak istnieją również enzymy zbudowane z RNA, nazywane rybozymami. Przykładem rybozymu jest rRNA w rybosomach, które katalizuje tworzenie wiązań peptydowych podczas syntezy białek.
2. Czy enzymy są zużywane w reakcjach?
Nie, enzymy są katalizatorami, co oznacza, że przyspieszają reakcje, ale nie są w nich zużywane. Po przekształceniu substratu w produkt, enzym uwalnia produkt i jest gotowy do katalizowania kolejnej reakcji. Dzięki temu niewielka ilość enzymu może przetworzyć dużą ilość substratu.
3. Co to jest denaturacja enzymu?
Denaturacja to proces, w którym trójwymiarowa struktura enzymu (zwłaszcza miejsce aktywne) ulega nieodwracalnym zmianom, najczęściej pod wpływem zbyt wysokiej temperatury, skrajnego pH, silnych kwasów, zasad, metali ciężkich lub rozpuszczalników organicznych. Denaturacja powoduje utratę funkcji enzymu, ponieważ jego miejsce aktywne nie jest już w stanie prawidłowo wiązać substratu i katalizować reakcji.
4. Czym różni się model klucza i zamka od dopasowania indukowanego?
Model klucza i zamka zakłada, że miejsce aktywne enzymu ma sztywny, niezmienny kształt, który idealnie pasuje do substratu. Model dopasowania indukowanego jest bardziej dynamiczny; sugeruje, że miejsce aktywne enzymu jest elastyczne i zmienia swój kształt po związaniu się z substratem, aby zapewnić optymalne dopasowanie i warunki do reakcji. Ten drugi model jest obecnie powszechniej akceptowany, ponieważ lepiej wyjaśnia złożoność interakcji enzym-substrat.
5. Co się dzieje, gdy enzymy nie działają prawidłowo?
Nieprawidłowe funkcjonowanie enzymów może prowadzić do poważnych problemów zdrowotnych i chorób metabolicznych. Na przykład, brak lub defekt enzymu laktazy powoduje nietolerancję laktozy, uniemożliwiając trawienie cukru mlecznego. Choroby spichrzeniowe, takie jak choroba Gauchera czy mukowiscydoza, są często spowodowane brakiem lub defektem konkretnych enzymów, co prowadzi do gromadzenia się szkodliwych substancji w komórkach. Wiele leków działa poprzez celowanie w konkretne enzymy, hamując ich aktywność w przypadku chorób.
Podsumowując, enzymy są absolutnie fundamentalne dla życia. Ich precyzyjna kontrola nad reakcjami biochemicznymi sprawia, że są nie tylko fascynującym obiektem badań, ale także niezastąpionym narzędziem w biotechnologii i medycynie. Zrozumienie ich struktury, mechanizmów działania i czynników wpływających na ich aktywność to klucz do głębszego poznania procesów życiowych i otwieranie nowych dróg w nauce i technologii.
Zainteresował Cię artykuł Enzymy: Klucz do Życia i Biologii na Poziomie 2? Zajrzyj też do kategorii Biologia, znajdziesz tam więcej podobnych treści!

