05/11/2006
Alkohole to niezwykle ważna klasa związków organicznych, odgrywająca kluczową rolę zarówno w przyrodzie, jak i w przemyśle. Ich wszechstronność wynika z obecności grupy hydroksylowej (-OH), która nadaje im specyficzne właściwości fizyczne i chemiczne. Zrozumienie reakcji, w jakie wchodzą alkohole, jest fundamentalne dla każdego, kto zgłębia tajniki chemii organicznej. Od prostych alkoholów, takich jak metanol czy etanol, po bardziej złożone, wszystkie charakteryzują się zdolnością do szeregu przekształceń, które pozwalają na ich syntezę, modyfikację i identyfikację. W tym artykule przyjrzymy się najważniejszym reakcjom chemicznym alkoholi, zwracając uwagę na ich mechanizmy, warunki przebiegu oraz praktyczne zastosowania.
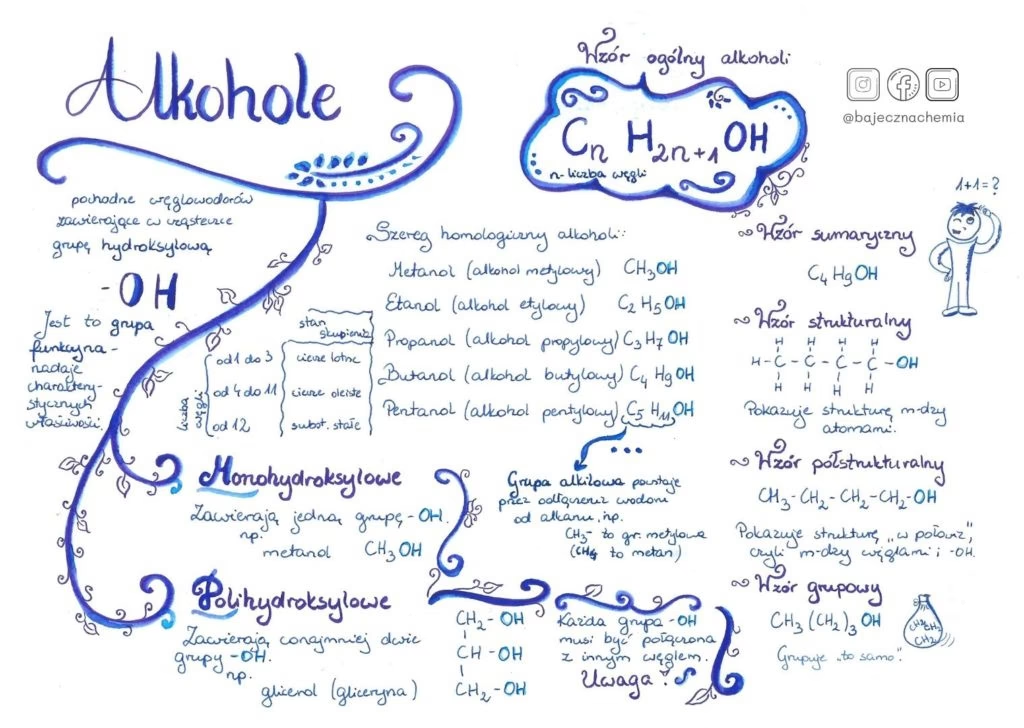
Alkohole monohydroksylowe, czyli takie, w których jedna grupa hydroksylowa (-OH) jest przyłączona do atomu węgla o hybrydyzacji sp³, posiadają ogólny wzór CnH₂n₊₁OH. Są to związki o ogromnym znaczeniu praktycznym, używane w syntezach chemicznych, przemyśle farmaceutycznym, jako rozpuszczalniki, a także jako paliwa. Ich reaktywność jest ściśle związana z rzędowością atomu węgla, do którego przyłączona jest grupa -OH. To właśnie ta klasyfikacja jest kluczem do przewidywania ich zachowania w różnych warunkach reakcji.
Podstawowe Klasyfikacje Alkoholi – Klucz do Zrozumienia Reaktywności
Rzędowość alkoholi odnosi się do liczby atomów węgla, z którymi jest bezpośrednio połączony atom węgla niosący grupę hydroksylową. To rozróżnienie jest fundamentalne, ponieważ decyduje o ich reaktywności, zwłaszcza w reakcjach utleniania i substytucji.
- Alkohole I-rzędowe (pierwszorzędowe): Grupa -OH jest związana z atomem węgla, który jest połączony z jednym innym atomem węgla lub tylko z atomami wodoru (np. metanol CH₃OH, etanol CH₃CH₂OH). Ten typ alkoholi charakteryzuje się dużą reaktywnością w procesach utleniania.
- Alkohole II-rzędowe (drugorzędowe): Grupa -OH jest połączona z atomem węgla, który jest połączony z dwoma innymi atomami węgla (np. izopropanol CH₃CHOHCH₃). Alkohole drugorzędowe również łatwo ulegają utlenianiu, ale do innych produktów niż alkohole pierwszorzędowe.
- Alkohole III-rzędowe (trzeciorzędowe): Grupa -OH jest połączona z atomem węgla, który jest połączony z trzema innymi atomami węgla (np. tert-butanol (CH₃)₃COH). Alkohole trzeciorzędowe są najbardziej oporne na utlenianie, co jest ich charakterystyczną cechą.
Utlenianie Alkoholi: Od Aldehydów po Kwasy Karboksylowe
Utlenianie to jedna z najważniejszych reakcji chemicznych, jakim ulegają alkohole. Proces ten polega na usunięciu atomów wodoru lub dodaniu atomów tlenu do cząsteczki organicznej. W przypadku alkoholi, przebieg utleniania i produkty końcowe zależą od ich rzędowości oraz siły użytego utleniacza. Symbolicznym przedstawieniem utleniacza w równaniach chemicznych jest często symbol [O] nad strzałką reakcji, co oznacza, że użyto niesprecyzowanego czynnika utleniającego, który usuwa atomy wodoru lub dodaje atomy tlenu.
Utlenianie Alkoholi I-rzędowych
Alkohole pierwszorzędowe mogą być utleniane dwuetapowo, w zależności od warunków i użytego utleniacza:
- Do aldehydów: W kontrolowanych warunkach, przy użyciu łagodnych utleniaczy, takich jak chlorek pirydyniowo-chromowy (PCC) lub tlenek miedzi(II) (CuO), alkohole I-rzędowe przekształcają się w aldehydy. Reakcja jest delikatna i pozwala zatrzymać utlenianie na etapie aldehydu. Przykładowo: CH₃CH₂OH + PCC → CH₃CHO + H₂O.
- Do kwasów karboksylowych: Gdy reakcja jest przeprowadzana w bardziej agresywnych warunkach, np. w środowisku kwaśnym z silnymi utleniaczami, takimi jak nadmanganian potasu (KMnO₄) lub dichromian(VI) potasu (K₂Cr₂O₇), alkohole I-rzędowe utleniają się bezpośrednio do kwasów karboksylowych. Jest to całkowite utlenienie. Przykładowo: 3CH₃CH₂OH + K₂Cr₂O₇ + 4H₂SO₄ → 3CH₃COOH + Cr₂(SO₄)₃ + K₂SO₄ + 7H₂O.
Utlenianie Alkoholi II-rzędowych
Alkohole drugorzędowe ulegają utlenieniu do ketonów. Jest to jedyny możliwy produkt utleniania, ponieważ atom węgla związany z grupą -OH nie posiada już żadnego atomu wodoru, który mógłby zostać dalej utleniony. Ketony są stosunkowo odporne na dalsze utlenianie, co ułatwia ich izolację. Przykładowo: CH₃CHOHCH₃ + PCC → CH₃COCH₃ + H₂O. Podobnie, silne utleniacze, takie jak KMnO₄ czy K₂Cr₂O₇, również prowadzą do powstania ketonów.
Utlenianie Alkoholi III-rzędowych
Alkohole trzeciorzędowe są odporne na utlenianie w standardowych warunkach. Dzieje się tak, ponieważ atom węgla, do którego przyłączona jest grupa -OH, nie posiada żadnego atomu wodoru, który mógłby zostać usunięty w procesie utleniania. W reakcjach utleniania alkoholi kluczowe jest utworzenie podwójnego wiązania węgiel-tlen, co wymaga usunięcia atomu wodoru z tego węgla. W przypadku alkoholi trzeciorzędowych, atom węgla jest związany tylko z innymi atomami węgla, a wiązania węgiel-węgiel są znacznie trudniejsze do zerwania w łagodnych warunkach utleniania. Dopiero w ekstremalnych warunkach (wysokie temperatury, stężone utleniacze) może dojść do rozerwania łańcucha węglowego.
Porównanie Utleniaczy
W chemii organicznej rozróżnia się utleniacze słabe i mocne, co ma kluczowe znaczenie dla przebiegu reakcji utleniania alkoholi:
| Słabe Utleniacze | Mocne Utleniacze |
|---|---|
| ➤ CuO (tlenek miedzi(II)) | ➤ KMnO₄ / H⁺ (nadmanganian potasu w środowisku kwaśnym) |
| ➤ PCC (chlorokromian pirydyniowy) | ➤ K₂Cr₂O₇ / H⁺ (dichromian(VI) potasu w środowisku kwaśnym) |
| ➤ CrO₃ / H⁺ (tlenek chromu(VI) w środowisku kwaśnym) | |
| Utleniają alkohole I-rzędowe do aldehydów, II-rzędowe do ketonów. | Utleniają alkohole I-rzędowe do kwasów karboksylowych, II-rzędowe do ketonów. |
| Z tlenku miedzi tworzy się miedź metaliczna. | Powstają jony manganu(II) lub chromu(III). |
Dehydratacja Alkoholi: Droga do Alkenów i Eterów
Dehydratacja, czyli eliminacja wody z cząsteczki alkoholu, to kolejna fundamentalna reakcja. Reakcja ta prowadzi do powstania związków nienasyconych – alkenów. Jest to proces odwrotny do hydratacji alkenów. Aby reakcja zaszła, potrzebny jest silny czynnik odwadniający (higroskopijny) oraz podwyższona temperatura.

- Tworzenie alkenów: Reakcja polega na usunięciu grupy -OH z atomu węgla i atomu wodoru z sąsiedniego atomu węgla w tej samej cząsteczce. Typowymi katalizatorami są mocne kwasy tlenowe, takie jak stężony kwas siarkowy (H₂SO₄), kwas fosforowy (H₃PO₄) lub tlenek glinu (Al₂O₃) w wysokiej temperaturze. Przykładowo: CH₃CH₂OH → CH₂=CH₂ + H₂O (w obecności H₂SO₄, w wysokiej temperaturze). Reakcja ta często przebiega zgodnie z regułą Zajcewa, która mówi, że wodór jest usuwany z tego atomu węgla, który jest związany z mniejszą liczbą atomów wodoru, co prowadzi do powstania bardziej podstawionego (i zazwyczaj stabilniejszego) alkenu.
- Tworzenie eterów: W odpowiednich warunkach, zwłaszcza w niższej temperaturze i przy odpowiednim stężeniu kwasu, dehydratacja może zajść między dwoma cząsteczkami alkoholu, prowadząc do powstania eteru. W tym przypadku cała grupa -OH z jednej cząsteczki alkoholu i atom wodoru z grupy -OH drugiej cząsteczki są usuwane. Przykładowo, dwie cząsteczki etanolu mogą utworzyć eter dietylowy: 2CH₃CH₂OH → CH₃CH₂OCH₂CH₃ + H₂O.
Estryfikacja: Tworzenie Zapachowych Związków
Estryfikacja to reakcja alkoholu z kwasem karboksylowym, która prowadzi do powstania estru i cząsteczki wody. Jest to reakcja równowagowa, często katalizowana przez silne kwasy, takie jak stężony kwas siarkowy (H₂SO₄). Kwas siarkowy pełni tu podwójną rolę: katalizuje reakcję i jednocześnie wiąże wodę, przesuwając równowagę w stronę produktów i zwiększając wydajność estru.
Ogólne równanie estryfikacji to: R-OH (alkohol) + R'-COOH (kwas karboksylowy) ⇌ R'-COOR (ester) + H₂O (woda). Przykładowo, reakcja etanolu z kwasem octowym (etanowym) prowadzi do powstania octanu etylu, estru o charakterystycznym, przyjemnym zapachu: CH₃CH₂OH + CH₃COOH → CH₃COOCH₂CH₃ + H₂O.
Estry są szeroko stosowane w przemyśle spożywczym (jako substancje zapachowe i smakowe), kosmetycznym (w perfumach), a także jako rozpuszczalniki. Octan etylu jest jednym z najczęściej używanych rozpuszczalników w laboratoriach i przemyśle.
Reakcje z Aktywnymi Metalami: Gdy Alkohol Staje się Kwasem
Alkohole, choć są związkami o obojętnym odczynie w roztworach wodnych (pH ≈ 7), wykazują bardzo słaby charakter kwasowy. Ich kwasowość jest znacznie mniejsza niż kwasów karboksylowych, ale wystarczająca, aby reagować z aktywnymi metalami, takimi jak sód (Na) czy potas (K). W wyniku tej reakcji powstają alkoholany (nazywane również alkoksynami) oraz wydziela się gazowy wodór.
Równanie ogólne to: 2ROH + 2Na → 2RONa + H₂↑. Przykładowo, reakcja etanolu z sodem wygląda następująco: 2CH₃CH₂OH + 2Na → 2CH₃CH₂ONa + H₂↑. Reakcja jest gwałtowna, szczególnie w przypadku potasu, i towarzyszy jej intensywne pienienie się roztworu spowodowane wydzielaniem się wodoru. Alkoholany są silnymi zasadami i znajdują zastosowanie w syntezach organicznych jako silne nukleofile lub zasady w reakcjach eliminacji.
Test Lucasa: Jak Rozróżnić Rzędowość Alkoholi?
Test Lucasa to klasyczna metoda laboratoryjna, która pozwala na szybkie rozróżnienie alkoholi I-, II- i III-rzędowych na podstawie ich reaktywności z odczynnikiem Lucasa. Odczynnik Lucasa to roztwór stężonego kwasu solnego (HCl) w obecności bezwodnego chlorku cynku (ZnCl₂), który pełni rolę katalizatora.
Reakcja przebiega mechanizmem substytucji nukleofilowej typu SN1, w którym kluczowym etapem jest tworzenie i stabilność karbokationu. Im stabilniejszy karbokation powstaje, tym szybciej zachodzi reakcja, co objawia się zmętnieniem roztworu (powstaniem nierozpuszczalnego halogenku alkilowego).
| Rodzaj alkoholu | Przykład | Szybkość reakcji | Obserwacja |
|---|---|---|---|
| I-rzędowy | Etanol (CH₃CH₂OH) | Bardzo wolno (kilka godzin lub brak reakcji w temperaturze pokojowej) | Brak natychmiastowego zmętnienia, ewentualnie powolne zmętnienie po długim czasie. |
| II-rzędowy | Izopropanol (CH₃CHOHCH₃) | Umiarkowanie szybko (kilka minut) | Szybsze zmętnienie roztworu. |
| III-rzędowy | Tert-butanol ((CH₃)₃COH) | Natychmiastowa | Natychmiastowe i wyraźne zmętnienie roztworu (tworzenie się dwóch faz). |
Alkohole III-rzędowe reagują najszybciej, ponieważ tworzą najstabilniejsze karbokationy III-rzędowe, co ułatwia etap rozpadu wiązania C-OH i przyłączenia chloru. Zrozumienie rzędowości alkoholi i mechanizmu testu Lucasa pozwala na ich efektywną identyfikację w laboratorium.
Inne Ważne Reakcje i Właściwości Alkoholi
Spalanie Alkoholi
Alkohole, podobnie jak inne związki organiczne, ulegają reakcjom spalania. W zależności od dostępności tlenu, może to być spalanie całkowite lub niecałkowite.
- Spalanie całkowite: W obecności wystarczającej ilości tlenu, alkohole spalają się do dwutlenku węgla i wody, wydzielając dużą ilość energii. Przykładowo: C₆H₁₃OH + 9O₂ → 6CO₂ + 7H₂O.
- Spalanie niecałkowite: Przy niedoborze tlenu, produktami spalania mogą być tlenek węgla (czad) lub sadza (węgiel pierwiastkowy) oraz woda. Przykładowo dla etanolu: C₂H₅OH + 2O₂ → 2CO + 3H₂O.
Właściwości Fizyczne
Właściwości fizyczne alkoholi są silnie uwarunkowane obecnością grupy hydroksylowej, która umożliwia tworzenie wiązań wodorowych między cząsteczkami. To właśnie wiązania wodorowe odpowiadają za wiele charakterystycznych cech alkoholi:
- Temperatura wrzenia: Alkohole mają znacznie wyższe temperatury wrzenia w porównaniu z węglowodorami o podobnej masie cząsteczkowej. Na przykład, etanol (78,5°C) wrze znacznie wyżej niż etan (-89°C), pomimo zbliżonej masy. Wynika to z energii potrzebnej do zerwania wiązań wodorowych podczas przejścia ze stanu ciekłego do gazowego.
- Rozpuszczalność w wodzie: Alkohole krótkołańcuchowe (np. metanol, etanol) są bardzo dobrze rozpuszczalne w wodzie, ponieważ mogą tworzyć wiązania wodorowe z cząsteczkami wody. Rozpuszczalność maleje wraz ze wzrostem długości łańcucha węglowego, ponieważ wzrasta hydrofobowa część cząsteczki.
Otrzymywanie Alkoholi
Alkohole można otrzymać na wiele sposobów, z których najważniejsze to:
- Hydratacja alkenów: Addycja wody do wiązania podwójnego w alkenie, często katalizowana kwasem, zgodnie z regułą Markownikowa (np. CH₂=CH₂ + H₂O → CH₃CH₂OH). Istnieją również metody addycji niezgodnej z regułą Markownikowa, np. w obecności nadtlenków.
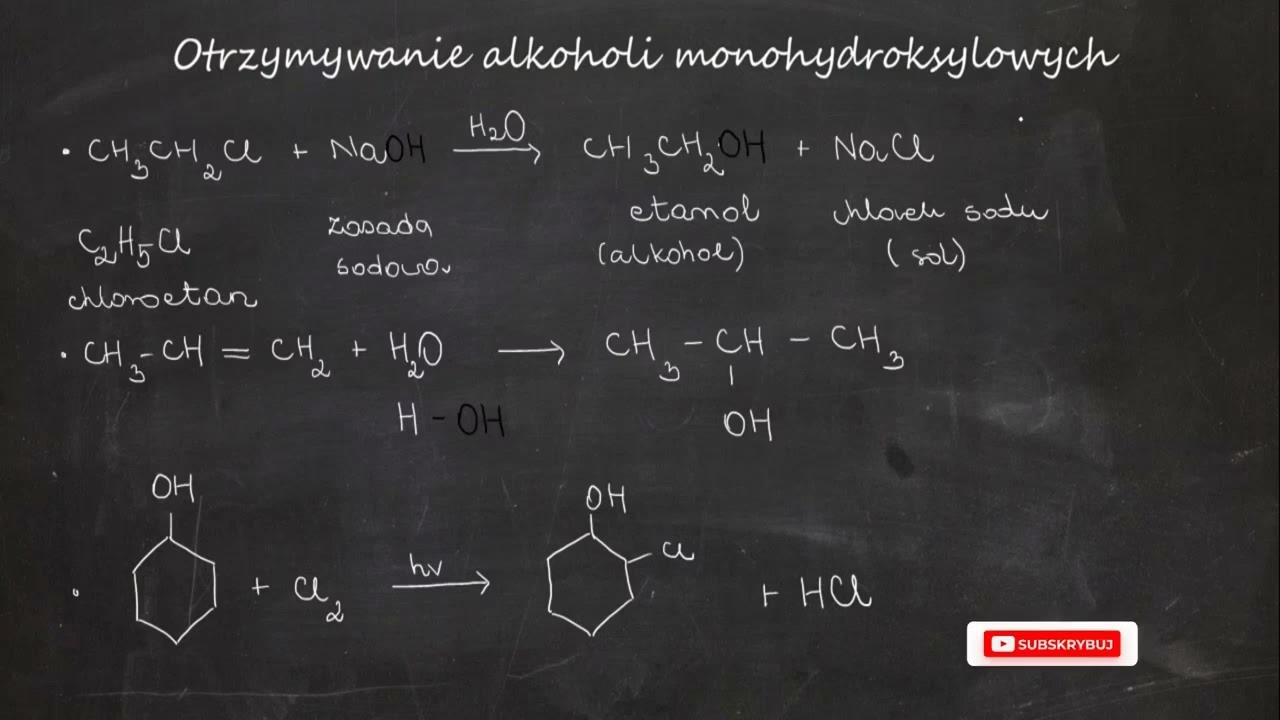
- Substytucja nukleofilowa halogenoalkanów: Reakcja halogenoalkanu z zasadą, np. NaOH, prowadząca do wymiany atomu halogenu na grupę -OH (np. CH₃CH₂Cl + NaOH → CH₃CH₂OH + NaCl).
- Redukcja aldehydów i ketonów: Aldehydy redukują się do alkoholi I-rzędowych, a ketony do alkoholi II-rzędowych, przy użyciu wodoru w obecności katalizatorów (Ni, Pt) lub reduktorów (NaBH₄, LiAlH₄).
- Fermentacja alkoholowa: Biologiczny proces, w którym drożdże przekształcają cukry (np. glukozę) w etanol i dwutlenek węgla (C₆H₁₂O₆ → 2C₂H₅OH + 2CO₂).
Reakcje Nie Zachodzące – Klucz do Identyfikacji
Wiedza o tym, z jakimi substancjami alkohole nie reagują, jest równie ważna, co znajomość ich reaktywności. Pozwala to na odróżnienie alkoholi od innych klas związków organicznych w testach laboratoryjnych:
- Brak reakcji z chlorkiem żelaza(III) (FeCl₃): W przeciwieństwie do fenoli, które tworzą z FeCl₃ charakterystyczne fioletowe kompleksy, alkohole nie reagują z tym odczynnikiem.
- Brak reakcji z wodorotlenkiem sodu (NaOH): Alkohole są zbyt słabymi kwasami, aby reagować z mocnymi zasadami takimi jak NaOH. Odróżnia to je od kwasów karboksylowych i fenoli, które reagują z NaOH.
- Brak reakcji z wodorowęglanem sodu (NaHCO₃): Alkohole nie reagują z wodorowęglanem sodu, co jest cechą charakterystyczną odróżniającą je od kwasów karboksylowych, które reagują z NaHCO₃ z wydzieleniem CO₂.
Ciekawostka: Dlaczego Nie Warto Mieszać Alkoholu z Paracetamolem?
Mieszanie alkoholu z paracetamolem (acetaminofenem) jest niezwykle niebezpieczne dla zdrowia i może prowadzić do poważnego, a nawet śmiertelnego uszkodzenia wątroby. Mechanizm tej interakcji jest złożony:
Zarówno alkohol, jak i paracetamol są metabolizowane w wątrobie. Paracetamol, szczególnie w dużych dawkach, prowadzi do produkcji toksycznego metabolitu o nazwie NAPQI. W normalnych warunkach organizm neutralizuje NAPQI za pomocą glutationu, naturalnego przeciwutleniacza wątrobowego. Jednakże, przewlekłe spożycie alkoholu lub nawet jednorazowe, duże spożycie, znacząco obniża poziom glutationu w wątrobie. Kiedy poziom glutationu jest niski, toksyczny NAPQI nie może być skutecznie zneutralizowany i zaczyna uszkadzać komórki wątrobowe, prowadząc do martwicy i niewydolności wątroby.
Objawy zatrucia mogą obejmować nudności, wymioty, bóle brzucha, a w ciężkich przypadkach żółtaczkę, krwawienia i śpiączkę wątrobową. W skrajnych sytuacjach jedynym ratunkiem może być przeszczep wątroby. Dlatego zawsze należy pamiętać o tej interakcji i unikać spożywania alkoholu przez co najmniej 24 godziny po zażyciu paracetamolu. Dla osób regularnie spożywających alkohol, nawet standardowe dawki paracetamolu mogą okazać się toksyczne.
Często Zadawane Pytania (FAQ)
P: Czym różni się utlenianie alkoholi I-rzędowych od II-rzędowych?
O: Alkohole I-rzędowe mogą być utleniane dwuetapowo: najpierw do aldehydów (przy użyciu słabych utleniaczy), a następnie do kwasów karboksylowych (przy użyciu silnych utleniaczy). Alkohole II-rzędowe utleniają się natomiast tylko do ketonów, niezależnie od siły utleniacza, ponieważ nie posiadają atomu wodoru przy węglu związanym z grupą -OH, który mógłby ulec dalszemu utlenieniu.

P: Dlaczego alkohole III-rzędowe nie ulegają utlenianiu?
O: Alkohole III-rzędowe są odporne na utlenianie, ponieważ atom węgla, do którego przyłączona jest grupa hydroksylowa (-OH), nie posiada żadnego atomu wodoru. W procesie utleniania alkoholi wymagane jest usunięcie atomu wodoru z tego węgla, aby utworzyć podwójne wiązanie węgiel-tlen. W przypadku alkoholi III-rzędowych, węgiel ten jest związany tylko z innymi atomami węgla, a wiązania C-C są znacznie trudniejsze do zerwania w warunkach utleniania.
P: Jakie są główne produkty dehydratacji alkoholi?
O: Głównymi produktami dehydratacji alkoholi są alkeny (w reakcji wewnątrzcząsteczkowej, przy wysokiej temperaturze i obecności katalizatora kwasowego) oraz etery (w reakcji międzycząsteczkowej, przy niższej temperaturze i odpowiednim stężeniu kwasu).
P: Czy alkohole są kwasami czy zasadami?
O: Wodne roztwory alkoholi są obojętne (pH około 7). Jednakże, alkohole wykazują bardzo słaby charakter kwasowy, co pozwala im reagować z aktywnymi metalami (np. sodem) z wydzieleniem wodoru i tworzeniem alkoholanu. Nie są natomiast zasadami w typowym rozumieniu, choć tlen w grupie -OH ma wolne pary elektronowe i może działać jako zasada Lewisa.
P: Do czego służy test Lucasa?
O: Test Lucasa służy do rozróżniania alkoholi I-rzędowych, II-rzędowych i III-rzędowych. Różnią się one szybkością reakcji z odczynnikiem Lucasa (HCl/ZnCl₂), co objawia się różnym czasem pojawienia się zmętnienia roztworu. Alkohole III-rzędowe reagują natychmiast, II-rzędowe w ciągu kilku minut, a I-rzędowe bardzo wolno lub wcale w temperaturze pokojowej.
Podsumowując, alkohole są fascynującą grupą związków chemicznych o bogatej i zróżnicowanej reaktywności. Ich zdolność do utleniania, estryfikacji, dehydratacji, a także reakcji z metalami, czyni je niezwykle użytecznymi w syntezie organicznej i wielu gałęziach przemysłu. Zrozumienie tych reakcji, ich warunków i produktów, a także metod identyfikacji, stanowi fundament wiedzy o chemii organicznej. Mamy nadzieję, że ten artykuł rozjaśnił Państwu najważniejsze aspekty chemii alkoholi i zachęcił do dalszego zgłębiania tej pasjonującej dziedziny.
Zainteresował Cię artykuł Tajemnice Reakcji Chemicznych Alkoholi", "kategoria": "Chemia? Zajrzyj też do kategorii Edukacja, znajdziesz tam więcej podobnych treści!
