06/07/2007
Zastanawiałeś się kiedyś, z jaką prędkością poruszają się niewidoczne cząsteczki powietrza wokół nas? To pytanie, choć pozornie proste, otwiera drzwi do fascynującego świata kinetyczno-molekularnej teorii gazów, która pozwala nam zrozumieć podstawowe pojęcia takie jak temperatura czy energia wewnętrzna. W tym artykule zagłębimy się w mikroskopowy świat gazów, by odkryć, co naprawdę wpływa na ruch ich cząsteczek i jaki wzór pozwala nam obliczyć ich średnią prędkość.
Kinetyczno-Molekularna Teoria Gazu Doskonałego – Podstawy
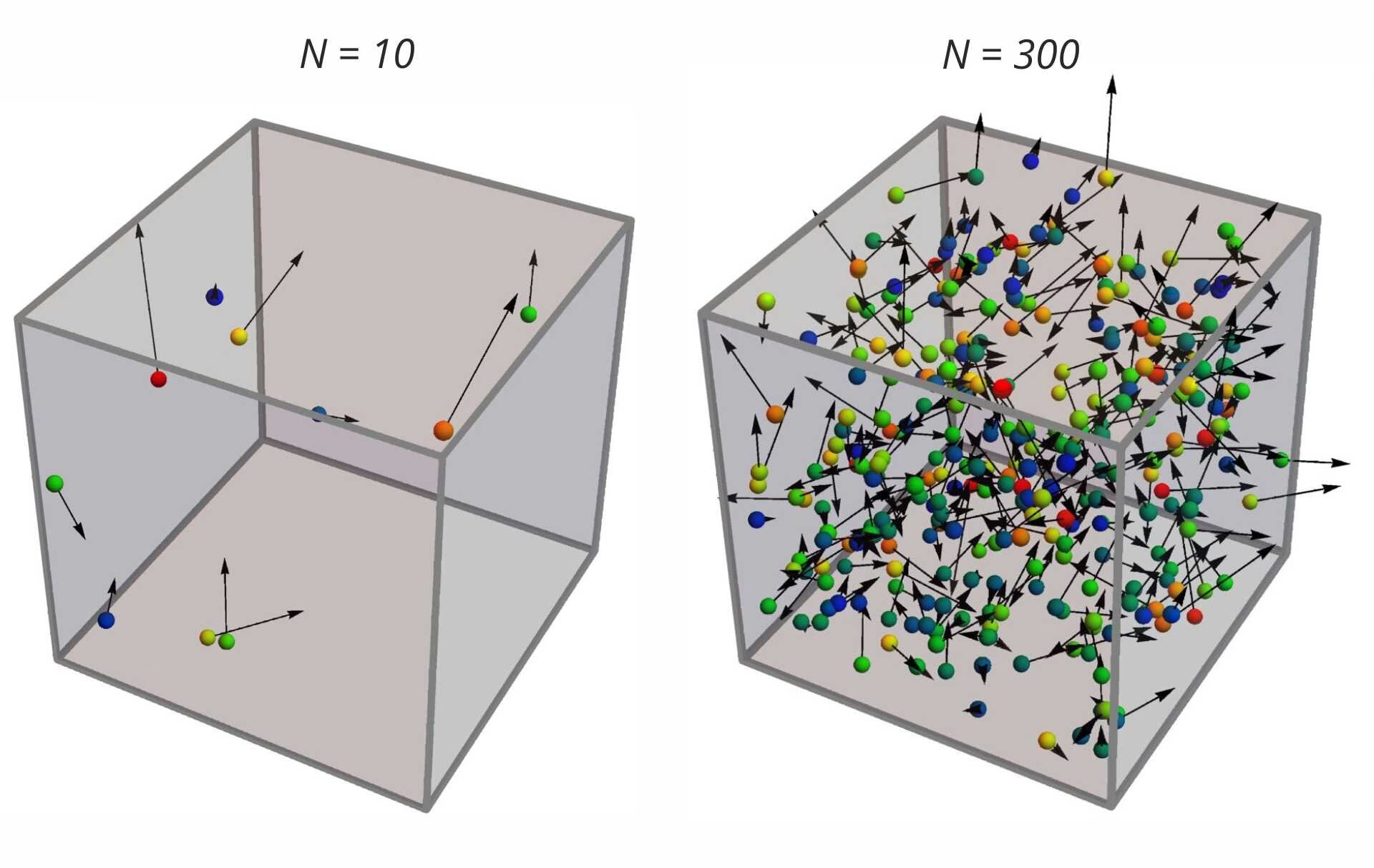
Aby zrozumieć prędkość cząsteczek, musimy najpierw poznać fundamenty kinetyczno-molekularnej teorii gazu doskonałego. Teoria ta opisuje gaz doskonały jako zbiór nieskończenie małych cząsteczek, które nieustannie poruszają się w chaotyczny sposób. Kluczowe założenia tego modelu to:
- Cząsteczki gazu mają zaniedbywalnie małe rozmiary w porównaniu do odległości między nimi.
- Poruszają się chaotycznie, zderzając się ze sobą i ze ściankami naczynia.
- Zderzenia te są idealnie sprężyste, co oznacza, że całkowita energia kinetyczna układu jest zachowana. Poza momentem zderzenia cząsteczki nie oddziałują ze sobą.
Model ten, choć uproszczony, doskonale opisuje zachowanie większości gazów rzeczywistych w warunkach nieodbiegających znacznie od normalnych. To właśnie dzięki niemu możemy precyzyjnie wyjaśnić, czym jest temperatura na poziomie mikroskopowym.
Temperatura a Średnia Energia Kinetyczna Cząsteczek
Jednym z najważniejszych odkryć płynących z kinetyczno-molekularnej teorii jest związek między temperaturą gazu a średnią energią kinetyczną jego cząsteczek. Okazuje się, że średnia energia kinetyczna ruchu postępowego cząsteczek (Ek)śr jest wprost proporcjonalna do temperatury gazu wyrażonej w skali Kelvina (T). Wzór ten ma postać:
(Ek)śr = 3⁄2 kBT
Gdzie kB to stała Boltzmanna, której wartość wynosi około 1,38 ⋅ 10-23 J/K. Ta uniwersalna stała fizyczna jest kluczowa dla zrozumienia mikroskopowych zjawisk termodynamicznych. Co to oznacza w praktyce? To, że temperatura jest niczym innym jak miarą średniej energii kinetycznej ruchu postępowego cząsteczek. Im wyższa temperatura, tym szybciej cząsteczki się poruszają, a co za tym idzie, mają większą energię kinetyczną. Rozumiemy też, dlaczego temperatura nie może być niższa od zera bezwzględnego (0 K), gdyż energia kinetyczna cząsteczek nie może być ujemna.
Warto zauważyć, że średnia energia kinetyczna nie zależy od masy poszczególnych cząsteczek. Oznacza to, że w mieszaninie różnych gazów, cząsteczki każdego z nich będą miały taką samą średnią energię kinetyczną ruchu postępowego, niezależnie od ich masy. Czy to samo dotyczy ich prędkości? Niekoniecznie!
Wzór na Prędkość Cząsteczek Gazu – Prędkość Średnia Kwadratowa
Skoro średnia energia kinetyczna nie zależy od masy, a prędkość jest bezpośrednio związana z energią kinetyczną (Ek = 1⁄2mv2), to musi istnieć związek między prędkością, masą i temperaturą. Ponieważ cząsteczki gazu poruszają się z różnymi, chaotycznymi prędkościami, nie możemy mówić o "jednej" prędkości dla wszystkich. Wprowadzamy zatem pojęcie prędkości średniej kwadratowej (vśrkw), która jest statystyczną miarą prędkości cząsteczek. Jest ona pierwiastkiem ze średniego kwadratu prędkości wszystkich cząsteczek:
vśrkw = √(<v2>)
Gdzie <v2> to średni kwadrat prędkości cząsteczek. Łącząc wzór na średnią energię kinetyczną z definicją energii kinetycznej i prędkości średniej kwadratowej, możemy wyprowadzić kluczowy wzór na prędkość cząsteczek gazu:
vśrkw = √(3kBT⁄m)
Gdzie:
- vśrkw to prędkość średnia kwadratowa cząsteczek (w m/s).
- kB to stała Boltzmanna (1,38 ⋅ 10-23 J/K).
- T to temperatura gazu w skali Kelvina (K).
- m to masa pojedynczej cząsteczki gazu (w kg).
Ten wzór jasno pokazuje, że choć średnia energia kinetyczna jest taka sama dla wszystkich gazów w danej temperaturze, to ich prędkości średnie kwadratowe już się różnią! Im większa masa cząsteczki (m), tym mniejsza będzie jej prędkość średnia kwadratowa przy tej samej temperaturze. Na przykład, cząsteczki helu (lekkie) będą poruszać się znacznie szybciej niż cząsteczki ksenonu (ciężkie) w tej samej temperaturze.
Energia Wewnętrzna Gazu Doskonałego – Rozszerzone Spojrzenie
Poza energią kinetyczną ruchu postępowego cząsteczek, gaz posiada także energię wewnętrzną (U), która jest sumą wszystkich rodzajów energii jego cząsteczek. Dla gazu doskonałego, energia wewnętrzna składa się z trzech głównych składników:
- Sumy energii kinetycznych w ruchu postępowym cząsteczek.
- Sumy energii potencjalnych oddziaływań między cząsteczkami.
- Sumy energii wewnętrznych samych cząsteczek (np. energii kinetycznej ruchu obrotowego czy drgającego atomów w cząsteczce).
Zgodnie z definicją gazu doskonałego, cząsteczki nie oddziałują ze sobą poza zderzeniami, więc drugi składnik (energia potencjalna oddziaływań) jest równy zero. Co do trzeciego składnika, jego uwzględnienie zależy od struktury cząsteczek:
- Gazy jednoatomowe (np. hel, neon): Cząsteczki są traktowane jako punkty materialne bez wewnętrznej struktury. Energia wewnętrzna pochodzi wyłącznie z ruchu postępowego: U = N ⋅ 3⁄2 kBT.
- Gazy dwuatomowe (np. tlen, azot): Cząsteczki mogą również rotować wokół własnych osi. W ich przypadku energia wewnętrzna jest większa: U = N ⋅ 5⁄2 kBT.
- Gazy trójatomowe liniowe (np. dwutlenek węgla): Mają jeszcze więcej stopni swobody ruchu (np. drgania atomów). Ich energia wewnętrzna to: U = N ⋅ 6⁄2 kBT.
Ogólny wzór na energię wewnętrzną gazu doskonałego to:
U = i⁄2 N kBT = i⁄2 n R T
Gdzie 'i' to liczba stopni swobody ruchu cząsteczki (3 dla jednoatomowych, 5 dla dwuatomowych, 6 dla trójatomowych liniowych), N to liczba cząsteczek, n to liczba moli, a R to stała gazowa (R = kB ⋅ NA, gdzie NA to liczba Avogadra). To pokazuje, że energia wewnętrzna gazu doskonałego zależy wyłącznie od jego temperatury i ilości, ale musi uwzględniać złożoność atomową cząsteczek.
Zmiana energii wewnętrznej (ΔU) danej porcji gazu jest zawsze związana ze zmianą temperatury: ΔU = i⁄2 n R ΔT.
Jak Szybko Poruszają Się Cząsteczki Gazu w Rzeczywistości?
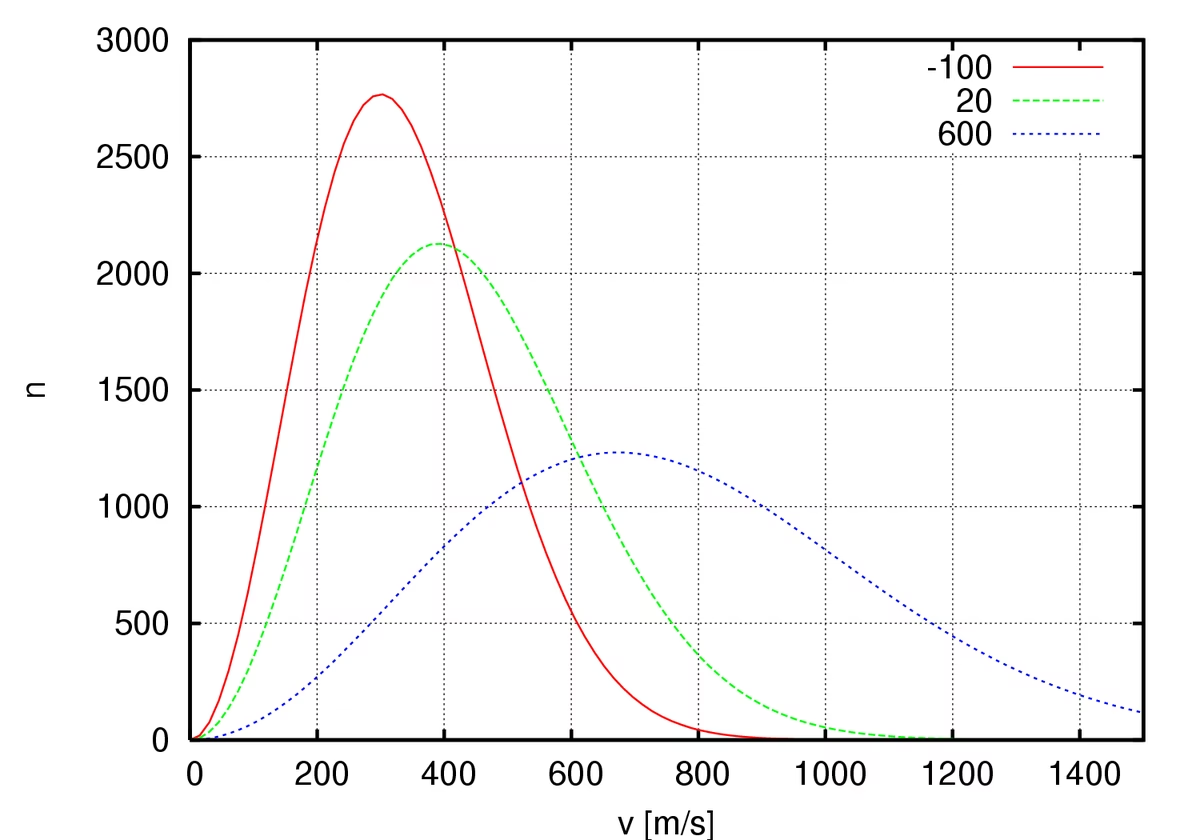
Chociaż mówimy o prędkości średniej kwadratowej, warto zdać sobie sprawę, że w rzeczywistości pojedyncze cząsteczki gazu poruszają się z bardzo różnymi, przypadkowymi prędkościami. Rozkład tych prędkości jest opisywany przez tzw. rozkład Maxwella-Boltzmanna. Niewiele cząsteczek ma prędkość bliską zeru lub bardzo dużą. Najwięcej z nich porusza się z prędkością zbliżoną do tzw. prędkości najbardziej prawdopodobnej.
Przykładem może być powietrze w warunkach normalnych (ok. 18°C i ciśnienie atmosferyczne). Średnia prędkość cząsteczek powietrza w tych warunkach wynosi około 500 metrów na sekundę. To prędkość porównywalna z prędkością kuli pistoletowej! Mimo tak dużych prędkości, cząsteczki te doznają ogromnej liczby zderzeń – około 1010 zderzeń na sekundę dla pojedynczej cząsteczki. Te częste zderzenia sprawiają, że ich tor ruchu jest zygzakowaty, a średnia droga swobodna (czyli odległość między dwoma zderzeniami) jest bardzo mała, rzędu 7 ⋅ 10-8 m w warunkach normalnych.

FAQ – Często Zadawane Pytania
Jaki jest wzór na prędkość cząsteczek gazu?
Wzorem opisującym statystyczną prędkość cząsteczek gazu jest prędkość średnia kwadratowa (vśrkw), obliczana ze wzoru: vśrkw = √(3kBT⁄m), gdzie kB to stała Boltzmanna, T to temperatura w Kelvinach, a m to masa pojedynczej cząsteczki.
Czy prędkość cząsteczek gazu zależy od ich masy?
Tak, zdecydowanie. Chociaż średnia energia kinetyczna cząsteczek w danej temperaturze jest taka sama dla wszystkich gazów, to ich prędkości średnie kwadratowe zależą od masy. Cząsteczki lżejszych gazów poruszają się szybciej niż cząsteczki gazów cięższych w tej samej temperaturze.
Jak szybko poruszają się cząsteczki powietrza w temperaturze pokojowej?
W warunkach normalnych (np. w temperaturze około 18°C), średnia prędkość cząsteczek powietrza (głównie azotu i tlenu) wynosi około 500 metrów na sekundę.
Co to jest gaz doskonały?
Gaz doskonały to fizyczny model gazu, w którym cząsteczki mają zaniedbywalnie małe rozmiary, poruszają się chaotycznie, a ich zderzenia są idealnie sprężyste. Poza zderzeniami cząsteczki nie oddziałują ze sobą. Jest to uproszczenie, które pozwala na precyzyjne matematyczne opisywanie zachowania gazów.
Co to jest stała Boltzmanna?
Stała Boltzmanna (kB) to uniwersalna stała fizyczna, która łączy średnią energię kinetyczną cząsteczek gazu z temperaturą w skali Kelvina. Jej wartość to około 1,38 ⋅ 10-23 J/K.
Słowniczek
- Gaz doskonały: Fizyczny model gazu, w którym cząsteczki mają zaniedbywalnie małe rozmiary, poruszają się chaotycznie, a zderzenia są idealnie sprężyste.
- Stała Boltzmanna (kB): Uniwersalna stała fizyczna, łącząca średnią energię kinetyczną cząsteczek z temperaturą.
- Liczba Avogadra (NA): Liczba molekuł (atomów lub cząsteczek) w 1 molu dowolnej substancji, około 6,022 ⋅ 1023.
- Stała gazowa (R): Stała fizyczna pojawiająca się w równaniu stanu gazu doskonałego (R = kB ⋅ NA), około 8,31 J/(mol·K).
- Prędkość średnia kwadratowa (vśrkw): Statystyczna miara prędkości cząsteczek gazu, pierwiastek ze średniego kwadratu prędkości.
Zrozumienie wzoru na prędkość cząsteczek gazu i jego powiązań z temperaturą oraz energią wewnętrzną jest fundamentalne dla fizyki i chemii. Pozwala nam to nie tylko opisać, ale i przewidywać zachowanie materii na poziomie mikroskopowym, otwierając drogę do głębszego poznania otaczającego nas świata.
Zainteresował Cię artykuł Prędkość cząsteczek gazu: Wzór i znaczenie? Zajrzyj też do kategorii Fizyka, znajdziesz tam więcej podobnych treści!