28/06/2014
Modele atomowe Thomsona i Rutherforda, choć stanowiły kamienie milowe w zrozumieniu budowy materii, nie potrafiły odpowiedzieć na kluczowe pytania dotyczące energii atomu i jego stabilności. Teorie te pozostawiały wiele do życzenia, gdy przyszło do wyjaśnienia, dlaczego elektrony krążące wokół jądra nie tracą energii i nie wpadają do niego, co powinno następować zgodnie z zasadami klasycznej fizyki. Właśnie w tym momencie na scenę wkroczył Niels Bohr, proponując w 1913 roku rewolucyjny model, który nie tylko wyjaśnił te zagadki, ale także otworzył drzwi do zupełnie nowego spojrzenia na świat kwantowy. Jego teoria, bazująca na pewnych śmiałych założeniach, stała się fundamentem dla dalszego rozwoju fizyki atomowej i kwantowej, dając początek erze mechaniki kwantowej i zmieniając nasze fundamentalne postrzeganie wszechświata na poziomie subatomowym.

Teoria Bohra – Podstawy Modelu Atomowego
W 1913 roku Niels Bohr zaproponował swój model struktury atomowej, opisując atom jako małe, dodatnio naładowane jądro, otoczone elektronami krążącymi po kołowych orbitach. Możemy to sobie wyobrazić jako miniaturowy układ słoneczny, gdzie elektrony pełnią rolę planet, a jądro – słońca, utrzymywane razem przez siły elektrostatyczne. Model ten, znany powszechnie jako model atomowy Bohra, był w zasadzie ulepszoną wersją modelu Rutherforda, pokonującą jego kluczowe ograniczenia. Bohr zgodził się z Rutherfordem w większości punktów, takich jak koncepcja jądra i elektronów krążących wokół niego, ale dodał do niej fundamentalne postulaty, które okazały się przełomowe. Główne cechy modelu atomowego Nielsa Bohra to:
- Elektrony krążą wokół jądra po stabilnych orbitach bez emisji energii promienistej. Każda orbita ma określoną energię i jest nazywana powłoką energetyczną lub poziomem energetycznym. To było kluczowe odejście od fizyki klasycznej, która przewidywała, że przyspieszające elektrony powinny ciągle emitować promieniowanie i w konsekwencji wpaść do jądra.
- Orbita lub poziom energetyczny jest oznaczany jako powłoki K, L, M, N. Gdy elektron znajduje się na najniższym poziomie energetycznym, mówi się, że jest w stanie podstawowym. Te dyskretne poziomy energii były dowodem na kwantyzację energii w atomie.
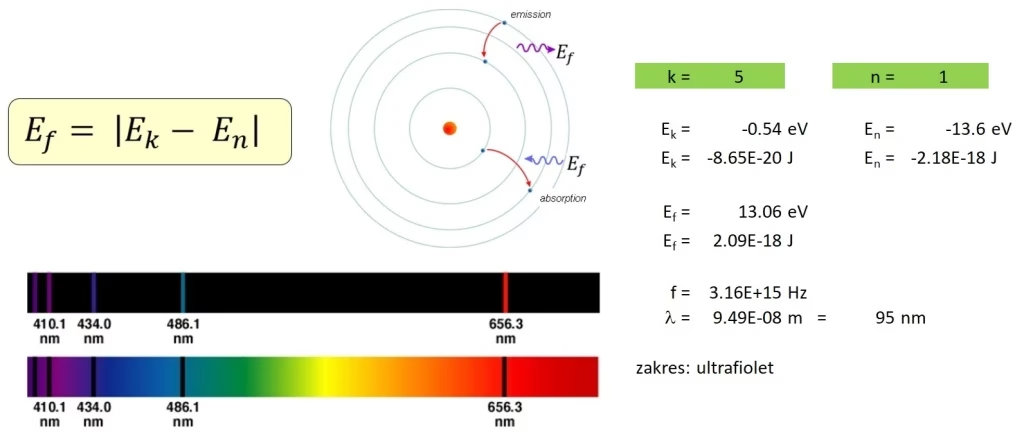
- Elektron emituje lub absorbuje energię, gdy przeskakuje z jednej orbity lub poziomu energetycznego na inną. Gdy przeskakuje z wyższego poziomu energetycznego na niższy, emituje energię. Natomiast absorbuje energię, gdy przeskakuje z niższego poziomu energetycznego na wyższy. To zjawisko jest znane jako przeskoki kwantowe.
- Absorbancja lub emisja energii jest równa różnicy między energiami dwóch poziomów energetycznych (E2, E1) i jest określona równaniem Plancka:
ΔE = E2 - E1 = hν
Gdzie:
- ΔE = energia zaabsorbowana lub wyemitowana
- h = stała Plancka
- ν = częstotliwość promieniowania elektromagnetycznego emitowanego lub absorbowanego
- Moment pędu elektronu krążącego po powłokach energetycznych jest dany wzorem:
mevr = nh/2π
Gdzie:
- n = numer odpowiadającej powłoki energetycznej; 1, 2, 3…
- me = masa elektronu
- v = prędkość
- r = promień
- h = stała Plancka
Ten postulat, znany jako kwantyzacja momentu pędu, był kolejnym fundamentalnym założeniem, które pozwoliło Bohrowi wyjaśnić stabilność orbit i dyskretne widma atomów.
Ograniczenia Modelu Atomowego Bohra
Mimo swojego rewolucyjnego charakteru i sukcesów w wyjaśnianiu widma wodoru, model atomowy Bohra nie był pozbawiony wad i ograniczeń. Jego uproszczona natura nie była w stanie sprostać wszystkim wyzwaniom, jakie stawiała przed nim rosnąca wiedza o świecie kwantowym. Do najważniejszych ograniczeń modelu Bohra należą:
- Naruszenie Zasady Nieoznaczoności Heisenberga: Teoria Bohra zakłada, że elektrony mają jednocześnie znany promień orbity i znany moment pędu, co oznacza, że ich położenie i pęd są dokładnie określone w tym samym czasie. Jest to niemożliwe zgodnie z zasadą nieoznaczoności Heisenberga, która stwierdza, że nie można jednocześnie precyzyjnie określić położenia i pędu cząstki.
- Ograniczona Przewidywalność dla Większych Atomów: Model Bohra dokonywał poprawnych przewidywań dla atomów o mniejszych rozmiarach, takich jak wodór (który posiada tylko jeden elektron). Jednakże, gdy rozważano większe atomy, przewidywania widmowe okazywały się niedokładne. Model ten nie był w stanie wyjaśnić złożonych widm atomów wieloelektronowych, ponieważ ignorował oddziaływania między elektronami.
- Brak Wyjaśnienia Efektu Zeemana: Model Bohra nie potrafił wyjaśnić efektu Zeemana, czyli zjawiska rozszczepienia linii spektralnych na kilka składników w obecności zewnętrznego pola magnetycznego. Sugerowało to, że elektrony mają dodatkowe właściwości (takie jak spin), których model Bohra nie uwzględniał.
- Brak Wyjaśnienia Efektu Starka: Podobnie, model Bohra nie był w stanie wyjaśnić efektu Starka, czyli rozszczepienia linii spektralnych na drobne linie w obecności zewnętrznego pola elektrycznego. To również wskazywało na niedoskonałości w jego opisie zachowania elektronów.
- Brak Wyjaśnienia Intensywności Linii Spektralnych: Model Bohra przewidywał pozycje linii widmowych, ale nie był w stanie wyjaśnić ich względnej intensywności, co jest kluczowe dla zrozumienia prawdopodobieństwa przejść między poziomami energetycznymi.
Ewolucja Zrozumienia Atomu: Od starożytności do kwantów
Koncepcja atomu sięga starożytnej Grecji, gdzie filozof Demokryt twierdził, że cała materia składa się z niepodzielnych cząstek zwanych atomami, otoczonych pustą przestrzenią. Od tego czasu, aż do sformułowania współczesnej idei atomu w XIX i XX wieku, pojawiło się wiele teorii, które stopniowo przybliżały nas do obecnego zrozumienia mikroskopijnego świata.
Model Atomowy Daltona
John Dalton, angielski naukowiec, zaproponował pierwszy nowoczesny model atomowy na początku XIX wieku. Stwierdził, że cała materia składa się z atomów, które są niepodzielne. Oto niektóre z właściwości, które Dalton przypisał atomowi:
- Wszystkie atomy tego samego pierwiastka mają tę samą masę.
- Atomy nie mogą być dzielone na mniejsze cząstki.
- Podczas reakcji chemicznych atomy ulegają przegrupowaniu.
- Cząsteczki składają się z kilku rodzajów atomów różnych pierwiastków, a związki chemiczne mają różne proporcje pierwiastków.
Model Daltona, choć fundamentalny, był uproszczony i nie uwzględniał wewnętrznej struktury atomu.
Model Atomowy Thomsona
Wraz z odkryciem elektronów przez brytyjskiego naukowca J. J. Thomsona stało się jasne, że atom składa się z jeszcze mniejszych cząstek, odpowiedzialnych za przenoszenie ładunku elektrycznego. Naukowcy w czasach Thomsona uważali, że atomy są zasadniczo neutralne. Thomson zaproponował, że atomy mają małe, ujemnie naładowane cząstki (elektrony) unoszące się w "zupie" dodatniego ładunku. Model ten jest również znany jako "model ciastka z rodzynkami" (plum pudding model).
Model Atomowy Rutherforda
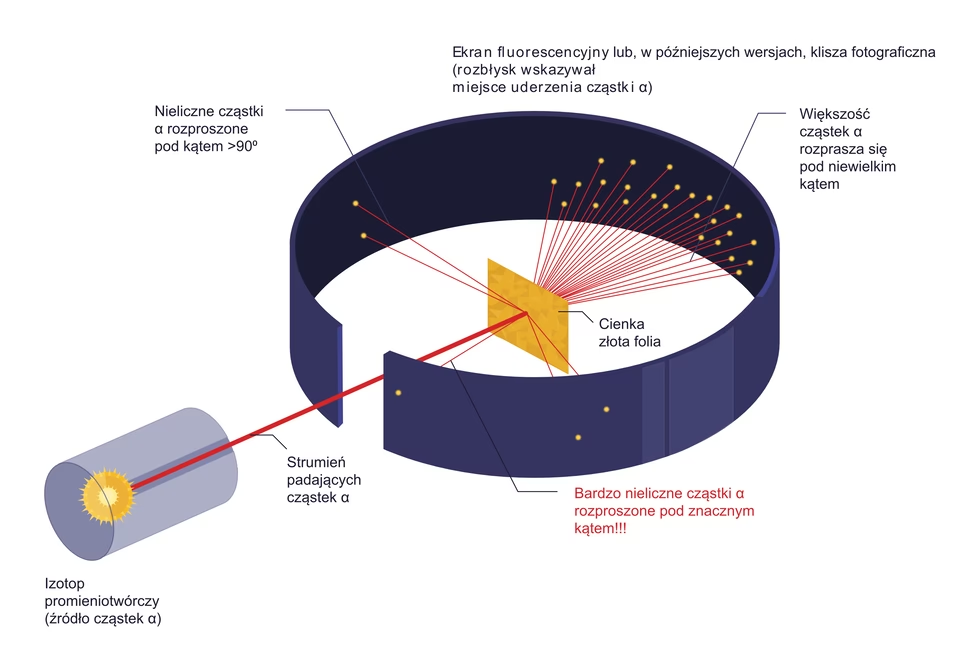
Nowozelandzki naukowiec Ernest Rutherford, wraz z niemieckim naukowcem Hansem Geigerem, zaprojektował eksperymenty, które przeprowadził student Ernest Marsden. Polegały one na bombardowaniu cienkiej folii złota cząstkami alfa. Gdyby atom był solidną kulą dodatniego ładunku z kilkoma elektronami na wierzchu, jak proponował model Thomsona, większość wystrzelonych cząstek nie dotarłaby na drugą stronę folii. Jednakże, eksperyment dowiódł, że Thomson się mylił. Atom był w środku niemal pusty, ponieważ niewiele cząstek uderzyło w jądra atomów. Rutherford zaproponował, że atom zawiera jądro, w którym skoncentrowany jest cały ładunek dodatni. W jego modelu elektrony krążyły wokół centrum. Model Rutherforda, choć przełomowy, miał poważną wadę: nie wyjaśniał stabilności atomu, ponieważ krążące elektrony powinny tracić energię i wpaść do jądra.
Model Atomowy Bohra
Jak już wspomniano, model Rutherforda nie zyskał pełnej akceptacji ze względu na problem stabilności. Nierówności w modelu atomowym Rutherforda skłoniły Nielsa Bohra do zaproponowania nowego. Model Bohra był podobny do Rutherforda, ale kluczowa różnica dotyczyła sposobu poruszania się elektronów. Według Bohra, elektrony mogą poruszać się tylko po pewnych orbitach, w zależności od ich poziomu energetycznego, i mogą przemieszczać się między orbitami, uwalniając lub absorbując energię. Model Bohra wyjaśnił widmo atomu wodoru, ale miał trudności z bardziej złożonymi elementami i efektami zewnętrznych pól.

Kwantowy Model Atomu
Współczesne modele atomu, znane jako kwantowe modele, bazują na mechanice kwantowej i koncepcji, że elektrony nie poruszają się po precyzyjnie określonych orbitach, lecz zajmują obszary przestrzeni zwane orbitalami, gdzie prawdopodobieństwo ich znalezienia jest największe. Jest to rozwinięcie idei, że elektron ma naturę falową i cząsteczkową jednocześnie, co zostało sformułowane przez de Broglie'a i rozwinięte przez Schrödingera. Model kwantowy jest znacznie bardziej złożony, ale też znacznie dokładniejszy w opisie zachowania atomów i ich interakcji.
Pierwsze Postulaty Bohra i ich Podłoże Kwantowe
Postulaty Bohra, choć początkowo formułowane ad hoc, znalazły swoje głębsze uzasadnienie w rozwoju mechaniki kwantowej. Zwłaszcza pierwszy postulat, dotyczący kwantyzacji momentu pędu, można wyprowadzić z falowej natury mikroświata, co zostało później rozwinięte przez Louisa de Broglie'a.
Elektron w atomie nie jest idealnie małą kulką, jak to sobie wyobrażaliśmy w fizyce klasycznej. Zamiast tego, lepiej jest wyobrazić sobie elektron jako rozmytą "chmurę prawdopodobieństwa", która miejscami jest gęstsza (tam, gdzie elektron znajduje się z większym prawdopodobieństwem), a miejscami rzadsza (gdzie szanse znalezienia elektronu są małe). Dodatkowo, ta "chmura" nie jest stała w czasie, ale faluje zgodnie z równaniem Schrödingera. Tak jak równanie Newtona opisuje zachowanie dużych obiektów pod wpływem sił, tak równanie Schrödingera opisuje, jak chmura prawdopodobieństwa zmienia się wraz z ruchem elektronu i jego oddziaływaniem z innymi cząstkami.
Równanie Schrödingera przewiduje, że chmura prawdopodobieństwa faluje podobnie jak struna w gitarze. Długość fali tych drgań zależy od prędkości cząstki. Elektron w atomie krąży wokół jądra, więc przypisana mu chmura prawdopodobieństwa otacza jądro, falując wokół niego. Aby to zobrazować, wyobraźmy sobie strunę zwiniętą w okrąg. Taka struna może drgać stabilnie tylko wtedy, gdy długość okręgu jest wielokrotnością długości fali. Mając daną prędkość rozchodzenia się fali (v), jej długość (λ) oraz promień okręgu (r), powyższy warunek możemy zapisać jako:
2πr = nλ
gdzie n jest liczbą naturalną (1, 2, 3...).
Jak wspomniano wyżej, długość fali materii (fali de Broglie'a) zależy od pędu cząstki (mv), zgodnie ze związkiem:
λ = h / mv
Związek ten został oryginalnie zaproponowany przez de Broglie’a w 1924 roku, wprowadzając koncepcję dualizmu korpuskularno-falowego. Łącząc ze sobą te dwa równania (podstawiając λ z drugiego równania do pierwszego), otrzymujemy postulat Bohra dotyczący kwantyzacji momentu pędu:
mvr = nh/(2π)
Ten wzór jest bezpośrednim potwierdzeniem, że tylko te orbity, na których elektron może tworzyć stabilne fale stojące, są dozwolone. To właśnie to zjawisko tłumaczy, dlaczego elektrony nie tracą energii na tych specyficznych orbitach i dlaczego atom jest stabilny. Jest to jeden z najbardziej eleganckich przykładów zastosowania zasad mechaniki kwantowej do wyjaśnienia struktury atomu.
Tabela Porównawcza Kluczowych Modeli Atomowych
| Model Atomowy | Kluczowa Idea / Opis | Główne Ograniczenia / Wpływ |
|---|---|---|
| Demokryt (Starożytność) | Materia składa się z niewidzialnych, niepodzielnych cząstek (atomów) i pustej przestrzeni. | Brak dowodów eksperymentalnych; spekulacyjny charakter. |
| Dalton (Początek XIX w.) | Atomy są niepodzielne i niezmienne; atomy tego samego pierwiastka są identyczne; atomy łączą się w prostych proporcjach. | Nie uwzględnia istnienia subatomowych cząstek; atomy mogą być podzielone (rozszczepienie jądra). |
| Thomson ("Ciastko z rodzynkami", 1904) | Atom to jednorodna, dodatnio naładowana kula, w której zanurzone są ujemne elektrony. | Nie wyjaśnia wyników eksperymentu Rutherforda (rozpraszania cząstek alfa); nie przewiduje jądra atomowego. |
| Rutherford (Model planetarny, 1911) | Atom posiada małe, gęste, dodatnio naładowane jądro, wokół którego krążą elektrony na orbitach. | Nie wyjaśnia stabilności atomu (elektrony powinny tracić energię i wpaść do jądra); nie wyjaśnia dyskretnych widm atomowych. |
| Bohr (1913) | Elektrony krążą po stabilnych, kwantowanych orbitach energetycznych; emisja/absorpcja energii tylko przy przeskokach między orbitami. | Działa tylko dla atomów jednelektronowych (np. wodoru); nie wyjaśnia efektu Zeemana i Starka; sprzeczny z Zasadą Nieoznaczoności Heisenberga. |
| Kwantowy (Lata 20. XX w. i później) | Elektrony istnieją w orbitalach (obszarach prawdopodobieństwa); dualizm korpuskularno-falowy; opis oparty na równaniu Schrödingera. | Bardziej złożony i abstrakcyjny; trudniejszy do wizualizacji bezpośredniej niż wcześniejsze modele. |
Często Zadawane Pytania (FAQ)
Poniżej przedstawiamy odpowiedzi na najczęściej zadawane pytania dotyczące modelu atomowego Bohra i związanych z nim koncepcji.
P1: Jakie są główne ograniczenia modelu atomowego Bohra?
Model atomowy Bohra nie był w stanie wyjaśnić efektu Zeemana (rozszczepienia linii spektralnych w polu magnetycznym) ani efektu Starka (rozszczepienia w polu elektrycznym). Ponadto, narusza on zasadę nieoznaczoności Heisenberga, zakładając, że położenie i pęd elektronu są jednocześnie dokładnie znane. Model ten również słabo przewidywał widma dla atomów wieloelektronowych, skupiając się głównie na atomie wodoru.
P2: Jakie jest znaczenie teorii atomowej Bohra?
Bohr był pierwszym naukowcem, który odkrył, że elektrony poruszają się wokół jądra po różnych, dyskretnych orbitach energetycznych. Jego teoria wyjaśniła stabilność atomu i dyskretny charakter widm emisyjnych i absorpcyjnych. Pozwoliło to również na zrozumienie, że właściwości pierwiastka można w dużej mierze określić na podstawie liczby elektronów w powłoce walencyjnej. Był to kluczowy krok w rozwoju mechaniki kwantowej.
P3: Jak elektrony poruszają się w modelu Bohra?
Według Bohra, elektrony poruszają się wokół centralnego jądra po ustalonych, kołowych orbitach. Te orbity mają specyficzne energie i są również nazywane powłokami energetycznymi lub poziomami energetycznymi. Elektrony mogą przeskakiwać między tymi orbitami, absorbując lub emitując ściśle określone kwanty energii.
P4: Kto był pierwszym naukowcem, który odkrył elektrony?
J. J. Thomson był pierwszym, który odkrył elektrony podczas badania właściwości promieni katodowych pod koniec XIX wieku. Jego eksperymenty doprowadziły do obalenia koncepcji atomu jako niepodzielnej cząstki.
P5: Ile elektronów znajduje się w powłoce L?
W powłoce L (n=2) może znajdować się maksymalnie 8 elektronów. Ogólna zasada dla maksymalnej liczby elektronów w danej powłoce (n) wynosi 2n2. Dla n=1 (powłoka K) to 2(1)2=2, dla n=2 (powłoka L) to 2(2)2=8, dla n=3 (powłoka M) to 2(3)2=18 itd.
Model atomowy Bohra, pomimo swoich ograniczeń, stanowił fundamentalny krok w zrozumieniu struktury atomu i zachowania elektronów. Otworzył on drogę dla dalszego rozwoju fizyki kwantowej, która ostatecznie doprowadziła do powstania znacznie bardziej złożonych, ale i dokładniejszych modeli, takich jak model kwantowy. Dziś, choć nie jest to najpełniejszy opis, model Bohra pozostaje cennym narzędziem dydaktycznym, pozwalającym zrozumieć podstawowe zasady kwantyzacji i stabilności materii.
Zainteresował Cię artykuł Model atomowy Bohra: Przełom w zrozumieniu atomu? Zajrzyj też do kategorii Fizyka, znajdziesz tam więcej podobnych treści!